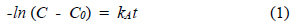VOCs emissions from industries cause the air pollution and odor. In the industrial facilities, the existing odor treatment techniques have limits and problems. In this study, the optimum essential oil and metal oxide selected by screening test. lavender oil, cypress oil and TiO2 were determined by deodorant materials and those were blended by 5%, 45%, 10%, respectively. In addition, the result of batch type experiments depending on the dilution rate, injection, rate, temperature showed that the optimum condition of deodorant is 6 mL of injection rate, and 200 times of dilution rate and the removal efficiency increased in proportion with temperature. In addition, the activation energy was calculated from the rate equation, which appeared in the 3-4 times lower than conventional deodorants.
생활수준이 향상되고 경제가 성장함에 따라 악취는 중요한 환경문제로 인식되고 있다. 악취는 원인이 되는 물질의 종류와 성질이 매우 다양하고 악취물질 상호간의 복합적 작용하기 때문에 이를 효과적으로 처리하기에 어려운 문제중 하나로 취급되고 있다. 현재 우리나라에서는 암모니아, 황화합물 등을 포함한 22가지 물질을 지정악취 물질로 규제하고 있다[1]. 이러한 악취 물질은 다양한 산업시설로부터 배출되고 있으며 특히 석유화학공장, 중공업, 자동차 도장공정 등에서는 휘발성유기화합물질(VOCs)이 주요 악취 물질로 대두 되고 있다[2]. 휘발성유기화합물질은 저 농도로 악취를 유발하고 피부접촉 또는 호흡기로 흡입되어 신경계 등의 장애를 일으키는 유해물질로 분류되고 있다[3].
특히 자동차 산업의 경우 경제적, 사회적 영향과 함께 범지구적 환경문제에 대한 인식이 증가하고 있음에도 불구하고 생산공정이나 보수과정에서 발생하는 휘발성유기화합물질을 완벽하게 제어하지 못하고 있어 외부로 확산될 경우 주변지역 악취오염원이 될 수 있다[1,4]. 자동차 산업의 경우 도장공정 특성상 풍량이 매우 높기 때문에 휘발성유기화합물질의 처리 효율이 떨어지고 처리 비용 증가로 인해 경제성이 떨어진다는 단점이 존재한다. 또한 기존의 미생물을 이용해 처리하는 방지시설은 특정한 악취성분에만 반응하는 미생물 특성상 휘발성유기화합물질의 제거 효율이 낮으며 미생물의 배양과 시스템의 유지관리가 어렵고 부하 변동에 취약해 처리효율이 떨어짐으로써 주변지역으로 휘발성유기화합물질이 확산될 우려가 있다[2,5]. 또한 일부 휘발성유기화합물질은 최소감지농도가 매우 낮기 때문에, 이를 기술적으로 처리하는데 어려움이 있다. 이처럼 높은 풍량으로 배출되는 휘발성유기화합물질을 처리하기 위해 추가적인 탈취제의 적용이 필요한 실정이다.
주변으로 확산되는 휘발성유기화합물질을 처리하기 위한 방법으로 마스킹이나 탈취제 분사법을 적용할 수 있으나 마스킹은 근본적인 악취제거 방안이 아니고, 기존 상용화 탈취제는 합성 화학물질을 포함하고 있기 때문에 2차 오염물질이 발생될 수 있으므로 인체에 무해한 천연 화학물질 사용의 필요성이 대두되고 있다[7-9].
이러한 문제점을 해결하기 위해 천연 식물정유를 탈취제로 적용할 수 있으며, 대표적인 식물정유물질로는 녹나무, 전나무, 편백나무, 소나무 등의 수목계열과 라벤더 정유 등이 있다. 이외에도 짚초액, 페퍼민트, 제라늄, 베르가못, 기타 과일 정유 등을 이용하여 탈취제로 활용하는 연구와 특허 개발이 수행되고 있다. 식물정유물질은 eucalyptol, linalool 등의 monoterpene 류가 50% 이상의 비율로 구성되어 있으며, terpene 물질들은 알코올, 알데히드, 케톤, 에테르, 에스테르, 유기산 등의 작용기를 포함한다. 이러한 작용기들을 포함하는 미세입자는 산성, 중성, 염기성 등의 악취물질을 산화, 중화 반응을 통해 무취 물질로 전환시키게 된다[13-18].
기존 연구에서 악취 물질 중 황화합물과 아민계열에 대한 악취 처리 효과가 입증됐지만 휘발성유기화합물질에 대한 연구가 부족하고, 정유물질별 정량적인 효율연구가 이루어지지 않았다. 따라서 본 연구에서는 휘발성유기화합물질 제거에 효과적일 것으로 예상되는 식물정유 물질들을 대상으로 최적 휘발성유기화합물질 제거 및 탈취제 제조를 위한 기초 실험을 수행하였다.
이를 위해 본 연구에서는 자동차 도장 공정을 대상으로 배가스를 포집하여 악취물질의 종류 및 발생농도를 측정하여 탈취제 제조를 위한 주요 악취 대상물질을 선정하였다. 그리고 다양한 종류의 식물성 정유 중 우수한 성능의 정유를 정성적으로 분석하기 위해 라벤더, 레몬그라스, 소나무, 편백나무, 시나몬, 전나무를 문헌조사를 통해 후보물질로 선정하여 선별 실험을 수행하였고[13-18] 탈취 효율을 증가시키기 위한 목적으로 첨가제를 선정하여 식물 정유 물질 종류 및 첨가제의 혼합 비율을 결정하였다. 또한 혼합된 탈취제의 최적 분사 및 탈취조건을 파악하기 위해 희석배수, 분사량, 온도에 따른 회분식 휘발성유기화합물질 제거 실험을 수행하였으며, 온도에 따른 실험을 통해 반응속도상수 및 활성화에너지를 예측하였다.
기존 문헌을 참고하여 최적의 식물정유 물질을 선정하기 위해 라벤더, 레몬그라스, 소나무, 편백나무, 시나몬, 전나무를 후보물질로 선정하였다[13-18]. 추출법은 모두 수증기 증류법을 통해 추출된 순도 100% 식물정유를 사용하였고 소나무(아로마비즈, Korea), 전나무(Lazurin Ltd 151a, Russia), 시나몬(Herbskin, Australia)의 경우 잎을 추출, 편백나무(이노하이, Korea)의 경우 잎과 가지, 라벤더(Agarbatti, India)의 경우 꽃을 레몬그라스(Agarbatti, India)는 풀을 추출한 정유물질을 사용하였다. 또한 에탄올과 증류수를 1:1로 혼합하여 용매로 사용하였다. 첨가제의 경우, 제올라이트(Zeolite, 200 mesh, Wako, Japan), 오산화바나듐(V2O5, 99%, 대정화금, Korea), 이산화티타늄(TiO2, 대정화금, Korea), 산화아연(ZnO, 99%, 대정화금, Korea) 4종류를 선정하여 선별실험을 수행하였다[19-24]. 본 연구에서는 도장공정 내 악취 원인물질 분석을 통해 휘발성 유기화합물질 중 아세트알데히드와 자일렌, 톨루엔, 뷰틸 아세테이트, 에틸벤젠(50 ppm, Rigas, Korea)을 선정하였고, 농도는 99.99% 질소(경동가스, Korea)를 사용하여 조절하였다.
2.2. 휘발성유기화합물질 및 아세트 알데히드의 시료 채취 및 분석
2.2.1. 휘발성유기화합물질
본 연구에서는 휘발성유기화합물질을 채취하기 위해 흡착제를 이용한 흡착관법을 사용하였다. 흡착제는 시료 포집시 유속에 저항을 주지 않고 원활하게 시료를 포집하기 위하여 입자 크기가 0.18 ~ 0.25 mm (60 ~ 80 mesh)인 흡착제를 사용하였다, 각각의 흡착제는 충진 후 비활성기체를 채워주며, 300 ℃ 정도의 온도에서 4시간 정도 가열하여 세척한 후 사용하였다. 넓은 범위의 휘발성유기화합물을 효율적으로 포집할 수 있는 3단 흡착트랩(Carbotrap, Carbopack B, Carbosieve S III)을 사용하였다.
흡착제를 충진하는 용기의 경우 유리튜브는 충진물의 충진상태를 확인 가능하므로 흡착제의 충진상태에 대한 성능 파악이 용이하여 유리튜브를 사용하였다.
휘발성유기화합물질분석의 경우 2단 열탈착시스템 및 가스크로마토그래피/질량분석기(Gas chromatography/mass spectrometry)를 이용하여 분석을 수행하였다. 열탈착시스템 및 가스크로마토그래피/질량분석기의 분석조건을 Table 1에 나타내었다.

The condition of low concentration systems and gas chromatography / mass spectrometry of VOCs
2.2.2. 아세트 알데히드
알데하이드류의 시료 채취는 Dinitrophenylhydrazine (DNPH) 카트리지를 이용한 유도체화 포집 방법을 사용하였다. 현장에서 DNPH카트리지로 채취할 때에는 시료공기를 유속 약 1 L min−1으로 5분 동안 총 5 L의 시료를 채취하였다.
시료채취 시 시료 중 오존에 의한 방해를 제거하기 위해 폴리프로필렌 튜브에 요오드화칼륨 결정을 채운 오존 세정기를 연결하여 시료를 채취하였다.
채취된 시료는 알루미늄호일로 포장하여 외부공기와 차단할 수 있는 비닐봉지에 이중으로 밀봉하여 저온, 차광, 밀봉상태로 보관(10 ℃ 이하)하여 운반하였으며, 용매로 추출하기 전까지 냉장(4 ℃ 이하) 보관하였다.
DNPH 카트리지에 포집된 시료를 아세토나이트릴을 이용하여 용출한 뒤 가스크로마토그래피/질량분석기를 이용하여 분석을 수행하였다. 분석조건은 Table 2에 정리하여 나타내었다.

The condition of low concentration systems and gas chromatography / mass spectrometry of acetaldehyde
추출에 사용하는 모든 유리기구는 아세토나이트릴로 세척한 후 60 ℃ 이상에서 건조한 후 사용하였고, 스탠드에 10 mL 주사기(Luer type)를 고정시켰다. 이후 눈금이 매겨진 시험관를 바닥에 고정시킨 후 주사기에 채취된 DNPH 카트리지를 끼우고 분사기(10 mL용량)를 이용해 주사기에 아세토나이트릴을 4.5 mL를 주입하였다. 주입한 아세토나이트릴 용매로 약 1 분 동안 DNPH 유도체를 추출하였다. 추출된 용액에 아세토나이트릴을 이용하여 정확히 5 mL로 표선하였다. 최종적으로 갈색시험관 용출액에서 1 mL를 피펫을 이용해 갈색주사용 유리병에 옮겨 분석용 시료로 하였다.
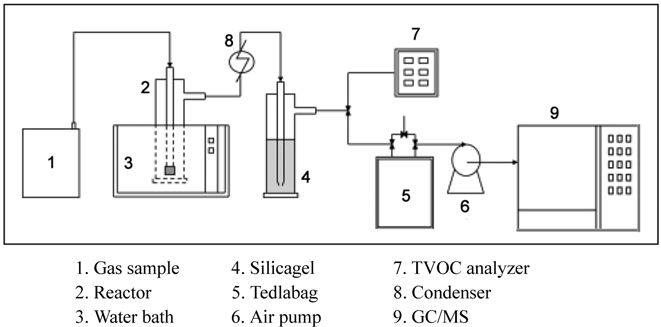
본 실험에서 사용한 선별 실험 장치는 Figure 1과 같이 구성되어 있으며 성능이 우수한 식물정유를 선별하기 위해 라벤더, 레몬그라스, 소나무, 편백나무, 시나몬, 전나무를 후보물질로 선정하였다. 후보로 선정된 식물정유는 각각 0.5 vol% 농도로 제조한 후 용매를 이용하여 10배 희석하여 사용하였다. 정유를 20 mL씩 200 mL 흡수병에 주입한 후 항온조 내에서 약 30분간 방치하였고, 휘발성유기화합물질을 테드라백에 일정한 농도로 주입 후 흡수병 전단에 연결하였다. 흡수병 후단에 연결된 감압장치를 통해 전단의 테드라백의 압력을 강하시키게 되면 휘발성유기화합물질이 흡수병으로 유입되어 식물정유와 반응하고, 실리카겔과 응축기를 통과한 이후 휘발성유기화합물질은 감압장치 전단에 연결된 테드라백에 포집되도록 하였다. 휘발성유기화합물질의 제거 효율 및 경향을 파악하기 위해 TVOC(총휘발성유기화합물; Total Volatile Organic Compounds) 분석기(2020 COMBO Photoionization Air Moniter, INFICON)를 이용하여 실시간으로 분석하였으며, 휘발성유기화합물질의 개별농도를 파악하기 위해 테드라백에 포집된 시료를 GC/MS를 이용하여 분석하였다. 반응 전 · 후의 농도를 비교함으로써 각각 식물정유에 대한 악취 탈취효율을 산정하였다. 첨가제 선별 실험은 제올라이트, V2O5, TiO2, ZnO를 후보로 하여 0.1% 탈취제 제조후 위와 동일한 조건으로 실험을 진행하였다. 실험은 총 3회 반복 실험하였으며 평균값을 적용하였다.
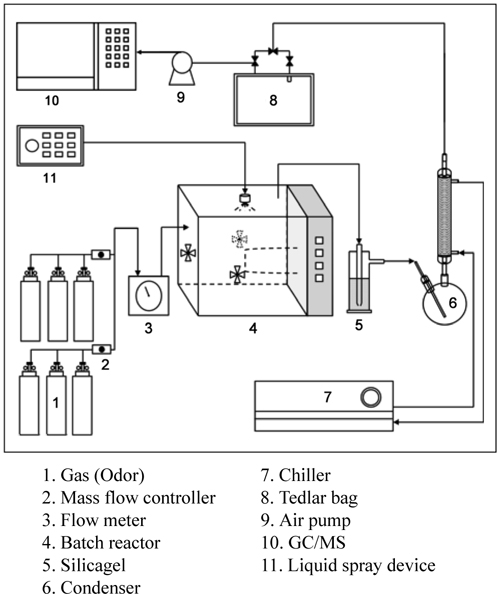
본 실험은 반응 시간, 분사량, 탈취제 희석배수, 온도 변화에 따른 탈취 효율을 분석하기 위한 실험으로 Figure 2에 회분식 반응조를 나타냈다. 반응조의 규격은 400 mm (L) × 250 mm (W) × 250 mm (H), 두께는 10 mm의 아크릴 소재를 사용하여 제작하였다. 반응조 내에는 순환팬이 설치되어 있으며, 열선을 이용하여 온도 조절을 하였다. 대상 가스의 경우 질량 유량조절계(Brookfield 5850, USA)를 이용하여 휘발성유기화합물질과 질소의 유량을 조절하였으며, 일정한 양의 흡수제를 분사하기 위해 액체 자동 노즐 분사기(GK, Korea)를 반응조 상단에 설치하였다. 반응 후 가스 시료를 포집하기 위해 반응조 후단에 실리카겔과 응축기를 설치하였다. 포집된 시료는 TVOC 분석기를 이용하여 실시간으로 농도를 측정하였으며, 개별 물질 농도를 파악하기 위해 흡입펌프를 이용하여 테드라백에 시료를 포집하여 GC/MS를 이용하여 분석하였다.
자동차 도장공정내 악취 원인물질을 파악하기 위하여 A회사 자동차 도장 도장공정내 발생하는 가스를 배출구에서 포집하여 GC/MS로 농도분석을 실시하였다. 이때, 샘플 가스의 경우 도장공정 내 상도와 중도로 구분하여 포집하였다.
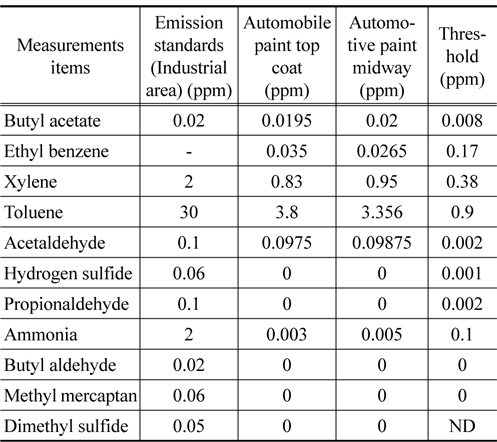
Table 3은 도장공정 내 악취물질 측정 결과로, 뷰틸 아세테이트의 경우 상도와 중도에서의 농도가 0.020 ppm로 나타났다. 이는 뷰틸 아세테이트의 최소감지농도인 0.008 ppm보다 높으므로 악취 원인물질로 작용하는 것으로 판단되었다. 에틸벤젠의 경우 정해진 배출허용기준은 없지만 상도, 중도 모두 최소감지농도보다 높은 것으로 나타났다. 자일렌과 톨루엔, 아세트알데히드 농도의 경우 배출허용기준보다 낮았으나, 최소감지농도보다 높아 악취 원인물질로 작용할 것으로 판단하였다. 이외에 암모니아 물질도 기기분석 결과 0.003 ppm, 0.005 ppm로 나타났지만 최소감지농도인 0.1 ppm보다 낮아서 악취원인물질로 분류하지 않았다. 전반적으로 상도, 중도에서 비슷한 결과를 나타내고 있었으며, 이를 바탕으로 도장공정내 악취원인물질로 아세트알데히드, 뷰틸 아세테이트, 자일렌, 톨루엔, 에틸벤젠 5가지 항목을 선정하였다.
[Table 3.] The values of odor concentration of each VOC in the car paint booth
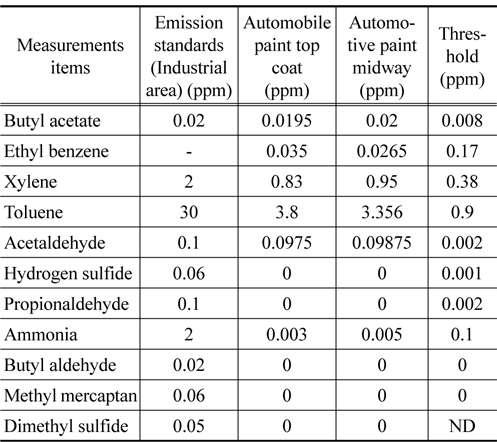
The values of odor concentration of each VOC in the car paint booth
3.2.1. 식물 정유 물질 선정
본 실험에서는 기존 문헌을 바탕으로 6가지의 0.5 vol%의 식물정유(라벤더, 레몬그라스, 편백나무, 전나무, 시나몬, 소나무) 탈취제를 제조한 후 이를 용매로 10배 희석하였다[13-18]. 이후 아세트알데히드, 휘발성유기화합물질 가스를 대상으로 제거 효율을 파악함으로써 최적 탈취제 제조를 위한 식물정유를 선별하였다.
Table 4에서 볼 수 있듯이 뷰틸 아세테이트의 경우 모든 식물정유에 대해서 90%이상의 높은 효율을 보였고, 그 중 라벤더에 대한 제거 효율이 가장 높았다. 톨루엔에 대한 제거 효율은 라벤더, 편백나무 정유 분사 시 99.48%, 95.47%로 높은 효율을 나타냈다. 에틸벤젠의 경우에는 편백나무 정유가 99.04%로 탈취 효율이 가장 높은 것으로 나타났다. 모든 단일 식물정유의 경우 자일렌에 대한 효율이 90% 이상으로 높았으며, 라벤더 정유의 경우 99.96%로 제거 효율이 가장 높은 것으로 나타났다. 아세트알데히드의 경우 60 ~ 75%의 효율로 다른 휘발성유기화합물질에 비해 제거 효율이 다소 낮았다.
[Table 4.] Concentration and removal efficiency of VOCs depending on essential oils
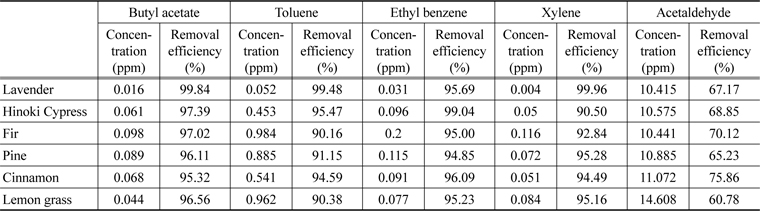
Concentration and removal efficiency of VOCs depending on essential oils
Figure 3은 Table 4의 결과값을 이용하여 각각의 단일 물질들의 악취 물질에 대한 효율을 비교하여 나타낸 것으로, 라벤더 정유와 편백나무 정유가 모든 VOCs에 대해 높은 제거 효율을 나타냈다. 다음으로 악취 효과가 큰 식물정유물질은 시나몬 정유, 소나무 정유, 전나무 정유인 것으로 나타났다. 이에 반해 레몬그라스 정유의 경우 제거 효율이 다소 떨어지는 것을 확인할 수 있었다. 이러한 분석 결과를 바탕으로 혼합탈취제 제조 시 탈취제의 제거 효율과, 종류를 고려하여 혼합할 항목을 선정하였다.
3.2.2. 첨가제 선정
식물정유 선별실험을 통해 상대적으로 낮은 아세트알데히드의 제거효율을 증가시키기 위해 증류수에 각각의 첨가제(제올라이트, V2O5, TiO2, ZnO)를 혼합하여 선별실험을 수행하였다.
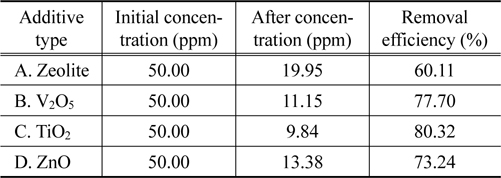
Table 5에서 나타난 바와 같이 휘발성유기화합물질 제거효율은 제올라이트 60.11%, V2O5 77.70%, TiO2 80.32%, ZnO 73.24%로 나타났으며, 이를 통해 TiO2가 첨가제로서 휘발성유기화합물질 제거 효율이 가장 높은 것으로 분석되었다.
[Table 5.] VOCs removal efficiency according to the additive type
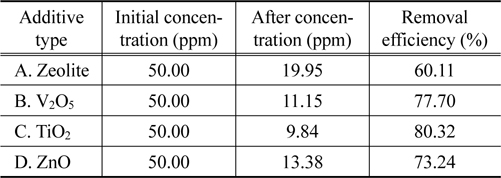
VOCs removal efficiency according to the additive type
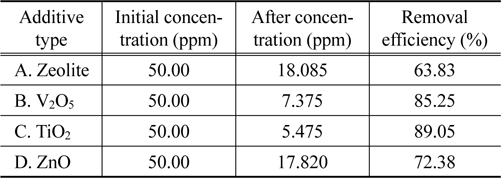
Table 6은 식물정유를 이용한 탈취 실험 시 효율이 낮았던 아세트알데히드를 단일 물질로 하여 첨가제 선별실험을 수행한 결과이다. 제올라이트 63.83%, V2O5 85.25%, TiO2 89.05%, 그리고 ZnO의 경우 72.38%의 제거효율을 나타냈다. 이를 통해 휘발성유기화합물질 실험과 동일하게 TiO2의 알데히드 제거 효율이 가장 높았으며, 이는 TiO2의 광촉매 역할로 인한 OH 라디칼 발생 및 산화작용에 의한 영향인 것으로 판단된다. 최종적으로 식물정유의 탈취 효율을 증진시키기 위한 최적의 첨가제는 TiO2로 결정하였다.
[Table 6.] Acetaldehyde removal efficiency according to the additive type
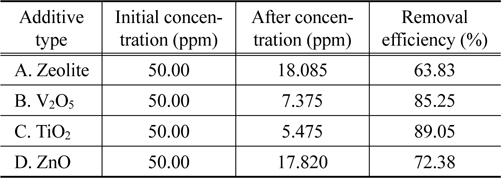
Acetaldehyde removal efficiency according to the additive type
3.2.3. 최적 혼합 비율
탈취제 혼합비율의 경우 3.2.1절과 3.2.2절의 선별실험을 통해 결정하였다. 동일한 조건 하에서 휘발성유기화합물질과 반응하여 높은 효율로 탈취작용을 하는 성분을 선정하고 동일한 양으로 혼합 비율을 결정하여 탈취제를 제조하였다. 에틸벤젠에서 가장 높은 효율을 보이는 편백나무 정유와, 뷰틸 아세테이트와 자일렌, 톨루엔에서 가장 높은 효율을 나타내는 라벤더 정유를 선정하였다. 또한 금속산화물의 선별 실험을 통해 휘발성유기화합물질, 아세트알데히드 두 실험 모두에서 가장 높은 효율을 나타낸 TiO2를 탈취제의 첨가제로 선정하였다. 최종적으로 라벤더 정유 45%, 편백나무 정유 45%, 첨가제 TiO2 10%의 비율로 하여 0.5 vol% 혼합 탈취제를 제조하였다.
3.3.1. 희석배수
식물정유물질의 경우 고유의 향을 가지고 있기 때문에 농도가 높을 경우 인체에 또 다른 악취로 작용할 수 있으므로, 이를 고려하여 희석배수 범위를 결정해야 한다. 따라서 본 절에서는 인체가 감지하기 어려운 수준인 100배 이상으로 탈취제를 희석함으로써 최적 희석배수 조건을 찾고자 하였다.
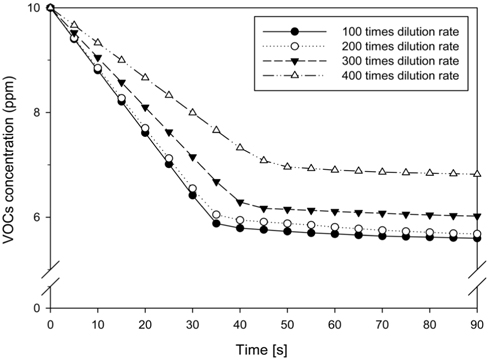
Figure 4는 온도 20 ℃에서 탈취제 희석배수(100, 200, 300, 400배) 및 반응시간에 따른 휘발성유기화합물질 농도를 나타낸 것이다. 휘발성유기화합물질 초기 농도는 10 ppm이며, 반응가스 25 L에 대한 탈취제 분사량은 2 mL로 고정하였다.
100, 200, 300, 400배 희석배수별 VOC 제거 효율은 각각 44%, 43.2%, 39.8%, 31.8%로 나타나, 희석배수가 낮을수록 제거효율이 높은 것을 알 수 있었다. 이는 희석배수가 낮아질수록 탈취제의 농도가 증가하게 되고, 식물정유물질 내의 모노테르핀(monoterpene)의 작용기들과 휘발성유기화합물질이 반응하여 새로운 화합물과 양이온으로 전환됨으로써 무취반응이 일어나기 때문인 것으로 판단된다.
반면 200배 희석배수를 가지는 탈취제의 경우 100배 희석한 탈취제와의 효율 차이는 미미하였으며, 경제적인 측면을 고려하여 최적의 희석배수를 200배로 선정하였다.
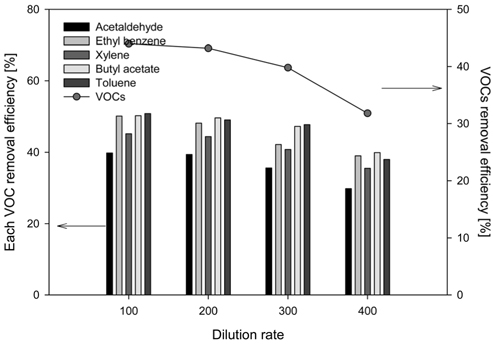
이와 함께 탈취제 희석배수에 따른 개별 휘발성유기화합물질 물질에 대한 제거 효율을 파악하였다. Figure 5에서와 같이 희석배수별 아세트알데히드, 에틸벤젠, 자일렌, 뷰틸 아세테이트, 톨루엔의 제거 효율을 측정한 결과 희석배수 200배를 기준으로 아세트알데히드 39.4%, 에틸벤젠 48.1%의 제거효율을 나타냈다. 또한 자일렌은 44.4%, 뷰틸 아세테이트 49.6%, 톨루엔의 경우 49%의 제거 효율을 나타냈다. 위의 실험 결과와 같이 모든 희석배수 조건에서 제거효율은 뷰틸아세테이트가 가장 높았으며, 톨루엔, 에틸벤젠, 자일렌, 아세트알데히드 순으로 나타났다. 이와 같이 아세트알데히드를 포함한 휘발성유기화합물질 물질의 경우 중성성분의 악취로써, 산화 및 중화 반응이 일어나기 어려움으로 인해 제거효율이 낮게 나타나는 것으로 사료된다[25].
3.3.2. 분사량
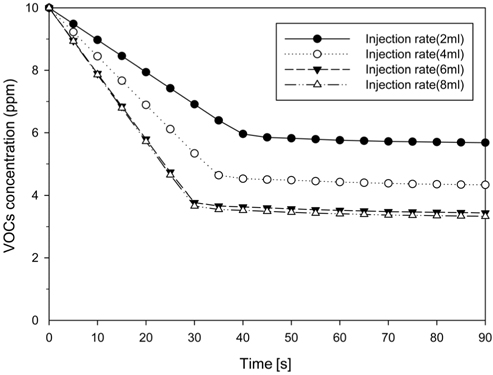
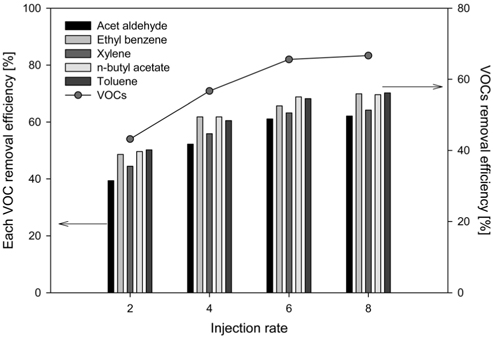
탈취제 분사량은 악취가스 제거 효율을 결정하는 중요한 요소 중 하나로서, 분사량에 휘발성유기화합물질 제거 영향을 알아보기 위한 실험을 수행하였다. 분사 유량은 반응조 25 L를 기준으로 탈취제를 2 ~ 8 mL를 분사하였고, 시간에 따른 휘발성유기화합물질 농도를 측정한 결과를 Figure 6에 나타냈다. 휘발성유기화합물질의 경우 분사량이 증가함에 따라 제거효율이 40%에서 66.7%까지 증가하였다. 이때 8 mL를 분사하였을 경우 가장 높은 제거효율(66.7%)을 나타냈으나 6 mL 분사량 실험 결과와의 효율 차이가 미미한 것으로 나타났다.
Figure 7은 휘발성유기화합물질 제거 효율 및 개별물질에 대한 실험 결과로 단위 시간당 분사 유량이 증가할수록 휘발성유기화합물질 제거 효율이 높은 것으로 나타났다. 이는 식물정유 속 terpene이 휘발성이 강하고 체류시간이 짧으며 반응성이 매우 높아 휘발성유기화합물질과 중화 반응이 매우 빠르게 일어나기 때문인 것으로 판단된다. 분사 유량이 높을수록 기체와 액체 계면에서 더욱 많은 양의 악취 물질이 탈취제와 반응하여 무취 물질로 바뀌는 것으로 판단된다. 또한 휘발성유기화합물질 제거 실험 결과와 동일하게 8 mL를 분사하였을 때 가장 높은 제거 효율을 보였으나 6 mL 분사량과의 차이가 매우 미미하여 최적 탈취제 분사량을 6 mL로 결정하였다. 최적조건에서 물질별 제거 효율을 분석한 결과 아세트알데히드의 경우 61.1%, 에틸벤젠 65.7%, 자일렌 63.2%, 톨루엔 68.2%, 뷰틸 아세테이트의 경우 68.8%의 제거 효율을 보였다. 이때 제거효율은 뷰틸 아세테이트, 톨루엔, 에틸벤젠, 자일렌, 아세트알데히드 순으로 높은 것으로 나타났다. 이 중 아세트알데히드의 제거효율이 다른 휘발성유기화합물질에 비해 낮게 나타났으며, 이는 산화 제거 시 아세트알데히드의 경우 다른 휘발성유기화합물질 물질에 비해 효율이 떨어진다는 기존 연구의 결과와 일치하는 것으로 나타났다[26].
3.3.3. 온도
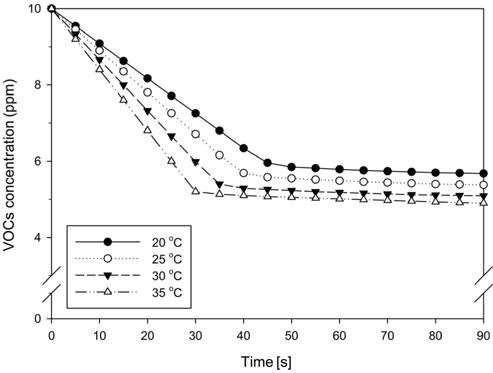
탈취제 분사 시 반응 온도에 따른 휘발성유기화합물질 제거영향을 파악하기 위해 선정된 혼합 탈취제를 이용하여 휘발성유기화합물질 및 개별 휘발성유기화합물질에 대해 온도에 따른 제거 영향을 살펴보았다. 온도는 20 ℃, 25 ℃, 30 ℃, 35 ℃ 변화시켰으며, 분사유량과 희석배수는 2 mL, 200배로 고정하였다. Figure 8에서 볼 수 있듯이 휘발성유기화합물질의 제거효율은 온도가 증가함에 따라 높아져, 20, 25, 30, 35 ℃에서 각각 43.2, 46.2, 49.1, 51.0%를 나타났다.
Figure 9는 개별 휘발성유기화합물질물질에 대한 제거 효율로써, 휘발성유기화합물질과 동일하게 온도가 증가함에 따라 제거 효율이 증가하였으며, 35 ℃의 반응 온도에서 아세트알데히드, 에틸벤젠, 자일렌, 톨루엔, 뷰틸 아세테이트의 제거효율은 각각 48.0, 55.7, 53.2, 58.0, 56.3%로 나타났다. 이는 반응온도가 증가함에 따라 분자의 확산, 충돌이 증가하고 이로 인해 반응속도가 증가하여 제거효율이 높게 나타나는 것으로 사료된다. 따라서 온도가 높은 여름철에 탈취제의 휘발성유기화합물질 제거 효과가 더욱 뛰어날 것으로 판단된다.
3.3.4. 반응속도
본 연구에서 개발한 탈취제의 성능을 정량적으로 평가하기 위해 반응속도 및 활성화 에너지를 산정하고 기존 문헌과 비교하고자 하였다. 이를 위해 시간에 따른 반응기 내 농도 변화를 이용하여 악취가스의 반응 속도 상수를 계산하였다. 시간에 따라 반응속도식을 나타내면 1차 반응식은 다음과 같이 나타난다.
여기서 r은 탈취제와 악취가스의 반응속도이며, C는 반응이 완료되어 더 이상 반응이 이루어지지 않는 지점의 악취농도이며, C0은 반응전 농도이며, t는 탈취제와 악취가스의 반응시간을 의미한다.
비반응속도상수 kA의 온도 의존성은 아레니우스에 의해 Equation (2)로 표현되며 자연로그를 취하면 Equation (3)과 같이 표현된다[23,24].
여기서 A는 전지수인자 또는 빈도인자를 나타내고, E는 활성화에너지, 단위는 J mol−1 또는 cal mol−1을 사용하며, R은 기체상수로 8.314 J mol−1 K−1 또는 1.987 cal mol−1 K−1로 나타낼 수 있고, T는 절대온도를 나타내며, 단위는 K를 사용한다.
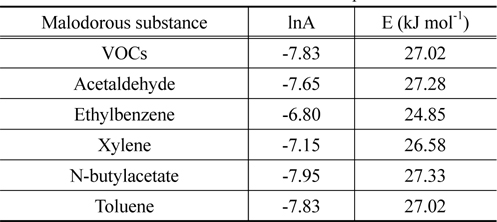
본 연구에서 개발한 탈취제와 휘발성유기화합물질 복합가스 및 단일가스에 대한 반응속도를 파악하기 위해 3.3.3절에서 수행한 실험을 토대로 반응속도상수 및 활성화 에너지를 산정하여 Table 7에 나타냈다.
[Table 7.] Reaction rate constants of Arrhenius plot
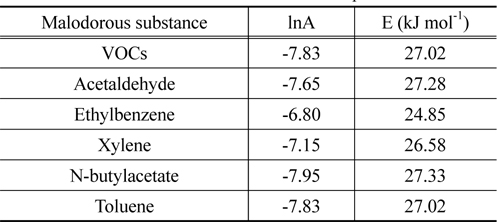
Reaction rate constants of Arrhenius plot
탈취제와 악취가스와의 반응은 Equation (3)과 같이 가역유사 1차 반응으로 결정되었고, 반응속도상수는 반응온도가 높아짐에 따라 증가하는 경향을 나타내었다.
Equation (3)에 비반응 속도 상수를 대입하여 반응식 도출 및 활성화 에너지 값을 구하였고 24 ~ 27 kJ mol−1로 나타났다.
기존 문헌에 따르면 단일 촉매인 망간산화물 촉매를 이용한 아세트알데히드 제거 시 활성화에너지가 72.42 ~ 99.52 kJ mol−1였으며[23], 광촉매 흡착기술을 이용한 포름알데히드 제거 시 활성화 에너지가 107 kJ mol−1로 조사되었다[24]. 본 연구에서 제조한 혼합탈취제의 경우 20 ~ 30 kJ mol−1로 기존 탈취제와 비교하여 활성화 에너지가 낮으므로 휘발성유기화합물질과의 반응이 상대적으로 빠르게 일어나는 것으로 판단된다.
1) 산업시설의 주요 악취 원인물질인 휘발성유기화합물질을 제거하기 위해 탈취제 최적 제조 조건을 파악한 결과, 휘발성유기화합물질 제거효율이 높은 라벤더 정유, 편백나무 정유를 탈취제 성분으로 선정하였다. 또한 첨가제의 경우 아세트알데히드에 대한 제거 성능을 개선할 수 있을 것으로 판단되는 TiO2를 첨가제로 선정하였다. 혼합 비율은 기존 문헌을 참고하여 라벤더 45%, 편백나무 45%, TiO2를 10%로 결정하였으며, 탈취제 농도는 증류수와 알콜을 1:1로 혼합한 용매를 이용하여 0.5 vol%로 제조하였다.
2) 휘발성유기화합물질 제거를 위한 최적 조건실험을 수행한 결과 희석배수가 낮을수록, 탈취제 분사량이 높을수록 제거 효율이 증가하였다. 그러나 실험 조건에 따른 제거 효율의 증가폭과 경제성을 고려한 결과 탈취제의 최적 희석배수는 200배, 분사량은 가스 25 L당 6 mL로 결정되었다. 반응온도의 경우 높을수록 휘발성유기화합물질 제거 효율이 증가하였으며, 온도가 높은 여름철 탈취제의 휘발성유기화합물질 제거효과가 더욱 뛰어날 것으로 판단된다.
3) 혼합 탈취제를 대상으로 변수에 따른 휘발성유기화합물질 제거 실험을 수행하여 반응속도 상수를 계산하였고, Arrhenius plot을 이용하여 반응속도식을 도출하였다. 이와 함께 휘발성유기화합물질의 반응속도 식으로부터 활성화 에너지를 산정한 결과 27.02 kJ mol−1로 나타났다. 본 연구에서 개발한 탈취제의 경우 기존 문헌에서 제시하고 있는 탈취제보다 높은 반응속도를 나타내고 있으며, 이는 기존 탈취제와 악취물질 사이의 활성화에너지보다 3~4배 가량 낮은 활성화에너지에 기인하는 것으로 판단된다.