스트레스란 다양한 자극에 대하여 나타나는 체내의 비특이적 반응이다(Selye, 1973). 어류는 상처와 포식활동, 질병, 오염물질과 같은 다양한 스트레스 요인에 노출되어 있으며, 과거부터 스트레스가 어류에 미치는 영향에 대한 많은 연구가 보고되었다(Barton and Iwama, 1991; Gamperl et al., 1994; Reid et al., 1998; Tort, 2011). 스트레스가 중추신경계에 전달되면 부신 피질자극호르몬 방출호르몬(corticotrophin-releasing hormone, CRH)이 뇌하수체에서 부신 피질자극호르몬(adrenocorticotropic hormone, ACTH)을 분비시키고, ACTH는 간신세포에서 글루코코르티코이드(glucocorticoid)의 방출을 촉진시킨다. 글루코코르티코이드는 지질성분으로 세포 막을 자유롭게 통과하다 글루코코르티코이드 수용체(glucocorticoid receptor)와 결합함으로써 음성 또는 양성 조절되며 스트레스에 대항하여 생체의 항상성을 유지하는데 중요한 역할을 한다(Mommsen et al., 1999). 에너지원인 혈당량을 증가시키고, 면역체계에서는 염증 관련 유전자의 전사를 억제하며 그 결과 염증부위로의 백혈구 이동, 사이토카인 유전자 및 고착분자의 발현이 억제되어 항 염증 작용을 나타낸다(Cato and Wade, 1996; De Bosscher et al., 2000). 그뿐만 아니라 염류세포와 Na+, K+-ATPase 활성에 관여해 이온과 삼투압을 조절하며, 성장과 번식을 억제하는 등 다양한 생리적 기능을 수행한다(Mommsen et al., 1999).
글루코코르티코이드 작용을 매개하는 글루코코르티코이드 수용체는 안드로겐 수용체, 에스트로겐 수용체, 프로게스테론 수용체와 같은 핵 호르몬 수용체의 한 종류로 N-terminal trans-activation domain (NTD), DNA binding-domain (DBD), C-terminal ligand binding domain (LBD)의 공통적인 도메인들을 가지고 있으며, 다음 과정을 통해서 전사 조절을 한다. 글루코코르티코이드와 결합하지 않은 경우 heat shock protein 90 (hsp90), hsp70, hsp50과 같은 샤페론 단백질과 결합하여 세포질에 존재하다가, 글루코코르티코이드와 결합하면 GR/hsp 복합체가 분리되어 글루코코르티코이드 수용체가 핵 안으로 이동하고, 핵 안으로 들어간 글루코코르티코이드 수용체는 glucocorticoid-responsive elements (GREs)와 결합해서 목표 유전자의 전사를 조절한다(Lee and Park, 2008; Nicolaides, 2010).
글루코코르티코이드 수용체는 rainbow trout (
빅벨리해마(
해마의 양식에서 다양한 병원성 질병이 발생하나 아직까지 뚜렷한 대체방안이 마련되지 않았으며 해마의 스트레스 반응과 면역에 대한 연구가 부족하다. 따라서 본 연구에서는 다양한 스트레스 자극 중 면역 자극에 초점을 맞추어 빅벨리해마(
>
HaGR (Hippocampus abdominalis Glucocorticoid Receptor)의 특징분석
454 GS FLX sequencing technique (Roche 454 Life science, USA)을 사용하여 빅벨리해마 cDNA 시퀀스 데이터베이스를 구축하였다. HaGR의 cDNA와 아미노산 서열은 BLAST(http://www.ncbi.nlm.nih.gov/blast/)와 Expert Protein Analysis System (http://www.expasy.org/)를 이용하여 분석하였고, Simple Modular Architecture Research Tool (SMART)(http://smart.embl-heidelberg.de/)을 이용하여 Domain을 확인하였다. EMBOSS Needle (http://www.ebi.ac.uk/Tools/psa/emboss_needle/)로 pairwise sequence alignment를 수행하였으며, ClustalW2 (http://www.ebi.ac.uk/Tools/msa/clustalw2/)로 multiple sequence alignment를 하였다. 계통발생학적 분석은 MEGA 5.5의 neighbour-joinging (NJ) method으로 5,000번의 bootstrap 반복하여 계통수를 그렸다.
제주도 제주시 제주 관상어 종묘센터(CCORA, http://www.ccora.com/) 에서 빅벨리해마를 구입하여 1주일간 32±1 psu, 18±2℃에서 순치시킨 후 실험에 사용하였다.
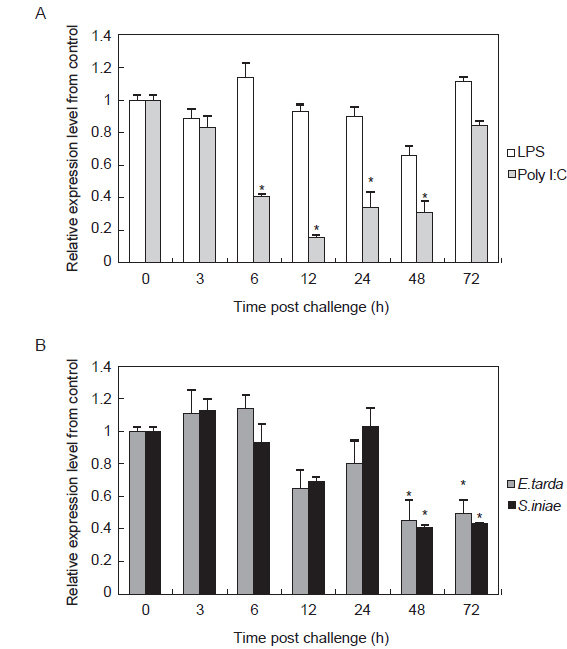
어류에 면역 스트레스를 주기위해 대조구(phosphate buffered saline), LPS (1.25 μg/μL), Poly I:C (1.5 μg/μL),
다양한 조직에서의 HaGR의 발현분포를 확인하고자 건강한 해마의 꼬리를 절단하여 채혈한 뒤 원심 분리(4℃, 3,000
HaGR의 발현양상은 Real Time System TP800 Thermal Cycler DiceTM (TaKaRa)를 이용하여 quantitative real-time PCR (qPCR)로 분석하였다. 빅벨리해마의 ribosomal protein S7 (Accession no. KP780177)을 reference gene으로 활용하였고 forward (5’-GCGGGAAGCATGTGGTCTTCATT-3’)와 reverse (5’-ACTCCTGGGTCGCTTCTGCTTATT-3’)의 oligonucleotide primer로 증폭하였다. HaGR의 cDNA 단편을 증폭하기 위해 사용된 oligonucleotide primer는 HaGR-F (5’-TATGGCGAGTCCACCACGATTCA-3’)와 HaGR-R (5’- GCTTCGTCCGAACACACCAAACA-3’)이다. 각 조직으로부터 합성된 cDNA는 qPCR을 수행하기 위한 주형으로 사용하였으며, qPCR은 SYBR Premix Ex Taq 2X (TaKaRa)을 사용하여 95℃에서 30초간 1 cycle, 95℃에서 5초, 58℃에서 10초, 72℃에서 20초를 45 cycle, 95℃에서 15초, 60℃에서 30초, 95℃에서 15초간 1 cycle 반응하였고, 각 반응은 3번 반복 수행하였다.
각 실험구와 대조구 사이는 SPSS Version 18 program (IBM, America)을 이용하여 one-way ANOVA를 실시한 후 Duncan’s multiple range test로
어류는 스트레스에 저항하여 다양한 반응을 보이는데 그 중 하나가 글루코코르티코이드의 방출이며(Chrousos, 1998; Barton, 2002), 이것이 수용체와 결합하여 중간 대사, 이온과 삼투압 조절, 면역 기능에 직·간접적으로 영향을 준다(McCORMICK, 1995; Bonga, 1997).
본 연구에서는 HaGR cDNA (Accession no. KJ756323)를 동정하였고, 특징과 발현 분석을 수행하였다. HaGR은 782개의 아미노산을 암호화하는 2,346 bp의 open reading frame (ORF)로 구성되었으며, 아미노산의 분자량은 86.8 kDa, 등전점은 6.26으로 추정되었다. 글루코코르티코이드 수용체의 도메인구조에서 NTD는 transactivation domain인 activation function-1 (AF-1)을 가지고 있고 리간드와 독립적으로 활성화된다. DBD는 핵 호르몬 수용체에서 가장 보존된 부위로 4개의 cysteine cysteine 잔기에 둘러싸여 아연과 반응하는 2개의 zinc finger가 존재하며 GREs 라 불리는 특정 DNA의 시퀀스에 부착한다. DBD와 LBD 사이에는 hinge 부위가 존재하는데 이는 구조적 유동성을 가지고 있어 하나의 수용체가 다양한 GREs와 결합하도록 하고, LBD는 가장 큰 도메인으로 AF-2를 포함하며 리간드 인식, 수용체의 이합체, 핵으로 전좌 등의 기능을 담당한다(Nicolaides et al., 2010). HaGR cDNA와 아미노산 시퀀스 분석결과, DNA-binding 특이성을 나타내는 AGGTCA motif가 확인되었고, 416-496번 아미노산은 핵 호르몬 수용체에 존재하는 C4 zinc finger이며, 570-734번 아미노산은 LBD였다(Fig. 1).
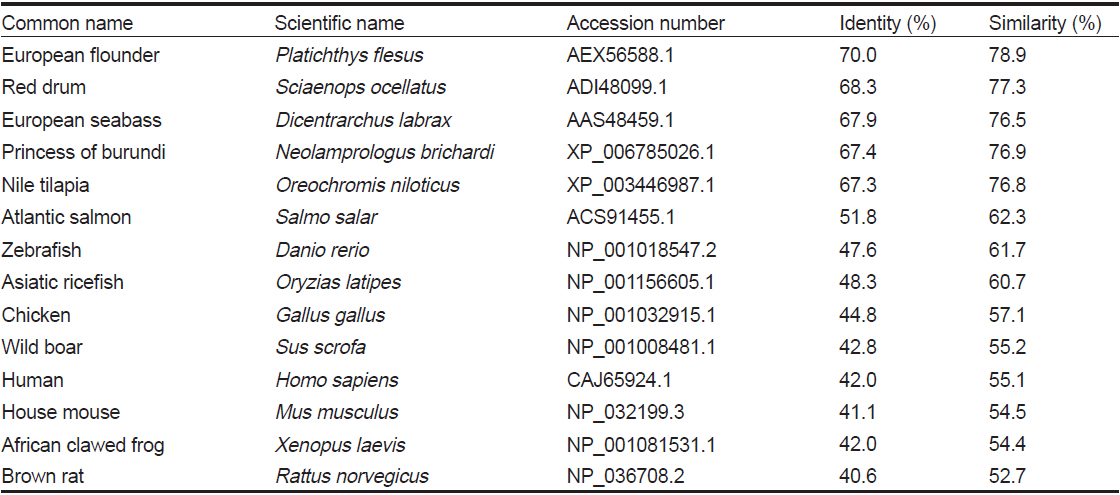
HaGR 아미노산을 다른 어종의 GR과 비교 분석(pairwise alignment)하였을 때, 동일성과 유사성은 European flounder에서 가장 높았으며, red drum과는 77.3%, princess of burundi와는 76.9%, Nile tilapia와는 76.8%, European seabass와는 76.5%의 유사성을 보였다(Table 1).
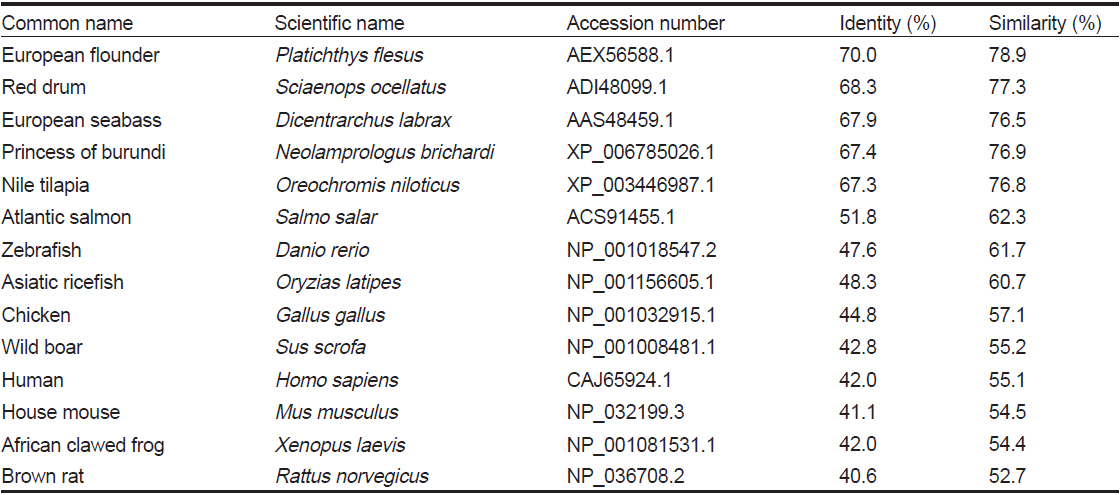
Percent identities and similarities of HaGR gene with glucocorticoid receptor genes from other species
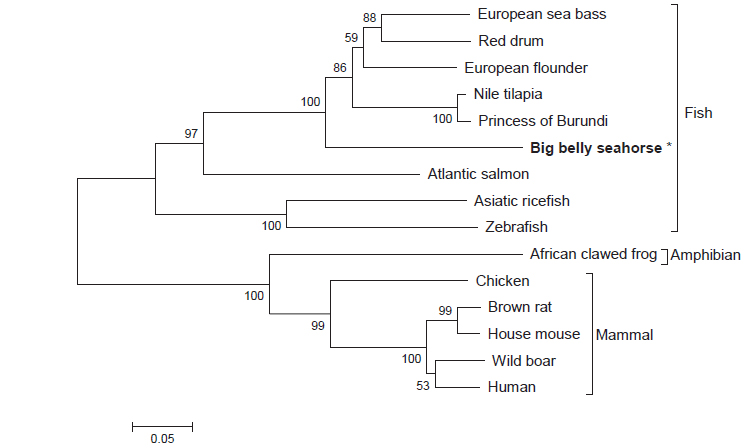
Multiple sequence alignment 결과 HaGR에서 하나의 C4 zinc finger domain에서 보존된 4개의 cysteine 잔기 C419, C422, C436, C439를 확인하였고, 다른 하나의 C4 zinc finger domain 에서도 4개의 cysteine 잔기 C464, C470, C480, C483을 확인할 수 있었다(Fig. 2). HaGR은 다양한 어류들과 계통발생학적으로 가까워 같은 cluster 안에 위치하고 양서류 및 포유류와는 계통발생학적으로 거리가 멀어 다른 cluster에 위치하였다(Fig. 3).
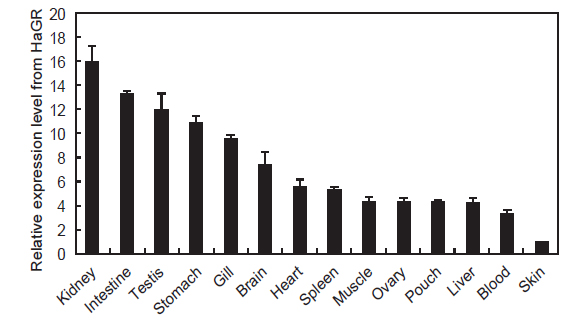
HaGR의 조직별 발현분석 결과를 Fig. 4에 나타내었다. 다른 어류의 글루코코르티코이드 수용체는 아가미, 신장, 비장, 뇌, 간을 포함한 다양한 조직에서 발현된다고 보고되었는데(Sandor et al., 1984; Lee et al, 1992; Vazzana et al., 2008), HaGR 역시 조직 별로 차이는 있었지만 모든 조직에서 광범위하게 발현되었다. 경골어류의 면역기관인 신장에서 HaGR의 발현이 가장 높았는데 이는 수용체와 결합한 글루코코르티코이드가 면역체계와 상호작용하여 다양한 면역을 조절하기 위함으로 생각된다(Weyts et al., 1998; Wang et al., 2005; Zapata et al., 2006; Castillo et al., 2009). 또한, 다른 조직에 비해 아가미와 장에서도 높은 발현을 보였다. 글루코코르티코이드는 아가미에서 Na+, K+-ATPase 활성을 높이고, 염류세포의 크기와 분화를 촉진하며 장에서는 이온 및 물의 흡수를 증가시키는 기능을 한다. 따라서, HaGR의 발현이 삼투압과 전해질 조절과 관련 있는 조직에서 높았음을 알 수 있다(Mommsen et al., 1999; Takahashi et al., 2006). 스트레스에 노출되었을때 글루코코르티코이드는 정소의 테스토스테론의 방출을 억제하여 번식 대신 다른 대사활동으로 우회시키는데, 이러한 기능을 수행하기위해서 정소에서 글루코코르티코이드 수용체의 발현이 높은것으로 보인다(Hu et al., 2008).
면역 자극에 따른 HaGR의 발현양상을 분석하고자 LPS, Poly I:C,
본 연구를 통해 HaGR을 분자학적 특성을 분석하였으며 건강한 빅벨리해마의 조직과 감염 후의 신장 조직에서의 HaGR의 발현양상을 확인함으로써 해마의 면역기전에 대한 이해를 도왔다. 추후 이 유전자의 면역, 삼투압과 전해질 조절과 같은 생리학적 기능을 이해하기 위한 연구가 필요할 것으로 사료된다.