불가사리는 수온 15-20℃의 범위에서 연안해역의 패류 양식장과 마을어장에 서식하는 피조개, 전복, 바지락, 가리비 등 유용 조개류를 무차별 포식함으로써 연안 패류자원을 감소시켜 양식 어업인에게 막대한 피해를 주어 심각한 문제를 야기하고 있다(Park et al., 1997). 특히 우리 나라 패류 양식어장에 피해를 주는 불가사리류는 아므르 불가사리(
그러나 이용 가공면에서 보면, 불가사리는 특정 무기질, 아미노산 및 신물질에 대한 연구를 통하여 기능성 식품소재로서의 가능성이 제시된다. 불가사리의 칼슘성분을 이용한 사료 또는 비료 첨가제(Lee et al., 1989) 활용연구, 산란 전 불가사리의 유문맹장과 생식선에 아미노산 함량 변화 및 높은 글리신 함량(Kishimura and Hayashi, 1990)에 관한 보고, 단백질분해효소를 이용하여 탄산칼슘을 제거한 불가사리 엑기스 농축액(Higashi et al., 1955) 무독성에 관한 연구 및 불가사리의 탄산칼슘과 콜라겐의 산업적 이용에 관한 보고(Park, 2003)를 통하여 불가사리의 식품소재로써의 영양학적 가치를 알 수 있다. 또한 극피동물에서 발견된 주된 신물질인 saponin계 물질에 관한 연구(Seo, 1997),
따라서 본 연구에서는 불가사리를 효율적으로 이용할 목적으로 연근해에 서식하는 별 불가사리와 아므르 불가사리를 대상으로 단백질 분해효소에 의한 가수분해 및 용매순차추출에 의한 각각의 용매 추출부를 분리하여 항균성, 항산화성 및 미백효과를 분석하였다. 본 연구의 결과는 극피동물에 대한 생리활성물질의 기초자료로 사용될 수 있으며 향후 불가사리로부터 고부가가치 제품 개발에 이용될 수 있을 것으로 기대한다.
별 불가사리(
>
용매추출 및 column chromatography에 의한 생리 활성물질의 분획
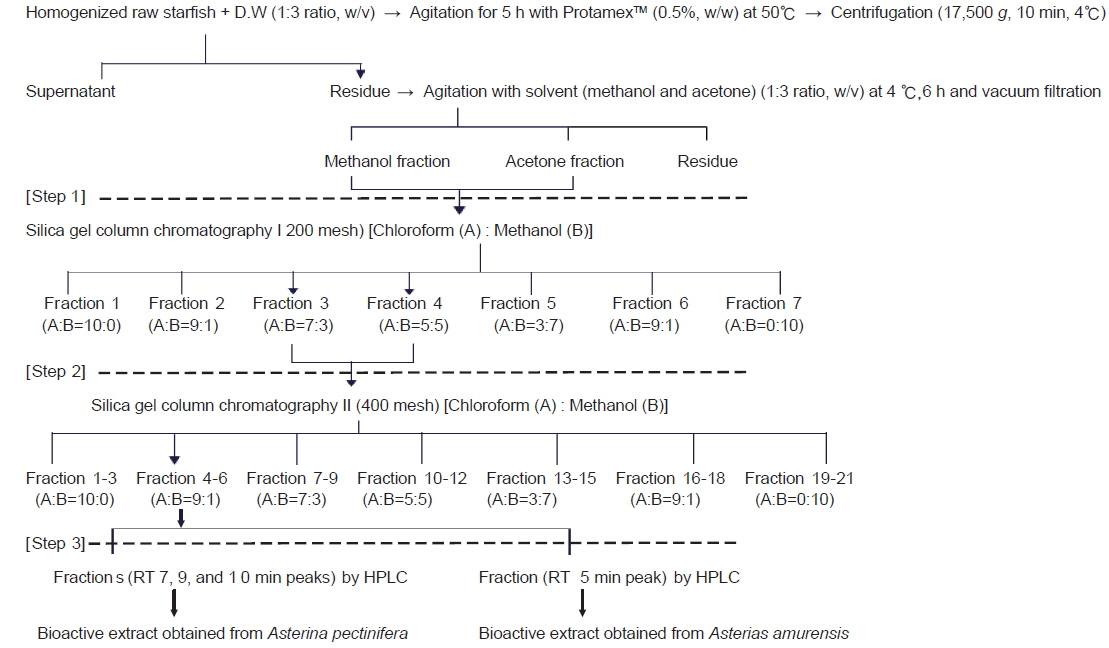
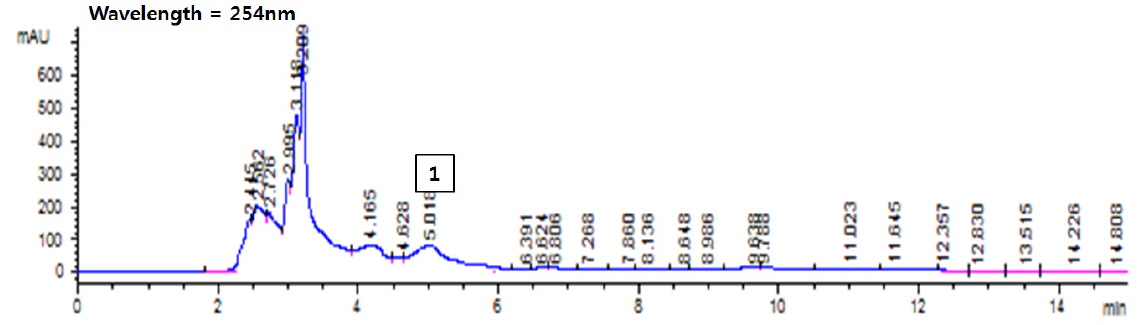
별 불가사리 및 아므르 불가사리로부터 생리활성물질을 가지는 물질의 추출은 Jung (2002)의 방법을 기초로 변형하여 Fig. 1과 같이 균질화된 생시료(5 kg)에 3배량의 증류수를 넣은 다음, 단백질 분해효소(ProtamexTM, Novo Nordisk Co., Denmark) 처리하여, 상등액을 제거하고 나서 용매순차추출에 의한 methanol과 acetone분획을 취하였다. 다음으로 200 mesh (I) 및 400 mesh (II) silica gel column chromatography (ø 10.0 mm×50 cm length)에서 chloroform : methanol 비율(v/v)에 따라 순차적으로 각각 7분획 및 21분획을 분취하여 이들 분획의 생리활성을 분석하였다. 그리고 활성이 우수한 분획을 취하여 모으고, 다시 HPLC (HP 1100 series, Hewlett-Packard Co., Palo Alto, CA, USA)를 이용하여 단일 피크의 활성이 우수한 분획을 분취하였다. HPLC로 분리·정제시 column은 C18 (HP Eclipse XDB, Hewlett-Packard Co, Palo Alto, CA, USA) (0.94 mm i.d, 25 cm length)을 사용하였으며, 검출기는 UV 254 nm, 이동상은 acetonitrile:methanol 용매계(80:20), 유속은 4 mL/min로 하였다.
실험균주로는 피부 백선균류,
항산화 효과 시험은 Blois (1958)의 방법에 준하여 DPPH(2,2-diphenyl-1-picrylhydrazyl, Aldrich Co., USA) radical 소거능을 측정하였다. 즉 조제한 DPPH 용액 0.8 mL에 에탄올 3-4 mL를 가하고 10초 동안 강하게 진탕하여 분광 광도계의 흡광도 값이 0.95-0.99가 되도록 에탄올의 양을 조정한 다음 시료 0.2 g을 취하여 앞에서 조절한 적정량의 에탄올과 DPPH용액 0.8 mL를 가하여 10초 동안 강하게 진탕한 후 10분 동안 방치하고 525 nm에서 흡광도를 측정하여, DPPH radical 소거능 (Electron donating ability, EDA%)을 구하였으며, 각 시료의 억제 강도는 free radical inhibition의 50% 억제 농도(EDA50)로 구하여 비교하였다. 그리고 미백효과는 Chen and Kubo (2002)의 방법을 변형한 tyrosinase 저해활성(inhibitory activity)을 측정하였다. 즉, 5% (w/v) 시료 0.1 mL, 0.1 M sodium phosphate buffer (pH 6.8) 1.8 mL, mushroom tyrosinase 0.1 mL (125 units) 및 2.5 mM L-DOPA 1 mL 등 총 4.5 mL의 반응액을 10초간 진탕 후 25℃ 에서 10분간 배양한 후 475 nm에서 측정하였다.
>
용매추출 및 column chromatography에 의한 분획물의 항균성 효능
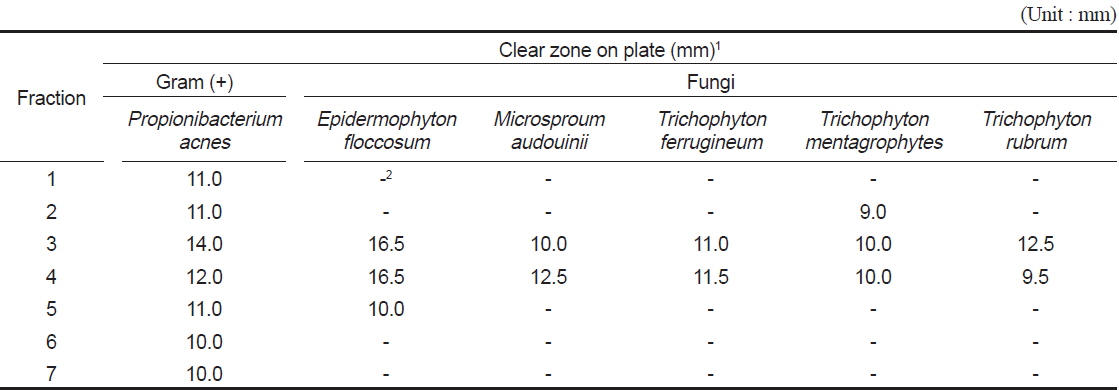
별 불가사리와 아므르 불가사리의 용매추출법(Fig. 1, Step 1)은 용매순차추출법에서 항균성, 항산화능 등과 같은 생리활성능이 우수한 분획으로 밝혀진(Jung, 2002) methanol 및 acetone추출물을 수거하여 본 실험에서 연속적 분획을 위한 원물로 하였다. Fig. 1 (Step 2)의 Silica gel column chromatography I (200 mesh)에서는 chloroform : methanol의 비율비에 따라 7개의 분획물을 얻었다. 피부백선균류 5종과 혐기성 여드름균 1종에 대해 별 불가사리로부터 얻어진 분획물(1,000 μg/disk)의 항균성을 측정한 결과는 Table 1과 같다. 3번 및 4번분획의 항균효과가 모든 균에서 효능이 나타났으며 다른 분획물에 비해 가장 높았다. 특히 3번 분획은 피부의 피지 안에서 증식하며 여드름의 대표적인 균(
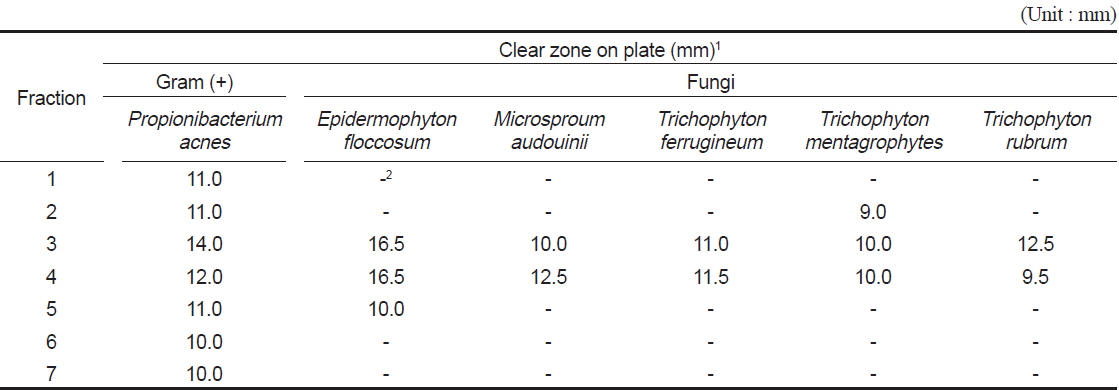
Antimicrobial activities of fractions obtained from methanol extract of Asterina pectinifera by silica gel column chromatography I (200 mesh)
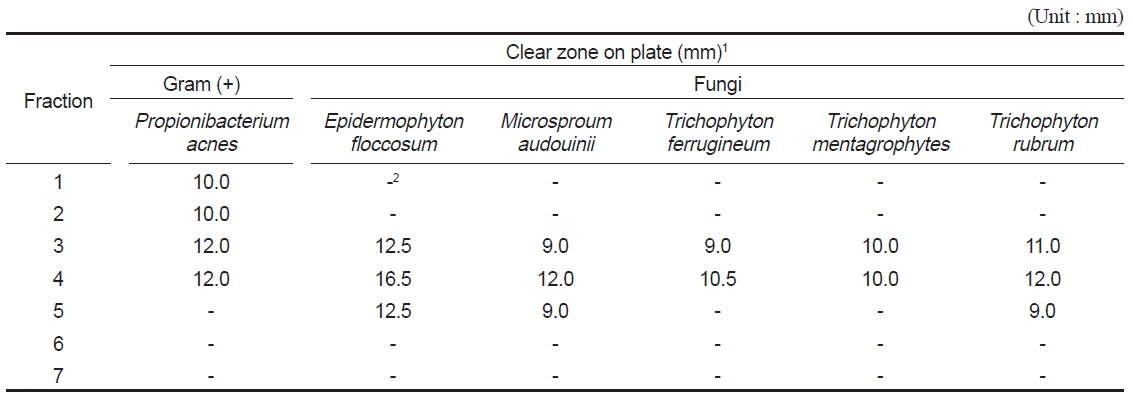
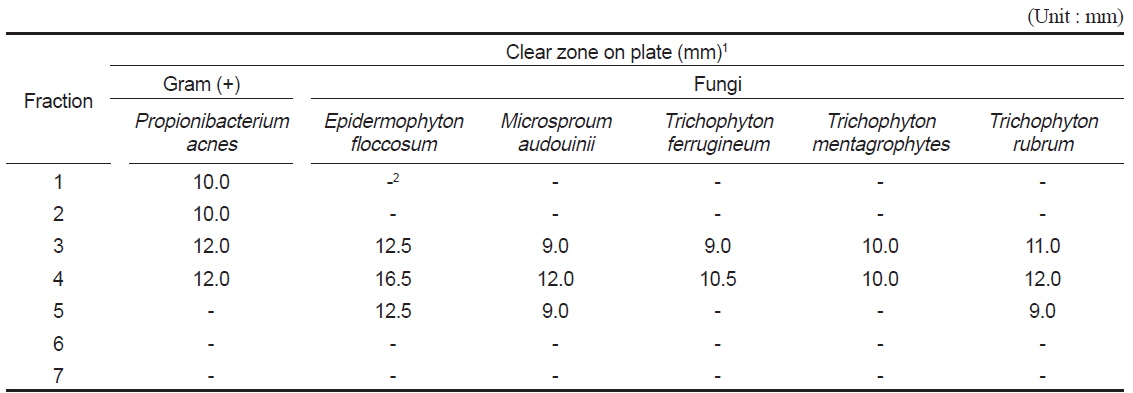
Antimicrobial activities of fractions obtained from methanol extract of Asterias amurensis by silica gel column chromatography I (200 mesh)
Choi et al. (1998)은
>
용매추출 및 column chromatography에 의한 분획물의 항산화성 효능
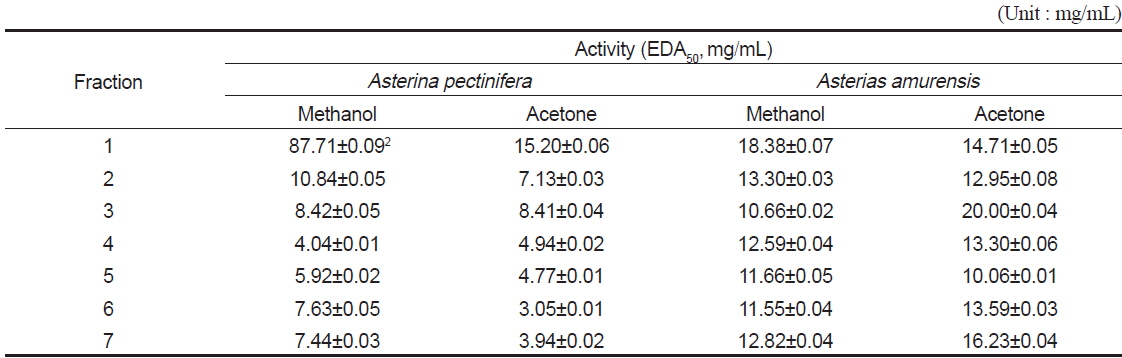
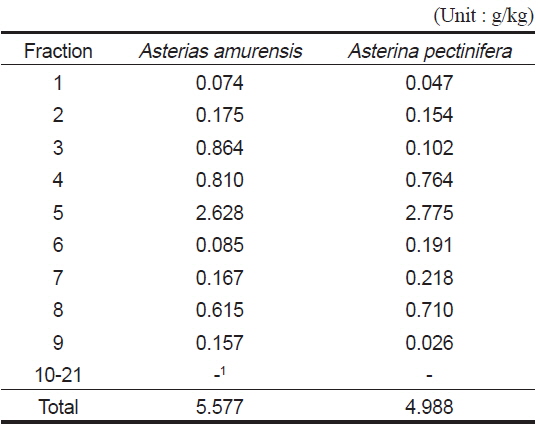
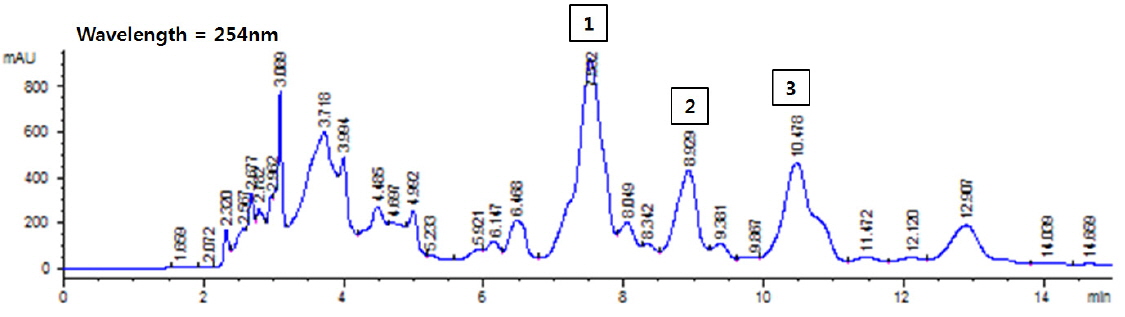
별 불가사리와 아므르 불가사리의 methanol 및 acetone 분획(Fig. 1, Step 2) 각각으로부터 분취한 7분획에 대한 항산화능(DPPH의 radical 소거능, %)을 EDA50 (mg/mL)으로 환산하여 Table 3에 나타내었다. 별 불가사리의 경우 methanol 및 acetone추출물에서 4번 분획물이 각각 4.04 및 4.94 mg/mL(EDA50)로 항산화능이 가장 높았으며, 아므르 불가사리의 경우 methanol추출물에서는 3번분획이 10.66 mg/mL, acetone 추출물에서는 5번분획이 10.06 mg/mL으로 가장 활성이 좋았다. 그러나 항균성효능(Table 1 및 2)과 뒤에서 언급할 미백효능(Table 6) 및 추출물로부터 회수되는 수득량(Table 4)을 고려하고, 산업적으로 공정의 효율성을 감안하여 분획 3 및 4번을 분취하여 다음 단계(Fig. 1, Step 3)인 silica gel column chromatography II (400 mesh)에서 21개의 분획으로 재 분리하였다. 이때에 수득율(Table 4)을 보면 5번분획이 별 불가사리에서는 2.628 g/kg이었고, 아므르 불가사리의 경우는 2.775 g/kg이었으며, 나머지는 모두 1.0 g이하였다. 그러나 분획당 분리가 어려워 별 불가사리에서는 4, 5번분획을 포집하여 HPLC로 재분획하여 Fig. 2에서처럼 RT 7.532, 8.929 및 10.478 min의 3개의 분획을 얻었다. 그리고 아므르 불가사리에서는 5번분획만을 포집하여 HPLC로 재 분획하여 RT 5.018 min의 1개 분획을 얻었다. 이러한 피크들은 TLC (thin layer chromatography)로 통하여 단일피크를 확인하였다.
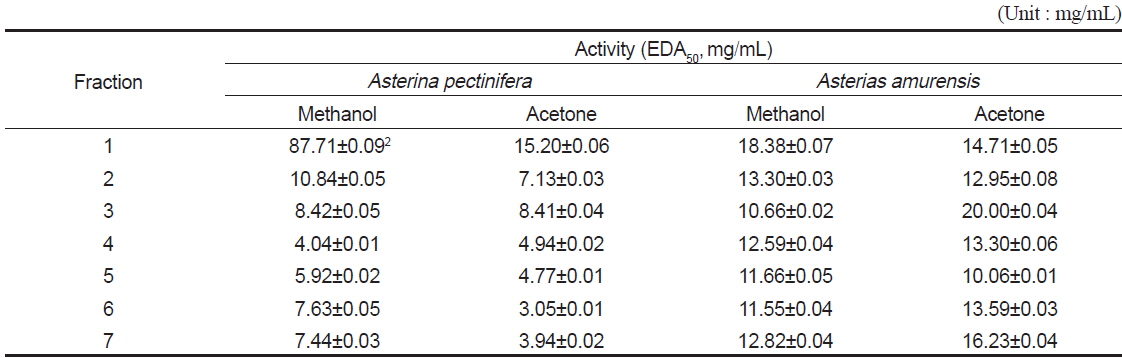
Antioxidant activities (EDA50, mg/mL)1 of fractions obtained from solvent extracts of starfishes by silica gel column chromatography I (200 mesh)
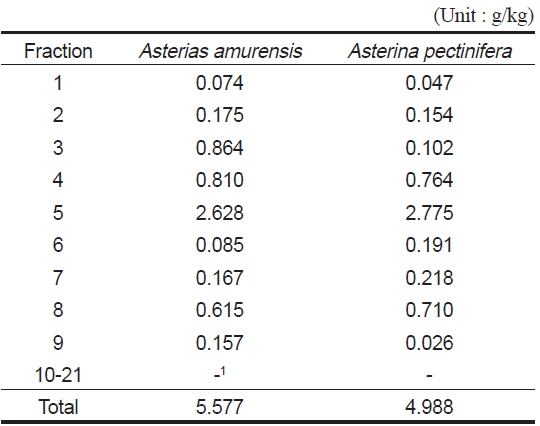
The yields of fractions obtained from methanol and acetone extract of starfishes by silica gel column chromatography II(400 mesh)
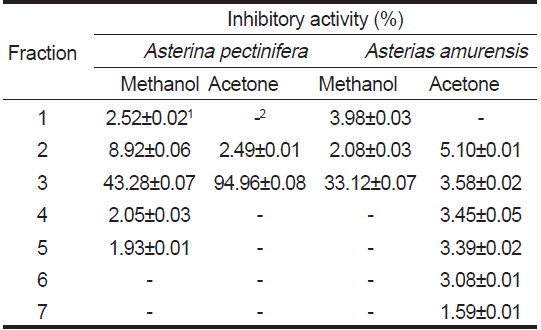
Tyrosinase inhibitory activity of fractions obtained from solvent extracts of starfishes by silica gel column chromatography I (200 mesh)
별 불가사리에서 HPLC로부터 재 분취한 3개의 분획(A)과 아므르 불가사리로부터 분취한 1개의 분획(B)으로 항산화능을 측정한 결과는 Table 5와 같다. 별 불가사리에서는 8.94 mg/mL로서 아므르 불가사리(15.59 mg/mL)에 비해 높은 활성을 나타내었지만, Table 3의 methanol 및 acetone추출물에 비해서는 낮았다. 이는 시료 추출과정과 보관의 장기화에 따른 기능성 물질의 산화의 결과로 추정되며, 이러한 문제는 산업화로 대량 생산 공정의 처리시간의 단축으로 실험실 수준의 문제점을 해결할 수 있다고 사료된다. 또한 L-ascorbic acid의 항산화효과 (EDA50=0.65 mg/mL) (Cho et al., 2001)와 비교하면 별 불가사리와 아므르 불가사리의 항산화능은 약 1/10-1/20배 정도로 활성이 낮았다.

Antioxidant activities (EDA50, mg/mL) of fractions separated from Asterina pectinifera and Asterias amurensis by HPLC compounds
Carotenoid계 색소류가 활성산소로부터 생체 세포와 조직을 보호하는 것으로 알려져 있어(Rau, 1985), 색소류와 항산화 활성은 밀접한 상관성을 가지고 있는 것으로 추정된다. 본 실험에서도 별 불가사리 추출물의 항산화능이 아므르 불가사리 보다 우수하였는데, 이것은 별 불가사리가 아므르 불가사리보다 total carotenoid 함량이 많은 것과 상관이 있을 것으로 추정된다(Jung, 2002). 세포의 노화방지와 관련이 깊은 항산화 효능을 가진 천연소재 개발은 기능성 화장품 분야에 매우 기여할 것으로 생각되며, 앞으로 이와 같은 생리기능성의 주체가 되는 물질의 규명에 관한 연구가 지속적으로 이루어져야 할 것으로 판단되었다.
>
용매추출 및 column chromatography에 의한 분획물의 미백 효능
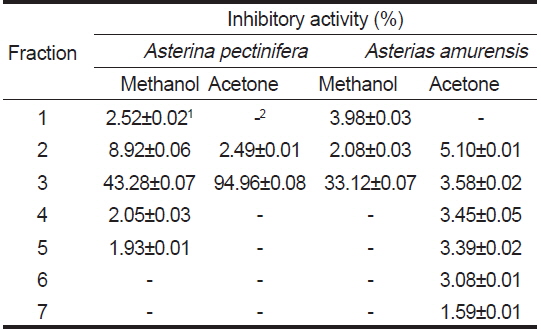
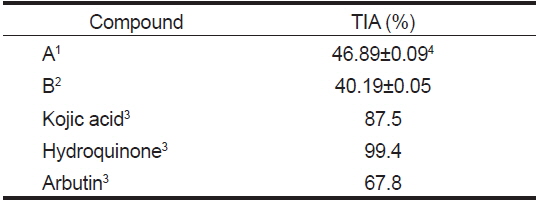
별 불가사리와 아므르 불가사리의 methanol 및 acetone분획(Fig. 1, Step 2) 각각으로부터 분취한 7분획에 대한 미백효능(tyrosinase활성저해능, %)을 Table 6에 나타내었다. 별 불가사리의 추출물이 아므르 불가사리에 비해 tyrosinase활성저해능이 높았으며, 두 시료 모두 methanol 및 acetone추출물의 3번 분획물이 다른 분획에 비하여 가장 높은 저해율을 나타내었다. 별 불가사리에서는 acetone추출물(94.96%)이 methanol추출물(43.28%)에 비해 2.2배 정도 활성저해율이 높았으나, 아므르 불가사리에서는 오히려 methanol추출물(33.12%)이 acetone추출물(3.58%)에 비해 효능이 9.3배로 더 높았다. 그러나 고부가가치성의 화장품 기본소재로서의 특성인 항균성 및 항산화능과 산업적으로 공정의 편리성을 고려하여 3-4번분획물을 취하였으며, silica gel column chromatography II (400 mesh)에서 다시 4-5번분획물(별 불가사리)과 5번분획물(아므르 불가사리)을 취하여 HPLC로 재 분취한 것의 tyrosinase활성저해능(%)을 Table 7에 나타내었다. 별(A) 및 아므르 불가사리 추출물(B)의 미백효과는 각각 46.89%와 40.19%로 높은 tyrosinase활성저해능을 나타내었다. 피부미백성분으로 널리 이용되고 있는 hydroquinone, kojic acid, arbutin 등의 tyrosinase 활성저해능은 각각 99.4%, 87.5%, 67.8%로 보고되었으며(Ji et al., 2004), Kim and Lim (1999)은 tyrosinase 저해 활성이 매우 높은 kojic acid의 유도체를 새롭게 합성하여 화장품으로서의 이용 가능성을 검토하였다. 위의 결과들로 볼 때 별 불가사리와 아므르 불가사리 추출물의 미백효과가 기존 미백활성 성분들보다 우수하지는 못하지만 의약품이 아닌 천연 기능성 화장품으로 응용할 수 있을 것으로 본다.
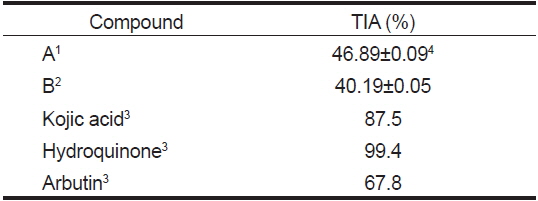
Tyrosinase inhibitory activity (TIA) of fractions separated from Asterina pectinifera and Asterias amurensis by HPLC compounds