We investigated the reproductive. characteristics of
벌레문치(
벌레문치 연구는 일본 남서해에서 트롤에 의해 어획된 등가 시치류의 서식밀도와 체장분포에 관한 연구(Balanove et al., 2011), 일본 Primor ’e 해역에서 벌레문치의 분포 및 생물의 일부 특성에 관한 연구(Saveliev et al., 2011), 일본 타타르 해엽에서 수심에 다른 서식밀도와 체장분포 등에 관한 연구(Saveliev et al., 2012)가 있으며, 국내는 등가시치아목 어류의 분류학적 재검토에 관한 연구(Kim and Kang, 1991), 한국산 등가시치아목 어류의 분류학적 연구(Kim, 2005), 한국 동해안 벌레문치 근육의 생화학적 구성(Lee et al., 2012), 벌레문치의 식성에 관한 연구(Choi et al., 2013) 가 되어 있을 뿐 벌레문치에 대한 생태학적 연구는 국내외적으로 매우 미비한 실정이다.
벌레문치는 우리나라 동해안에서 동해구기선저인망과 연안 자망에서 연중 어획되고 있는 어종이고, “장치” 라는 방언으로 불리어지면서 과거 어획 후 폐기되었던 어종이었으나, 점차 관심도가 높아지면서 상업적 가치가 증가하고 있다(NFRDI, 2012). 이는 우리나라의 연근해 어업자원의 감소현상에 의한 것으로 심해성 어종의 이용가치는 점차 높아지고 있기 때문에, 특히 벌레문치와 같은 미이용 미개발된 심해성 어종은 미래 자원으로서 활용과 자원관리를 위해 기초적인 생태학적 정보에 대한 많은 연구가 필요하다.
따라서 본 연구는 동해 중부연안에 분포하는 벌레문치의 자원 생태학적 정보를 얻기 위한 기초 연구로서, 생식소 발달과정 및 생식소 숙도지수의 월변화, 포란수, 성숙체장 등을 파악하여 재생산력과 관련된 산란생태를 밝히고자 한다.
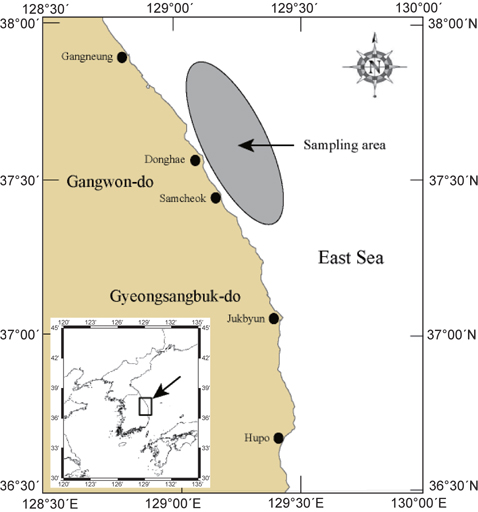
본 연구에서 사용한 벌레문치 시료는 2012년 1월부터 2013년 12월까지 동해 중부연안의 100-800 m 수심에서 동해구기선저인망 및 연안자망어업에 의해 어획된 것이다(Fig. 1). 채집된 시료는 실험실에서 암·수 구분하여 전장(TL)은 0.1 cm 까지, 체중(BW)은 0.1 g까지, 그리고 생식소중량(GW)은 0.01 g까지 측정하였다.
벌레문치의 생식소 발달과정을 알아보기 위하여 생식소의 외부형태를 조사하고, 생식소 크기, 색조, 난의 투명상태, 난립의 크기 등을 기준하여 생식소 성숙단계를 육안으로 관찰하였으며, 성숙단계는 미숙(Immature), 중숙(Maturing), 완숙(Marture), 방후(Spent) 의 4단계로 구분하였다.
생식소 숙도지수(GSI)의 월변화는 다음 식으로 구하였으며,
여기서, GW는 생식소중량(g)을, 그리고 BW는 체중(g)을 나타낸다.
난경은 난소 내 난괴를 개량 Gilson액(Love and Westphal, 1981)에 넣어 분리한 후, 해부현미경으로 난의 장경을 측정하였고, 1년의 난경변화를 보기 위해 2012년과 2013년의 난경측정결과를 월별로 합쳐서 분석하였다.
포란수(F)는 완숙단계의 개체 중 현미경으로 관찰한 결과, 산란하지 않은 것으로 판단된 개체를 선정하여 미세한 침으로 각각의 난을 완전히 분리한 후 해부현미경으로 계수하여 습중량법으로 구하였다.
여기서, A는 난소의 중량, B는 난소 껍질의 중량, C는 난소 일부의 중량, 그리고 e는 C의 난 수이다.
군성숙도는 산란기로 추정되는 시기에 중숙 이상의 개체를 당해연도 산란가능군으로 보고 성숙개체의 비율로써 구하였으며, 50% 성숙체장은 로지스틱(logistic)식 (Zhang, 1991)에 의해 추정하였다.
여기서, Pi는 i 체장계급에서의 군성숙비율, TLi 는 i 체장계급의 전장, 그리고 b1, b2는 상수이다.
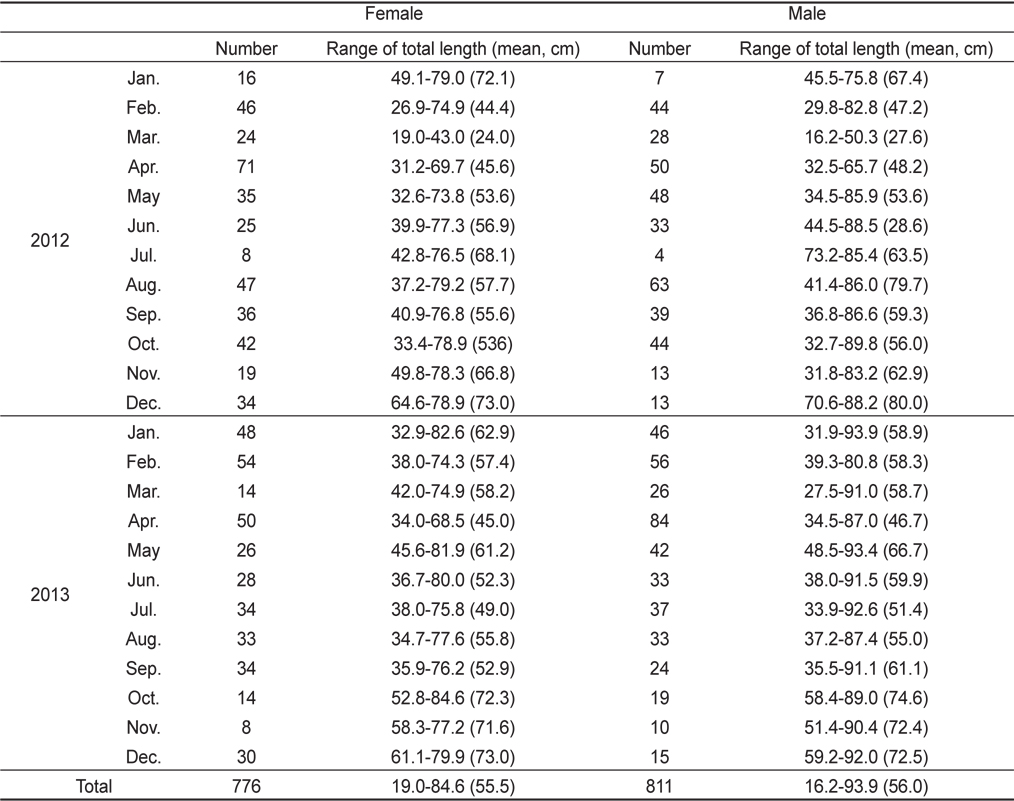
본 연구에 사용된 벌레문치는 총 1,587마리로 암컷 776마리, 수컷 811마리였으며, 이들의 전장범위는 암컷의 경우 19.0-84.6 cm, 수컷의 경우 16.2-93.9 cm 범위였고, 평균 전장은 암·수 각각 55.5 cm, 56.0 cm이었다 (Table 1).
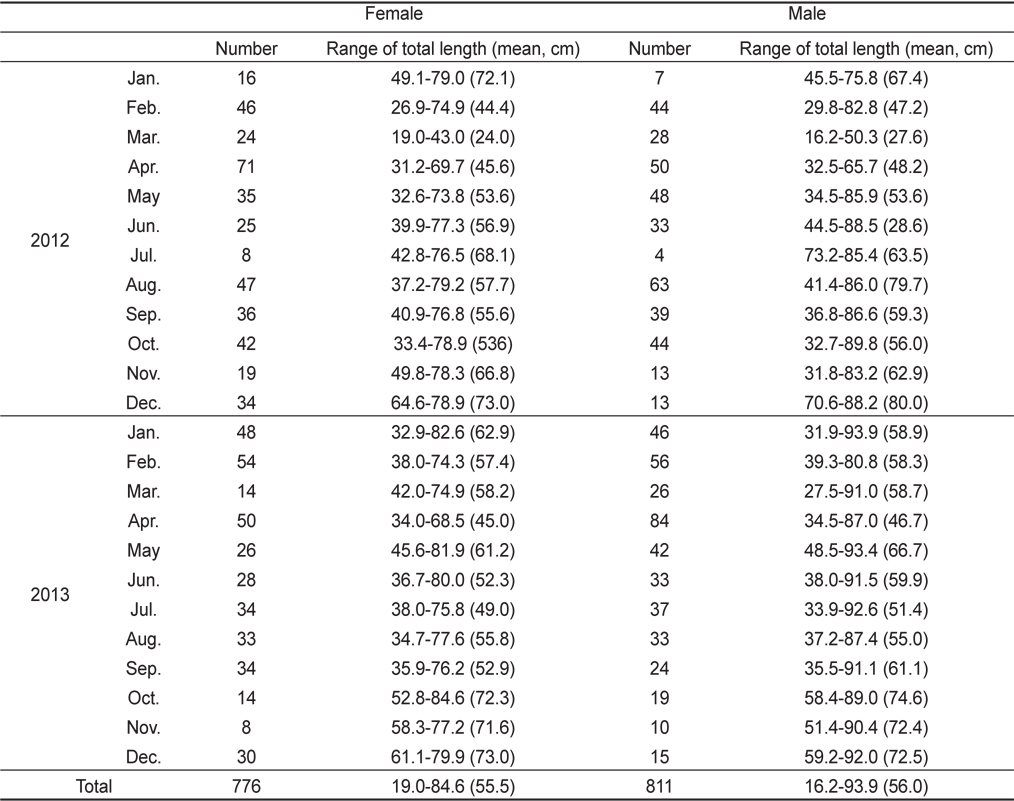
Number and size of Lycodes tanakae caught by eastern sea danish seine and gill net in the coastal waters of the middle East Sea
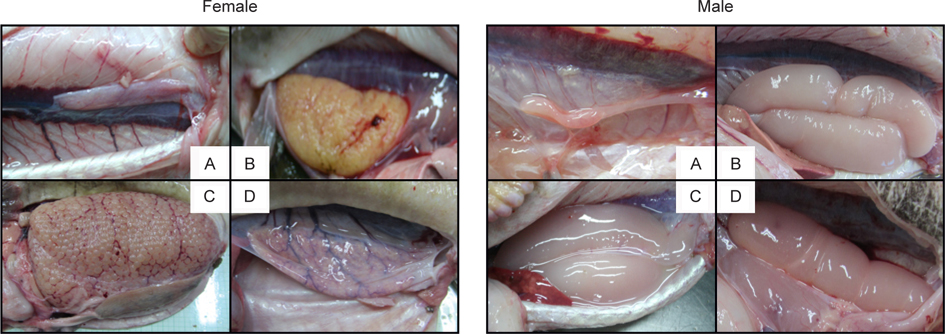
벌레문치의 생식소 성숙단계를 육안관찰로 외형적으로 구분하여 분석한 결과 (Fig. 2), 암컷의 미숙단계는 난의 크기가 매우 작으며 얇은 막을 형성한 연홍색을 띠고 있었고, 중숙단계는 난의 크기가 육안관찰이 용이할 정도로 성장하였고 소혈관이 산재되어 주황색을 띠고 있었다. 완숙단계는 난의 지름이 3 mm 이상으로 크게 성장하였으며, 대부분이 투명하고 소혈관은 보이지 않았다. 방후단계는 난막에서 완숙의 난이 빠져나갔고, 난막의 크기가 줄어들었으며, 미성숙의 작은 난들이 남아있었다. 수컷의 미숙단계는 다홍색을 띠며 크기가 약 2 cm 정도로 단단하였다. 중숙단계는 진한 붉은색과 유백색이 함께 나타났으며, 크기는 약 5 cm 정도로 성장하였다. 완숙단계는 유백색을 띠며 약 10 cm 이상으로 크게 성장하였고 젤리형태로 나타났다. 방정후의 단계는 유백색에서 다홍색의 비율이 높아졌고, 완숙상태 에 비해 크기가 줄어들었다.
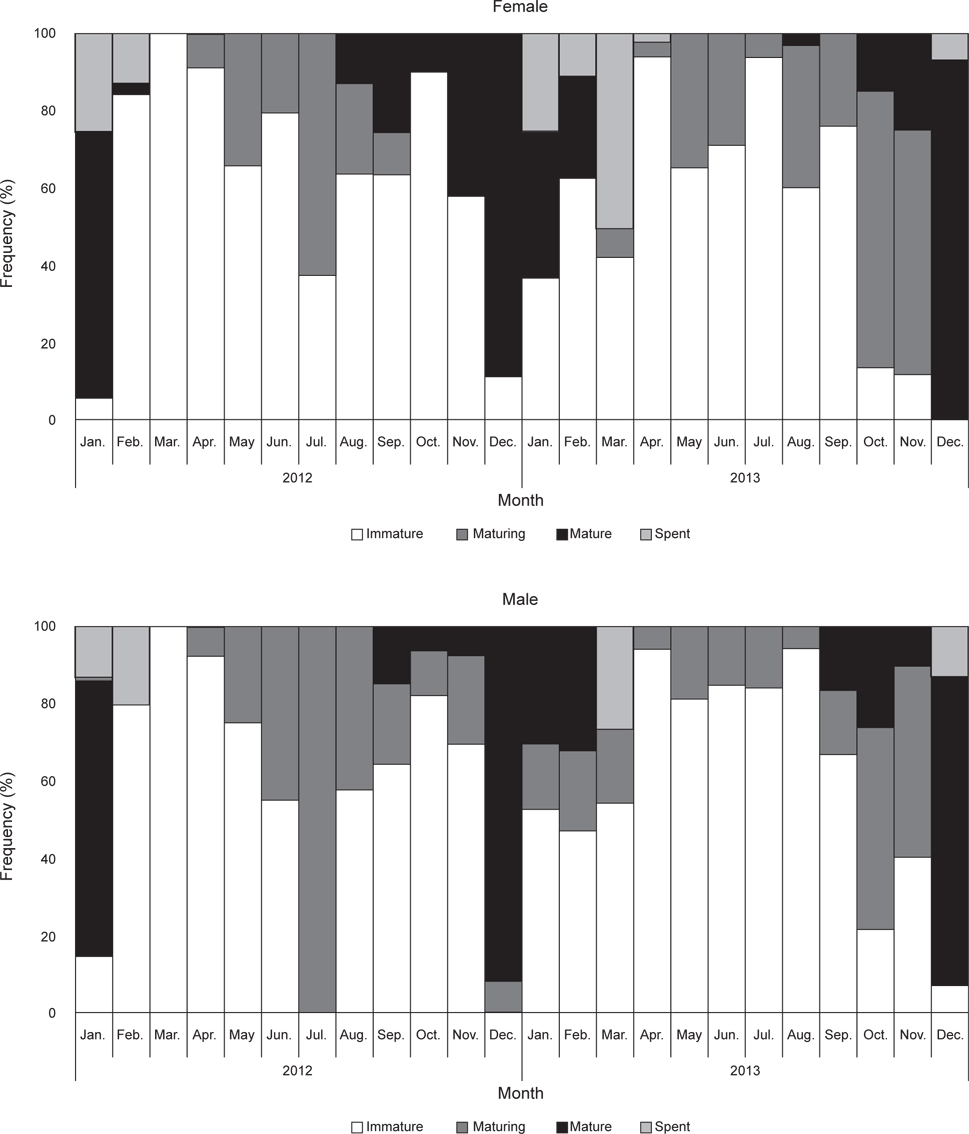
벌레문치의 월별 성숙도 변화를 살펴보면(Fig. 3), 암컷의 미숙단계는 2013년 12월을 제외하고 연중 출현하였고, 중숙단계는 5월에서 11월사이 높은 비율을 보였다. 완숙개체는 8월부터 출현하여 이듬해 2월까지 나타났고, 1월과 12월에 가장 높은 비율을 보였다. 방후단계는 12월에서 이듬해 4월 사이에 출현하였다. 수컷의 경우는 미숙단계가 2012년 12월을 제외하고 연중 출현하였고, 중숙단계는 2012년 4월부터 2013년 11월까지 출현하였다. 완숙단계는 9월부터 출현하여 이듬해 2월까지 나타났고, 1월과 12월사이에 가장 높은 비율을 보였다. 방후단계는 12월에서 이듬해 3월사이에 출현하였다.
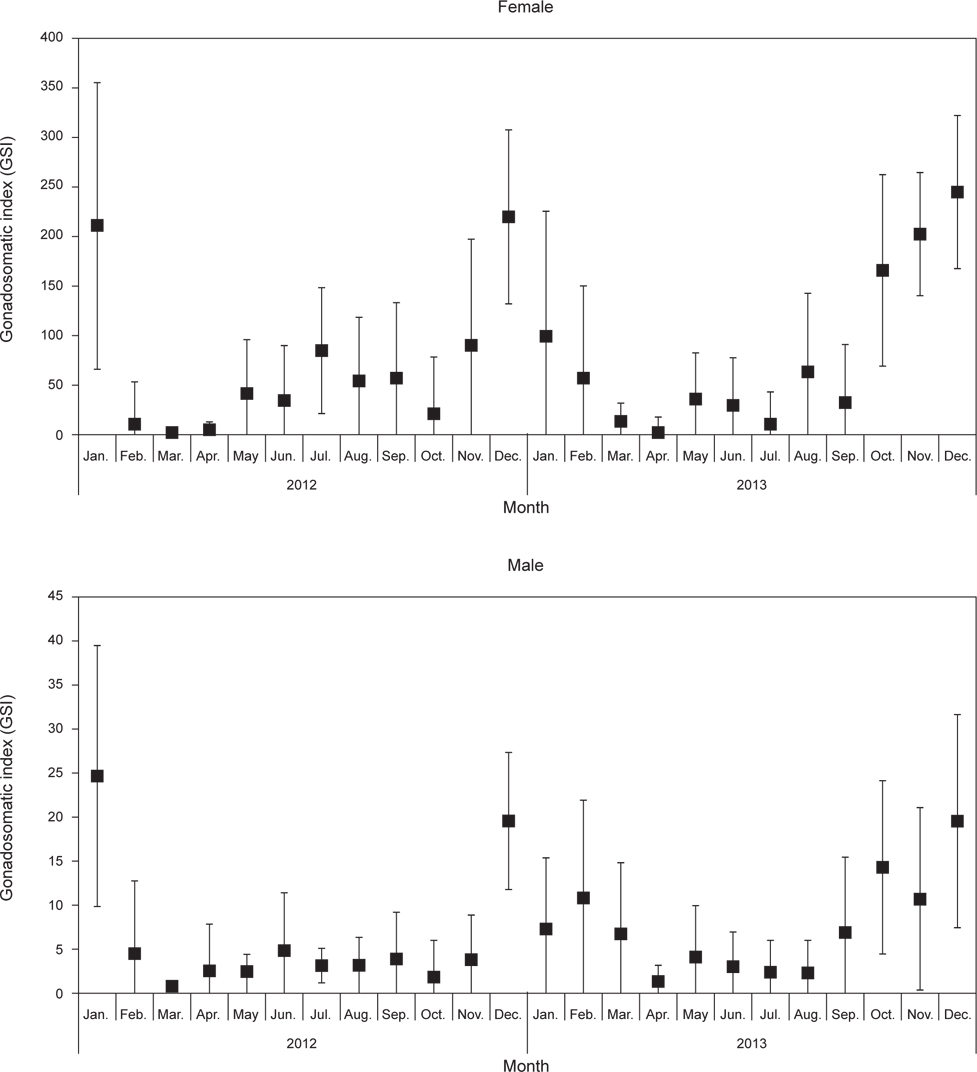
벌레문치 생식소숙도지수 (GSI)의 월 변화를 살펴보면 (Fig. 4), 암컷의 GSI변화는 2012년 1월에 209.7로 높은 값을 보였고, 2012년 2월에 급격히 낮아져 4월까지는 5이하의 낮은 값을 나타내었다. 2012년 5월부터 점차 높아지기 시작하여 11월에는 89.1로 크게 높아져 12월에는 219.5로 가장 높은 값을 나타내었다. 이후 2013년 2월까지 50이상의 높은 값을 보였고, 2013년 3월부터 급격히 낮아졌으며 7월까지 50이하의 낮은 값을 나타내었다. 2012년과 유사하게 2013년 8월부터 높아지기 시작하여 12월에 243.9로 가장 높은 값을 나타내었다. 수컷의 GSI변화는 2012년 1월에 24.7로 높은 값을 보였고, 이후 2012년 11월까지 5이하의 낮은 값을 유지하였다. 2012년 12월에 급격히 높아져 19.6으로 최고 값을 나타내었고, 2013년 3월까지 6.7-10.8로 높은 값을 보였으며, 2013년 4월 이후 GSI값이 5이하로 낮은 값을 나타내었다. 2013년 9월부터 높아지기 시작하여 12월에 19.6으로 가장 높은 값을 나타내었다. 수컷의 GSI의 월 변화는 암컷과 유사한 경향을 나타내었다. 따라서 생식소 발달과정 및 생식소 숙도지수의 월 변화로부터 벌레문치의 산란기는 12-2월로 추정된다.
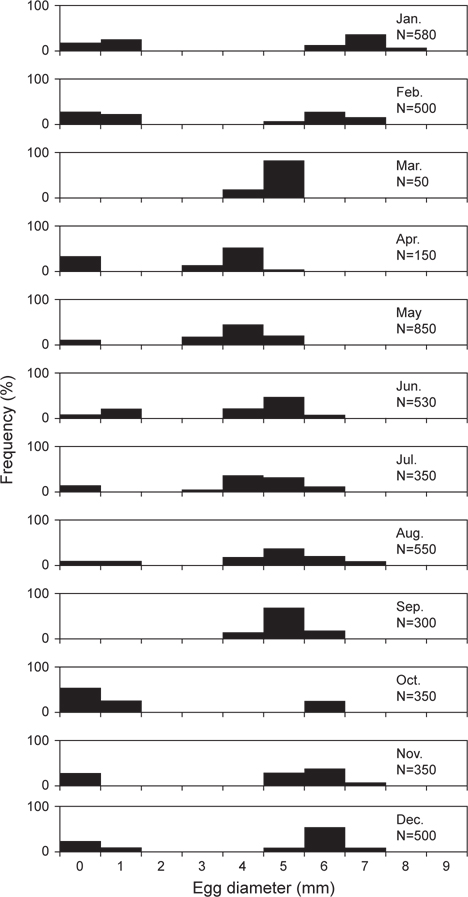
난경의 월 변화를 살펴보면 (Fig. 5), 3-11월까지는 미숙단계와 중숙단계로 대부분 2개의 모드를 나타냈고, 미숙단계의 난경은 1 mm 이하로 관찰되었으며, 점차 난이 성숙하면서 중숙단계의 난경은 2-7 mm의 범위까지 성장하는 경향을 보였다. 벌레문치의 산란기로 추정되는 12-2월의 완숙단계의 난경은 5-9 mm로 발달되어 산란에 참여하는 것으로 보였고, 산란 후 방후 및 미숙 단계의 난경은 1 mm 이하로 관찰되었다.
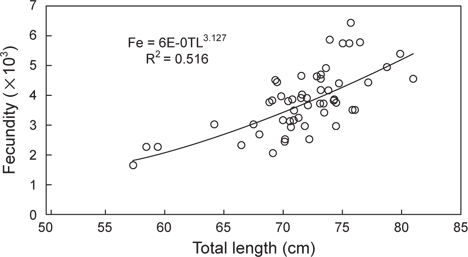
벌레문치의 산란기에 산란경험이 없다고 판단되는 성숙 개체 55 마리를 대상으로 포란수를 측정한 결과, 벌레문치의 포란수는 최소 1,677개 (57.3 cm), 최다 6,445개 (75.7 cm)로 계측되었고, 전장과 포란수간의 관계식은 Fe=6E-05TL3.127 (R2=0.516)로 나타나 전장이 증가할수록 포란수가 증가하는 경향을 나타내었다(Fig. 6).
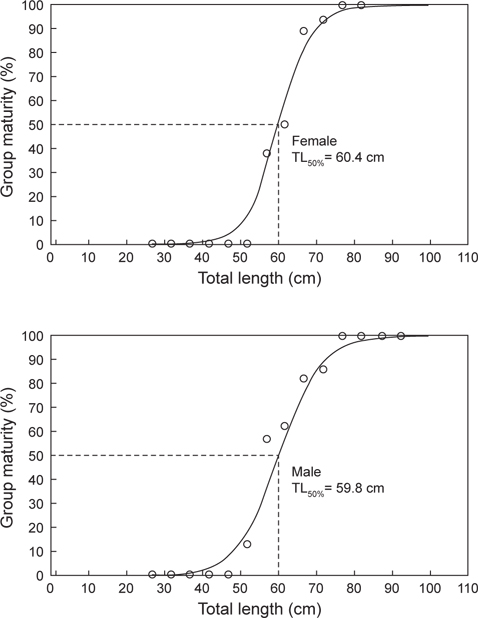
재생산에 참여하는 체장을 알아보기 위해 11-2월간 채집된 암컷 205마리와 수컷 153마리를 대상으로 중숙단계 이상의 개체가 당해연도 산란에 참여하는 것으로 간주하여 체급별(5 cm) 성숙개체의 출현율을 조사하였다(Fig. 7). 암컷은 전장 52.5 cm 이하에서 성숙개체가 출현하지 않았고, 57.5 cm 에서 37.5%, 67.5 cm에서 88.9%, 77.5 cm 이상에서 전 개체가 성숙한 것으로 확인되었다. 수컷은 전장 47.5 cm 이하에서 성숙개체가 출현하지 않았고, 52.5 cm에서 12.5%, 67.5 cm에서 83.3%, 77.5 cm 이상에서 전 개체가 성숙한 것으로 확인되었다. 벌레문치의 최소성숙체장은 암컷 57.3 cm, 수컷 55.6 cm 로 나타났고, 체급별 성숙개체의 출현율을 logistic 식에 적용시킨 결과, 벌레문치의 50% 성숙체장은 암컷 60.4 cm, 수컷 59.8 cm로 추정되었다.
본 연구에서 조사된 벌레문치의 최대전장은 암컷 84.6 cm였고, 수컷은 93.9 cm로 수컷이 암컷보다 조금 큰 것으로 나타났으나, 평균전장에서는 암컷 55.4 cm였고, 수컷은 56.0 cm로 나타나 벌레문치의 암·수간 전장이 유사하게 나타났다. 동해에서 조사된 벌레문치에 관한 연구결과를 보면, 벌레문치는 수심이 깊어질수록 크기가 큰 개체들이 서식하고(Balanov et al., 2011), 수심 50-200 m에는 30 cm 이하의 작은 개체가 수심 50-600 m에서는 30 cm 이상의 개체가 출현한다고 보고하였다(Seveliev et al., 2012). 또한 Sohn et al. (2010)의 우리나라 동해 심해 생태계의 수심별 조사결과에서 벌레문치는 수심 300-700 m에서 출현하였고, Park et al. (2007)의 동해심해트롤에 의한 연구결과에서 벌레문치는 300 m와 700 m에서 많은 양이 출현한 것으로 보고하였다. 이는 본 연구에서 채집된 벌레문치의 전장범위가 대부분 30 cm 이상이고, 우리나라 동해안에서 조사된 선행연구결과들을 통해 미루어보면 수심 200 m이상에서 조업이 이루어진 것으로 판단된다.
벌레문치의 생식소 성숙도 판별을 위하여 육안관찰한 결과 벌레문치의 생식소의 성숙도는 육안으로 충분히 관찰할 수 있을 정도로 성숙단계별로 생식소 크기와 색조에서 뚜렷한 차이를 나타냈다. 특히 산란기가 가까워진 완숙단계의 개체들은 암컷의 경우 난이 투명하게 변화하는 특징을 보였고, 수컷은 유백색을 나타냈다. 일반적으로 암컷의 생식소가 완전히 성숙되었을 때는 난소의 무게가 전체중의 약 10-25%를 차지하는 것으로 알려져 있다(Kim and Zhang, 1994). 벌레문치 암컷의 완숙단계의 생식소중량은 평균 699 g으로 체중의 24.7%로 나타나 생식소가 체중에 비해 큰 것으로 생각된다.
벌레문치의 산란시기를 파악하기 위해 생식소 발달과정과 생식소숙도지수를 살펴보았다. 벌레문치 암컷의 완숙단계는 9월 부터 이듬해 2월까지 나타났고, 1월과 12월사이에 가장 높은 비율을 나타내었다. 생식소숙도지수는 12월에 가장 높은 값을 나타내었고, 이듬해 2월까지 점차 낮아졌다. 벌레문치 수컷의 생식소 발달과정과 생식소숙도지수의 월별 변화는 암컷과 유사한 경향을 나타내었다. 따라서 생식소 발달과정 및 생식소 숙도지수의 월 변화로부터 벌레문치의 산란기는 12-2월로 추정된다.
Aida (1991)는 어류의 생식주기를 수온이나 광주기 등과 같은 환경적인 요인과 관련하여 춘계산란형(spring spawner), 춘하계산란형(spring to summer spawner), 하계산란형(summer spawner), 춘추계산란형(spring to autumn spawner), 추계산란형(autumn spawner) 및 동계산란형(winter spawner)의 6가지 유형으로 구분하였다. 본 연구결과인 동해 중부연안 벌레문치의 산란기는 12-2월이므로 동계산란형인 것으로 추정된다. 또한 어류의 성숙과 산란은 적합한 환경에서 비교적 동일한 주기에 이루어지는데, 산란기에 가까워지면서 생식소 내부구조의 발달 또한 일정한 주기성을 나타낸다. 이러한 주기적인 생식소의 발달은 생식현상의 직접적인 요인이 되는 어체의 내분비물 질의 변화에 의해 조절이 되는데 이러한 변화는 수온, 광주기 등과 같은 외적 요인에 많은 영향을 받는 것으로 알려져 있다(De Vlaming, 1972; Nishi, 1979; Shimizu and Hanyu, 1983). 하지만 벌레문치와 같은 심해성 어류의 내분비물질의 변화에 영향을 미치는 외적 요인에 대한 연구가 미비한 실정으로 이 부분에 대해서는 좀 더 심도 있는 연구가 필요하다.
어류의 산란형태는 난경조성을 통해 나타내는 모드의 수와 산란기 동안의 산란하는 횟수로 형태를 5 단계로 추측해 볼 수 있다(Kim, 1993). 벌레문치의 난경조성 결과를 토대로 분석해보면 산란시기인 12-2월에 난경모드가 미숙단계를 제외하면 완숙단계의 난경조성이 5-9 mm 에서 단일모드를 나타내어 1회 산란하는 것으로 판단되어 단봉 1회 산란형인 것으로 생각된다. 본 연구결과 벌레문치의 완숙단계 평균난경은 6.9 ± 0.7 mm를 나타내어 등가시치과(Zoarcids)의
벌레문치의 포란수는 최소 1,677개(57.3 cm), 최다 6,445개(75.7 cm) 로 계측되었고, 전장이 증가할수록 포란수가 증가하는 경향을 나타내어 일반 경골어류와 유사한 경향을 보였다(Kim and Zhang 1994). 또한 대부분의 등가시치과는 포란수가 1,000개 이하로 작게 나타났으나(Gusztonyi, 1977; Silverberg et al., 1987; Matallanas et al., 1990; Brodte et al., 2006),
본 연구결과 벌레문치의 50% 성숙체장은 암컷 60.4 cm, 수컷 59.8 cm로 추정되었고, 77.5 cm이상이면 모두 성숙한 개체가 출현하는 것으로 나타났다. Primor ’e 해역의 벌레문치 연구에 따르면 전장 30 cm이하 개체들을 유어(juvenile)로 보고하였고(Saveliev et al., 2011), 이는 본 연구결과에서 암컷 52.5 cm와 수컷 47.5 cm이하에서 성숙개체가 출현하지 않는 것으로 나타나 동해 중부의 벌레문치의 미성숙개체 크기에 포함되는 것으로 나타났다.
벌레문치의 성숙연령은 본 연구에서 성장에 대한 부분을 고려하지 않아 성숙연령을 추정할 수 없었으나, Primor ’e 해역의 벌레문치 연구결과(Saveliev et al., 2011)를 토대로 성숙연령으로 환산한 결과, 암·수 모두 5-6세로 추정되었다. 남극해의 등가시치과 Pachycara brachycephalum의 성숙연령은 5세, 성숙체장은 22-24 cm로 보고하였고(Brodte et al., 2006), 이는 소형의 등 가시치과에 속하는 어종으로 성숙체장은 벌레문치와 차이가 있지만 성숙연령에서는 유사하였다.
따라서 본 연구결과로 벌레문치의 산란생태에 관한 기초자료를 얻을 수 있었으나, 미래의 수산자원의 중요성에 비해 생태학적 연구가 미진한 상태로 본 연구결과를 바탕으로 연령과 성장, 식성, 분포특성 등 보다 종합적인 연구가 수행되어야 하며, 동해 중부연안의 벌레문치의 지속적인 생산을 위해 자원상태를 진단하고 자원관리를 실시하여야 할 것이다.