The increasing of atmospheric CO2 are changing the pH (ocean acidification) and temperature of the sea. Although the effects of ocean acidification on calcifying organisms have well-documented, only a few studies have examined the combined effects of ocean acidification and elevated temperature. This study investigated the effects of ocean acidification and elevated temperature for 2100 on survival and growth of juvenile abalone,
지난 세기 동안 화석연료의 사용은 급격하게 증가하였으며 화석연료의 연소에 의해 발생된 CO2 방출량도 지속적으로 증가되고 있다. 대기중 CO2는 19세기 중반까지만 하더라도 280 ppm 정도로 유지되었으나, 1958년에 315 ppm, 1994년에 355 ppm으로 증가되었고, 현재 400 ppm을 넘어섰다. 이러한 경향은 1950 년대 하와이 Mauna Loa에서 CO2 농도를 상시적으로 관측한 이래 지수함수적으로 증가하는 경향을 보이고 있으며, 앞으로도 CO2의 증가추세는 계속 될 것이다. 향후 CO2의 증가량을 예측하기는 어려우나 2007년 IPCC (기후변화에 관한 정부간 패널)가 발표한 4차 보고서에 의하면 화석연료의 소비형태 및 CO2 감축노력에 따라 100년 이내에 CO2 농도는 750-1,500 ppm 증가될 것으로 예상되며 지구 평균 온도는 1.5-4.5℃ 가량 오를 것으로 예측하였다(IPCC, 2007).
해양은 대기 중의 CO2를 흡수하여 지구온난화가 급속히 진행되는 것을 완화하는 역할을 해왔으나 대기 중 CO2 농도 증가에 의해 해양으로 유입되는 CO2가 증가되어 해수의 pH가 감소하는 해양산성화가 이미 진행되고 있다(Zeebe et al., 2008). 해양의 pH는 산업혁명이전과 비교하여 0.1 정도 감소되었고 향후 100년 이내에 0.2-0.4 정도 감소될 것으로 예측하고 있으며, 해수수온도 지난 세기와 비교하여 0.76℃ 증가되었으며, 향후 100년 이내에 2℃ 이상 증가될 것으로 예측하고 있다(Brewer, 1997; IPCC, 2007).
대기 중 CO2가 해양으로 유입되면 탄산(carbonic acid)을 형성하고, 이것은 다시 탄산염(carbonate)이나 중탄산염(bicarbonate)을 만들게 된다. 해수 pH의 감소로 중탄산염을 형성하는 쪽으로 평형이 이동하게 되면 물속의 탄산염 농도가 떨어지게 되며 탄산칼슘의 용해율이 증가되고 패각 형성에 필요한 충분한 탄산염을 공급받지 못하게 된다(Gattuso et al., 1998; Gattuso and Buddemeier, 2000; Caldeira and Wickett, 2005; Ries et al., 2009). 대기 중 CO2의 농도가 750 ppm정도만 되어도 석회화 플랑크톤 coccolithophorids의 석회 형성율은 현재 수준과 비교해 절반 정도로 떨어지는 것으로 알려져 있으며(Gattuso and Buddemeier, 2000), 성게, 굴 등 CaCO3를 이용하는 석회화 생물들의 산염기조절특성, 대사, 성장, 재생산 등 생태생리학적 기능에 영향이 나타나는 것으로 보고되고 있다(Pörtner et al., 2004). 또한 해양산성화와 함께 진행되는 수온 상승은 생물의 생존, 생리, 성장, 성숙 등에 영향을 미치게 되고 분포, 섭이, 번식장소 이동 등 서식여건 전반에 부정적인 영향을 주게 된다(Pörtner et al., 2005; Mueter and Litzow, 2008; Parker et al., 2013). 따라서 해양산성화에 의한 해양생물 및 생태계의 변화를 예측하기 위해서는 수온상승과의 상호영향에 대한 연구가 필요하다.
수많은 저서무척추동물은 고착생활을 영위하고 있어 행동이 늦어 환경변화에 대응하여 피난하는 능력이 부족하기 때문에 해양산성화와 같은 환경변화에 영향을 받기 쉽다(Fabry et al., 2008). 전복은 평평한 단일 패각을 형성하는 해양 복족류의 대표 종으로 전 세계적으로 약 100여종이 북반구와 남반구에서 서식하고 있으며, 최근 전복 어획량 감소와 관련하여 기후변화가 영향을 미치고 있음이 밝혀지고 있다(Hankewich and Lessard, 2007; Crim, 2010; Crim et al., 2011). 따라서 본 연구에서는 향후 미래에 발생가능한 해양산성화 농도 및 수온상승 환경에서 장기간 노출실험을 실시하여 전복치패의 폐사 및 성장에 대해서 알아보았다.
실험생물로 사용한 전복(
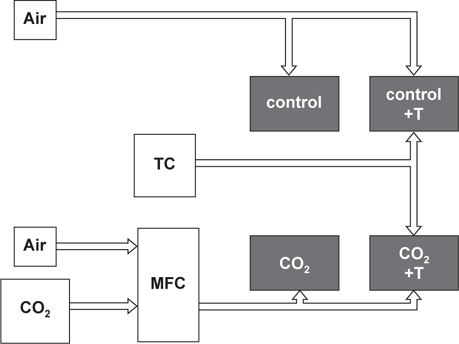
해양산성화 및 수온상승 영향을 살펴보기 위하여, 4개의 실험구(대조구, 대조구+2℃, CO2, CO2+2℃)를 설치하여 1차실험(1,500 ppm-CO2) 및 2차실험(1,000 ppm-CO2)을 실시하였다(Fig. 1). 수조는 전복을 수용하는 수조(Holding tank)와 여과장치, 폭기장치, 히터를 넣은 수조(Header tank)와 연결하여 순환여과 시켰으며 수량은 약 60 L가 되도록 하였다. 사용된 공기는 에어펌프를 이용하여 실내공기를 주입하였으며, CO2는 가스혼합장치(Koflock, MB2C)를 이용하여 압축공기와 CO2를 혼합시켜 CO2가 설정농도로 주입되도록 하였으며 Header tank에서 충분이 폭기 된 물이 사육수조로 들어가도록 하였다. 가스혼합장치로부터 배출되는 가스의 농도는 이산화탄소농도측정기(Telaire, 7001)를 사용하여 측정하였으며, Header tank의 CO2 농도변화는 pH를 측정하여 간접적으로 확인하는 방법을 사용하였다. Header tank의 pH는 pH meter (Thermo, Orion 3star)를 사용하여 매일 사육수조의 물을 교환하기 전에 측정하였다. 용존산소(YSI, 550A)와 염분(Atago, S/Mill-E)도 매일 측정하였으며 실험기간 동안 각각 약 6-7 mg/L, 30-33 psu로 유지되었다. 각 사육수조의 pH 및 온도조건은 Table 1에 나타내었다.
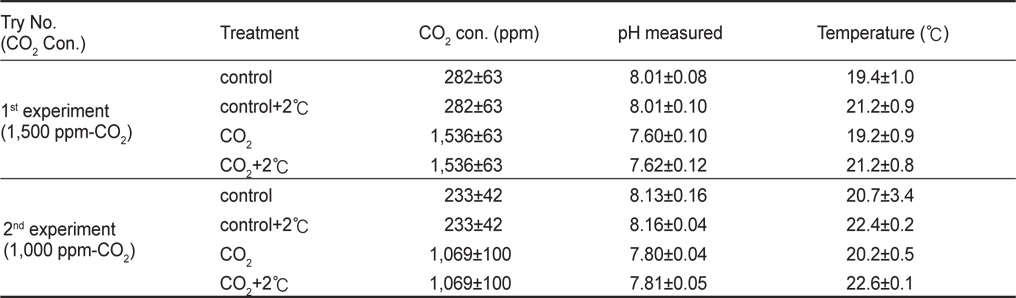
[Table 1.] Seawater pH and temperature (mean±SD) in animal holding tanks
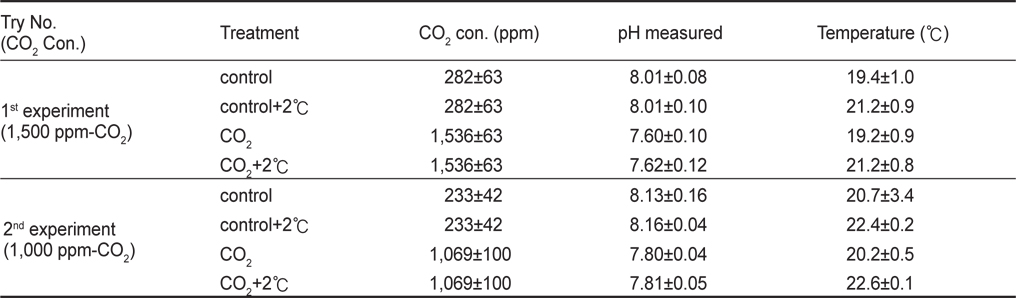
Seawater pH and temperature (mean±SD) in animal holding tanks
노출실험 하루전에 전복의 생체량을 측정한 후(1차실험: 각장 21-29 mm, 무게 1.3-2.7 g, 2차실험: 각장 19-29 mm, 무게 0.9-2.7 g), 1차실험에서는 80일 동안, 2차실험에서는 90일 동안 실험조건에서 노출시키면서 생존율 및 성장률을 측정하였다. 전복의 생존을 확인하기 위하여 매일 아침 및 저녁에 봉으로 건드려서 힘없이 판에서 떨어지는 개체는 폐사한 것으로 간주하고 수조에서 제거하였다. 전복의 평균성장률(Specific Growth Rate, SGR)은 아래의 식에 의해서 계산하였다.
[SGR=100×(lnWf –lnW0)/t]
W0: 실험개시시 생체무게
Wf: 실험종료시 생체무게
실험 후 얻어진 결과는 one-way ANOVA을 이용하여 대조구와의 유의성을 검사하였다(
전복의 생존율은 1차실험(1,500 ppm-CO2)에서는 초기 폐사가 발생하였으나 실험기간 중 전복의 생존율에는 유의적인 차이를 나타내지 않았다(
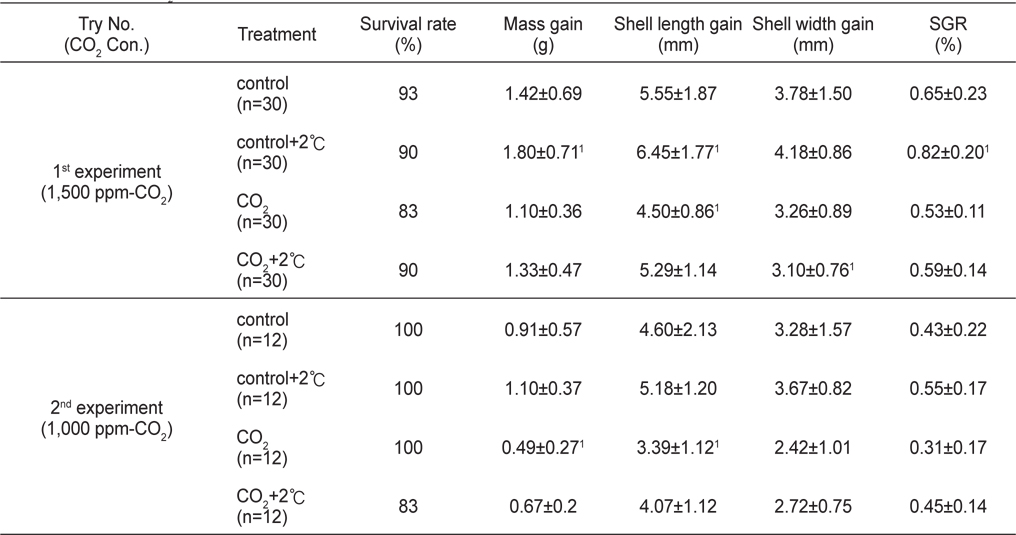
[Table 2.] Effects of CO2 and temperature on abalone survival rate and growth rates
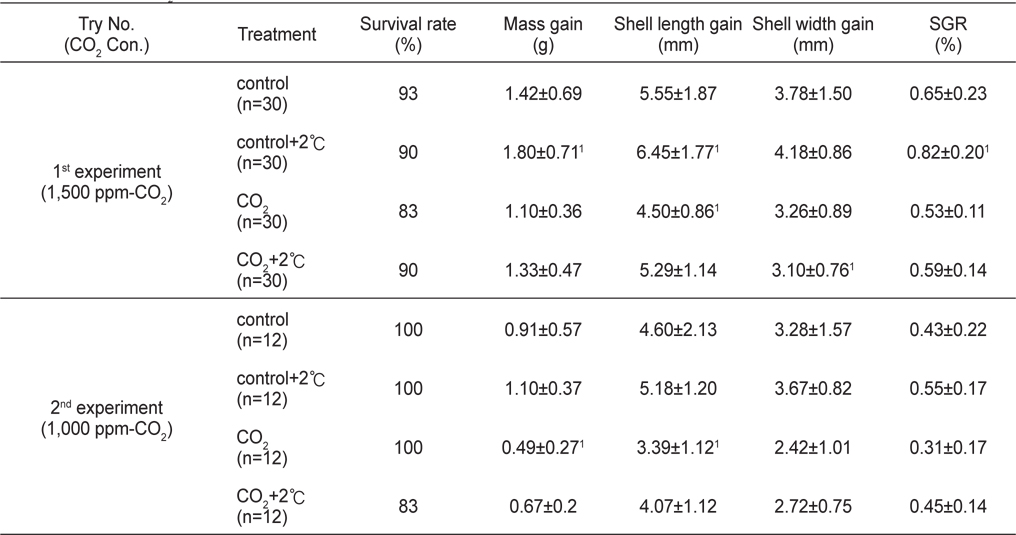
Effects of CO2 and temperature on abalone survival rate and growth rates
전복의 성장은 1차실험(1,500 ppm-CO2)에서는 대조구+2℃ 구에서 대조구와 비교하여 모든 성장지표들이 유의적으로 증가하였고 CO2구가 대조구에 비해 각장성장이 유의적으로 감소하였으며, 2차실험(1,000 ppm-CO2)에서는 무게성장 및 각장성장에 있어 CO2구가 대조구와 비교하여 유의적인 차이를 보였다(
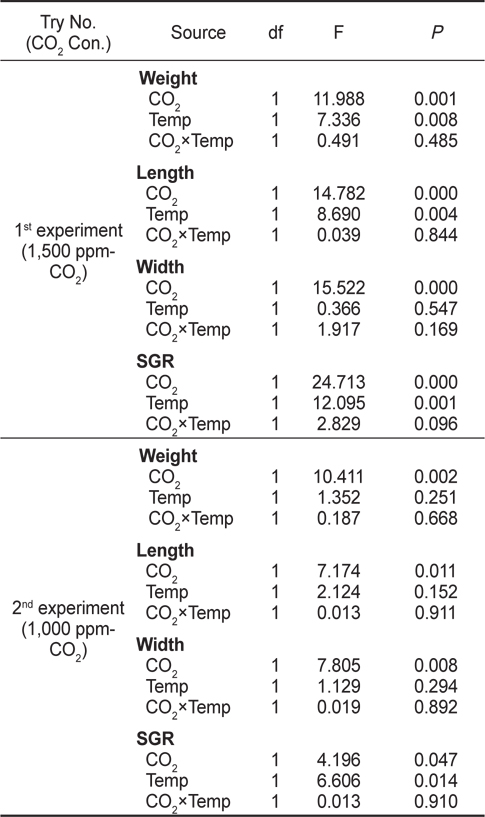
[Table 3.] Two-way ANOVA results indicating the effects of CO2 and temperature on growth rates
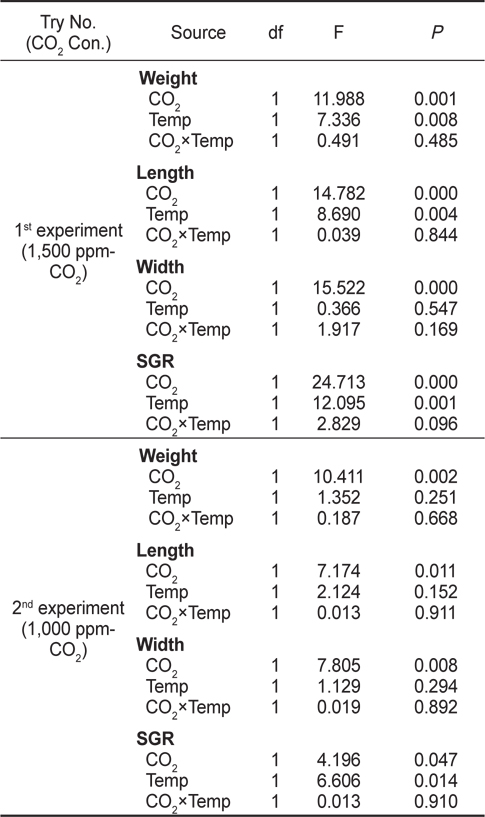
Two-way ANOVA results indicating the effects of CO2 and temperature on growth rates
Harris et al. (1999)는 pH에 의해 전복류
해수 CO2증가에 의한 pH저하환경에서 전복치패에서 나타난 성장반응과 유사하게 다른 석회화 생물들에게도 성장이 저해되는 예를 찾아볼 수 있다(Berge et al., 2006, Gazeau et al., 2007; Kuroyanagi et al., 2009; Lischka et al., 2011; Parker et al., 2013). Kuroyanagi et al. (2009)은 pH 7.7-8.3 범위에서 10주의 기간 안에 유공충
본 연구는 전복치패의 성장이 해양산성화에 의하여 억제되고 수온상승에 의하여 성장이 촉진되며 해양산성화 및 수온상승과의 상호영향에 의해 다소 완화되는 것을 확인하였다. 추후 패각의 CaCO3함량변화 및 패각구조 등 패각의 광물적 특성에 대한 분석을 통해 해양산성화 및 수온상승환경의 상호 작용기작에 대한 세부적인 검토가 이루어져야 할 것으로 사료된다. 또한 해양산성화 및 수온상승이 해양생태계 전반에 어떻게 작용하는가에 대한 이해를 위해서는 개별 생물의 생애주기에 걸쳐 나타나는 각각의 영향을 감지하고 그것이 생태계에 어떤 영향으로 작용하는가에 대해서 지속적인 연구가 필요할 것이다.