전 세계적으로 화석에너지 고갈과 지구온난화 대응을 위한 방안으로 환경친화성과 지속가능성이 인정된 바이오연료인 바이오디젤의 생산 및 보급이 급격히 증가하고 있다[1]. 동물성기름이나 식물성 오일을 알코올과 촉매 존재 하에 반응시켜 생산되는 바이오디젤은 재생 가능한 생물학적 연료로서 화석연료의 대체 연료로 사용이 가능하다[2]. 바이오디젤의 주성분인 지방산메틸에스테르(Fatty Acid Methyl Ester, FAME)가 디젤기관 연료로 검증된 1990년대 초부터 바이오디젤 생산에 대한 연구가 본격적으로 진행되었다. 바이오디젤은 탄소중립연료(carbon-neutral fuel)로 지구온난화에 영향이 작고 일산화탄소, SOx, 미세분진 등의 유해가스 배출이 석유계 디젤보다 훨씬 적어 많은 나라에서 5~20% 바이오디젤 혼합 경유가 보급되고 있으며 일부 유럽국가에서는 100% 바이오디젤을 경유 차량에 사용하고 있다[3-4]. 바이오디젤의 부산물인 글리세롤 또한 의약품, 식품 및 플라스틱의 원료로 활용하기 위한 연구가 활발히 진행되고 있다[5].
바이오디젤 생산 반응은 크게 세 가지로 분류가 되는데 효소 촉매이용법과 초임계유체법, 전이에스테르화법으로 나눌 수 있다. 효소촉매이용법은 전이에스테르화보다 온화한 조건에서 높은 선택도를 갖는 이점이 있지만 전환율을 높이기 위해서는 반응시간이 길다는 단점을 갖는다. 초임계유체법은 반응 속도가 매우 빠르지만 고온, 고압 반응으로 인해 설비비가 높은 단점이 있다. 현재 가장 보편적인 바이오디젤 생산 방법은 염기촉매를 이용한 트리글리세리드와 알코올을 혼합하여 반응하는 전이에스테르화법이다[6].
식물성 바이오디젤의 원료로는 대두유, 유채유, 팜유, 해바라기유, 자트로파유 등이 있다. 식물성 바이오디젤은 토지 기반으로 원료 작물 재배가 제한적이며 원료 가격이 높게 형성되어 바이오디젤 생산비를 증가시키는 요인으로 작용하며, 식량 및 토양 자원과 에너지 작물 자원의 경쟁이 유발되어 다양한 윤리적 문제들이 보고되고 있다[7,8]. 바이오디젤 생산량이 급격히 증가함에 따라 저가 원료유의 안정적 공급이 매우 중요하게 부각되고 있다. 부족한 원료유를 공급하기 위해 신규 미활용 유지 자원에 대한 다양한 검토가 진행되고 있으며, 알래스카 및 동남아시아의 수산업에서 발생하는 오일 자원의 활용이 검토되고 있다. 생선 부산물로 매년 약 백만톤이 발생되며, 이중 일부는 어분과 오일로 활용되지만 약 60%는 활용되지 않고 있다. 생선 부산물인 생선 머리, 내장, 뼈에는 다량의 오일이 함유되어 있다[9]. 바이오디젤에 대한 대부분의 연구는 식물성 오일에 초점을 맞추고 있으며 동물성 오일, 특히 어유를 이용한 연구는 매우 부족한 상황이다. 이러한 미활용수산 자원에서 어유를 수득하여 바이오디젤의 원료로 활용하기 위한 연구가 필요하다[10].
본 연구에서는 미활용 유지로 베트남산 메기에서 추출한 어유를 이용한 바이오디젤 생산에 대한 연구를 수행하였다. 바이오디젤 생산 반응의 주요 불순물인 유리지방산(Free Fatty Acid, FFA)을 효율적으로 제거하기 위해 어유의 정제 전처리로서 에스테르화 반응을 실시하고, 반응 변수별 영향을 조사하였다. 바이오디젤 생산 반응인 전이에스테르화 반응에 대한 3종의 염기촉매의 영향을 조사하고 반응 조건을 결정하여 어유 바이오디젤을 제조하였으며 그 물성을 평가하여 다른 동물성 및 식물성 바이오디젤과 비교 분석하였다[11,12].
실험에 사용된 오일은 GS바이오社로부터 공급받은 어유(베트남, 메기류)로 유리지방산 함량이 4%였다. 유리지방산을 제거하기 위한 에스테르화 반응에 세 가지 촉매를 사용하였다. 비균질 고체 촉매로 Rohm&Haas社의 Amberlyst-15와 Amberlyst BD-20을 사용하였으며 균질계 산촉매로는 OCI社의 95% 황산을 사용하였다. 알코올은 덕산社의 순도 99.8%의 무수메탄올을 에스테르화 반응 및 전이에스테르화 반응에 사용하였다. 전이에스테르화 반응에는 세 가지의 염기촉매를 사용하였다. DC Chemical社의 95% KOH, OCI社의 98% NaOH, 삼천 社의 97% NaOCH3를 GR grade로 구입하여 전이에스테르화 반응을 실시하였다. 에스테르화 반응과 전이에스테르화 반응실험에 사용된 반응장치는 중탕가열과 교반을 위해 실리콘오일 항온조와 마그네틱 바를 이용하였으며 반응기로는 메탄올 증발 방지를 위해 컨덴서가 설치된 2구의 50 mL 둥근바닥 플라스크를 사용하였다.
GS바이오社로부터 공급받은 어유는 산가 9.0 mgKOH/g, 수분 0.1092%로 전처리과정을 필요로 하여 황산, 고체 산촉매 및 메탄올을 이용하여 에스테르화 반응을 65 ℃에서 120분간 반응하여 유리지방산 제거율을 조사하였다[13,14]. 황산은 오일 질량 대비 1%를 투입하였으며 고체 산촉매인 Amberlyst-15, Amberlyst BD-20는 20%를 투입하였고 교반속도 400 rpm, 반응온도 65 ℃, 메탄올은 오일 질량 대비 20%로 동일한 조건에서 반응을 실시하였다. 황산 및 메탄올을 이용한 에스테르화 반응에서 황산 투입량 및 메탄올의 투입량을 변경하여 반응을 실시하였다. 황산 투입량을 오일 질량 대비 0.4, 0.6, 0.8, 1 wt%를 사용하였으며 메탄올은 오일 질량 대비 26.7%, 반응온도 65 ℃, 반응시간 180분, 교반속도 400 rpm으로 동일한 조건으로 반응하였다. 메탄올 투입량 변경실험에는 오일 질량 대비 15, 20, 25, 30 wt%로 메탄올을 투입하였으며 황산 1%, 반응온도 65 ℃, 반응시간 180분, 교반속도 400 rpm으로 동일한 조건으로 반응하였다. 황산 및 메탄올 투입량 변경실험 모두 20분 간격으로 샘플링하여 산가측정을 통해 유리지방산의 제거율을 살펴보았다.
전이에스테르화 반응에 대한 촉매 영향 조사를 위해 KOH, NaOCH3, NaOH 촉매를 각각 오일 질량기준 0.9%를 오일대비 33% 메탄올에 용해시킨 후 투입하여 65 ℃, 400 rpm의 조건에서 60분간 반응하였다. 반응 초기의 촉매영향을 살펴보기 위해 반응시작 후 1, 3, 7분 시점과 10분 간격으로 시료를 채취하였다. 반응혼합물 채취 시료는 0.1 N HCl 수용액(반응중지제)을 미리 투입해 놓은 시료병에 채취하자마자 흔들어 반응을 중지시킨 후 15,000 rpm에서 3분간 원심분리하여 오일의 중간층에서 GC 분석을 위한 시료를 채취하였다. 전이에스테르화 반응에 대한 원료 오일의 산가(유리지방산 함량) 영향 조사 실험에서는 전처리하여 유리지방산을 제거한 어유와 미전처리 어유를
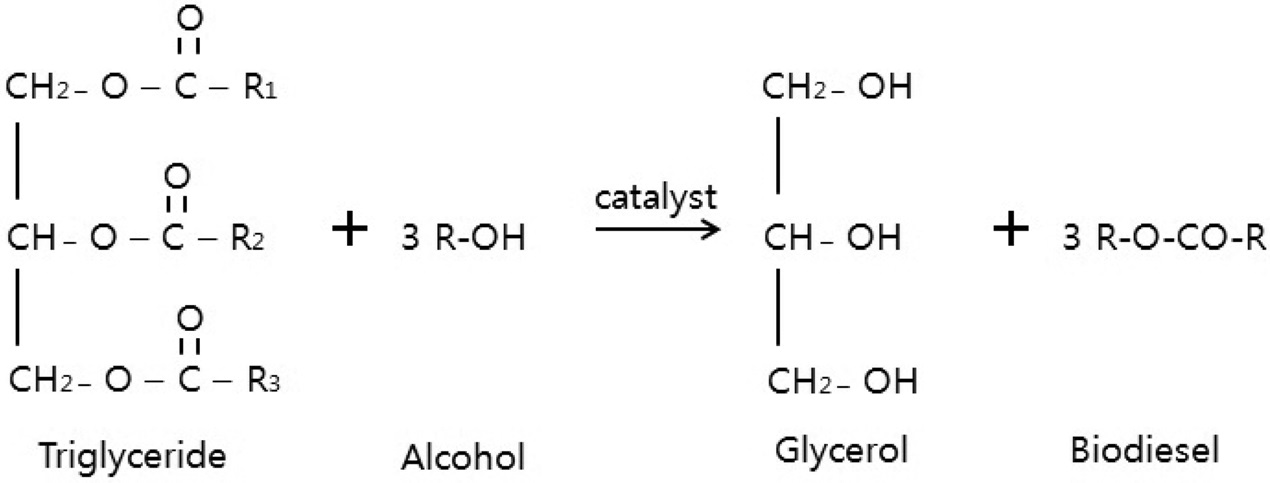
혼합하여 원료 오일의 산가를 1, 3, 5로 제조한 후 KOH 0.8 wt%, 메탄올 33 wt%, 반응시간 60분, 반응온도 65 ℃로 동일하게 적용하여 전이에스테르화 반응을 수행하여 FAME 분석을 실시하였고, 전이에스테르화 반응에 대한 반응온도 영향 조사실험에서는 60, 70, 80 ℃의 반응온도에서 KOH 0.8 wt%, 메탄올 33 wt%로 동일하게 적용하여 20분 간격으로 샘플링 후 FAME분석을 실시하여 바이오디젤 전환율을 살펴보았다. 염기촉매 투입량 변경실험은 KOH 0.3, 0.6, 0.9 wt%로 설정 후 메탄올 33 wt%, 반응온도 65 ℃로 동일하게 적용하여 60분간 반응을 실시하였다. 메탄올 투입량 변경실험에서는 오일대비 4 : 1, 6 : 1, 9 : 1, 12 : 1로 투입하여 반응시간 60분, KOH 0.9%, 반응온도 65 ℃, 교반속도 400 rpm으로 반응을 실시하였다. 바이오디젤 생산 반응 후 250 ℃에서 진공상태로 추가적으로 바이오디젤의 증류 정제를 진행하였다. 바이오디젤의 제조 반응인 전이에스테르화(trans-esterification) 반응은 트리-글리세리드(tri-glyceride) 한 분자와 메탄올 한 분자가 에스테르교환 반응을 통해 1개의 지방산메틸에스테르와 1개의 다이-글리세리드(di-glyceride)를 만들고 생성된 다이-글리세리드가 메탄올과 반응하여 1개의 모노-글리세리드(mono-glyceride)와 1개의 글리세롤 분자를 생성하는 3단계의 가역반응으로 총괄반응은 다음 Figure 1과 같이 표현된다.
원료와 반응물의 수분함량 분석은 Karl Fisher 분석방법으로 분석되었으며 산가(Acid Value, AV) 분석은 EN ISO 661 (Animal and vegetable fats and oils-Preparation of test sample)의 표준 분석법에 의해 분석되었다. 산가는 1 g의 시료 내에 함유된 Free Fatty Acid를 중화시키는데 필요한 수산화칼륨의 mg수로 정의되며 산가와 유리지방산 함량 계산법은 다음과 같다[15,16].
V : Volume of KOH solution (mL)
c : Molar concentration of KOH solution (mol/L)
m : Mass of sample (g)
FFA : Free fatly acid, AV : Acid value
FAME함량 분석은 EN 14103 분석법에 따라 Agilent 6890 capilliary gas chromatograph로 분석하였다[17-19]. 글리세롤(glycerol), 모노글리세리드(mono-glyceride), 다이글리세리드(di-glyceride), 트리글리세리드(tri-glyceride), 총글리세롤(total glycerol) 함량 분석은 EN 14105 분석법에 따라 Agilent 6890 on-columm gas chromatograph로 분석하였다. 필터막힘점(Cold Filter Plugging Point, CFPP) 분석 장치를 이용하여 저온유동성 분석을 실시하였으며, 산화안정성 분석은 EN 14112에 따라 Metrohm사의 743 Rancimat를 이용하여 분석하였다.
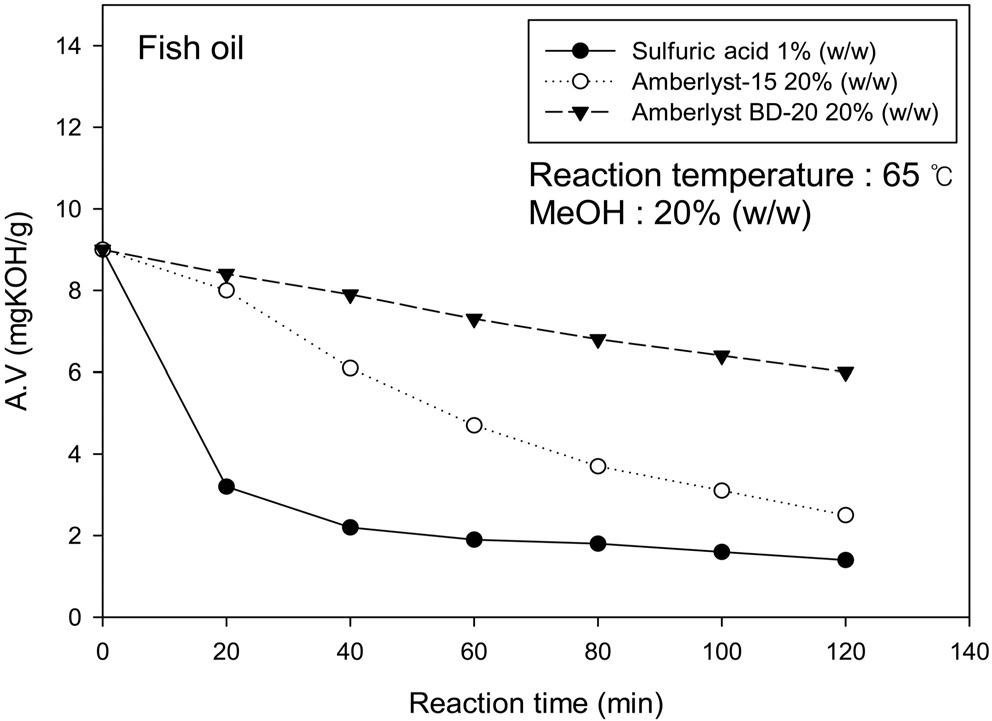
유리지방산 제거를 위한 에스테르화 반응 중 세 가지 촉매의 영향을 살펴본 결과를 Figure 2에 나타내었다. 황산이 유리지방산 제거에 있어 가장 높은 제거율을 나타내었으며 고체촉매인 Amberlyst-15와 Amberlyst BD-20은 낮은 유리지방산 제거율을 나타내었다. 고체인 Amberlyst-15와 Amberlyst BD-20은
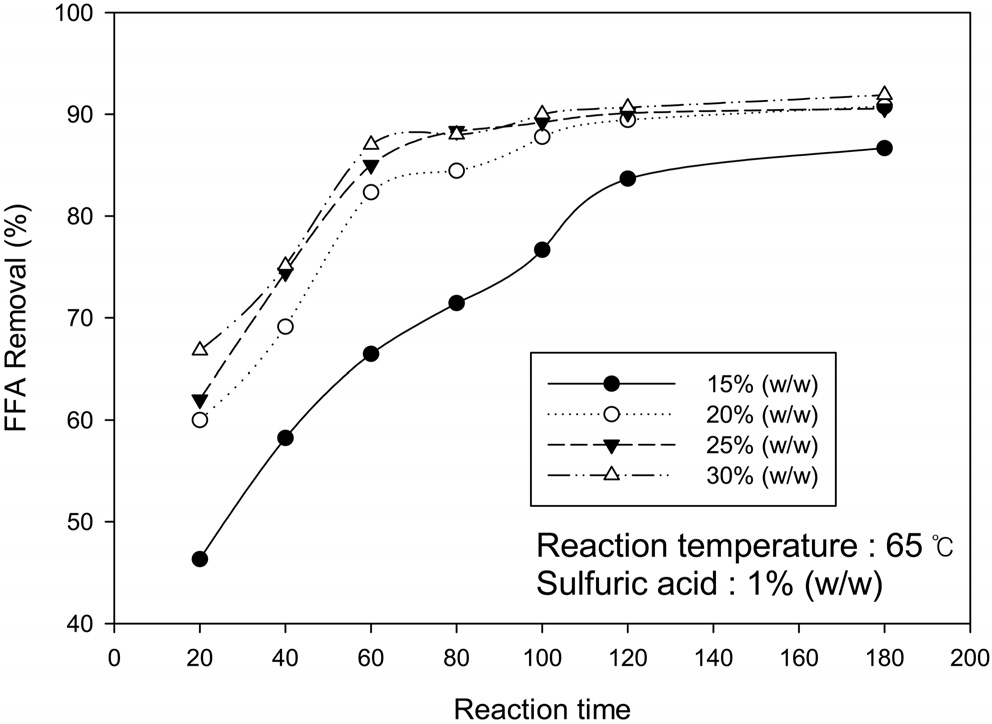
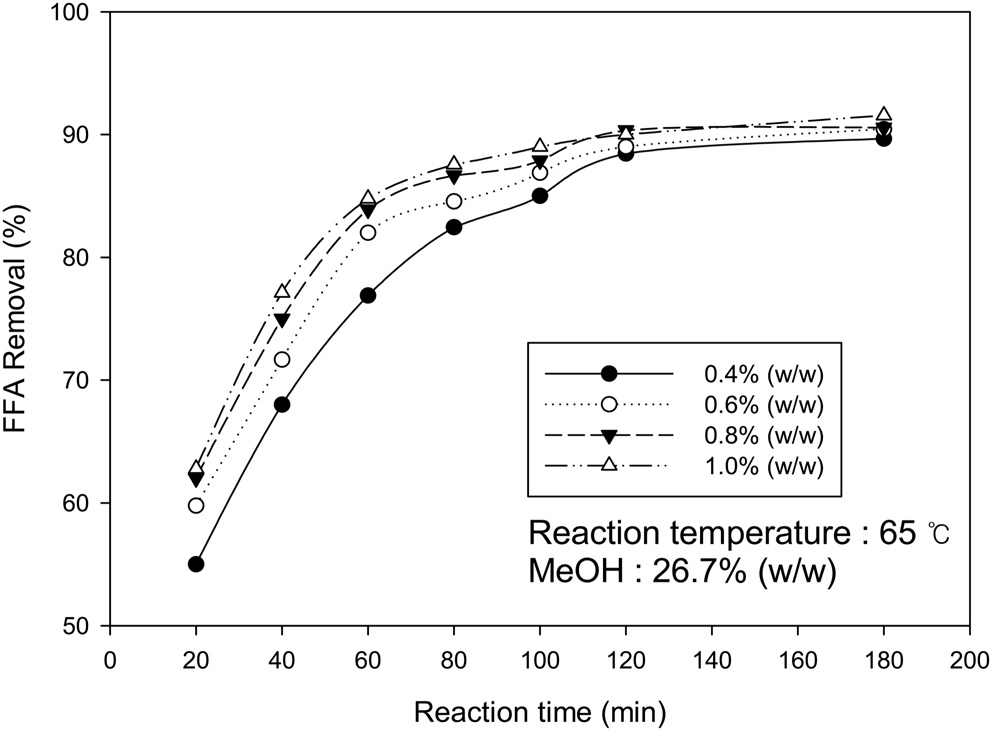
액체인 황산보다 반응표면적이 더 적어 활성도가 떨어지는 것으로 판단된다. Amberlyst-15는 Amberlyst BD-20보다 활성도가 좋지만 전처리로 사용하기에는 반응시간이 액체 산 촉매에 비해 반응시간이 길고 촉매의 회수에도 어려움이 있어 에스테르화 반응의 촉매로는 부적합한 것으로 판단된다. 알코올 투입량을 변경하여 조사한 결과에 대한 그래프를 Figure 3에 나타내었다. 메탄올이 과량으로 투입될수록 유리지방산 제거율이 높았으며 메탄올 투입량 15%일 때 낮은 유리지방산 제거율을 나타났고 메탄올 투입량 25%와 30%는 반응시간 초기 20분에서만 유리지방산 제거율이 차이가 나고 반응시간이 지날수록 유리지방산 제거율은 큰 차이를 보이지 않았다. 메탄올 투입량 30%와 25%에서 제거율이 큰 차이를 보이지 않아 메탄올 25%를 투입하는 것이 바이오디젤 생산 단가 측면에서 효과적이라 판단된다. 황산 촉매 투입량 변경실험 결과에 대한 그래프를 Figure 4에 나타내었다. 황산 투입량이 에스테르화반응에 미치는 영향 역시 알코올과 같이 과량으로 투입될 때에 높은 유리지방산 제거율을 보였으며, 0.4%가 가장 낮은 유리지방산 제거율을 보였다. 반응시간이 지날수록 유리지방산 제거율의 차이는 줄어드는 것을 알 수 있었다.
염기촉매의 종류 및 촉매 투입량, 메탄올 투입량에 따른 전이에스테르화 반응 결과를 Figure 5에 나타내었다. 가장 높은 FAME함량을 나타낸 염기촉매는 NaOCH3로 나타났지만 부분적으로 FAME 및 글리세롤이 고형화 되는 현상을 나타내었다. 반응 초기 촉매별 실험에서 KOH, NaOH, NaOCH3가 FAME 전환율에서 큰 차이를 보이지 않았다. NaOH, NaOCH3의 경우 메탄올양이 적고 염기촉매의 양이 많을수록 비누화가 진행되어 FAME 및 글리세롤이 고형화가 진행되는 경향을 보여 어유를 이용한 바이오디젤 생산 염기촉매로 NaOH, NaOCH3는 부적합한 것으로 판단된다. 고형화 된 바이오디젤을 Figure 6에 나타내었다. KOH의 경우 FAME 및 글리세롤의 상분리가 명확히 일어났으며 반응변수에 상관없이 고형화가 일어나는 현상이 일어나지 않았으며 94% 이상 높은 전환율을 나타내어 어유 바이오디젤 생산 반응의 염기촉매로 적합한 것으로 판단된다.
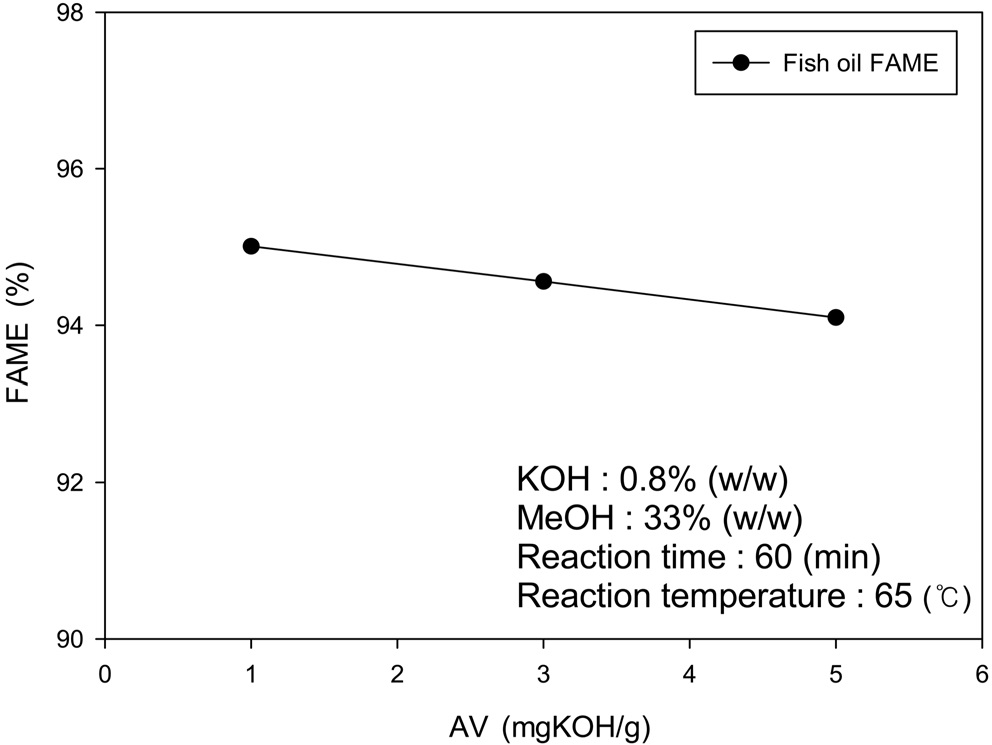
원료 오일 중의 유리지방산 함량이 전이에스테르화 반응에 미치는 영향 조사 결과를 Figure 7에 나타내었다. 산가가 낮을수록 높은 FAME 전환율을 나타내었으며, 산가 1 mgKOH/g일 때 95% 이상의 높은 FAME함유량을 나타내었다. 산가 3 mgKOH/g 및 5 mgKOH/g도 94% 이상의 FAME함량을 나타내어
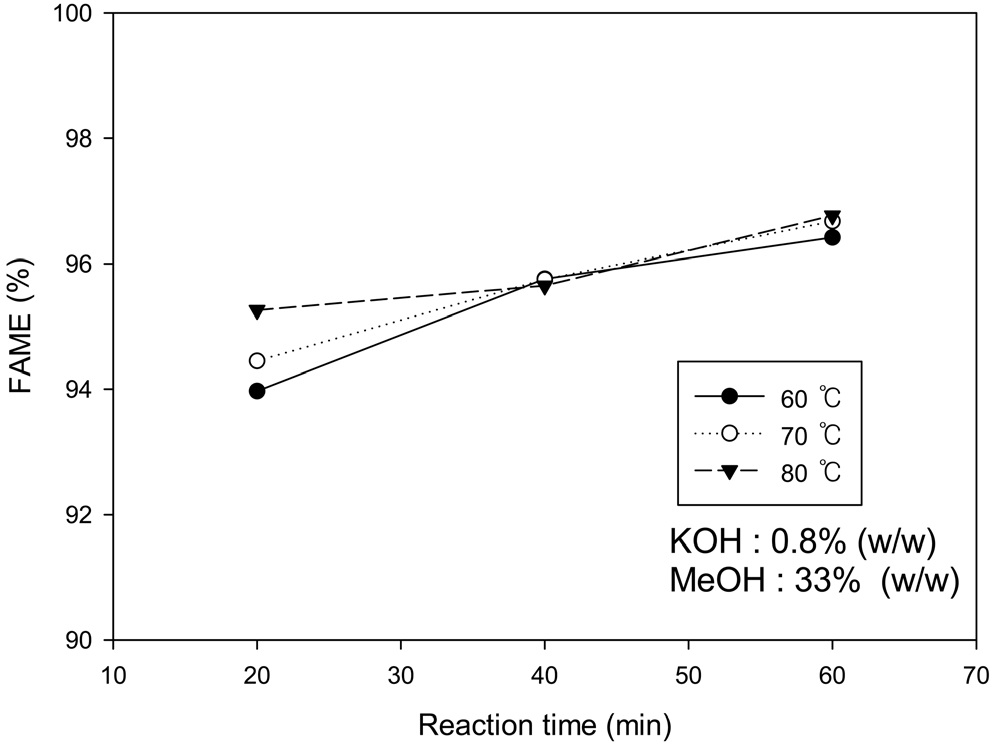
어유의 바이오디젤 전환 반응에 있어 높은 전환율을 나타내는 것을 알 수 있었다. Figure 8에 나타낸바와 같이 반응온도의 영향은 온도가 높을수록 초기 FAME 전환이 빠르게 진행되었으나 반응시간이 지남에 따라 FAME 함량의 차이는 줄고 반응시간 40분에 비슷한 FAME 함량을 나타내었다. 반응온도가 높을수록 메탄올의 활성도가 높아 초기 반응이 빠르게 진행되는 것으로 판단되며 트리글리세리드가 FAME으로 정반응에 의한 전환이 이루어지면 역반응과 평형을 이루어 비슷한 최종 전환율을 보이는 것으로 판단된다.
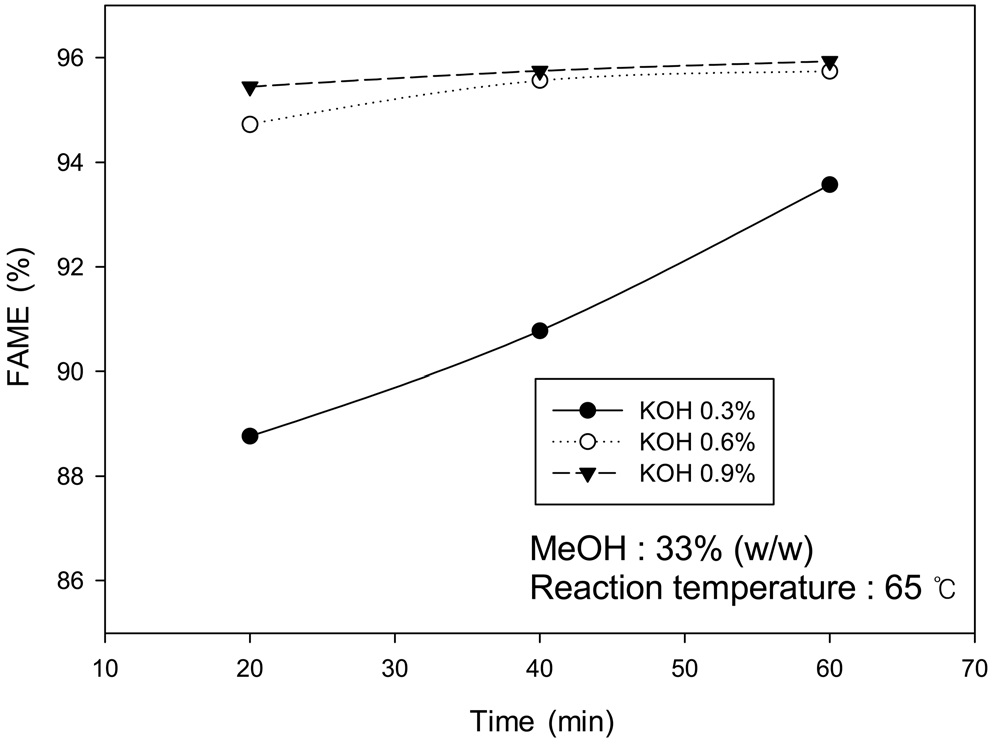
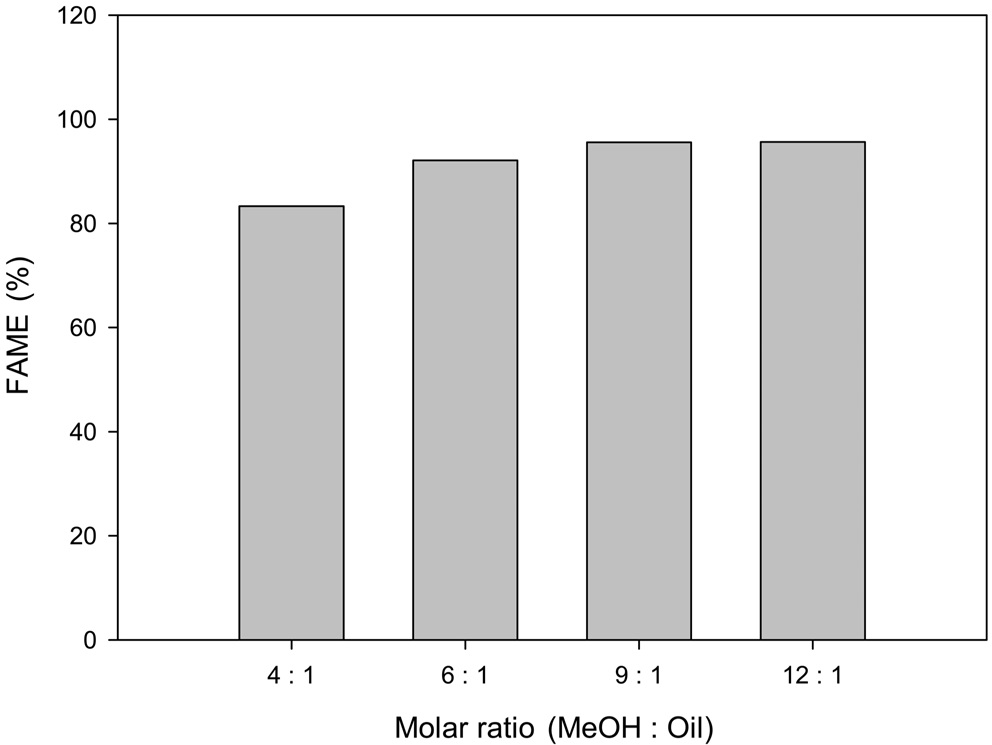
염기 촉매의 투입량 및 메탄올의 몰비가 전이에스테르화 반응에 미치는 영향에 대한 그래프를 Figure 9와 10에 나타내었다. KOH의 양이 0.3 wt%인 경우에는 FAME함량이 0.6 wt%나 0.9 wt%에 비해 매우 낮게 측정되었다. 0.6 wt%와 0.9 wt%는 반응초기인 20분에서 FAME함량이 조금 차이가 났지만 반응시간이 길어질수록 FAME함량의 차이가 좁혀지는 것을 알 수 있었다. 메탄올의 몰비 실험에서는 메탄올이 4 : 1일 때에 다른 몰비에 비해 현저히 낮은 FAME함량을 나타내었다. 6 : 1일
때에는 92% 정도의 FAME함량을 나타내었으며 9 : 1과 12 : 1에서 95% 이상을 보였으며 9 : 1과 12 : 1에서 0.1% 정도의 FAME함량 차이를 보이며 12 : 1이 가장 높은 FAME함량을 나타내었지만 바이오디젤 생산 단가를 고려할 때 9 : 1이 가장 적합한 것으로 판단된다.
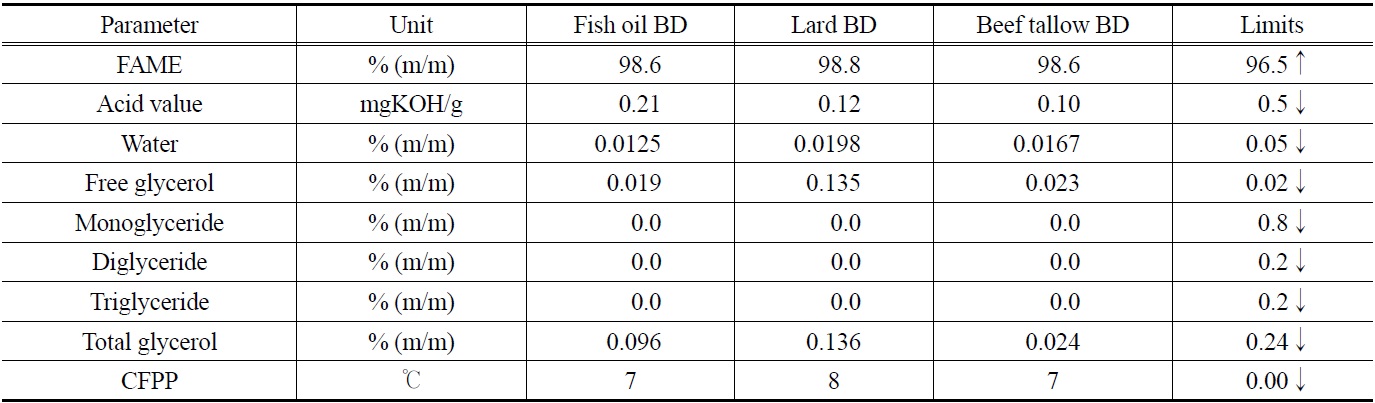
어유를 바이오디젤로 전환한 결과 산가 0.4 mgKOH/g, 수분 0.02%로 FAME함량은 95% 이상을 함유한 것으로 나타났으며 증류 후 바이오디젤에서는 0.21 mgKOH/g, 수분 0.01%로 품질규격을 만족하였다. CFPP는 7 ℃로 품질규격인 0.00 ℃ 이하를 만족하지 못하였으며 총 글리세롤도 품질규격인 0.24%를 만족하는 0.1%로 나타났다. CFPP가 낮게 측정된 원인으로는 불포화지방산의 함량이 높아 CFPP값이 낮게 측정된 것으로 판단된다. 어유 바이오디젤의 물성에 관한 분석 결과는 Table 1에 나타내었으며 어유 바이오디젤의 지방산 조성에 관한 분석결과와 참고문헌의 다른 동물성 및 식물성 바이오디젤

Comparison of bio-diesel standard quality parameters and fish & various bio-diesels properties
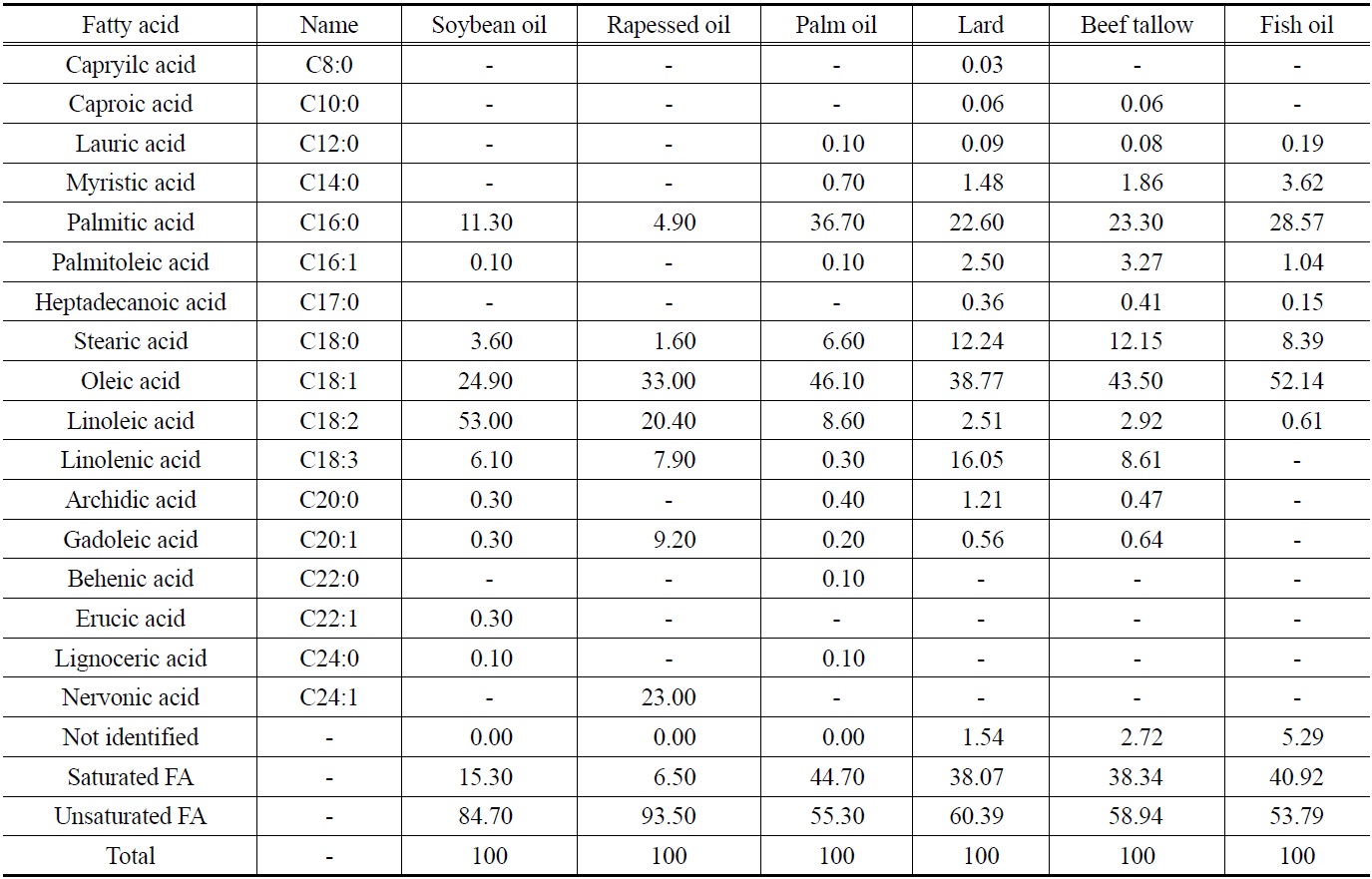
[Table 2.] Fatty acid composition of various bio-diesels
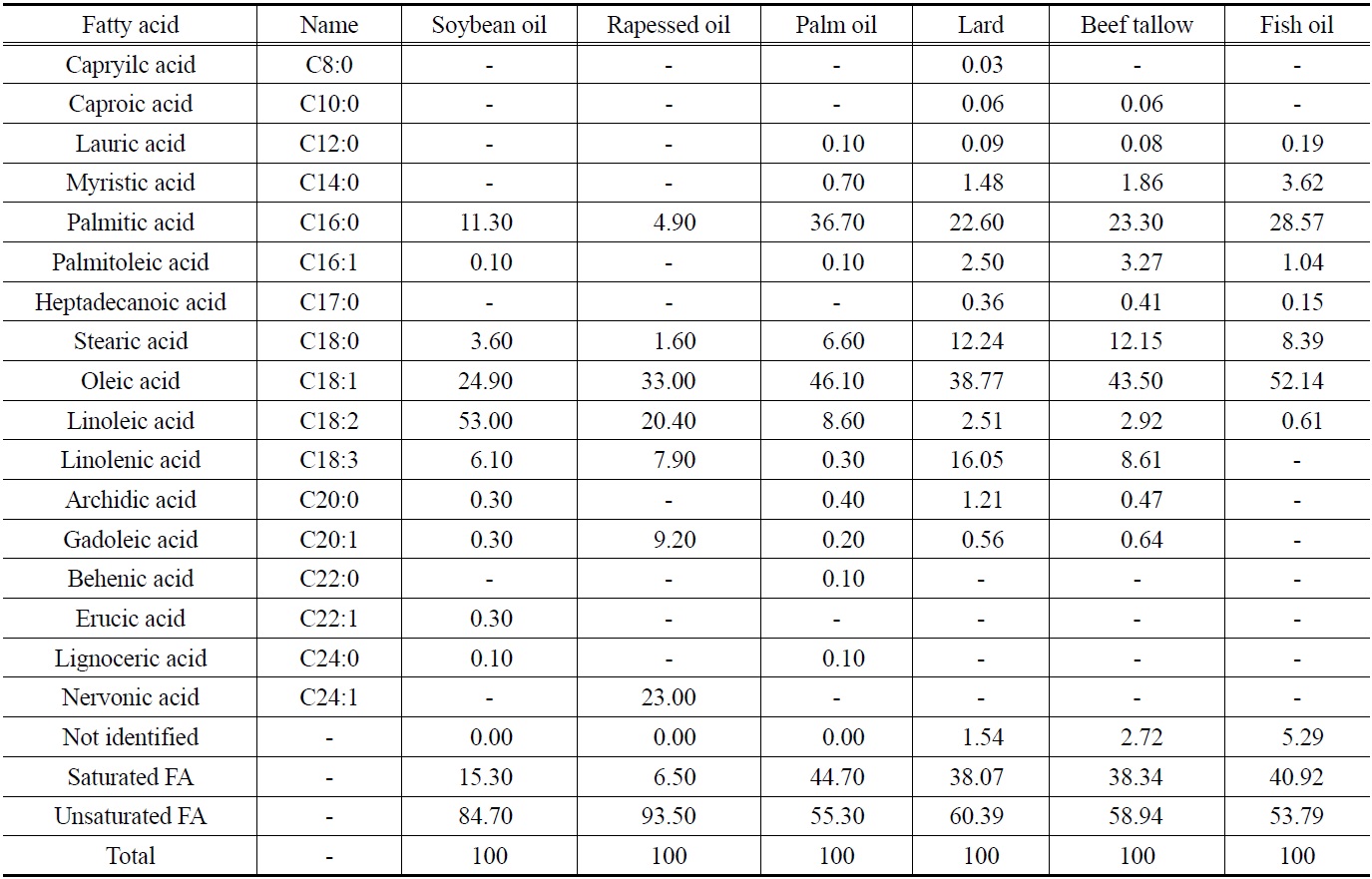
Fatty acid composition of various bio-diesels
어유 바이오디젤 제조를 위한 에스테르화 및 전이에스테르화 반응의 반응변수 영향 조사 실험을 수행한 결과 다음과 같은 결론을 얻었다.
1) 어유의 유리지방산 제거를 위한 에스테르화 반응에는 균질계 촉매인 황산이 가장 적합한 것으로 나타났다. 메탄올 30%와 황산 1%일 때에 가장 높은 유리지방산 제거율을 나타내지만 생산단가 및 공정 효율성을 고려할 때에 큰 차이를 보이지 않는 메탄올 25%와 황산 0.8%를 사용하는 것이 바이오디젤 생산 단가를 낮추는 데에 유리할 것으로 판단된다.
2) 어유를 FAME으로 전환하기 위한 전이에스테르화 반응에는 KOH가 가장 적합한 염기촉매로 나타났다. NaOCH3 및 NaOH를 사용하였을 때에 메탄올양이 적고 촉매의 양이 많아지면 글리세롤 또는 바이오디젤 및 글리세롤이 고형화가 되는 현상이 발생하였다. 이는 KOH 염기촉매에서는 나타나지 않은 현상으로 NaOCH3나 NaOH를 사용하기 보다는 KOH를 사용하였을 때에 바이오디젤 및 글리세롤의 상 분리가 원활히 진행되는 것을 확인할 수 있었다.
3) 본 실험에서의 어유 바이오디젤은 세정 및 수분증발 후 FAME 함량이 95%로서 품질규격인 96.5% 이상을 만족시키기 위해 추가적인 증류 정제가 필요하였으며 증류 결과 FAME 함량을 98.6%까지 높일 수 있었다.
4) 본 연구를 통해 베트남 메기(catfish) 추출 어유를 바이오디젤 원료로 이용 결과, 주요 품질규격을 만족하는 바이오디젤을 제조할 수 있었으며 바이오디젤 원료의 다양화에 일조할 수 있을 것으로 사료된다.