본 연구에서는 유기산과 여러 첨가제들을 사용하여 상수도의 정수장이나 배수지 벽면에 침적되어 있는 스케일 제거에 활용 할 수 있는 친환경적인 세정제를 개발하고 현장 적용을 수행하였다. 정수장의 벽면의 스케일 분석결과 산화규소(SiO2), 산 화알루미늄(Al2O3), 산화철(Fe2O3), 산화망간(MnO) 등 주로 금속산화물로 이루어져 있는 것을 알 수 있었다. 그리고 여러 유기산 중에서 말릭산(malic acid), 말론산(malonic acid), 시트릭산(citric acid)과 산화규소를 제외한 산화알루미늄, 산화철, 산화망간 등의 금속산화물에 비교적 좋은 용해력을 보여주었다. 이들 유기산들을 일정 무게비율로 배합하여 산화알루미늄, 산화철, 산화망간의 혼합 금속산화물의 용해력 실험 결과 여러 유기산 배합 비율 중 말릭산, 말론산, 시트릭산이 6 : 2 : 2 배합비율로 만든 10 wt% 유기산 혼합용액이 정수장 및 배수지의 스케일 제거효율이 약 29%로 가장 뛰어났음을 확인할 수 있었다. 이들 유기산 혼합용액에 비이온 계면활성제를 첨가하여 배합한 세정제 용액이 유기산 혼합용액만을 사용한 경우보다 더욱 높은 금속산화물 용해력을 가지는 것을 확인 할 수 있었다. 특히, 알콜에톡실레이트 계열의 LA-7 비이온계면활성제를 0.2% 첨가하는 경우 약 35%의 스케일 제거효율을 보여주었다. 그렇지만 유기산 혼합용액에 살균제를 첨가하는 경우 스케일 제거효율이 저하되었다. 이것은 계면활성제가 오염물의 유화분산 성질에 의해 스케일 제거력 향상에 도움을 주지만 살균제의 경우에는 살균제의 산화력에 의하여 스케일의 물에 대한 용해력을 떨어뜨려 스케일 제거에 방해를 하기 때문인 것으로 판단된다. 이러한 기초실험 결과를 바탕으로 유기산 혼합용액에 첨가제인 계면활성제, 살균제 등을 넣고 배합된 세정제를 사용하여 D시의 상수도 정수장 및 배수지의 스케일 세척시험에 성공적으로 적용시킬 수 있었다.
우리가 매일 가정에서 음용수나 생활용수로 사용하는 수돗물은 상수원에서 취수 후에 침전, 여과, 살균공정 및 필요에 따라 오존처리, 활성탄 처리, 고도정수처리과정을 거친 후 깨끗한 물을 정수장에서 일시 저장하고 정수장에서 송수관로를 따라 배수지에 공급하고, 그리고 배수지에서 급·배수관로를 통해 공급받고 있다. 이렇게 배달되는 수돗물의 부유물질, 냄새, 녹물 등에 의한 불신을 해소하기 위해선 정수장으로부터 가정의 수도꼭지까지의 수돗물 공급망인 송수관로, 배수지, 저수조, 급·배수관의 적절한 관리와 주기적인 세척 및 살균처리 과정이 필요하다[1].
이들 상수도 공급망 중에서 정수장과 배수지의 주기적으로 적절한 세척은 수돗물 불신을 크게 해소시킬 수 있게 기대되는 영역이다. 상수도 처리장에서 완전 정수 처리된 수돗물을 임시 저장하는 정수장과 가정이나 공장 등 수요자에게 공급하기 위하여 저장하는 배수지는 주로 에폭시수지로 코팅된 콘크리트로 구성되어 있다. 이 콘크리트 벽면에는 수돗물에 녹아있는 철, 칼슘, 마그네슘, 망간 등의 금속산화물과 조류와 같은 유기퇴적물들이 물때나 생물막을 형성하여 전염성 세균이 성장할 수 있는 서식 근거지를 만들어 주기 때문에 정수장과 배수지 벽면에 침착된 이들 물때나 생물막 퇴적물을 주기적으로 세척하고 살균 소독이 필요하다. 또한 대형건물이나 아파트 단지에서 사고 및 단수 시에도 수돗물 사용에 지장이 없도록 예비용 수돗물을 저장하는 물탱크도 주기적 세척과 살균 소독이 필요하다[2,3].
상수도의 정수장과 배수지의 바닥면이나 벽면에 생성되는 물때나 생물막은 탈착되면서 부유물을 발생시켜 수돗물의 불신을 초래하고 박테리아 같은 미생물의 좋은 성장 환경을 줄 수 있어 주기적인 세척이 필요하다. 현재까지는 국내에서는 고압수나 고농도의 무기산을 함유한 세정제로 세척하여 왔다. 그러나 국내에서 많이 사용하는 고압수 세척은 물리적인 힘에 의한 단순 세척으로 특별한 기술이 필요하지 않고 물을 사용함으로 음용수 관리에 문제점은 없으나 정수장과 배수지의 물때 및 침적 퇴적물, 그리고 조류나 퇴적물 등 생물막의 제거가 불충분하고 고압세척에 의한 에폭시 코팅물질을 훼손 할 가능성이 크며 세척에 다량의 세척수가 필요하여 물 낭비를 초래하고 세척시간이 매우 길어 가정용 급수 공급에 차질을 가져올 수 있는 단점이 많다. 그리고 고농도의 무기산을 함유한 세정제는 세정력은 탁월하여 세척시간은 빠르나 인체에 유독성이 있고 환경에 유해성이 있는 고농도의 술팜산(sulfamic acid), 염산, 인산과 같은 무기산을 사용하여 사용자의 안정성과 사용에 문제점이 있어 현장 적용에 어려운 실정이다.
이와 같이 상수도의 정수장과 배수지의 벽면과 바닥면을 세척하는 연구는 몇몇 국내외 발표된 특허를 제외하고 지금 까지 거의 이루어지고 있지 않다.
Schaal[4]은 음용수 저장조의 조류와 미생물로 이루어진 생물막과 칼슘, 철, 망간 등의 침적물들을 세정하기 위하여 술팜산(sulfamic acid), 니트로트리아세틱산(nitrotriacetic acid), 이 소프로판올(isopropanol, IPA) 등의 화합물과 과산화아세트산 (peroxoacetic acid)와 같은 살균제로 구성된 수계세정제를 제조하고 세척하는 방법을 발표하였지만 구체적인 적용사례를 제시하지 못하였다. Schuloff et al.[4,5]가 제시한 세정제 조성물에 금속침전물과의 반응성을 높이기 위하여 과량의 염산이나 인산을 추가하는 수계세정제 조성물을 개발하였지만 이들 세정제 조성물은 인체 유해성이 있고 사용에 위험성이 있어 국내 현장 적용에 어려움이 있다.
Reimann-Philip and Schulgoff[6], Zwanziger et al.[7,8]은 물과 접촉하는 표면의 생물막과 물때를 제거하기 위하여 고농도의 NaOH나 KOH 또는 이들의 혼합물을 주성분으로 하고 다량의 과산화수소와 같은 활성산소 주개(active oxygen donor), 그리고 소량의 계면활성제, 거품방지제를 첨가제로 구성되는 강알칼리성의 조성물을 사용하여 물과 접촉하고 있는 저수조의 벽면을 1차 세정한 다음 물로 헹구고 다음에 고농도의 술팜산, 염산, 인산 등의 무기산과 시트릭산, 글리콜릭산 등의 소량의 이소프로판올, 트리에틸렌글리콜 등의 용제로 구성되는 강산성의 조성물로 2차 세정 후 헹구어 물 저수조의 벽면 생물막과 금속 침적물을 동시에 제거하는 세정제 및 세정방법을 제시하였다. 그러나 이 방법은 두 종류의 세정제를 사용 하고 두 번의 세정과 헹굼 과정으로 저수조 세척시간이 길며 다량의 세척폐수가 발생한다는 단점이 있다. 또한, 이 방법은 인체 안정성과 환경 유해성이 염려되는 고농도의 알칼리와 무기산을 사용함으로써 상수도용 정수장 및 배수지, 그리고 음용수 저장 물탱크의 벽면 및 바닥면을 처리하는 데는 부적 합하다. 그리고 Zwanziger and Reimann-Philip[7]은 이러한 화학세정을 통하여 정수장 또는 배수지 벽면에 침착된 무기물질과 유기물질을 제거함으로써 이들 물질과 염소 등의 살균제와의 반응에 따른 트리할로메탄(trihalomethane)과 같은 발암성 부산물의 발생을 줄이고 수돗물 공급과정에서 살균제인 자유염소(free chlorine) 농도값 저하를 막아 자유염소 농도 값을 일정 값 이상으로 유지할 수 있는 사례를 발표한 바 있다.
Kim[9,10]은 시트릭산, 아스코빅산, 글리콜릭산 및 글루콘 산등 유기산과 계면활성제인 도데실글리세롤 폴리에톡실레이트를 혼합하여 유기산 수계세정액을 제조하여 실험적으로 제조된 이끼와 조류제거에 어느 정도의 효과를 보여주었지만 물과 접촉하고 있는 저수조의 벽면 및 바닥면에 부착된 산화철, 산화알루미늄 등의 금속산화물을 주성분으로 하는 물때나 조류와 같은 유기퇴적물로 단단하게 벽면에 고착된 생물 퇴적막 제거 결과는 보여주지 못하였다. 이밖에 Lee et al.[11,12]은 유기산을 주축으로 하고 소량의 무기산인 염산, 계면활 성제, 살균제, 부식방지제 등을 첨가하여 옥내급수관 세척용 화학세정제를 개발하였지만 적은 양이나마 염산을 첨가하여 세정제를 만든 한계점이 있다. 그리고 Panias et al.[13]은 유기산인 옥살산(oxalic acid)을 이용하여 철산화물의 용해 메커니즘을 규명하는 연구를 수행하여 유기산이 약산이지만 스케일 제거 가능성을 보여주었다.
따라서 본 연구에서는 현재 상수도 현장에서의 고압세척, 그리고 인체 안전성이 문제시되는 무기산을 주성분으로 하는 화학세척의 문제점을 해결하고자 인체에 비교적 안전하고 생분해성이 있어 환경 친화적인 여러 종류의 유기산을 주축으로 하고 친환경 계면활성제, 살균제를 소량 첨가하여 상수도 정수장 및 배수지의 퇴적된 물때와 생물퇴적막 등의 침적스케일을 제거하는 세정제를 개발하였고[15] 이를 현장에 적용하여 보았다.
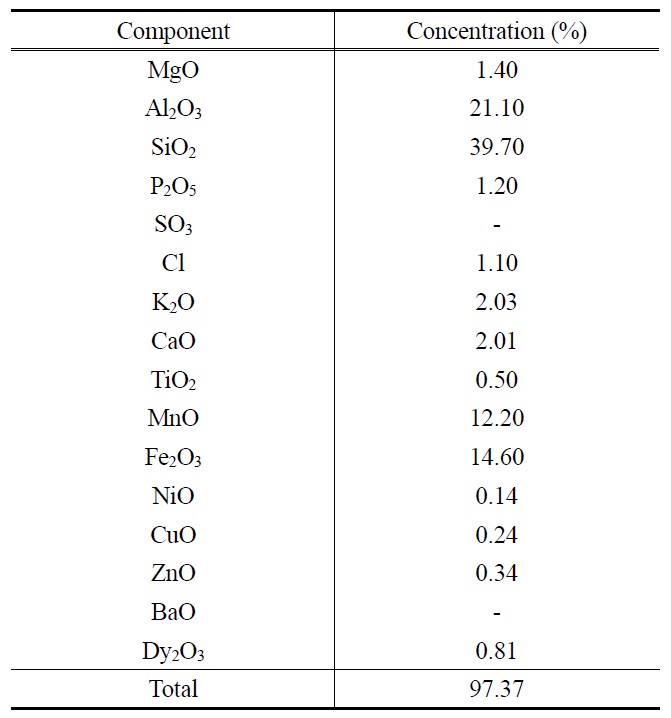
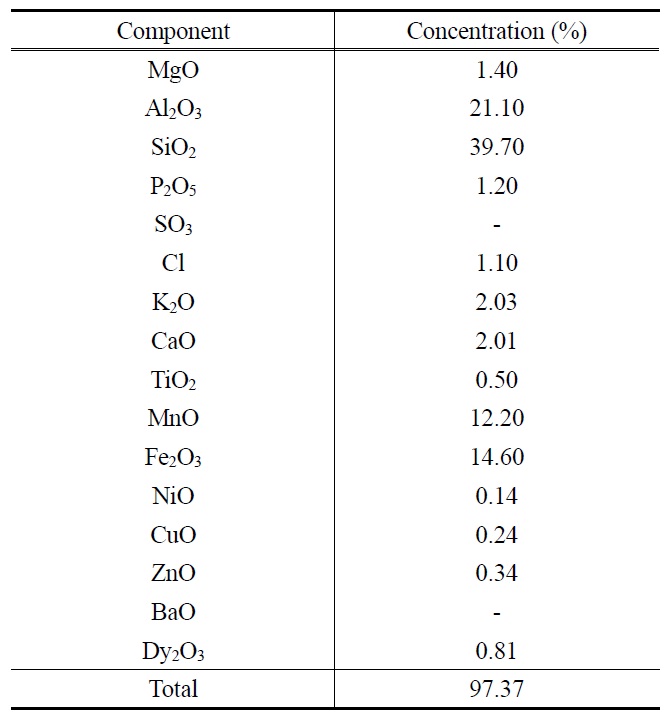
본 연구에서는 D시 정수장의 벽면에 부착된 금속산화물과 유기퇴적물로 이루어진 스케일을 채취하여 건조 후 미세분말로 만든 다음 이를 550 ℃에서 30분간 강열시켜 무게비로 약 20%되는 유기물질을 제거한 후에 3 kW X-선 발생장치(X-ray generator)를 갖춘 X선 형광분석기(Bruker AXS, SRS 3400)를 이용하여 분석한 결과를 Table 1에 나타내었다. X선 형광분 석장치(X-ray fluorescence, XRF)에 의한 측정값은 스케일 중에 어느 금속류가 어느 정도 함유되어 있는지, 어느 금속류를 많이 함유되어 있는지의 대략적인 분석자료로 Table 1에서 보는 바와 같이 정수장 스케일의 주성분은 산화규소(SiO2), 산화알루미늄(Al2O3), 산화철(Fe2O3), 산화망간(MnO) 등으로 이루어져 있는 것을 알 수 있다. 이들 금속산화물 중에 불산(HF) 이외에는 용해되지 않는 산화규소(SiO2)를 제외하고 가장 많은 비율을 차지한 산화알루미늄(Al2O3), 산화철(Fe2O3), 산화망간 (MnO)을 세척대상 오염물질로 선정하였다.
화학세정제의 주요 성분으로는 유기산을 선정하였다. 유기산은 저농도에서는 비교적 인체에 안전하고 생분해성이 있고 분자 내의 카르복실 그룹(carboxyl group, COOH-)이 스케일의 주성 분인 금속이온과 착염을 형성함으로써 금속스케일을 용해 및 제거시킬 수 있기 때문이다[13]. 예비 실험 결과 여러 유기산 중에서 금속산화물에 대한 용해력이 비교적 우수한 말릭산, 말론산,
[Table 1.] Composition of scale on the wall of the clean wall in water works
Composition of scale on the wall of the clean wall in water works
시트릭산(Samchun Pure chemical Co., Ltd)을 선정하고 이를 순수에 희석하여 금속산화물의 용해력 측정 실험을 진행하였다. 그리고 이들 혼합 세정제 조성물에 세척된 오염물의 탈착 촉진 과 재부착 방지 목적으로 첨가제로 생분해가 용이하고 친환경적인 알콜에톡실레이트 계열의 LA-2, LA-3, LA-7, LAE-5, LAE-7 (Honam Petroeum Chemical Co., Ltd)와 솔비탄에스테르계열의 Tween 60 등의 친환경 비이온계면활성제 그리고 살균제로 잘 알려지고 상수도에 이용되고 있는 차아염소산나트륨(NaClO, sodium hydrochlorite), 차아염소산칼슘(Ca(ClO)2, calcium hydrochlorite), H2O2 (Samchun Pure Chemical Co., Ltd) 등의 살균제를 이들 유기산에 첨가하여 금속산화물 용해력의 영향을 비교 평가하였다.
용해력 측정 실험에서 유기산을 주성분으로 하고 필요한 경우 계면활성제 또는 살균제를 첨가하여 세정제 조성물을 만들어 사용하였다. 세정제 조성물 제조시에 단일 유기산 또는 두가지 종류 또는 세가지 종류의 유기산 혼합물을 만들고 필요 시에 수산화나트륨을 사용하여 pH를 중성에 가깝게 적절히 조절하여 완충용액의 성질을 띠게 하였다. 이러한 완충용액은 세정액에 다른 물질이 첨가되면서 pH가 급격하게 증가 또는 감소하는 것을 방지할 수 있다.
세정제 조성물의 용해력 평가 실험에서는 세정대상 오염물질로 스케일의 주성분인 알루미늄, 철, 망간 등 금속산화물을 Table 1의 구성 배율비로 1 g의 혼합금속산화물 시료를 만들고 세정제 조성물에 주입 후 상온에서 1시간 교반 후에 세공크기(pore size)가 1 μm인 여과지로 감압?여과 하였다. 그리고 105 ℃ 에서 15분간 건조 후 무게를 측정하여 건조 전과 건조 후의 무게를 비교함으로 용해력을 측정하여 혼합금속산화물의 용해력이 가장 좋은 세정제조성물을 선정하였다.
세정제 조성물의 혼합금속산화물의 용해효율은 초기 혼합 금속산화물의 무게와 세정제와 접촉 후 잔류 혼합금속산화물 의 무게를 비교하여 식 (1)과 같은 계산 방법을 이용하였다.
E = removal efficiency of mixed metallic oxide by cleaning agent
Wi = weight of initial metallic oxide before cleaning
Wr = weight of remaining metallic oxide after cleaning
앞서 실험한 결과 중 가장 좋은 배합비율을 보인 배합 후보 세정제에 계면활성제 및 살균제의 종류 및 첨가량에 따른 영향을 알아보기 위한 실험을 진행하였다. 계면활성제의 영향을 알아보기 위하여 친환경 비이온 계면활성제인 LA-2, LA-3, LA-7, LAE-3, LAE-5, LAE-7, Tween 60을 선정하여 농도와 pH를 변화시켜 혼합금속산화물의 용해력 변화를 측정하였다. 또한 살균제에 따른 영향을 실험하기 위하여 배합 후보세 정제에 NaClO, Ca(ClO)2 H2O2 등의 살균제를 선정하여 용해력 평가를 진행하였다[14].
2.4. 최적 배합 세정제 조성물의 혼합금속산화물 용해력 평가 및 현장 적용 연구
앞서 진행했던 용해력 평가실험과 유기산 배합비율과 계면 활성제, 살균제 등의 첨가제 선정 실험 결과를 토대로 최적배 합세정제 조성물들을 제조하여 D시의 정수장과 배수지 세척 실험을 진행하였다.
3.1.1. 단일 유기산의 금속산화물 용해력 평가 실험
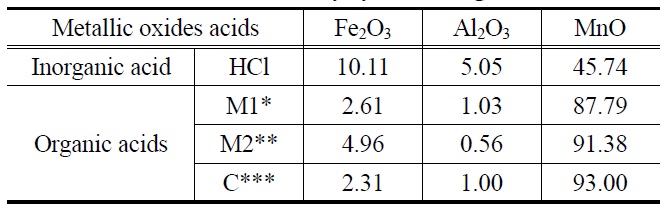
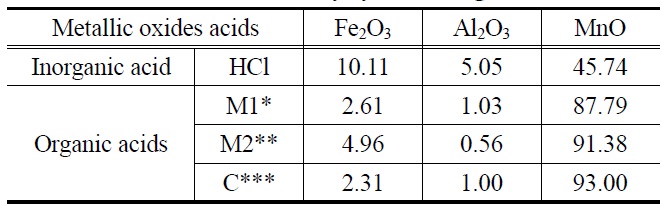
배합세정제의 제조에 앞서 세정제의 주성분을 결정하기 위해 여러 종류의 유기산을 각각 초순수에 희석하여 상수도 정수장과 배수지의 스케일의 주성분인 금속산화물의 용해력 평가 실험을 하였다. Table 2에 10 wt%로 희석한 여러 유기산과 염 산의 산화망간, 산화철, 산화알루미늄의 용해력 평가 결과를 나타내었다. Table 2에서 보는 바와 같이 산화망간의 경우 모든 유기산들이 염산보다 높은 용해력을 보여 주었다. 이에 비하여 산화철과 산화알루미늄의 경우 단일 유기산들은 염산에 비하여 높은 용해력을 보여주지 못하였다. 그러나 염산은 이들 금속산화물에 대한 용해력은 뛰어나지만 매우 강한 산성을 나타내므로 친환경세정제와 부합하지 않아 본 연구에서 개발하고자하는 배합후보세정제의 원료 물질 후보에서 제외시켰다. 그리고 유기산 중에 옥살산은 산화망간과 반응을 하여서 수산 망간(manganese oxalate)라는 침전물질을 형성하여 이후의 연구에서는 옥살산을 원료 후보물질에서 배제하였다. 따라서 말
[Table 2.] Metallic oxides solubility by various organic acids and HCl
Metallic oxides solubility by various organic acids and HCl
릭산(M1),말론산(M2), 시트릭산(C) 등의 유기산이 산화망간 등 금속산화물에 대하여 비교적 좋은 용해력을 보여 본 연구에서 개발하고자 하는 배합 세정제의 주요 원료 성분으로 선정하여 실험을 수행하였다. 그리고 유기산의 경우 10 wt% 이상의 농도에서는 유기산의 수용성도 떨어지고 금속산화물에 대한 용해력의 증가가 정체되어 이후의 연구에서는 유기산 조성물 전체의 농도를 10 wt% 이하의 농도로 제한하여 실험에 임하였다[10].
3.1.2. 단일 유기산의 혼합금속산화물(mixed metallic oxides)의 용해력 평가 실험
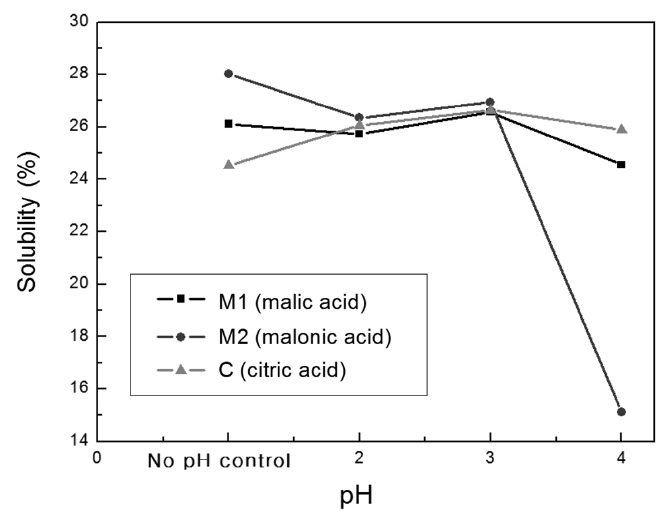
상수도 정수장 및 배수지 스케일 오염물의 경우 불산 이외에는 용해되지 않는 산화규소를 제외하고 가장 많은 비율을 차지한 산화철, 산화망간 그리고 산화알루미늄의 금속산화물 3가지를 Table 1의 배합 비율로 혼합한 금속산화물(mixed metallic oxides)을 제조하여 pH를 변화시키면서 혼합금속산화물에 대한 용해력 평가를 진행하였다. 이때 유기산의 pH 조절은 유기산에 수산화나트륨을 첨가하여 만들어진 완충용액을 통하여 이루어 졌다. 이러한 완충용액은 세정액에 산이나 염기와 같은 다른 물질이 첨가되어도 pH가 급격하게 감소 또는 증가하는 것을 방지 할 수 있다. 이렇게 유기산으로 제조된 세정액은 정수장 및 배수지의 스케일에 함유된 금속산화물과 킬레이트 반응을 일으키면서 스케일을 제거가 가능한 것으로 판단된다[13]. 유기산의 혼합 금속산화물에 대한 용해력 평가 실험결과를 Figure 1에 나타내었다. Figure 1에서 보는 바와 같이 말릭산과 시트릭산의 경우
pH가 4까지 증가하여도 낮은 pH에서와 같이 용해력을 유지해주고 있음을 보여 주었지만 말론산의 경우 pH가 3 이상으로 증가함에 따라 급격히 용해력이 감소하는 것을 볼 수 있다.
3.2. 유기산 혼합용액에 의한 혼합금속산화물의 용해력 평가 실험
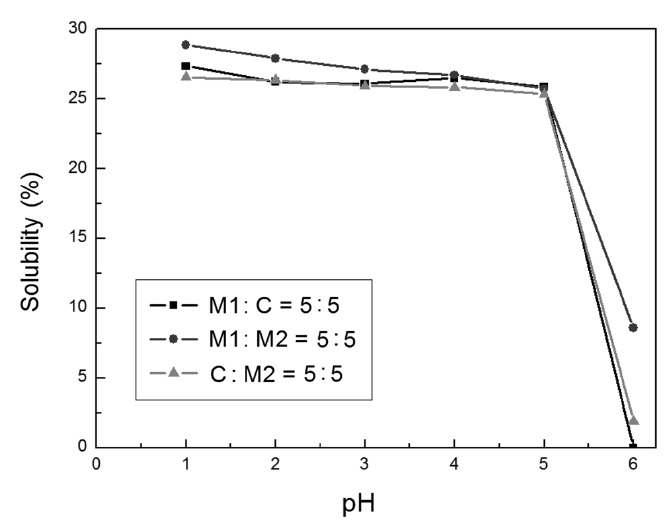
금속산화물에 대한 용해력이 비교적 좋은 말릭산, 말론산, 시트릭산 중에서 두 종류의 유기산을 취하여 이들 배합비율을 5 : 5로 하여 제조한 10 wt% 유기산 혼합용액에 pH 변화에 따른 혼합금속산화물의 용해력 평가를 진행하였고 실험 결과를 Figure 2에 나타내었다. Figure 2에서 보는 바와 같이 말릭산을 주축으로 한 유기산 혼합 용액이 비교적 금속산화물 용해력이 뛰어나고 pH 6에서는 유기산 혼합용액의 용해력이 모두 급격히 감소하는 것을 알 수 있다. 다음에 말릭산, 말론산, 시트릭산 등 세 종류의 유기산을 배합 비율을 달리하여 pH 조절 없이 혼합금속산화물의 용해력 평가를 진행하였다. 배합비율 및 용해력 평가결과를 Table 3에 나타내었다. Table 3에
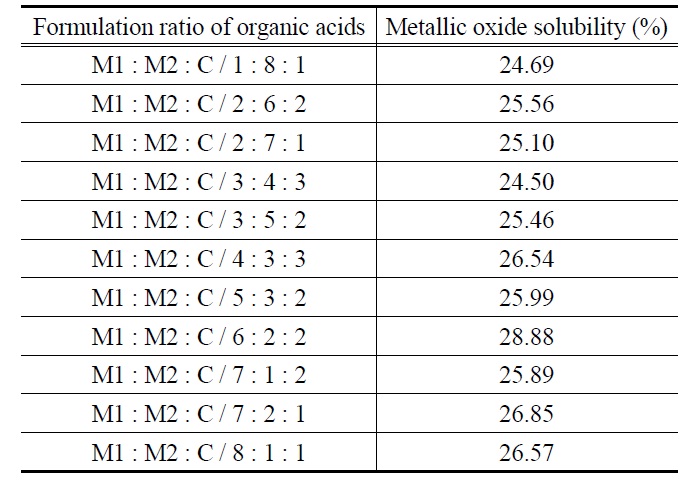
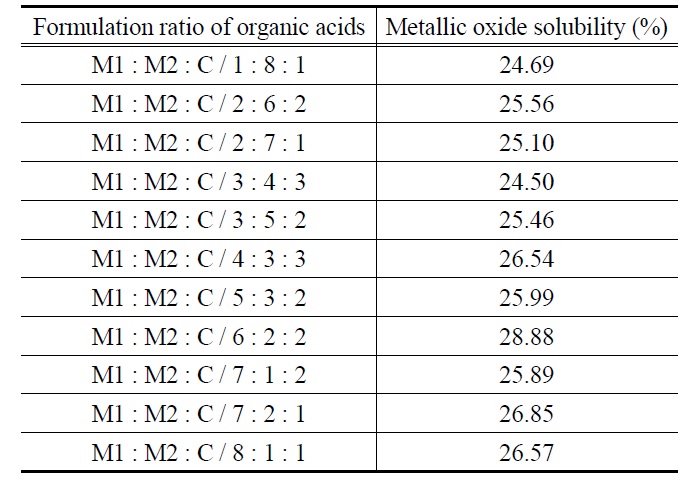
[Table 3.] Mixed metallic oxide solubility in three organic acid without pH control
Mixed metallic oxide solubility in three organic acid without pH control
서 보는 바와 같이 여러 유기산 혼합용액 중에서 말릭산, 말론산, 시트릭산의 배합비율이 6 : 2 : 2로 배합된 유기산 혼합 용액의 금속산화물의 용해력이 28.88%로 가장 높은 용해력을 보여주었다. 유기산을 주성분으로 하는 세정제에 의한 혼합 금속산화물의 용해력 평가를 위한 이후의 실험에서는 배합세 정제 제조시에 유기산 배합 비율을 6 : 2 : 2의 비율을 기본으로하여 진행하였다.
3.3.1. 계면활성제 선정 및 농도 결정 실험
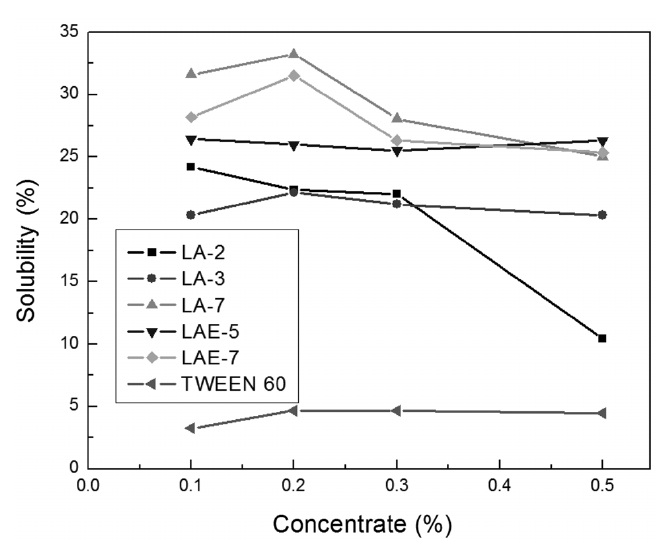
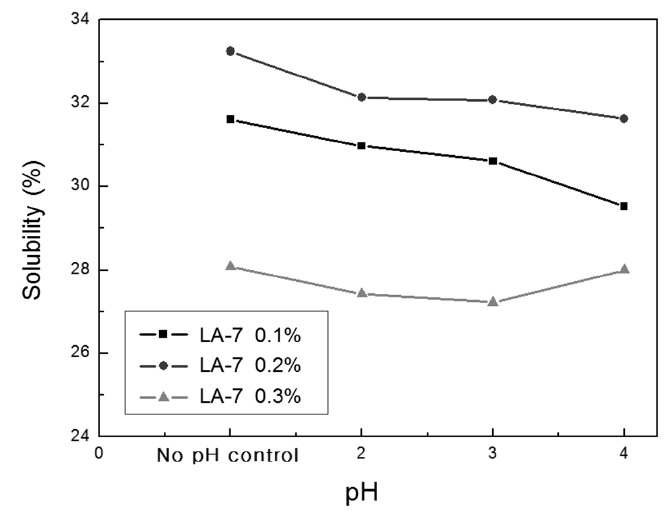
위에서 선정한 유기산 배합 세정제 조성물(말릭산, malic acid: 말론산, malonic acid: 시트릭산, citric acid = 6 : 2 : 2)에 비이온 계면활성제(LA-2, LA-3, LA-7, LAE-5 ,LAE-7, TWEEN 60)를 소량 첨가하여 혼합금속산화물 용해력에 대한 계면활성제의 영향력을 알아보기 위해 실험을 진행하였다. 배합 후보세정제에 계면활성제를 각 농도별(0.1%, 0.2%, 0.3%, 0.5%)로 첨가하여 혼합물 용해력 평가 실험을 진행한 결과를 Figure 3에 나타내었다. Figure 3에서 보는 바와 같이 계면활성제 중에서 알콜에톡실레이트 계의 계면활성제인 LA-7, LAE-7을 제외하고는 유기산 혼합용액만의 금속산화물 용해력인 28.88%보다 떨어지고 특히 에스테르 계통의 계면활성제인 TWEEN 60은 아주 용해력이 저조한 것으로 나타났다. 이것은 비이온계면활성제 중에서 알콜에톡실레이트 계열이 에스테르 계통보다 유기산과 금 속산화물의 킬레이트 생성물의 유화 분산력이 우수한 것으로 판단된다. 그리고 알콜에톡실레이트 계열의 LA-2 계면활성제는 농도가 높아질수록 급격히 금속산화물의 용해력이 떨어지는 것은 친수성을 나타내는 EO (etylene oxide) 부가몰수가 작아 농도가 증가할수록 친수성이 떨어지기 때문인 것으로 판단된다. Figure 3에서 보는 바와 같이 계면활성제 LA-7을 0.2% 첨가시에 혼합금속산화물의 용해력이 가장 높은 용해력을 보여주었다. Figure 4는 본 연구에서 사용한 계면활성제 중에서 가장 유화분
산력이 높아 유기산 용액의 금속산화물 용해력을 촉진시키는 LA-7을 첨가제로 선정하여 pH 변화에 따른 유기산 혼합용액의 금속산화물 용해력을 평가하였고 그 결과를 나타내었다. Figure 4에서 보는 바와 같이 세정액의 pH가 증가함에 따라 금 속산화물의 용해력은 전반적으로 약간 감소하는 것을 볼 수 있다. 이것은 유기산의 금속 용해력이 용해력이 킬레이트 반응과 양성자(proton, H+) 반응으로 이루어지는데 pH가 높을수록 양성자 반응이 저하되기 때문인 것으로 추론된다[13,15].
3.3.2. 살균제 선정 실험
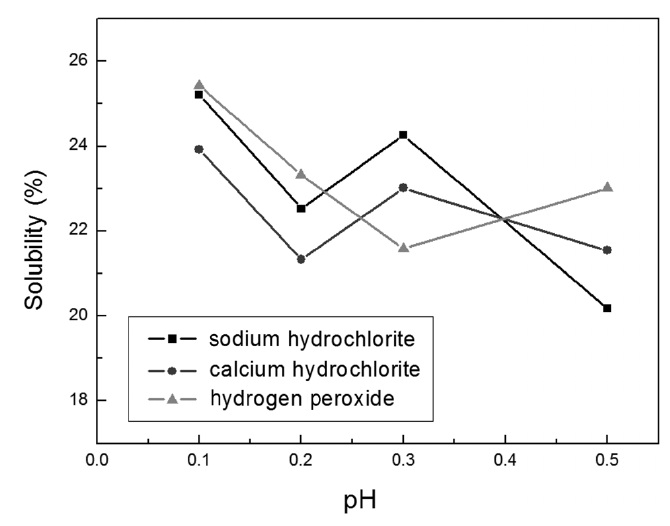
유기산 말릭산, 말론산, 시트릭산을 6 : 2 : 2 배율로 배합하고 여기에 계면활성제 LA-7을 첨가한 용액을 만들고 여기에 정수장이나 배수지에서 존재할 수 있는 미생물들을 제어하기 위한 살균제인 차아염소산나트륨, 차아염소산칼슘, 과산화수소 (hydrogen peroxide) 등을 선정하여 각 용액에 0.1%, 0.2%, 0.3%, 0.5%첨가하여 이들 용액의 혼합금속산화물 용해력 평가를 진행하여 그 결과를 Figure 5에 나타내었다. Figure 5의 실험결과에서 보듯이 배합세정제에 살균제를 넣었을 때 본 연구에서 실험한 모든 살균제가 배합세정제의 혼합금속산화물의 용해도를 크게 감소시키고 다소 기복이 있지만 살균제의 주입농도가 높을수록 전반적으로 혼합금속산화물의 용해도가 감소하는 경향이 있다. 그리고 살균제 중에서 금속산화물 용해력 저하는 차아염소산칼슘이 가장 크고 차아염소산나 트륨과 과산화수소는 유사하며 이들의 함량 농도가 0.1%일 경우 금속산화물의 용해력이 25% 정도로 저하되는 것을 알 수 있다. 이것은 본 연구에서 사용한 살균제들은 산화력에 의해 미생물을 살균하는 작용을 하기 때문에 배합세정제에 살균제를 첨가 시에는 배합세정제의 일부가 산화 분해되기 때문에 배합세정제의 금속산화물 용해력이 저하되는 것으로 추론된다. 그리고 배합세정제에 살균제의 함량이 높을수록 배합 세정제의 혼합금속화합물 용해력이 대체적으로 떨어지는 것은 배합세정제에 살균제의 함량이 증가함에 따라 배합세정제의 분해량이 커지기 때문으로 판단된다. 따라서 이러한 살균제
첨가에 따른 배합세정제의 분해를 최소화 하기 위해선 배합 세정제를 제조 시에 여러 첨가제를 함유한 유기산 혼합용액에 살균제를 첨가한 일액형 배합세정제를 만들 것이 아니라 배합세정제와 살균제 용액을 별도로 준비하고 사용 현장에서 혼합하여 사용한다면 배합세정제의 세정력 저하를 최소화할 수 있을 것이다.
본 연구를 바탕으로 말릭산, 말론산, 시트릭산의 혼합비를 6 : 2 : 2로 유기산 혼합용액을 만들고 계면활성제 LA-7을 소량 첨가한 용액에 과산화수소를 첨가하여 D시의 상수도 정수장과 배수장에 적용시켰다. 세정조건은 저압살포방식(스프레이세정)으로 분사압력은 10 bar로 분무하였으며 세정액과 정수장 및 배수지의 스케일과의 반응 시간을 위해 세정제 분무 후 15 분간 방치하였다. 그리고 깨끗한 물을 살포하여 헹굼(rinsing) 과정을 거쳐 현장적용을 진행하였다. 그 결과를 각각 Figure 6,
7에 나타내었다. 그림에서 보는 바와 같이 본 연구에서 개발한 배합세정제는 상수도 정수장과 배수지에 잘 세척되어짐을 알 수 있다.
본 연구에서는 유기산과 여러 첨가제들을 이용하여 상수도의 정수장과 배수지의 스케일 세척용 친환경 세정제를 개발하여 현장에 적용하고자 하였다. 정수장과 배수지 스케일의 주성분인 금속산화물들에 대한 여러 유기산들이 용해력을 평가한 결과 말릭산, 말론산, 시트릭산이 다른 유기산들보다 산화철, 산화알루미늄, 산화망간 등 금속산화물에 대한 용해력이 뛰어남을 보여주었다. 이들 말릭산, 말론산 그리고 시트릭산 등 세 종류의 유기산을 여러 배합비로 혼합하여 산화철, 산화알루미늄, 산화망간이 혼합된 금속산화물의 용해력 평가 실험 결과 말릭산, 말론산, 시트릭산의 배합비가 6 : 2 : 2일 때 가장 높은 용해력을 보여주었다.
이들 유기산 혼합용액에 소량의 생분해성 비이온 계면활성 제를 첨가할 경우 계면활성제의 유화 분산의 성질에 의하여 금속산화물 용해력이 크게 증가하였지만 살균제를 첨가할 경우는 살균제의 산화력에 의하여 금속산화물의 용해력이 저하 하였다. 그리고 유기산 혼합용액에 소량의 계면활성제 및 살균제를 첨가하여 배합세정제를 제조하여 상수도 정수장 및 배수지의 스케일을 성공적으로 제거할 수 있었다.
본 연구는 상수도 정수장 및 배수지 세척에 있어서 친환경 소재의 화학세정제가 이용될 수 있어 보다 안정적이고 효과적인 수돗물 공급에 크게 기여할 것으로 판단되며 수돗물에 대한 불신 해소 등 매우 우수한 효과를 기대할 수 있다.