코크에 의한 촉매의 불활성화는 산업현장에서 촉매가 사용되는 동안 매우 중요하다. 본 연구에서는 프로판 탈수소 반응을 위한 Pt-Sn 촉매에서 반응조건인 수소의 비율이 코크생성에 미치는 영향과 코크버닝에 의한 촉매 활성의 회복여부, 그리고 코크양에 따른 코크버닝 중의 백금소결여부, Pt-Sn-K 촉매에서 Sn의 함량이 코크생성과 불활성화에 미치는 영향을 확인하고자 하였다. Pt-Sn-K는 Pt와 Sn, K를 순차적으로 각각 θ-알루미나와 γ-알루미나에 담지 하여 제조하였다. 프로판 탈수소 반응은 먼저 반응물중의 수소비를 달리하여 620 ℃에서 수행한 후, 코크버닝을 통해 재생하고 다시 프로판 탈수소 성능을 비교하였다. 재생촉매의 B.E.T 분석과 코크분석, XRD (X-ray diffraction)와 같은 물리분석을 동시에 수행하였다. 촉매의 활성테스트와 특성분석을 통하여 반응물 상에서 수소의 비와 촉매의 Sn함량이 촉매표면의 코크 형성에 영향을 줄 수 있다는 것을 알 수 있다. 또한, 과량의 코크는 Air 재생 과정에서의 백금입자의 소결을 일으키고 촉매의 활성을 저하시킬 수 있다.
The loss of activity by coke is an important cause of catalyst deactivation during industrial operation. In this study, hydrogen ratio of reaction condition, which has influenced on coke formation over Pt-Sn catalyst, and regeneration of catalysts activity by coke burning, Pt sintering of coke burning as coke contents, effects of coke formation and deactivation with different Sn contents were confirmed. Pt-Sn-K catalyst supported on θ-alumina and γ-alumina was prepared progressively. Activity of regenerated catalyst for propane dehydrogenation was compared with fresh catalyst by coke burning, after propane dehydrogenation was carried out with different hydrogen ratio at 620 ℃ on fresh catalyst. Regenerated catalyst’s physical characterization such as BET, coke analysis and XRD was investigated. Through catalytic activity test and characterization, Sn contents of catalyst and hydrogen ratio in feed stream could affect coke formation on catalyst surface. Excessive coke makes loss of activity and Pt sintering during air regeneration process.
프로필렌은 폴리프로필렌, 프로필렌옥사이드, 아크릴로니트릴과 같은 다양한 화학물질들의 원료로 이용되기 때문에 석유화학산업에서 매우 중요하게 여겨져 왔다. 프로필렌은 주로 납사 수증기 분해 또는 중유의 촉매분해를 통하여 생산되었다[1-6]. 하지만 원유의 감소와 프로필렌의 수요증가로 인해 프로필렌을 주 생산물로 생산하는 공정개발에 대한 관심이 증대되고 있다. 프로판 탈수소 공정은 두 개의 C-H결합의 수소를 끊어내어 프로필렌을 제조하는 것이다[7]. 프로판 탈수소 반응은 열역학적인 제한으로 인해 원료인 프로판의 전환율이 낮다. 또한 일반적으로 촉매가 존재하지 않는다면 프로판에서 원하는 생성물로 선택적 제조는 굉장히 어렵다[8-12]. 즉, 높은 전환율과 선택도를 달성할 수 있는 촉매개발이 필요하고 더 나아가 열적으로 안정한 촉매개발이 계속적으로 연구되어야 한다.
백금촉매는 oleflex, PACOL 탈수소와 같은 공정뿐 아니라 다른 여러 산업에서 광범위하게 사용된다[1,2,5]. Pt는 일반적으로 탈수소에 높은 활성을 보이면서 많은 양이 필요하지는 않다. 즉 적은 양으로도 높은 활성을 가지기 때문에 여러 공정에 많이 쓰이게 된다. Pt의 높은 분산도는 탈수소의 높은 전환율과 선택도를 달성할 수 있다[1]. 백금촉매에 증진제(Sn, Pd, Zn, Ga)나 알칼리 금속(Li, K, Na)을 가할 경우 백금과의 상호작용과 더불어 지지체와의 상호작용은 백금의 전자구조 변화와 물리적인 입자크기와 결정구조가 달라져 활성의 변화가 존재한다[13,14]. 증진제를 가하면 고온의 반응조건에서 백금의 소결을 막아 분산도를 크게 높여주어 탈수소 반응에서 촉매의 활성점의 양을 늘려주고 탄화수소의 수첨분해 반응과코크의 형성을 저해시켜 촉매의 활성유지에 도움이 된다고 알려져 있다[13]. Vu et al. [13]은 활성물질인 Pt와 증진제 Sn과의 합금형성이 프로판 탈수소 반응에 미치는 영향을 연구했다. 이와 같이 증진제의 특성은 항상 중요하게 생각되고 있다.
프로판 탈수소화 반응은 흡열반응으로 반응온도 조절은 전체적으로 프로필렌 생산에 있어서 중요한 인자가 된다. 일반적으로 프로판 탈수소는 높은 온도가 필요하다. 하지만 이러한 높은 온도에서 백금 알루미나 촉매는 반응 중에 촉매표면에서 탄소침적이 생성되는데 이는 촉매의 불활성화를 초래한다[15]. 그렇기 때문에 이러한 불활성화를 피할 수 있는 다양한 방법들이 개발되고 있다. 또한 귀금속 촉매는 대부분 비싼 가격 때문에 불활성 된 촉매를 재생하여 사용하는 과정이 매우 중요하다. 불활성 된 백금을 재생하기 위하여 Park et al. [14]은 여러 온도별로 실험을 하여 활성을 회복하였고 Gascon et al. [16]은 산소의 양에 따라 실험을 하여 활성을 회복하였다.
본 연구에서는 프로판 탈수소 촉매의 불활성화를 초래하는 요인 중 반응온도가 백금 소결에 미치는 영향과 코크버닝에 의한 백금소결의 영향을 비교하기 위하여, 반응물중의 수소비율을 달리하며 코크양을 다르게 생성시킨 후, 이 촉매들의 재생에 따른 촉매 표면 백금입자의 특성변화와 활성의 재생여부를 확인하고, 코크의 생성을 저하시킬 수 있는 증진제로 주석을 선택하여 주석의 첨가에 대한 영향을 연구하였다.
본 연구에서 사용된 알루미나(Sasol)는 지름 2 mm의 구(ball type)의 형태이고, 담지한 후 20-40 mesh로 분쇄하여 실험을 하였다. Pt-1 wt%, Sn-0.5 wt%를 각각 상업용 γ-알루미나와 θ-알루미나에 함침법을 이용하여 촉매를 제조하였다. Pt를 알루미나에 담지하기 위하여 H2PtCl6・H2O를 Hydrochloric acid (HCl, 35%, Daejung)과 Nitric acid (HNO3, 60%, Daejung)을 사용하여 녹인 후 함침 하였다. 그 후에 120 ℃에서 12시간 건조한 후 580 ℃에서 3시간 소성하였다. Pt를 담지한 촉매는 Sn을 담지하기 위하여 SnCl2을 Hydrochloric acid와 Nitric acid를 사용하여 함침하였다. 그 후에 120 ℃에서 12시간 건조 후 600 ℃에서 3시간 소성하였다. K가 담지된 촉매의 경우에는 주석의 함량에 대한 불활성화 확인하기 위하여 위와 같은 방법으로 제조한 Pt-Sn 촉매에 KMnO4를 Hydrochloric acid와 Nitric acid를 사용하여 120 ℃에서 12시간 건조 후 600 ℃에서 3시간 소성하였다.
제조된 촉매는 액체질소 온도 하에서 질소 흡탈착을 통한 비표면적, 기공크기, 기공부피 측정을 BEL사의 Belsorp II mini를 통하여 측정하였다. 기공 크기 계산은 Barrett-Joyner-Halenda (BJH) 식을 이용하여 구하였다. 백금, 주석 및 칼륨의 조성을 확인하기 위하여 ICP-AES 측정을 하였다. 반응 전후와 재생 후의 금속성분의 입자를 확인하기 위하여 XRD (M/S, Shimadzu Instruments, japan)를 사용하였다. 반응 후의 촉매표면의 코크의 양을 Fisons사의 EA 1108 장비를 사용하여 CHNS 분석을 실시하여 측정하였다.
프로판의 탈수소화 실험은 고정층 반응기에 내부직경 18 mm의 일자모양 석영반응기를 이용하여 상압 조건 하에서 실험을 실시하였다. 프로판 탈수소화 반응실험은 0.35 g의 촉매를 이용하였고 10.3 ℃ min−1의 승온 속도로 620 ℃에서 1시간 환원 하였다. 이때 기체는 99.99%의 고순도 수소를 사용하였고 유량은 32 mL min−1이다. 환원 후 C3H8과 H2비를 각각 1 : 2, 1 : 1, 2 : 1, 3 : 0으로 64 mL min−1으로 흘려주며 수소비가 촉매의 코크 생성량에 미치는 영향을 알아보고, 코크양에 따른 이 촉매들을 코크 버닝하여 재생한 후 다시 프로판 탈수소 반응실험을 수행하였다. 이때 온도 조건은 620 ℃에서 실험하였다. 이 때 탈수소 된 기체는 GC (FID detector, 5890 series2 plus, Hewlett Packard, USA)를 이용하여 분석하였다. GC에서 사용된 컬럼은 capillary column (gs-Alumina, Agilent Technologies, USA, i.d. : 0.53 mm, length : 50 m)이다. 이후 주석의 영향을 알아보기 위해 동일한 반응기에 C3H8:H2를 각각 32 mL min−1으로 흘려주어 실험하였다.
사용한 촉매표면의 코크를 제거하기 위하여 Air를 60 mL min−1의 유량으로 코크를 연소시킨다. 온도는 상온에서 620 ℃까지 1시간 동안 승온하고 온도에 도달한 후 3시간 동안 유지한다.
촉매의 불활성에 미치는 영향은 반응물 중의 수소의 비에 따라서 다르다. 본 연구는 Sn 0.5 wt%가 담지된 1 wt%의 Pt 촉매를 사용한다.
3.1.1. 촉매의 활성테스트
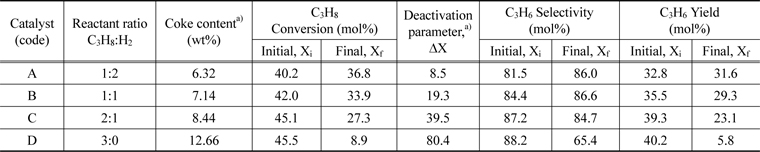
Table 1은 프로판 탈수소시 프로판과 수소의 양이 다를 때의 활성을 보여준다. 수소의 양이 증가할수록 촉매 전환율의 변화가 적은 것을 알 수 있다. 반응 과정에서 촉매표면에 생긴 코크는 반응의 불활성화를 초래하게 되는데 수소의 비와 코크는 밀접한 관계가 있다. 수소의 비는 따라 코크의 양은 6.32%에서 12.66%로 증가하는 것을 볼 수 있다. 특히 반응 중 수소를 넣지 않았을 경우 불활성화 파라미터는 80.4%로 급격하게 증가한다. 코크가 생기는 탈수소화 반응에서 수소의 영향으로 코크생성 반응인 deep dehydrogenation이 억제되어 코크가 적게 생기는 결과로 사료된다.
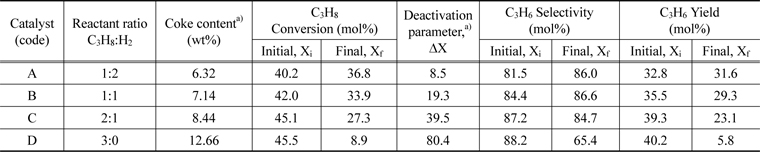
Activity (conversion, selectivity and yield) and deactivation parameter of 1Pt0.5Sn/θ-Al2O3 catalysts with different reactant flow rate ratio (C3H8: H2) and coke content of used catalysts
반응 과정에서 생긴 코크는 반응의 불활성화를 초래한다. 이는 air를 이용한 촉매 버닝을 통해 코크를 일정부분 제거할 수 있는데 본 연구에서는 서로 다른 코크의 양을 가지고 있는 촉매를 air 재생을 한다. 재생을 한 후의 촉매를 활성비교 하였고 촉매 특성은 XRD를 통해 보여준다.
3.2.1. 촉매 재생 전후의 XRD
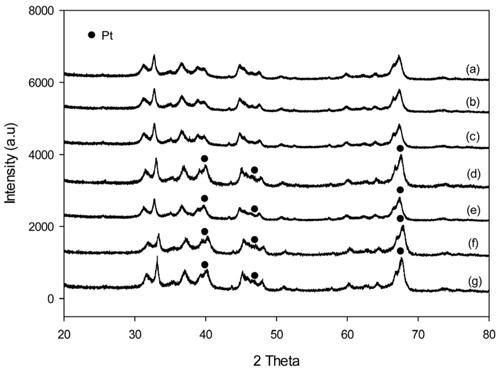
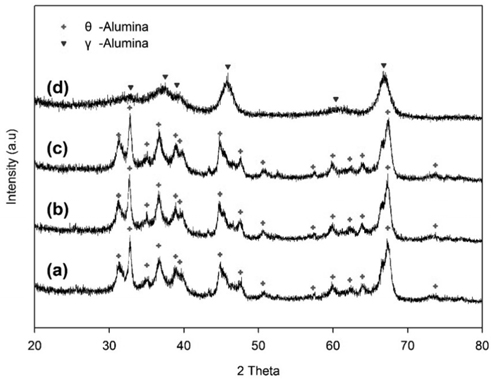
Figure 1은 반응 전과 후 그리고 프로판과 수소의 서로 다른 양으로 실험한 후 재생하였을 때의 촉매 표면의 금속성분인 백금의 결정 크기를 알기 위하여 XRD로 보여준다. Sn은 XRD 피크에 나타나지 않았다. 촉매의 반응 전후의 변화는 적은 것으로 보이는데 코크 버닝후의 Pt입자의 변화는 뚜렷하게 보인다. Pt입자들의 소결로 인해서 XRD상에서의 변화가 나타난 것으로 보인다. 이는 코크가 제거되면서 초기활성이 90% 정도 회복되었지만 Figure 2를 보면 소결로 인하여 불활성화가 빠르게 진행된다. XRD 회절 패턴 분석에서 Scherrer 식을 이용하여 제조된 촉매표면에 형성된 백금입자의 결정 크기를 계산하였다. Scherrer 식은 다음과 같다.
Equation (1)에서 L은 결정 크기이며, λ는 X-ray의 파장(0.154 nm)이다. 그리고 β는 회절 피크의 최대의 반가 폭이며, θ는 Bragg의 회절 각도이다[17]. Scherrer식에 의해 구한 (d)~(g)까지 Pt의 입자크기는 (d) 4.176 nm (e) 3.257 nm (f) 4.172 nm (g) 3.693 nm이다. 반응 전 촉매(b)와 반응 후 촉매(c)는 알루미나(a) XRD피크와 비교하였을 때 큰 변화를 보이지 않는 것으로 보아, 촉매 표면의 백금의 입자가 작고 고르게 분산되었고, 이 상태가 반응 전과 후에 큰 변화가 없는 것으로 보인다. 반응 전과 후에 입자크기의 큰 변화를 보이지 않고 있는 것으로 보아 반응과정에서 소결 현상은 크지 않은 것으로 보이지만 코크 버닝 재생한 후의 백금입자의 크기는 반응 전, 반응 후 촉매와 비교하였을 때 증가한 것을 확인할 수 있고, 코크 버닝 재생과정에서 백금의 소결이 일어나는 것을 알 수 있다. fresh 촉매의 활성저하는 코크에 의해 발생하지만, 재생 후의 빠른 비활성화는 백금의 소결로 인해 일어나는 것으로 보인다. 그렇기 때문에 코크 버닝으로는 완벽한 재생이 되었다고 할 수 없기 때문에 Pt의 재분산이 Air 재생 이후에 필요할 것으로 예상된다.
3.2.2. 재생촉매의 활성테스트
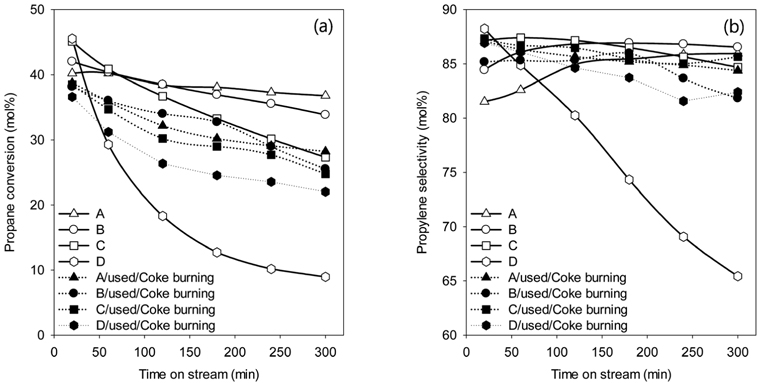
촉매는 Air 60 mL min−1 유량으로 620 ℃에서 5시간 버닝 하였다. 버닝 후의 촉매의 활성은 모두 같은 조건(620 ℃, 5시간)으로 실험한다. 코크의 양에 따른 촉매의 활성 회복은 차이가 난다. Figure 2는 코크의 양이 다른 촉매를 같은 조건으로 재생한 후 실험한 결과를 보여준다. 반응 초기와 반응 5시간 후의 활성을 비교해 보면 촉매에 코크가 많이 있을수록 촉매 재생 효과는 떨어지며 특히 불활성화가 강하게 일어난다.
촉매의 버닝 후의 프로판 탈수소의 활성은 어느 정도 회복이 된 것으로 보인다.촉매 표면의 코크의 양이 많은 프로판만 흘려준 촉매에서의 재생 효과는 많이 떨어진다. 그 외의 다른 촉매들의 재생효과는 반응시간에 따라 조금씩 달라지지만 초기와 마지막 반응에서는 코크의 양이 가장 작은 촉매에서의 전환율이 가장 크다. 하지만 전체적으로 air 재생한 후의 촉매를 재사용 할 경우 촉매의 불활성화는 더 빠르게 진행된다.
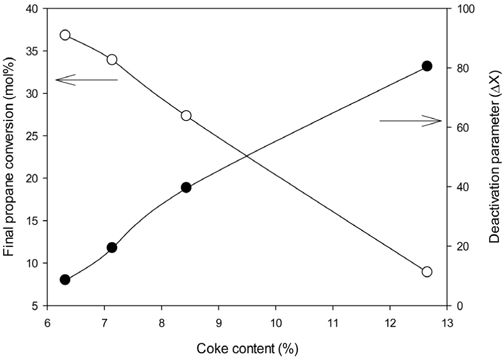
Figure 3은 촉매 코크양에 따라서 재생 후의 프로판 전환율과 불활성화 정도를 보여준다. 촉매의 코크양은 프로판 전환율 감소에 크게 영향을 끼치며 그에 따른 불활성화 또한 크게 증가한다. 이는 촉매의 코크가 활성변화에 크게 영향을 주며 재생과정을 거치더라도 재생 전의 코크의 양이 적을수록 재생이 잘 된다는 것을 뜻한다. Figure 2의 XRD결과와 연관 지어 해석하면, 재생과정에서 코크의 산화로 인해 코크가 제거되게 대는데 이 과정에서 백금의 소결이 일어난다. 즉 코크의 양이 많아질수록 많은 열이 발생하며 백금의 소결은 더 일어나게 되며 재생 후에도 활성이 저하되어 촉매의 불활성화의 원인이 된다.
코크의 양을 억제할 수 있는 방법으로 조촉매인 Sn의 양을 다르게 제조하여 효과를 살펴보았다.
3.3.1. 주석의 함량에 따른 백금촉매 특성분석
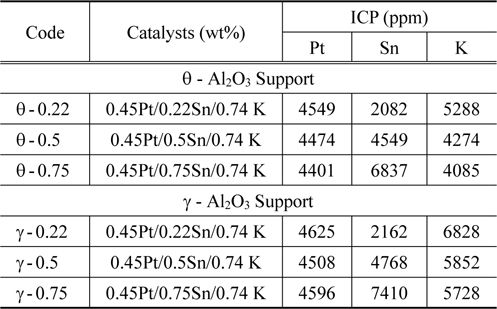
Pt0.45SnxK0.74촉매는 각각 θ-Alumina와 γ-Alumina에 담지 하여 촉매를 제조하였다. Table 2는 촉매의 담지량을 확인하기 위하여 ICP-AES분석을 한 값이다. 전체적으로 Pt는 고르게 담지가 되었고 Sn은 담지량이 증가하면 할수록 Sn의 함량이 일정하게 증가했다. 하지만 K의 함량은 Sn의 함량이 증가할수록 감소하는 것을 볼 수 있다. Sn의 함량이 커진다면 K가 담지 될 수 있는 활성점이 줄어들기 때문에 감소하는 것으로 보인다.
[Table 2.] Pt0.45Snx.xK0.74/Al2O3 catalysts with different tin contents
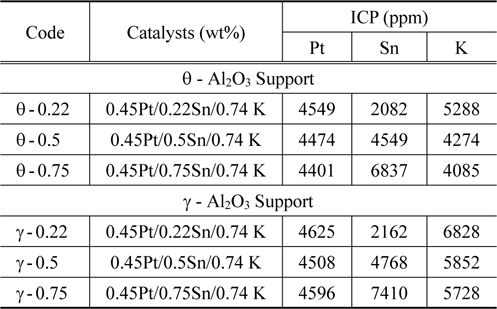
Pt0.45Snx.xK0.74/Al2O3 catalysts with different tin contents
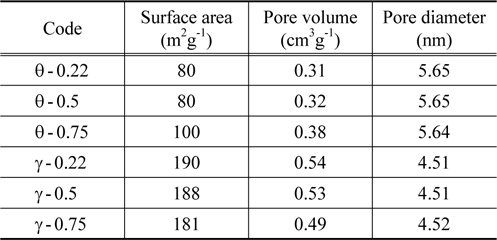
Table 3은 서로 다른 Sn의 함량에 따른 BET 분석 결과를 보여준다. 전체적으로 θ-alumina의 비표면적은 γ-alumina보다 작다. γ-alumina의 경우에는 190~181 m2 g−1으로 Sn의 담지량이 많아질수록 비표면적이 감소한다. 표면적뿐 아니라 기공의 부피 또한 비표면적과 비례하게 증감하지만 기공의 크기는 Sn의 담지량과 관계없이 크게 변화하지 않는다. θ-alumina의 기공부피는 Sn의 함량이 증가할수록 커지고 기공크기는 Sn 함량에 관계없이 일정하다.
[Table 3.] BET surface area and pore size distribution the fresh catalysts
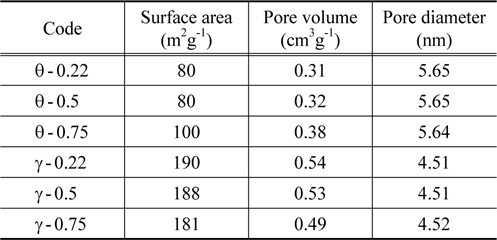
BET surface area and pore size distribution the fresh catalysts
3.3.2. 촉매의 활성테스트
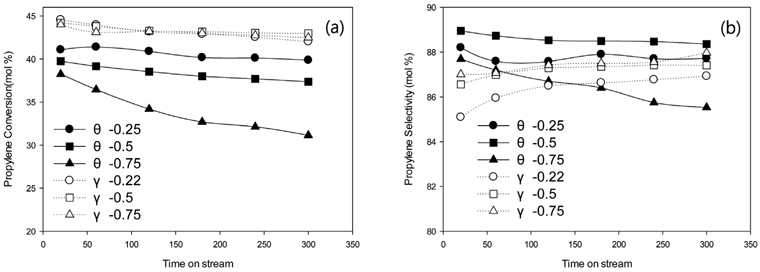
Figure 4는 θ-0.22, θ-0.5, θ-0.75, γ-0.22, γ-0.5, γ-0.75 각각의 촉매활성을 보여준다. 전체적으로 γ-alumina에 Pt-Sn-K가 담지된 촉매의 전환율이 θ-alumina에 Pt-Sn-K가 담지된 촉매의 전환율에 비해 높게 나왔다. Sn이 0.75 wt% 들어간 θ-alumina 촉매의 전환율이 가장 낮으며 불활성화도 가장 빠르게 일어난다. 또한 θ-0.22, θ-0.5, θ-0.75촉매는 초기 전환율이 각각 41.1%, 39.8%, 38.2%로 Sn함량에 따른 전환율이 큰 차이를 보였다. γ-alumina에 Pt-Sn-K가 담지된 촉매는 Sn함량에 관계없이 초기 전환율이 44%로 굉장히 높다. Flankin et al. [18]은 크롬을 3 wt% 담지한 비표면적 160 m2 g−1인 γ-alumina촉매에서 Sn의 함량이 0.3-1%까지는 활성의 변화가 크게 없다고 연구했다. 즉, Sn함량의 영향은 주촉매의 함량과 비표면적에 영향을 받는다고 볼 수 있다. 이와 비슷한 경향으로 γ-alumina에 담지한 백금촉매의 Sn함량에 따른 활성변화가 θ-alumina에 비해 크지 않은 이유는 Sn의 함량이 낮을 경우 γ-alumina의 비표면적이 크기 때문에 Sn함량의 영향이 적었을 것으로 보인다. 하지만 전체적인 선택도는 θ-alumina에 Pt-Sn-K가 담지된 촉매가 γ-alumina에 Pt-Sn-K가 담지된 촉매보다 높다. 선택도 또한 θ-alumina에 Pt-Sn-K가 담지된 촉매는 Sn의 함량에 따라 달라진다. 선택도는 Sn이 0.5 wt%일 때 가장 높다. γ-alumina의 선택도를 보면 Sn의 함량이 증가할수록 조금씩 높아진다. 하지만 θ-alumina와 다르게 Sn의 영향이 상대적으로 적었다. θ-alumina는 γ-alumina에 비해 2~4배 정도 산점이 적다. 산점은 크래킹 반응을 촉진시킬 수 있어 촉매의 선택도에 영향을 준다[19]. 그렇기 때문에 θ-alumina의 전환율이 상대적으로 낮은 반면에 선택도가 높은 것으로 보인다. 자세한 값은 Table 4에서 보여준다.
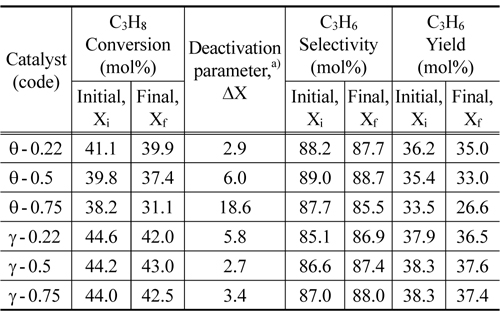
Activity (conversion, selectivity and yield) and deactivation parameter of Pt0.45Snx.xK0.74 / θ-Al2O3 and Pt0.45Snx.xK0.74 / γ-Al2O3 catalysts with different Sn contents for propane dehydrogenation
Table 4는 프로판 전환율, 프로필렌 선택도, 수율을 보여주고 전환율의 불활성화 정도를 보여준다. Sn의 함량이 가장 낮은 0.22%가 담지된 θ-alumina의 경우에는 초기의 전환율이 41.1%에서 5시간 반응 후의 전환율이 39.9%로 더 많은 함량의 Sn이 담지된 θ-alumina촉매들에 비해 불활성화 파라미터가 2.9%로 가장 낮은 불활성화를 보여준다. Pt-Sn-K/θ-alumina 촉매는 Sn의 함량이 커질수록 불활성화는 커진다. θ-alumina에서 지나친 Sn첨가는 촉매의 불활성을 유발할 수 있다. γ-alumina를 촉매의 담체로 사용할 경우에는 Sn의 함량이 증가함에 따라 대체적으로 높은 수율을 나타냄과 동시에 낮은 불활성화를 달성하였다.
Figure 5는 서로 다른 Sn함량에 따른 Pt-Sn-K/θ-alumina와 Pt-Sn-K/γ-alumina 촉매의 XRD 결과를 보여준다. Pt의 2θ값은 39.76x, 46.240.53, 67.450.31 (ICDD file no.: 04-0802)이다. 그리고 Sn의 2θ값은 15.570.5, 16.35x, 22.190.2, 27.640.35, 28.990.15 (ICDD file no. : 19-1365)이다. XRD 피크에는 Pt나 PtOx의 값 뿐 아니라 Sn과 SnOx의 값이 보이지 않고 alumina의 피크들만 보인다. 이는 Pt와 Sn이 담체 위에서 높은 수준으로 분산이 되어, Pt와 Sn이 너무 작아졌기 때문에 측정이 되지 않은 것으로 추정된다.
본 연구는 프로판 탈수소 반응용 백금촉매의 불활성화를 유발하는 탄소침적에 영향을 주는 인자들을 확인하기 위하여 반응물 중에서 수소의 비와 백금촉매의 주석의 함량을 다르게 하여 실험하였다. 수소의 비에 따른 촉매의 불활성화가 눈에 띄게 나타났다. 반응 중에 흘려주는 반응물에서 수소의 비가 커질수록 코크의 생성이 억제되는 효과를 볼 수 있었다. 또한 코크가 많이 생성이 된다면 촉매의 활성이 빠르게 감소하는 것을 볼 수 있었다. 코크가 생겨 불활성이 된 촉매는 Air 재생을 통해 어느 정도의 활성을 되찾았지만 재생 전 촉매에 비해 불활성화가 더 빠르게 일어났다. 백금의 소결은 반응과정에서 생기는 것이 아니며 반응 후의 촉매를 재생하는 과정에서 높은 열로 인해 생기는 것을 XRD 분석을 통하여 알 수 있었다. 따라서 촉매의 코크가 많을수록 코크를 산화하는 과정에서 나오는 높은 열로 인해 소결이 더 많이 일어났으며 이로 인해 재생 후에 불활성화가 빠르게 일어난 것으로 보인다. 이러한 코크양을 줄일 수 있는 방법으로 증진제인 주석을 첨가하여 효과를 살펴보았다. θ-alumina는 Sn의 함량에 따른 활성변화가 크게 나온 반면에 γ-alumina는 Sn의 함량 변화에 따른 활성변화는 거의 나타나지 않았다. 촉매를 θ-alumina에 담지할 경우 Sn의 함량이 적을 때 코크의 생성이 억제되어 촉매의 불활성이 가장 낮았으며 가장 높은 수율을 달성할 수 있었다. 촉매를 γ-alumina에 담지한 경우에는 Sn의 함량을 0.5 wt%로 담지했을 때 미세하게 낮은 불활성화와 높은 수율을 달성했다. 실제 공정에서 프로판 탈수소화 반응을 하기 위하여 백금촉매를 사용할 경우 촉매의 탄소 침적을 억제하기 위하여 반응물을 흘려줄 때 수소의 비와 조촉매의 함량을 조절하는 것이 매우 중요하며 air 재생은 촉매 표면의 코크를 제거할 수 있지만 백금입자를 소결시킬 수 있기 때문에 백금입자의 재분산 공정이 필요함을 알 수 있다.