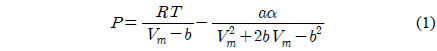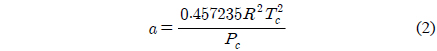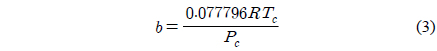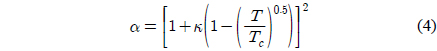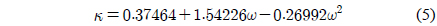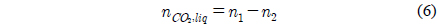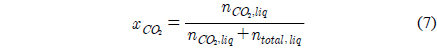The constant-volume method was used to determine the solubility of CO2 in various physical absorbents such as DMPEG (dimethyl ether of polyethylene glycol), DEC (diethyl carbonate), DMC (dimethyl carbonate), and TAT (triacetin) in the total pressure range from 5 to 30 bar. The Peng-Robinson equation of state has been used to describe the equilibrium behavior of these mixtures. It was found that the solubility of absorbents was in the of DMPEG250 > TAT > DEC > DMC at the same temperature. Futhermore, the solubiity of blended absorbent of DMPEG250 and DEC is higher than that of DMPEG 250 alone. Therefore, blended absorbent of DMPEG250 and DEC is expected to be an effective and low cost absorbent for physical absorption in precombustion CO2 capture.
전 지구적으로 화석연료사용이 증가함에 따라 대기 중의 이산화탄소 농도가 급격히 증가하고 있으며 이 같은 이산화탄소의 배출을 억제하는 것은 긴급한 이슈가 되었다. 이산화탄소 배출 억제와 관련한 혁신적인 기술로 제시된 것이 이산화탄소 포집과 결합된 석탄가스화 복합발전(integrated gasification combined cycle, IGCC)이다.
IGCC에서는 고압조건하에서 연소전에 이산화탄소를 포집하기 때문에 물리 흡수(physical absorption)가 유리하다. 연소 전 이산화탄소의 포집을 위한 고용해도 저비용 흡수제의 사용은 추가적인 이산화탄소 공정 도입에 따른 전력 생산 비용의 증가를 효과적으로 줄일 수 있다.
연소전 이산화탄소 포집에 사용되는 대표적인 물리 흡수제로서는 RectisolⓇ(메탄올), Purisol (N-methyl-2-pyrrolidone, NMP), SelexolTM (dimethyl ether of polyethylene glycol, DMPEG)등이 있다[1]. 메탄올을 사용하는 Rectisol공정은 열화학적으로 안정하고 부식성, 거품형성이 적다는 장점이 있으나 저온냉각에 따른 낮은 에너지효율과 흡수제 손실이 단점으로 지적되고 있다. NMP를 사용하는 Purisol공정은 열적 안정성과 흡수액의 부식성이 적지만 초기투자비가 높고 재생과정에서 압력 손실이 발생할 수 있다. SelexolTM공정에 사용되는 흡수제는 DMPEG로서 이는 과거 오랫동안 산 가스의 흡수나 천연 또는 합성가스로부터 머캡탄(mercaptans)을 제거하는데 사용되어 왔다. DMPEG는 높은 분자량을 갖는 용매로서 낮은 증기압, 물과의 혼화성을 가지고 있다. 낮은 증기압에 따른 낮은 증발 엔탈피는 탈거과정에서의 에너지 요구량이 적다는 것을 의미한다. 그러나 DMPEG는 점도가 높고 고가이며 흡수제 재생과정 중에 압력 손실에 따른 영향이 크다는 단점이 있다. 그럼에도 불구하고 SelexolTM공정은 공정 고유 특정에너지, 냉각, 가열에 소비되는 에너지가 타 공정에 비해 낮은 장점이 있어 IGCC에 적합한 공정으로 알려져 있다[1-3].
이산화탄소의 물리 흡수를 위해 개발된 메탄올, NMP, DMPEG 등과 같은 물리 흡수제들의 흡수능이 여전히 만족할 만한 수준은 아니며 종래의 이산화탄소 포집 기술 적용에 따른 비용 역시 높은 것으로 알려져 있다. Chang과 Rousseau는 고압조건에서 메탄올과 메탄올-물 혼합물에 대한 이산화탄소의 용해도를 측정하고 이들 혼합물의 평형 거동을 설명하기 위해 Mathias의 극성 보정 인자(polar correction factor)를 이용한 상태방정식을 사용하였다[4]. Gainer와 Anitescu는 고압에서 DMPEG에 대한 이산화탄소와 질소 그리고 수소의 용해도를 측정하였고 DIPA (diisopropanolamine)를 첨가했을 경우 이산화탄소의 용해도는 증가하였으나 흡수제의 점도가 높아지는 문제점이 보고되었다[5]. Heintz 등은 플로린화합물을 이용하여 합성가스로부터 이산화탄소를 물리적으로 흡수하는데 필요한 용해도 데이터, 속도론 데이터 및 수력학적 특성 데이터를 측정하였다[6]. Gui 등은 물리흡수제로서 DMC (dimethyl carbonate)를 제안하고 고압에서의 이산화탄소에 대한 용해도를 측정하였다. DMC는 높은 이산화탄소 로딩 값과 선택도를 가지면서 친환경적인 용매로 알려져 있다[7].
본 연구에서는 현재까지 이산화탄소의 물리적인 흡수에 적용되는 공정 중 가장 에너지가 적게 요구되는 SelexolTM에서 사용되는 DMPEG를 기준으로 이보다 더 높은 이산화탄소 용해도를 가지는 단일물리 흡수제 및 혼합 물리 흡수제를 찾기 위해 DMPEG를 포함하여 DEC (diethyl carbonate), DMC 및 TAT (triacetin)에 대한 용해도를 측정하였다.
본 연구에서는 Sigma-Aldrich의 DMPEG250(평균분자량 250), 대정화학의 DEC (≥99.8%), DMC (≥99.8%) 및 트리아세틴(≥99.5%)이 흡수제로 사용되었다. 혼합흡수제는 DMPEG에 DEC를 혼합하여 사용하였다. 공급가스로는 순도 99.99%의 이산화탄소를 사용하였다.
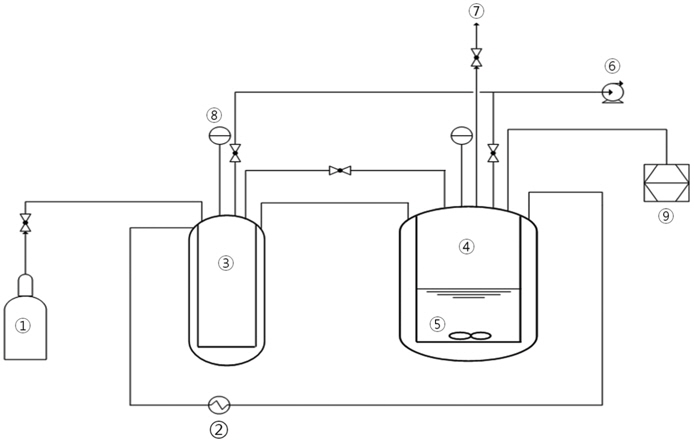
흡수제에 대한 이산화탄소의 용해도를 측정하기 위해서 Figure 1과 같은 평형셀을 사용하였다. 본 연구에 사용된 이산화탄소 용해도 측정 장치는 일정 부피법(constant volume method)에 기초하고 있다[7]. 일정부피법의 원리는 정해진 양의 용질 가스를 일정량의 흡수제와 접촉시켜 평형에 도달할 때까지 교반하는 것이다. 이 때 흡수제에 대한 기체 용해도는 물질 수지식을 통해 계산된다.
가스쳄버는 스테인리스 강으로 제작되었으며 일정한 온도와 압력의 이산화탄소를 평형셀로 공급하기 위해 이를 평형셀과 함께 항온조에 설치하였다. 가스챔버와 평형셀에는 T-type thermocouple 및 고정밀급 압력트렌스듀서((주) 센서시스템기술)를 설치하여 시스템 내부의 온도 및 압력을 확인할 수 있도록 하였으며 이들 데이터는 PC와 연결되어 저장되게 하였다. 압력센서의 측정범위는 -1~50 bar이고 정밀도는 ±0.15%FS이다. 평형셀에서의 이산화탄소 용해를 위해 마그네틱 바를 사용하였다.
먼저 항온조를 통해 전체 시스템의 온도를 일정하게 유지한 후 평형셀에 흡수제 50 g를 투입한다. 진공펌프를 이용하여 용해도 측정전에 평형셀 및 가스챔버 내 불순물을 제거한다. 이후 가스챔버에 전압기준 5~30 bar의 압력 범위에서 일정 압력에 도달할 때까지 고순도 이산화탄소를 주입한 후 가스챔버와 평형셀 사이의 밸브를 열어 이산화탄소를 평형셀 내로 주입한다. 이 때 마그네틱 바를 이용한 교반을 실시하여 기체와 흡수제가 충분히 혼합되도록 한다. 평형셀 내부 압력은 시간이 경과함에 따라 감소하게 되며 시간에 따른 더 이상의 압력변화가 없는 지점을 흡수평형 지점으로 간주하여 이때의 이산화탄소 압력을 측정, 흡수된 이산화탄소의 양을 계산한다.
버퍼탱크의 압력(
여기에서
윗 식에서
흡수제에 대한 이산화탄소 용해도는 몰분율로써 아래와 같이 계산된다.
여기에서
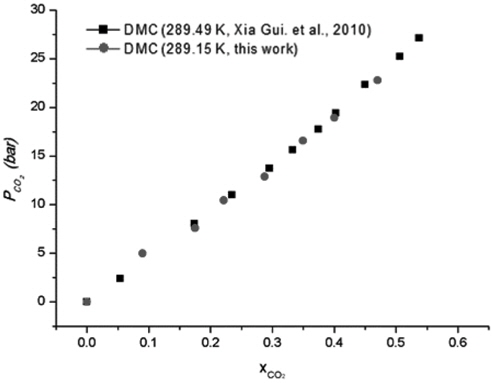
Figure 2에서는 본 연구에서 사용된 용해도 측정 장치의 신뢰성 확인을 위해 DMC에 대하여 문헌에서 보고된 결과와 본 연구를 통해 얻은 데이터를 비교하였다. 그림에서 보듯이 Gui 등이 얻은 용해도 데이터와 본 연구에서의 데이터가 일치함을 알 수 있다.
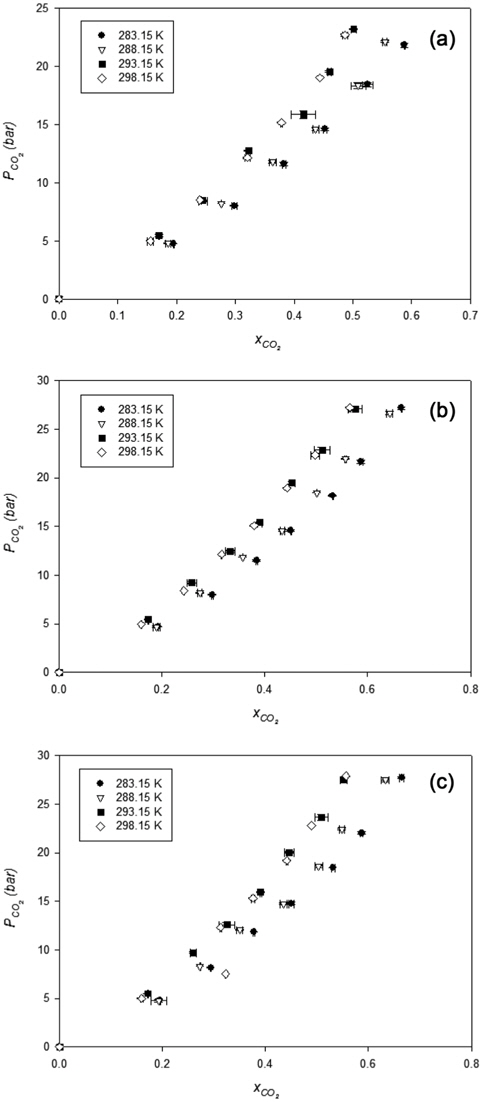
Figure 3에서는 이산화탄소의 압력과 조업 온도에 따른 DMC, DEC, 그리고 TAT의 용해도 측정 결과를 보여주고 있다. 모든 물리 흡수제에 대한 조업은 283.15 K과 298.15 K 사이의 온도 범위와 4 bar에서 25 bar 사이의 이산화탄소 압력 범위 내에서 이루어 졌다. 물리흡수제에서의 이산화탄소 용해도는 압력에 따라 증가했으며 온도에 따라 감소하였다. 이러한 경향성은 기존에 알려진 물리 흡수제 뿐 아니라 화학흡수제에 의한 이산화탄소 흡수에서도 동일하다. DMC의 경우 온도가 5 K 증가할 때
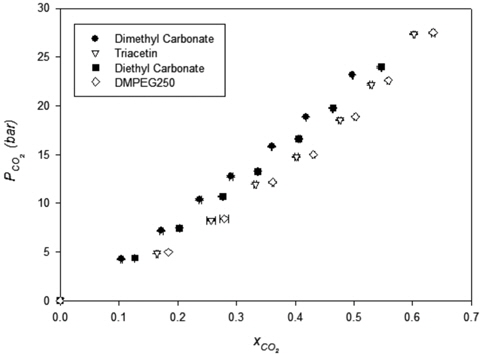
Figure 4에서는 동일한 조업온도에 대해 물리 흡수제별 이산화탄소 용해도를 비교하여 나타내었다. 이산화탄소 용해도는 DMPEG250 > TAT > DEC > DMC 순으로 나타났다. DEC의 경우 DMC와는 이산화탄소 용해도에 있어 큰 차이가 없음을 알 수 있으며 DEC가 DMC에 비해 낮은 증기압을 가짐을 고려할 때 DEC가 실제 공정으로의 적용에 있어서 유리할 것으로 사료된다.
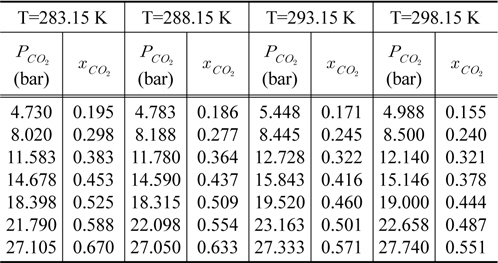
[Table 1.] CO2 solubility of DMC at various temperature
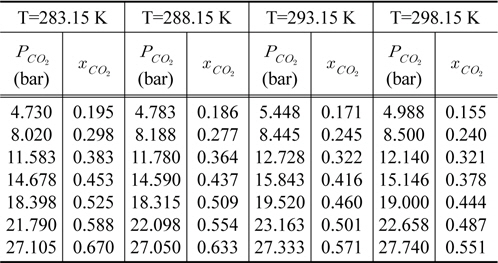
CO2 solubility of DMC at various temperature
[Table 2.] CO2 solubility of DEC at various temperature
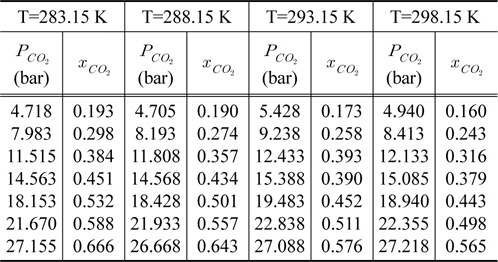
CO2 solubility of DEC at various temperature
[Table 3.] CO2 solubility of triacetin at various temperature
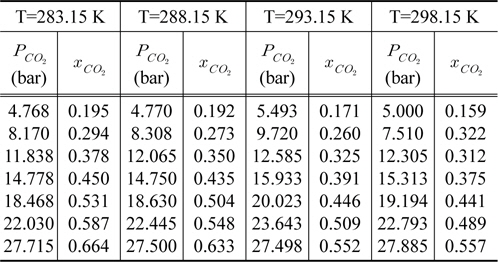
CO2 solubility of triacetin at various temperature
기존 물리 흡수제로 널리 사용되는 DMPEG의 경우 SelexolTM공정 등에 적용되어 왔으나 흡수제의 가격이 비싸다는 단점을 갖고 있다. 따라서 본 연구에서는 DEC를 DMPEG250에 혼합한 흡수제의 용해도를 측정하였다.
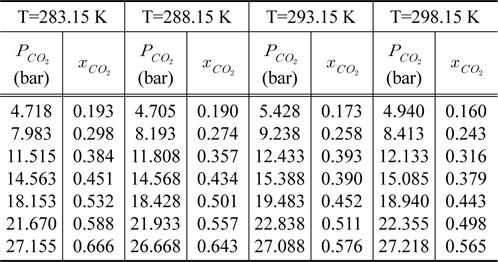
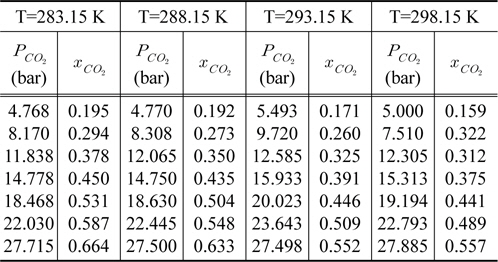
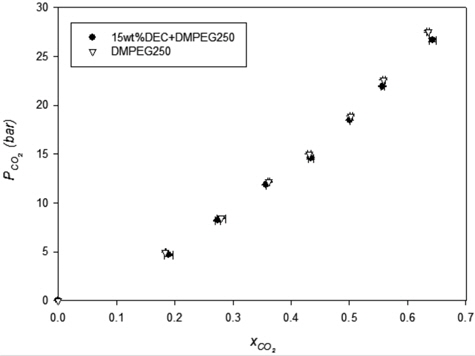
Figure 5에서는 DEC가 15 wt%가 혼합된 DEC/DMPEG250 혼합 흡수제에 대한 이산화탄소 용해도를 보여주고 있다. 그림에서 보듯이 고압 영역에서의 미세한 차이를 제외하고는 혼합 흡수제와 DMPEG의 이산화탄소에 대한 용해도는 거의 차이가 없었다.
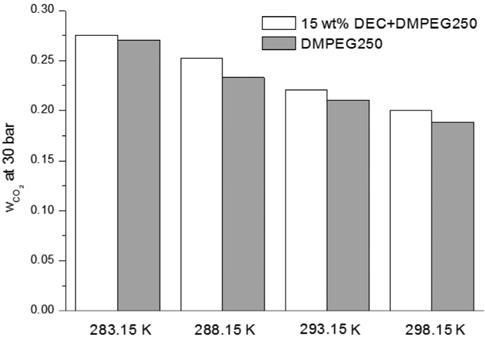
Figure 6에서는 30 bar로 일정한 압력을 유지한 상태에서 다양한 조업온도에 대한 DEC/DMPEG 혼합 흡수제와 DMPEG 흡수제의 용해도를 비교하였다. 혼합흡수제의 이산화탄소 용해도는 DMPEG에 비해 평균적으로 약 9% 가량 향상되었음을 알 수 있다.
본 연구를 통해 얻은 결론은 다음과 같다.
1) 기존의 이산화탄소 물리 흡수제인 DMPEG250를 포함한 DEC, DMC, TAT의 이산화탄소 용해도 측정을 위한 일정 부피법을 이용한 실험장치의 신뢰성을 기 보고된 DMC 데이터를 이용하여 확인할 수 있었다. 2) 283.15~298.15 K의 온도영역에서 본 연구에 사용된 모든 물리흡수제의 용해도는 온도의 증가와 압력의 감소에 따라 감소하였다. 3) 흡수제별 이산화탄소 물리흡수능은 DMPEG250 > TAT > DEC > DMC의 순으로 나타났다. 4) 기존 물리 흡수제로 널리 사용되는 DMPEG에 DEC를 혼합하여 사용한 결과 DMPEG250을 단독으로 사용한 경우에 비해 평균 약 9%의 흡수성능 향상을 거둘 수 있었다. 이는 DEC와 DMPEG250이 혼합된 흡수제의 가격이 DMPEG250보다 낮으므로 향후 연소 전 이산화탄소 포집에 적용될 수 있는 가능성이 높다고 할 수 있다.