본 연구는 Protox 제초제내성 벼 재배가 토양 미생물에 미치는 영향과 수평적 유전자 이동성을 알아보기 위해 수행되었다. 생육단계별 토양 미생물 군집밀도의 경우 제초제내성 벼를 재배한 근권 토양 미생물 군집밀도가 비 형질전환 벼의 근권 토양과 유사하여 제초제저항성 벼 재배가 근권 토양 미생물에 미치는 영향은 비슷할 것으로 추정되었다. 근권 토양의 우점 미생물 분포 양상을 분석한 결과, Proteobacteria, Firmicutes와 Actinobacteria 순으로 나타났으며 우점종과 점유율은 거의 유사하였다. 근권 토양 DNA에 대한 DGGE 분석 결과, 제초제내성 벼와 비 형질전환 벼의 근권 토양 미생물 군집의 profile 변화는 나타나지 않았다. 제초제내성 벼 재배에 따른 토양 화학성을 분석한 결과, 비 형질전환 벼의 근권 토양간 화학성은 차이가 없는 것으로 나타났다. 제초제 내성 벼에 도입된 유전자군을 대상으로 근권 토양 DNA에 대한 PCR 분석 결과, 도입 유전자의 잔존성이 길지 않아 수평적 유전자 이동성은 희박할 것으로 추정되었다.
Rice (
Microorganisms were isolated from the rhizosphere of GM and non-GM rice cultivation soils. Microbial community was identified based on the culture-dependent and molecular biology methods. The total numbers of bacteria, fungi, and actinomycete in the rhizosphere soils cultivated with GM and non-GM rice were similar to each other, and there was no significant difference between GM and non-GM rice. Dominant bacterial phyla in the rhizosphere soils cultivated with GM and non-GM rice were
These data suggest that transgenic rice does not have a significant impact on soil microbial communities, although continued research may be necessary.
제초제내성 대두가 상업적으로 재배된 1996년 이후 유전자변형(Genetically modified, GM) 작물의 재배면적은 해마다 증가하고 있다. 2011년 전 세계 유전자변형 작물의 재배면적은 1억 6,000만 ha(James, 2011)로, 대한민국 국토면적 (221,336㎢)의 약 7.2배에 해당된다. 유전자변형 작물 중 제초제내성 대두, 옥수수, 유채, 면화의 재배면적은 약 9,400만 ha로 전 세계 유전자변형 작물 재배면적의 59%를 차지하고 있다. 일반적으로 제초제내성 작물은 glyphosate나 glufosinate 제초제에 내성을 가짐으로써 잡초방제에 소요되는 노동력과 농기계 사용 절감에 따른 경제적 이익(Owen, 2000), 무경운농법에 의한 토양 환경 보존 및 화석연료 사용 절감에 따른 기후 변화 대응 효과(Brookes and Barfoot, 2006) 등의 장점이 있다. 반면 도입 유전자의 이동(gene flow)에 의한 슈퍼잡초 발생 가능성(Ellstrand, 1992)과 생태계 교란(Conner
원핵생물은 생존을 위한 방법으로 접합(conjugation), 형질도입(transduction), 형질전환(transformation) 등을 통해 종간 또는 종내에서 유전자 이동이 일어나며(Ochman
유전자변형 작물의 상용화를 위해서는 환경위해성 평가를 통한 안전성 검정이 필수적이며, 특히 우리나라에서 주곡으로 오랜 기간 동안 이용해온 벼는 토양 미생물상을 비롯한 농업환경 영향에 대한 자세한 연구가 필요하다. 프로토포르피리노겐 옥시다아제(Protoporphyrinogen oxidase, Protox)는 엽록소/헴 생합성 경로의 핵심적인 효소로 protoporphyrinogen IX (Protogen IX)를 protoporphyrin IX (Proto IX)로 산화시키는데 촉매 역할을 한다. Protox 저해 제초제가 작용하면 Protox의 산물인 Proto IX가 세포질에 축적되며, 이로 인해 광조건에서 막이 과산화되면 세포가 사멸하게 된다. 본 연구에서는 토양 미생물인
토양 미생물(
채취한 토양 10 g에 멸균한 0.85% NaCl 90 mL를 첨가하고 진탕 배양기에서 30분간 200 rpm으로 현탁하였다. 현탁액은 일련의 희석과정을 거친 후 28℃ 조건에서 도말하여 세균, 진균 및 방선균을 배양하였으며, 각각 cycloheximide(0.05 g/L)를 첨가한 R2A agar(NA, Difco, MI) 배지에서 2일간, chloramphenicol(0.02%)을 첨가한 R2A agar 배지에서 4일간, Sodium caseinate agar 배지에서 5일간 배양한 후 계수하였다. 배양된 미생물 수는 페트리디쉬에 나타난 균체를 3반복 계수한 평균값을 생균수(colony forming unit, CFU/g건토)로 산출하였다.
형질전환 벼와 비 형질전환 벼를 재배한 토양 미생물 간의 군집 변화를 알아보기 위해 Denaturing gradient gel electrophoresis(DGGE) 분석을 하였다. FastDNA Spin Kit(Qbiogen, USA)로 토양 미생물 DNA를 추출하고, 진정세균의 미생물상 변이 여부를 분석하기 위하여 16S rRNA의 V9 부위를 증폭하는 1070f(5'-ATGGCTGTCGTCAGCT-3')와 여분의 G+C clamp(CGCCCGCCGCGCCCCGCGCC CGGCCCGCCGCCCCCGCCCC)가 부가된 1392r(5'-AC GGGCGGTGTGTAC-3') primer를 이용하여 PCR 반응을 수행하였다. PCR 반응은 각각 5 μL 10 x PCR buffer, 10 ng 주형 DNA, 25 pmol 양방향 프라이머, 200 μM dNTP, 2.5 U f-
식물뿌리의 존재에 의해 토양 미생물이 영향을 받는 토양내의 공간을 근권이라고 하는데 근권의 토양부분에서 세균을 동정하기 위하여 FastDNA Spin Kit로 DNA를 추출하고, 27mf (5' -AGAGTTTGATCMTGGCTCAG-3' ) 와 1492r(5'-GGYTACCTTGTTACGACTT-3') primer를 사용하여 세균의 전체 16S rRNA 부위를 증폭하였다. PCR 반응물의 조성과 조건은 미생물 군집 분석 방법과 동일하게 수행하였으며, 1% agarose gel에서 확인된 DNA를 pGEM-T easy vector(Promega, USA)에 삽입하고 E. coli DH5α에 형질전환하여 배양하였다. 형성된 콜로니를 무작위로 선발하여 DNA clean kit(Bioneer, Daejeon, Korea)로 정제하고 우점세균의 동정을 위해서 특이적인 27mf와 519r(5'-ACGG GCGGTGTGTAC-3') primer를 사용하여 삽입 절편을 증폭하였다.
토양 화학분석은 농촌진흥청의 토양 및 식물체 분석법 (NIAST, 2000)에 준하여 형질전환 벼와 비 형질전환 벼의 근권 토양을 음지에서 건조시키고 2 ㎜체를 통과한 토양을 분석하였다. pH와 EC는 토양과 증류수를 1:5로 혼합하여 30분간 진탕한 후 현탁액을 측정하였으며, 유기물 함량은 Walkley와 Black법(Walkley and Black, 1934), 유효인산은 Bray No. 1법(Bray and Kurtz, 1945)으로 각각 분석하였다. 칼륨, 칼슘, 마그네슘, 나트륨 등 치환성양이온은 1N Ammonium acetate(pH=7.0)로 침출한 후 유도결합플라즈마가 장착된 원자발광분광기(ICP-730-ES)로 분석하였다.
형질전환 벼로부터 근권 주변 미생물로의 수평적 유전자 이동성 여부를 확인하기 위하여 근권 토양에서 DNA를 분리하고 PCR증폭을 통해 토양 내 잔존성을 조사하였다. 도입유전자(protox)를 증폭할 수 있는 primer(Protox F, 5'-ATG CATCACATGCCAAGA-3', R, 5'-CTACCCTACGGTG CATGAGAAGT-3')와 벼의 내재유전자(Actin)를 증폭할 수 있는 primer(Actin F, 5'-ATCTTTGGCCTTGGTAGTTTG-3', R, 5'-GTACCCGCATCAGGCATCTG-3')를 사용하여(Jung
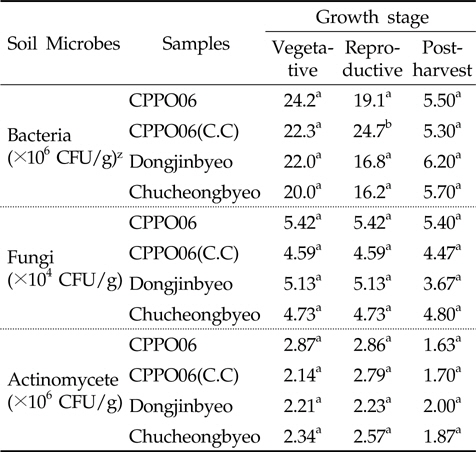
Protox 제초제내성 벼 재배가 근권 토양의 미생물상에 미치는 영향을 구명하기 위하여 생육단계에 따른 제초제내성벼(CPPO06)와 비 형질전환 벼(동진벼, 추청벼)의 근권 토양에 대한 세균, 방선균 및 진균의 밀도를 비교 분석하였다 (Table 1). 제초제내성 벼와 비 형질전환 벼에서의 근권 토양유래 세균, 방선균 및 진균의 밀도는 유의성이 없어(P>0.05), 제초제내성 벼 재배에 의한 근권 토양 미생물상의 영향은 비형질전환 벼 재배와 유사할 것으로 추정되었다. 그러나 protox 저해 제초제가 아닌 관행제초제를 처리하여 재배한 제초제내성 벼[CPPO06(C.C)]의 토양 세균 밀도는 생식생장기에 증가하였다(P<0.05). 식물 뿌리에서 배출되는 삼출물은 미생물 군집 및 활성의 변화를 초래하며, 근권 토양 미생물상의 변화는 유기물의 분해와 순환에 영향을 주어(Sharma
[Table 1.] Number of microbial population in the GM and non-GM rice cultivation soil
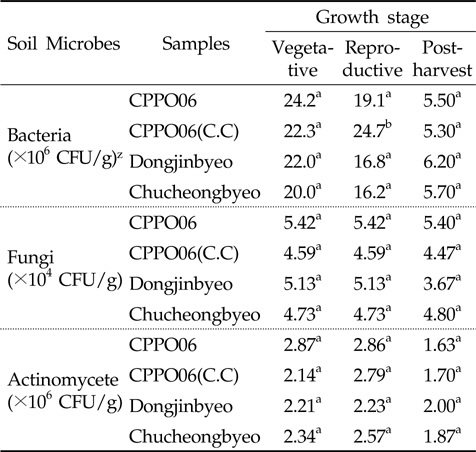
Number of microbial population in the GM and non-GM rice cultivation soil
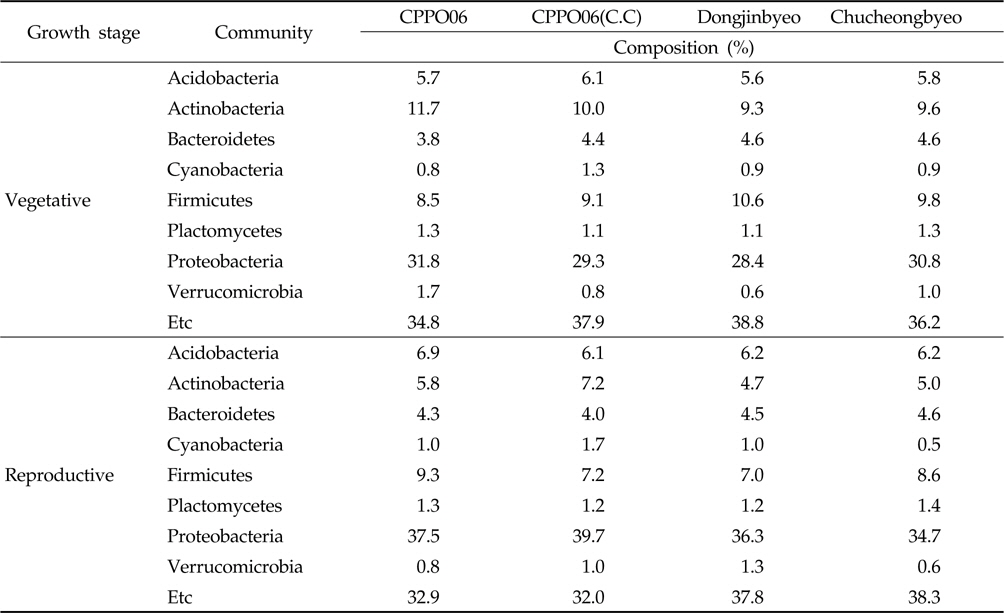
제초제내성 벼 재배에 의한 토양 내 우점 미생물의 변화를 확인하기 위하여 근권 토양으로부터 DNA를 분리하고 미생 물의 16S rRNA 염기서열을 분석하였다. 근권 토양에서 동정된 세균들의 분포를 phylum 수준에서 비교한 결과(Table 2), 제초제내성 벼와 비 형질전환 벼의 근권 토양에는
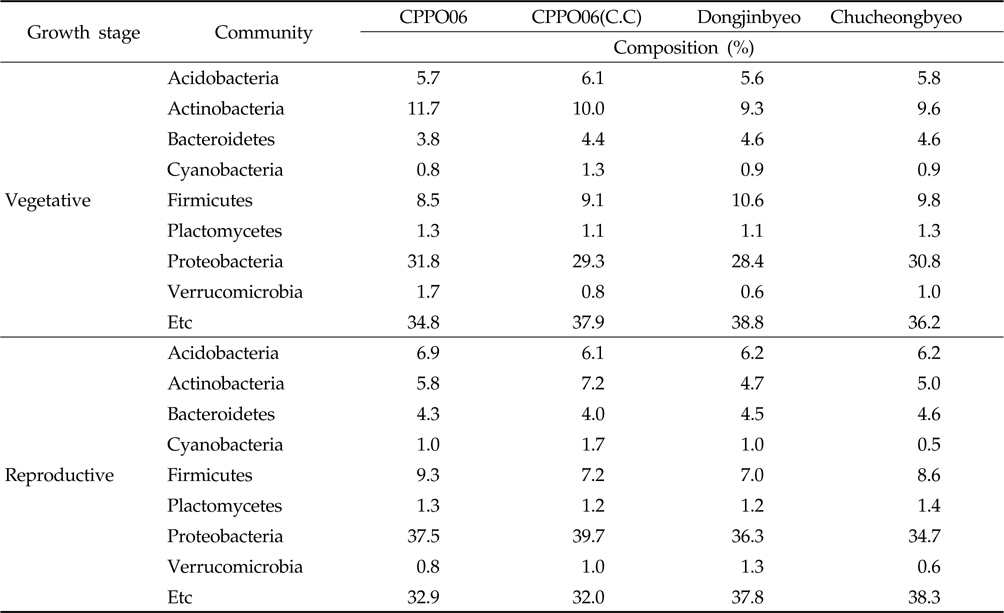
Bacteria isolated from the rhizosphere soils cultivated with GM and non-GM rice in the fields
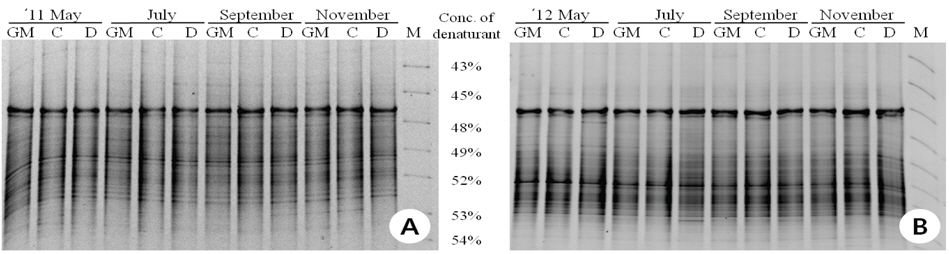
제초제내성 벼와 비 형질전환 벼를 재배한 토양 DNA를 추출하고 16S rRNA를 특이적으로 증폭하여 DGGE 분석법으로 근권 토양 미생물 군집을 비교하였다(Fig. 1). 제초제내성 벼, 동진벼(모본)와 추청벼(재배종)의 시기별 근권 토양 DGGE profile은 거의 유사하였다. DGGE profile을 기반으로 밴드가 나타난 양상을 분석한 결과, 공시재료인 벼의 종류에 따른 그룹이 형성되기 보다는 토양의 채취 시기에 따라 그룹이 형성되는 것으로 나타나 제초제내성 벼 재배에 의한 토양 미생물 군집의 변화는 거의 일어나지 않을 것으로 추정되었다. Glufosinate 제초제내성 벼 재배토양의 시기별 DGGE 분석(Kim
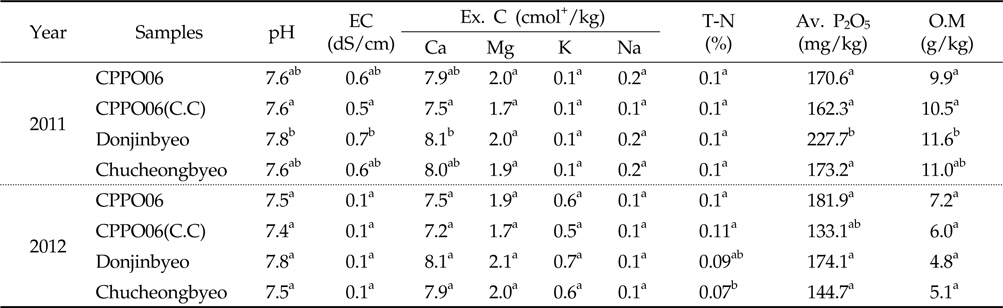
토양 미생물 군집의 변화에 의한 토양 화학성 변화는 상호반응하므로 토양 pH, 유효인산, 전기전도도, 양이온, 전질소, 유기물 함량 등을 분석하여 제초제내성 벼와 비 형질전환 벼재배에 의한 근권 토양의 화학성 변화를 조사하였다(Table 3). 토양 pH는 7.4-7.8로서 우리나라 논 토양의 평균 pH인 5.8(Jung
[Table 3.] Chemical properties in the rhizosphere soils cultivated with GM and non-GM rice
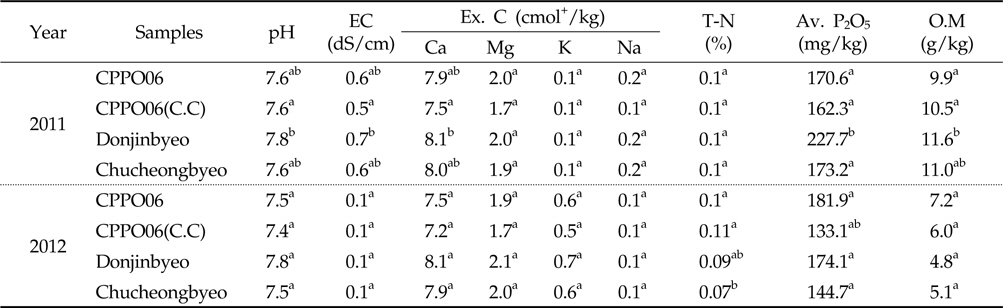
Chemical properties in the rhizosphere soils cultivated with GM and non-GM rice
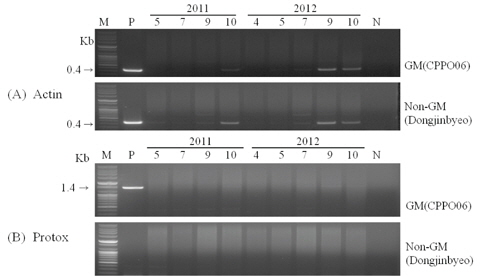
형질전환 시 도입된 유전자의 근권 토양 미생물로의 수평적 유전자 이동을 위해서는 우선 충분한 양의 DNA가 토양내에 존재해야만 가능하다. 도입 유전자의 잔존성을 확인하기 위하여 식물체 및 식물체를 재배한 근권 토양으로부터 DNA를 분리하고 도입 유전자를 특이적으로 증폭하는 primer로 PCR을 수행하였다(Fig. 2). 식물체의 PCR 결과, 제초제내성 벼는 도입 유전자와 내재 유전자가 함께 증폭되었지만, 비 형질전환 벼는 내재 유전자 밴드만 검출되었다. 근권 토양 DNA의 내재 유전자 PCR 결과, 생육중기까지는 증폭된 밴드가 검출되지 않다가 생육후기인 9월과 10월 토양 DNA에서 증폭된 밴드가 나타났지만 월동 후 차년도에 채취한 4월 토양 DNA에서는 증폭된 밴드를 검출할 수 없었다. 도입 유전자(protox)는 전체 생육시기에 걸쳐 증폭된 밴드가 나타나지 않아 토양 내 잔존성은 내재 유전자보다 낮을 것으로 예상되어 근권 토양 미생물로의 수평적 유전자 이동 가능성은 희박할 것으로 추정되었다. Widmer 등(1997)은 형질전환체 선발에 이용된 항생제 저항성
본 실험 결과 근권 토양에서 도입 유전자가 일정 기간이후 잔존하지 않고 식물로부터 토양 미생물로의 유전자 전달 빈도는 매우 낮거나 제한적이기 때문에, 현재의 과학기술로 검출할 수 있는 한계 이하로 존재할 것으로 예상되어 Germida와 Dunfield(2004)의 연구 결과와 같이 제초제내성 벼로부터 주변 생물체로의 수평적 유전자 이동 가능성은 매우 희박 할 것으로 추정되었다. 그러나 연작 등으로 유전자변형 벼의 재배가 지속적으로 이루어질 경우 유전자변형 작물로부터 근권 토양 미생물로의 유전자 이동 가능성은 높아질 것으로 예상되기 때문에 추후 장기적인 모니터링을 포함해 지속적인 연구가 이루어져야 할 것으로 예상되었다.