석회시용에 의한 카드뮴의 부동화와 식물이용성 저감효과를 구명하기 위해 우리나라의 대표적인 석회비료인 소석회를 선정하여 소석회에 의한 논토양 내 카드뮴의 부동화 기작과 벼의 카드뮴 흡수특성을 조사하였다. 소석회는 토양의 pH와 음하전도를 증대시켜 카드뮴의 흡착을 증대시키는 것으로 조사되었다. 소석회의 처리량을 증가시킴에 따라 식물이 이용하기 쉬운 형태인 유효태 카드뮴과 치환성 및 carbonate 결합태 카드뮴의 함량이 유의적으로 감소하였다. 소석회를 8,000mg/kg 과량으로 시용하였을 때 CdCO3 형태로의 침전이 가능하였을 것으로 판단되나 8,000 mg/kg 이하로 처리하였을 때 CdCO3나 Cd(OH)2 형태로의 침전은 없었던 것으로 조사되었다. 또한 토양의 pH와 음하전도는 유효태 카드뮴과 치환성 및 carbonate 결합태 카드뮴의 함량과 유의한 부의 상관관계를 나타내었다. 따라서 소석회에 의한 토양 내 카드뮴의 부동화는 CdCO3나 Cd(OH)2 형태로의 침전형성에 의한 것이 아니라 pH와 음하전도의 증대에 기인된 카드뮴 이온의 흡착에 의한 것으로 판단되어 졌다. 논토양의 현장조건에서 소석회의 시용에 의한 벼의 카드뮴 흡수농도 저감효과를 시험한 결과, 소석회의 시용량을 증가시킴에 따라 벼의 카드뮴 흡수농도는 유의적으로 감소하는 결과를 나타내었다.
Many studies associated with cadmium (Cd) immobilization using lime fertilizer have been conducted for several decades. However, these studies did not suggest exact mechanism of Cd immobilization using lime fertilizer and evaluated effect of lime fertilizer on Cd phytoavailability in rice paddy soil under field condition.
This study was conducted to determine exact mechanism of Cd immobilization using lime fertilizer and evaluate liming effect on Cd uptake of rice in contaminated paddy soil. Ca(OH)2 was mixed with Cd contaminated arable soil at rates corresponding to 0, 1,000, 2,000, 4,000, and 8,000 mg/kg. The limed soil was moistened to paddy soil condition, and incubated at 25℃ for 4 weeks. NH4OAc extractable Cd concentration in soil decreased significantly with increasing Ca(OH)2 rate, since Ca(OH)2 markedly increased net negative charge of soil by pH increase, and decreased bioavailable Cd fractions (F1; exchangeable + acidic and reducible Cd fraction). Calculated solubility diagram indicated that Cd solubility was controlled by soil-Cd. NH4OAc extractable Cd and F1 concentration were negatively related to soil pH and negative charge. Ca(OH)2 was applied at rates 0, 2, 4, and 8 Mg/ha and then cultivated rice in the paddy soil under field condition. Cadmium concentrations in grain, straw, and root of rice plant decreased significantly with increasing application rate of Ca(OH)2.
Alleviation of Cd phytoavailability with Ca(OH)2 can be attributed primarily to Cd immobilization due to the increase in soil pH and negative charge rather than precipitation of Cd(OH)2 or CdCO3, and therefore, Ca(OH)2 is effective for reducing Cd phytoavailability of rice in paddy soil.
광물학적으로 카드뮴(Cd)은 금(Au)과 함께 산출되며 금속광산에서 채광 후 선광과 제련의 과정에서 외부환경으로 노출된다. 토양이 카드뮴으로 오염되는 주요원인은 금속광산에서 채광⋅선광⋅제련과정의 광업활동으로 인하여 배출되는 광산폐기물(폐석⋅광미⋅광재⋅광산폐수 등)에 의한 것이다. 전 세계적으로 카드뮴은 우리나라를 포함한 동북아시아, 북미, 호주 등 넓은 지역에서 산출되고 있으며, 특히 우리나라는 연간 2,582 ton을 생산하는 세계최대의 카드뮴 생산국가이다(Hetherington
광산인근 카드뮴으로 오염된 농경지 토양을 복원하는 방법은 처리방법에 따라 크게 생물학적 처리방법, 물리적 처리방법, 화학적 처리방법으로 구분할 수 있다. 현재까지 이 부분에 대한 연구는 눈부신 발전을 거듭해왔으나, 각 기술의 현장 적용성은 늘 의문시되어 왔다. 또한 광산인근 농경지는 주로 산간지에 위치하고 있어 토지가격이 낮고 개발가능성과 생산성이 매우 낮아 복원을 위해 경제적 타당성이 있는 복원방법을 선발하는 것이 무엇보다 중요한 요인이라 할 수 있다. 농경지에 값싼 농자재인 석회비료를 처리하여 화학적으로 카드뮴을 안정화하는 기술은 비용 면에서 타 기술에 비해 높은 경쟁력을 가지고 있을 것으로 분석된다. 또한 석회비료는 농민들이 현재 영농활동에 이용하고 있는 자재로써 시중에서 구입이 용의하다는 장점을 가지고 있어 광산인근 카드뮴 오염 농경지 복원에 가장 적용성이 높을 것으로 평가된다.
토양 내에서 카드뮴은 양이온의 형태로 존재하며 이동성이 다소 높아 비교적 식물에 흡수가 용이한 것으로 알려져 있다. 토양 내 카드뮴의 이동성과 식물에 대한 카드뮴의 이용성은 토양의 이화학적 특성에 크게 영향을 받는다(Naidu
석회를 시용하면 토양의 pH를 개선할 수 있으며 카드뮴의 이동성을 크게 저감할 수 있다. 석회를 시용하여 토양 내카드뮴의 용해도와 식물체 흡수를 저감시키기 위한 연구는 과거부터 오랜 기간 연구되어 왔으며 이미 국내외적으로 여러 연구에서 석회의 효과를 입증해 왔다(오왕근, 1981;이민효등, 1984; 정구복 등, 1999; 김민경 등, 2004; Anderson and Siman, 1991; Kreutzer, 1995; Gray
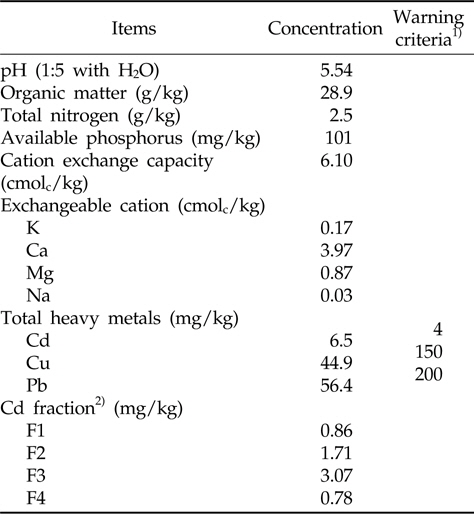
본 연구를 수행하기 위해 경남 합천군 술곡리의 봉산광산(128°01'N 34°37'E) 인근 논토양을 공시토양으로 선정하였다. 대상지역의 토양은 칠곡통에 속하는 토양이었으며 점토6.1%, 미사 35%, 모래 58.9%를 포함하는 사질양토(sandy loam)이었다. 공시토양의 이화학적 특성은 Table 1에 나타냈다. 공시토양 내 조사된 중금속 중 카드뮴(Cd)의 함량은 토양오염우려기준(4.0 mg/kg)을 초과하였다. 공시토양 내 존재하는 카드뮴의 형태는 주로 유기물 결합태 카드뮴(F3; oxidizable Cd fraction)과 철⋅망간 산화물 결합태 카드뮴(F2; reducible Cd fraction)인 것으로 조사되었다.
[Table 1.] Chemical properties of the soil before the test
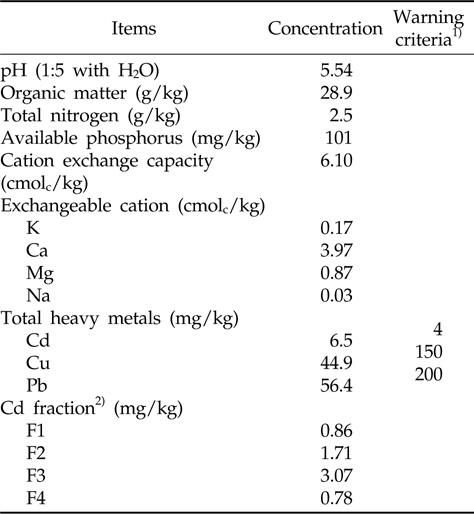
Chemical properties of the soil before the test
논토양 내 카드뮴의 부동화에 대한 석회의 효과를 조사하기 위하여 시중에서 판매되고 있는 소석회비료를 공시석회제재로 선발하였다. 인큐베이션 시험을 위해 플라스틱 용기 내 건토 500 g에 소석회를 건중량으로 1,000, 2,000, 4,000, 8,000mg/ kg으로 처리를 하였다. 플라스틱 용기에 소석회와 혼합된 토양을 가비중이 1.2 g/ cm3이 되도록 충진하고 진비중(2.65 g/cm3)을 이용하여 pore volume 227.6 cm3을 얻었다. 논토양 조건을 유지하기 위해 증류수 300 ㎖씩 첨가하였으며 토양의 일정한 환원상태를 유지하기 위해 2일에 한 번씩 무게를 측정하여 유실된 수분을 보충하였다. 처리되어진 토양은 암조건의 인큐베이터에 25℃에서 4주간 놓아졌다. 처리구는 3반복으로 설치되었으며 각 처리구는 인큐베이터 안에 완전임의배치법에 따라 놓아졌다. 4주간의 인큐베이션 후 토양 내 유효태 카드뮴(NH4OAc extractable Cd)함량(Gommy et al., 1998; Brun et al., 2001)과 토양 pH와 음하전도가 측정되어졌다.
현장조건에서 소석회의 처리에 따른 벼의 카드뮴 흡수특성을 조사하기 위해 2007년 6월 중순에 동진벼를 이앙하여 동년 10월 중순에 수확하여 알곡, 볏짚, 뿌리 내 카드뮴농도를 조사하였다. 처리구는 소석회를 0, 2, 4, 8 Mg/ha로 벼이앙 2주 전에 시용하여 3반복으로 실시하였다. 모든 처리구에 질소(N 110 kg/ha)와 인산(P2O5 30 kg/ha)과 가리(K2O 30 kg/ha)를 동일한 양으로 처리하였다.
공시토양의 이화학적 분석방법은 다음과 같은 방법을 따랐다: pH(1:5 토양:물), 유기물 함량(Wakley and Black method; Allison 1965), 총질소 함량(Kjeldahl method; Bremner, 1965), 치환성 양이온 K+, Ca2+, Mg2+, Na+ (1 M NH4-acetate pH 7.0, ICP-OES, inductively coupling plasma optical emission spectroscopy, Perkin elmer model DV 4300, Shelton, CT, USA). 유효인산의 함량은 Lancaster method (RDA, 1988)를 이용하여 분석하였다.
유효태 카드뮴의 함량은 토양:용액 비 1:5의 비로 1 M NH4OAc로 1시간 침출한 후 여과하여 ICP-OES로 Cd의 함량을 분석하였다.
토양의 음하전도를 측정하기 위하여 토양 5 g을 centrifuge tube에 담고 1 M NaCl 30ml을 가하여 1 시간 동안 교반한후 원심분리하여 상등액을 따라내고 남아 있는 토양에 ethyl alcohol 20 ml을 가하여 남아있는 침출액을 3회 반복하여 씻어냈다. ethyl alcohol을 분리시킨 후 상등액은 따라내고 남은 토양에 1 M NH4OAc 30 ㎖을 가하여 1 시간 동안 침출하였다. 침출 후 여과시켜 여과액 내의 나트륨(Na)의 함량을 ICP-AES (Inductively Coupled Plasma Absorption Emission Spectrophotometer, GBC model X-100, Australia)로 분석하여 음하전도를 구하였다.
카드뮴 형태별 함량은 연속추출법에 의해 조사하였다(Ure
수확 후 벼를 알곡, 볏짚, 뿌리로 분리시킨 후 드라이 오븐에서 70℃에서 72시간 동안 건조 후 분쇄하였다. 분쇄된 시료 1 g을 채취하여 ternary solution 으로 분해시킨 후 ICP-AES로 Cd의 함량을 측정하였다.
실내시험 후 토양 용액 내 카드뮴 화학종의 침전양상을 조사하기 위해 Visual MINTEQ (ver 2.23)모델링 프로그램을 사용하였다. 모델링을 실시하기 위해 이온세기와 pH는 각 처리구에서 조사된 수치로 고정되었으며 양이온 (Cd, Ca, K, Mg, Na, Pb, Ni, Zn, Fe, Mn, NH4)과 음이온(PO4, Cl, CO3, NO3, SO4)의 함량을 몰(mol/L)단위로 대입하고 dissolved organic carbon (DOC)의 함량도 대입되었다.
4주간의 실내시험 후 토양 내 카드뮴 화학종 규명을 위한 모델링을 실시하기 위해 표층수를 따라낸 후 플라스틱 용기내 습토를 15 분간 6,000 rpm으로 원심분리하여 토양 용액(pore water)을 얻었다. 상등액은 0.45 ㎛ membrane filter로 여과된 후 양이온 (Cd, Ca, K, Mg, Na, Pb, Ni, Zn, Fe, Mn, NH4)과 음이온(PO4, Cl, CO3, NO3, O4) 그리고 DOC의 함량 분석에 이용되었다. 양이온 중 Cd, Ca, K, Mg, Na, Pb, Ni, Zn, Fe, Mn은 ICP-AES에 의해 측정되었으며 NH4의 함량은 비색법으로 측정되었다(Sparks, 1996). 음이온 중 PO4, Cl, NO3, SO4의 함량은 이온크래마토그래피(Ion Chromatograph Dionex Corporation Model ICS-2000 IC, USA)에 의해 측정되었으며 CO3의 함량은 적정법에 의해 측정되었다(U.S. Sanlinity Laboratory Staff, 1954). DOC의 함량은 TOC 분석기 (Shimadzu Model TOC-VCPN, Japan)에 의해 분석되었다.
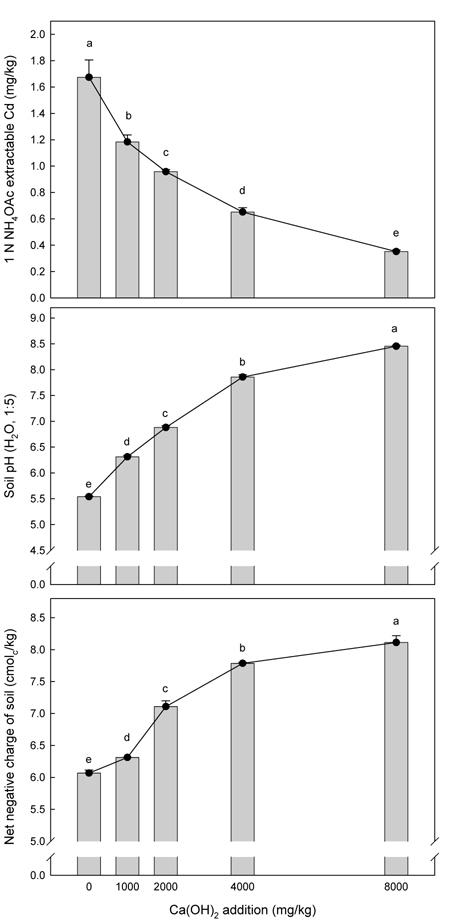
실내에서 4주간 인큐베이션 시험을 실시한 결과, 소석회의 처리량을 증가시킴에 따라 유효태 카드뮴의 함량은 유의하게 감소하는 것으로 나타났다(Fig. 1). 유효태 카드뮴의 함량은 무처리의 1.67 mg Cd/kg에서 소석회를 8,000 mg/kg로 처리하였을 때 0.35 mg Cd/kg까지 감소하였다. 토양의 pH는 토양교질의 가변전하를 변화시키는 중요한 요인 중의 하나이며(Barrow, 1985), 토양의 pH가 증대하게 되면 토양교질과 유기물의 작용기로부터 수소이온(H+)이 토양 용액으로 해리되어 나와서 토양의 음하전도는 증대하게 된다(Thoma and Hargrove, 1984; Curtin
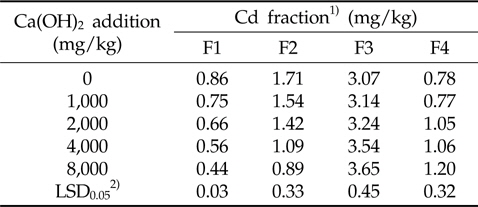
연속 침출법을 이용한 중금속의 분획특성조사는 중금속으로 오염되어진 토양 내 중금속의 이동특성을 평가하는데 이용되어져 왔다(Sposito
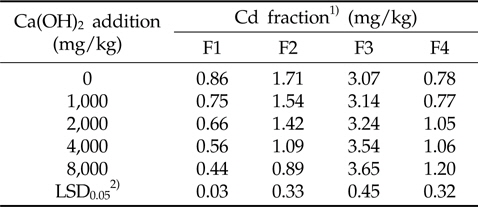
Distribution of Cd fractions in soil amended with different rates of Ca(OH)2 after 4 weeks of incubation at 25 ℃
소석회의 시용에 의해 카드뮴은 토양 내 침전반응을 통해 CdCO3나 Cd(OH)2를 형성하여 부동화되어질 수 있다. 토양 내 화학반응 예측 모델인 Visual MINTEQ에 의해 조사된 카드뮴화합물(Cd minerals)의 반응식은 Table 3에 나타내었다.
[Table 3.] Solubility products of cadmium minerals (Lindsay, 1979)

Solubility products of cadmium minerals (Lindsay, 1979)
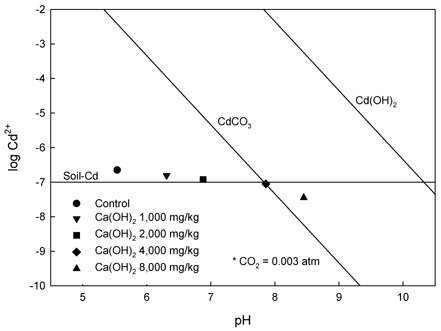
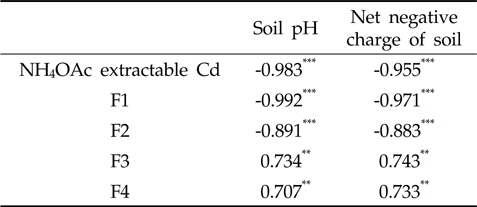
소석회를 8,000 mg/kg으로 처리하였을 때 토양 용액 내 카드뮴의 농도는 CdCO3에 대하여 과포화상태로 존재하는 것으로 나타났으나 8,000 mg/kg 이하의 처리량에서 토양 내카드뮴의 용해도는 Soil-Cd(토양교질에 흡착된 카드뮴)에 의존하는 것으로 나타났다(Fig. 2). 토양의 pH가 8.0 이상이 되면 카드뮴은 CdCO3를 형성하여 부동화되게 된다(Lindsay, 1979). 소석회를 8,000 mg/kg 과량으로 시용하였을 때 토양의 pH는 8.5까지 증대되어 CdCO3 형태로의 침전이 가능하였을 것으로 판단된다. 그러나 소석회를 8,000 mg/kg 이하로 처리하였을 때 토양의 pH는 8.0 이하로 나타났으며 카드뮴은 주로 토양교질에 흡착되어 부동화되는 것으로 판단된다. 이러한 결과는 토양 내 카드뮴의 함량과 토양 pH 및 음하전도와의 상관관계에 의해 증명되어진다(Table 4). 토양의 pH와 유효태 카드뮴의 함량 및 F1의 함량은 유의한 부의 상관관계를 나타내었다. 또한 토양의 음하전도와 유효태 카드뮴의 함량 및 F1의 함량은 유의한 부의 상관관계를 나타내었다. 즉, 이러한 결과는 토양의 pH와 음하전도가 증대하게 되면 토양교질에 대한 카드뮴의 흡착이 증대하게 되어 부동화되어 진다고 해석될 수 있다. 이상의 결과를 토대로 볼 태 소석회에 의한 토양 내 카드뮴의 부동화는 CdCO3나 Cd(OH)2 형태로의 침전형성에 의한 것이 아니라 pH와 음하전도의 증대에 기인된 카드뮴 이온의 흡착에 의한 것으로 판단된다.
[Table 4.] Correlation coefficient between soil Cds and soil properties
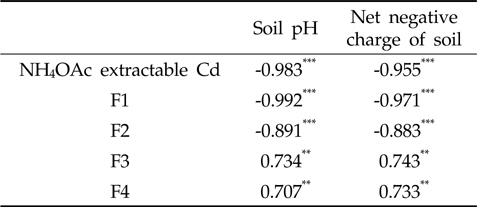
Correlation coefficient between soil Cds and soil properties
벼의 재배기간 동안 가시적인 독성현상은 관찰되지 않았다. 카드뮴은 식물의 생육을 저해하거나 가시적인 독성을 유발할 수 있다(John
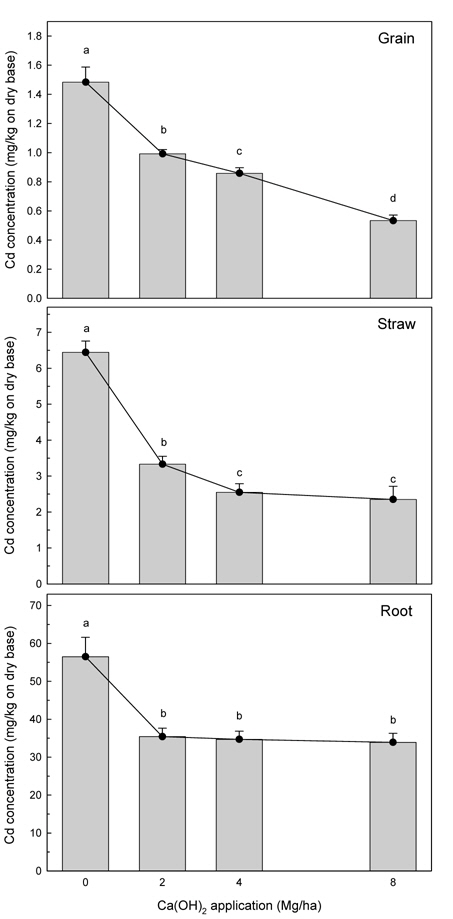
소석회 무처리구에서 벼의 카드뮴 흡수농도는 알곡에서 1.48 mg Cd/kg, 볏짚에서 6.44 mg Cd/kg, 뿌리에서 56.5 mg Cd/kg으로 각 부위별로 카드뮴의 흡수농도가 현저히 다른 것으로 나타났다(Fig. 3). 벼의 카드뮴 흡수농도는 뿌리>볏집>알곡 순으로 높았으며 뿌리 내 카드뮴의 흡수농도가 볏짚과 알곡에 비교하여 상당히 높은 것으로 나타났다. 이러한 결과는 알타리무의 카드뮴 흡수특성과 다른 것으로 발견되었다. 밭토양 조건에서 실시되어진 이전의 연구결과에서는 알타리무의 지상부의 카드뮴 흡수농도가 지하부의 카드뮴 흡수농도보다 약 2 배가량 높은 것으로 조사되었다(Bingham, 1979; Hong
소석회의 시용량을 증가시킴에 따라 벼의 각 부위별 카드뮴의 흡수농도는 유의적으로 감소하였다(Fig. 3). 소석회의 시용량을 최대 8 Mg/kg으로 시용하였을 때 무처리에 비해 각부위별 카드뮴 흡수량은 알곡에서 64%, 볏짚에서 63.5%, 뿌리에서 40%로 현저히 감소되어 졌다. 몇몇 연구자들이 밭토양의 조건에서 소석회의 처리에 의해 식물체 내 카드뮴의 흡수농도가 저감된다는 사실을 보고하였다(Basta and Sloan, 1999; Gray