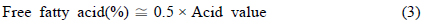The focus of this study was to observe the growth of
석유파동과 환경오염 등의 복합적인 문제는 신재생에너지의 확보와 개발을 위한 다양한 연구와 노력으로 이어져 한편에서는 전기, 수소 등의 새로운 구동 시스템을 이용하기 위한 노력을 진행하고 있으며 다른 한편에서는 기존의 연료를 대체하는 새로운 연료들을 개발하고 있다(Brennan and Owende, 2010). 휘발유 또는 디젤을 대체할 수 있는 가장 유력한 연료로 인식되고 있는 것은 지속적으로 이용할 수 있는 재생자원인 바이오매스를 통해서 생산되는 바이오연료들이다(Demirbas, 2009). 이미 브라질 등에서 이용하고 있는 바이오 에탄올, 바이오 디젤 등은 대체 연료로서 인정을 받고 있다. 바이오디젤(biodiesel)은 석유 기반인 경유의 대안으로 식물성 기름이나 동물성 지방과 같이 재생 가능한 자원을 바탕으로 제조된다(Demirbas, 2009; Halim et al., 2012). 바이오디젤은 긴 지방산 고리를 가진 단일알킬 에스터 혼합물이며 지방산 메틸에스테르로 구성되어 있고 에스테르 작용기의 산소 2개를 분자내에 포함하고 있어 함산소 연료라고 할 수 있다. 바이오디젤과 같은 함산소 연료(Oxygenated Fuel)는 연소시 분자에 포함하고 있는 산소가 반응에 참여하면서 연소반응을 촉진하여 완전연소가 쉽고 그에 따른 배기가스 저감효과도 탁월하다(Xu et al., 2006). 바이오디젤은 1 kg 당 3.2 kg의 CO2를 저감할 수 있으며, 특히, SOx 99%, CO2 20%, 탄화수소 32%, 검댕 50%, 입자 39%를 저감할 수 있어 배기가스가 현저하게 개선된다(Gong and Jiang, 2011; Halim et al., 2012). 바이오디젤은 재생 가능한 연료로서 현재의 엔진 기름을 대체할 수 있고, 기존의 시설을 통해 운반, 판매가 가능하기 때문에, 가장 중요한 교통 에너지 자원인 화석 연료의 유력한 대안으로 꼽히고 있다. 그러나 아직까지 바이오디젤은 순수 초저유황 연료의 낮은 윤활성을 향상시키기 위해 경유와 섞어 쓰는 경우가 많다(Demirbas, 2009; Gong and Jiang, 2011). 바이오디젤의 생산과 사용은 특히 유럽과 미국, 아시아에서 급격히 증가하고 있지만, 전체 연료 시장에서 차지하는 비율은 아직 미미하다.
유채, 곡물, 팜, 옥수수 등을 이용하여 바이오 디젤을 생산할 경우 지구상의 식량문제가 아직 해결되지 않은 상태에서 윤리적인 문제에서 자유로울 수가 없고, 환경오염의 문제가 따르기 때문에 상대적으로 자유로운 미세조류는 바이오디젤을 생산할 수 있는 새로운 원료로 주목받고 있다(Choi et al., 2013; Wijffels and Barbosa, 2010). 또한 미세조류는 바이오디젤 뿐만 아니라 건강식품, 바이오 수소, 이산화탄소 고정 및 어류의 먹이로도 사용할 수 있다. 그러나 현재 미세조류의 생산성은 아직까지 기존 화석연료에 비해 1/5 - 1/10 수준으로 경제성이 떨어진다(Chisti, 2007). 이에 따라 최근에는 미세조류의 생산성을 높이기 위해 우수 세포주의 탐색과 동시에 생명공학 기술을 이용하여 고지질 및 고생산성 미세조류를 개발하는 연구가 진행되고 있다(Chisti, 2007; Choi and Lee, 2014). 미세조류 바이오에너지가 기존 화석연료에 대해 경쟁력을 가지기 위해서는 지질생산성을 높이는 것이 중요하다(Brennan and Owende, 2010). 미세조류는 염색체의 수가 2개에서 24개까지 다양하고, 지금까지 알려진 미세조류 유전체의 크기(genome size)는 11 Mb에서 138 Mb 이다. 수많은 미세조류를 대상으로 지질함량을 조사한 결과, 미세조류의 종(species) 및 세포주에 따라서 건중량(dry weight) 대비 지질함량이 1%에서 85%까지로 다양하며, 지방산의 사슬길이(chain length)도 C10에서 C24까지 다양하다(Schenk et al., 2008). Wijffels and Barbosa (2010)는 높은 광 조건에서 잘 자라고, 얇은 막을 가지며, 세포의 크기가 커야하며, 고농도 산소조건에서 잘 생장할 수 있고, 증식과 동시에 지질 축적이 가능하고, 세포들이 잘 응집되어 수확이 편리하고, 감염 등에 강하고, 세포밖으로 지질 분비할 수 있는 미세조류 세포주가 바이오에너지 용도로 이상적 일 것으로 제안하였다. 향후 미세조류의 생명 공학적 개량방법을 이용하여 광합성에 영향을 주는 여러 요인들을 조작함으로써 생장속도를 높여 바이오매스 생산이 수배 증가할 것으로 기대되며, 지방산생합성 및 Triacylglycerols (TAG) 축적량을 증가시킴으로써 지질생산량을 높이는 것이 가능할 것이다.
미세조류의 지질 함량은 배양환경에 차이를 보이며,
본 연구에 사용된
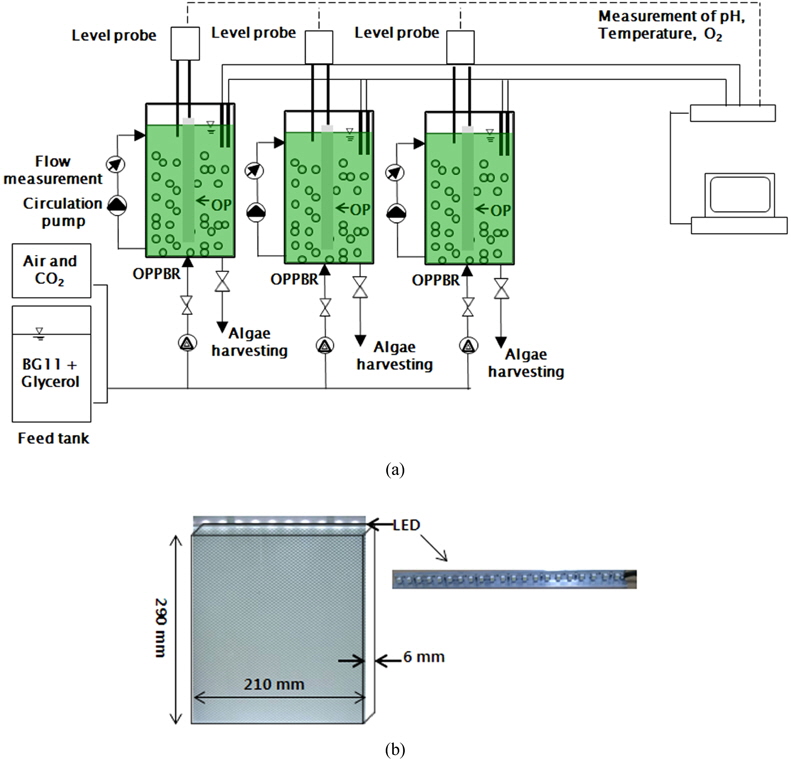
Glycerol은 미세조류의 바이오디젤을 생산한 후에 발생한 것을 사용하였으며 15 L의 OPPBR (Optical panel photobioreactor) 반응기에 BGII를 넣고 복합영양소로 Glycerol을 각각 0, 2, 5, 10 g/L를 투입하여 Glycerol 양이 미세조류 생산량과 지방산함유량에 미치는 영향을 알아보았다. 미세조류 배양을 위하여 배양기의 광원은 LED (Light Emitting Diode)를 사용하였다. LED는 미세조류에 필요한 파장의 빛을 선택적으로 사용할 수 있어 효율적이다. 실험에 사용한 LED 램프는 optical panel (OP)에 삽입되는 빛의 집중도를 향상시키기 위해 bar 형식의 LED 램프를 특별 제작하였으며, LED에 공급되는 전원은 모델 FP-60-12 파워공급기(AD & Lighting, Suwon, Kyonggi-Do, Korea)를 사용하였다. 모든 광원은 위에서 아래로 공급하였다. LED는 white색상을 사용하였으며 광합성에 사용되는 빛의 양을 나타내는 광량은 ~250 μmol photon/m2/s, 초기
Fig. 1(b)에 도광판(optical panel)을 나타내었다. 실험에 사용한 도광판은 210 mm (가로) × 290 mm (세로) 크기이며, 빛의 투과율이 좋은 Poly-Methylmethacrylate (PMMA)로 제작하였다. 일반적인 v-cut 방식은 뒷면에 홈을 내어 반사판을 이용하여 전면으로 빛을 방출시키나 본 실험에서는 도광판 양면에 v-cut 을 제작하여 빛이 양면으로 분산되게 하였다. v-cut 방식은 빛의 분포를 최대한 균일하게 분사시키기 위해 광원으로부터 멀어질수록 v-cut의 간격을 줄이고, 깊이를 늘리는 방법을 사용한다. 따라서 v-cut 방식은 홈의 간격과 홈의 각도를 이용하여 빛의 분산도를 조절하기 때문에 홈이 없는 flat plate에 비해서 빛의 효율이 높다 (Choi et al., 2013). v-cut 도광판은 비중이 1.19, 광투과율이 93%, 열변형 온도는 94°C 그리고 성형 수축률은 0.2 - 0.6% 이다.
OPPBR 반응기(Fig. 1(a))는 230 mm (가로) × 230 mm(세로) × 300 mm (높이) 의 크기이며, 반응기의 총용량은 15 L, 공기 주입률은 0.5 L/min로 지속적으로 공기를 주입했으며, 공기 주입률에 따른 CO2의 주입량은 0.02 vvm 이다.
도광판은 반응기의 정 가운데에 삽입하여 빛이 반응기 전체에 균일하게 전달되도록 하였으며 도광판 삽입 양쪽반응기의 거리는 각각 115 mm 였다. 선행연구(Choi and Lee, 2014) 결과 도광판은 6 mm 두께가 경제성이나 빛의 분산율에서 다른 두께보다 뛰어나 본 실험에서는 6 mm 두께의 도광판을 사용하였다(Fig. 1(b)).
628 g에서 15분 동안 원심분리를 이용하여 수확한 미세조류는 습식오일 추출을 하였으며, 용매추출법에 사용된 용매는 핵산(Junsei 96%)을 사용하였다. 습식오일 추출은 습중량 1 g 의 미세조류를 포함한 3.3 mL 시료를 이용하였으며, 미세조류의 양은 용매 대비 5%(w/w)였다. 핵산과 혼합한 미세조류를 3시간 동안 교반한 후 오일을 포함한 용매층을 회수하여 감압증발(Genevac, EZ2 PLUS)하였고, 용매를 휘발시키고 남아있는 오일을 회수하였다. 오일의 완전한 회수를 위하여 위와 같은 추출법을 3번 반복하였다. 미세조류 오일 추출량은 다음과 같이 계산하였다.
미세조류 및 추출된 미세조류 오일의 총 지방산 함량을 측정하기 위해 수정된 direct trans-esterification법을 사용하였다(AOCS, 2003). 건조 미세조류와 추출 오일 각각 10 mg에 클로로포름-메탄올(2:1, v/v) 2 mL를 넣고 10분간 섞은 후, 내부 표준물질인 heptadecanoic acid-chloroform solution(Sigma-Aldrich, 500 μg/L) 1 mL, 메탄올 1 mL 그리고 황산 0.3 mL을 투입하였다. Vortex mixer로 10분간 섞어준 뒤 100°C 항온조에서 10분간 반응시킨 후 충분히 식혀 증류수 1 mL을 첨가한 뒤 2469 g 에서 10 min 동안 원심분리하여 분리된 용액 중 아래층을 주사기로 뽑아 필터로 여과후 GC (Gas Chromatography, Agilent 7890A, Santa Clara, Califonia, USA)로 분석하였다. 외부 표준물질(Mix RM3, Mix RM5, GLC50, GLC70(Supelco))을 사용하여 지방산의 정량 분석을 수행하였고, 추출된 미세조류 오일 중의 유리지방산 함량은 적정법에 의한 산가분석을 통하여 측정하였다. 산가 및 유리지방산 함량은 다음과 같은 식을 이용하여 계산하였다(Lepage and Roy, 1984).
V = 사용한 KOH 용액의 부피(mL), c = KOH 용액의 몰 농도(M), m = 시료의 질량(g)이다.
미세조류의 지방산 분석은 추출된 오일의 지방산 함량(mg/g oil) 분석 후, 표준 분석조건 EN ISO 5508 (Animal and vegetablefats and oils - Preparation of test sample) 과 EN ISO 550에 따라 분석하였다(CEN, 2001). 250 mg 시료가 내부 표준물질인 methyl heptadecanoate-heptane solution(Fluka, 10 mg/g) 5 mL와 교반한 후 GC (Gas Chromatography, Agilent 7890A, Santa Clara, Califonia, USA)로 분석하였다. FAME의 검출 및 분리를 위해 사용한 컬럼은 capillary Alltech AT-FAME (30 m × 0.25 mm× 0.25 μm)이다. Carrier gas로는 질소(Nitrogen)를 사용하였고, split mode의 split ratio는 45:1로 하였으며 가스 유속은 2.2 mL/min이었다. 오븐의 온도는 250°C까지 증가하며, Injector의 온도는 250°C, 검출기의 온도는 275°C로 하였다.
바이오매스의 증가량을 알 수 있는 미세조류의 건중량은 10 mL의 샘플을 GF/C (Watmann, 영국)로 여과한 후 105°C에서 24시간 건조한 후 그 질량을 측정하였다.
P 는 바이오매스의 생산량(g/L/day), X1 및 X0 는
미세조류의 specific growth rate (생장률)는 아래와 같이 계산하였다.
3.1. Effect of glycerol concentration on the growth of investigated algae species
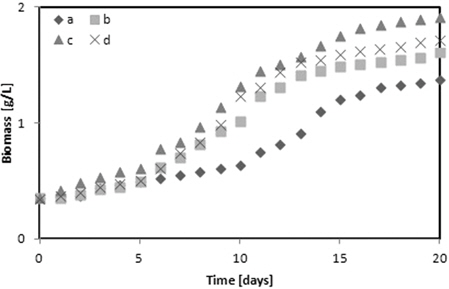
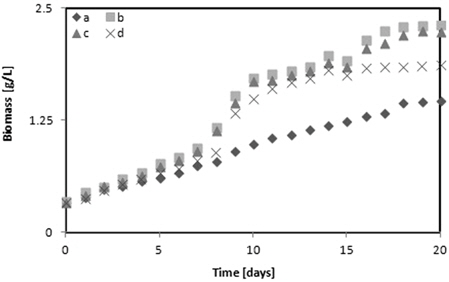
Glycerol은 유기 탄소원으로 미세조류의 광합성과 유기물의 흡수 능력을 향상시켜주는 역할을 한다(Kong et al,.2013). Fig. 2에 다양한 glycerol의 농도가
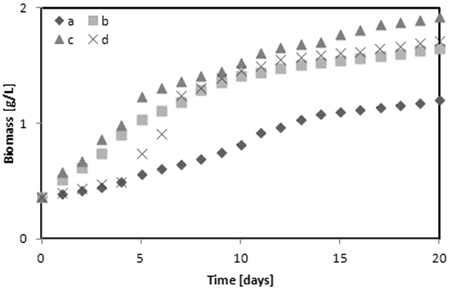
Fig. 3에 다양한 glycerol의 농도에 따른
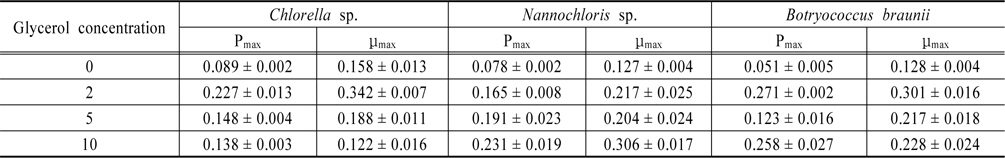
Table 1에 다양한 glycerol의 농도에 따른 최대 바이오매스 생산량(Pmax)와 최대 생장률(μmax)을 나타내었다.
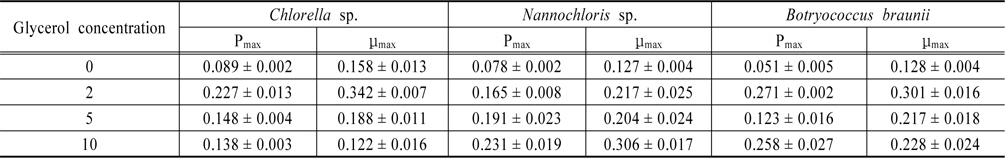
The maximum biomass productivity Pmax and maximum specific growth rate μmax of investigated algae species
Hsieh and Wu (2009)는 투명한 사각형 반응기에 일반 flat panel과 LED를 이용하여
Li et al. (2007)은
3.2. Total fatty acid of investigated algae speci
TAG의 양은 미세조류 종 및 세포주에 따라 다르지만 생장환경에 따라서 크게 차이가 난다. 최적 생장조건에서는 생산된 지방산이 주로 막지질 합성에 사용되며, 이때 막지질의 양은 건중량의 5-20%에 달한다. 그러나 생장환경이 좋지 않거나 스트레스 조건에서는 합성된 지방산이 주로 TAG 축적에 사용되고, 스트레스 조건이 계속되면 세포내 단백질도 TAG 합성에 사용된다(Cagliari et al., 2011; Msanne et al., 2012). 이때의 TAG 함량은 전체 지질의 80%에 달하기도 한다.
바이오디젤은 미세조류에 함유된 TAG (Triacylglycerols)를 에스테르 교환반응(Trans-esterification)을 통하여 전환함으로써 생성된다. 따라서 TAG 함량이 많을수록 바이오디젤의 생산량 또한 많아진다.
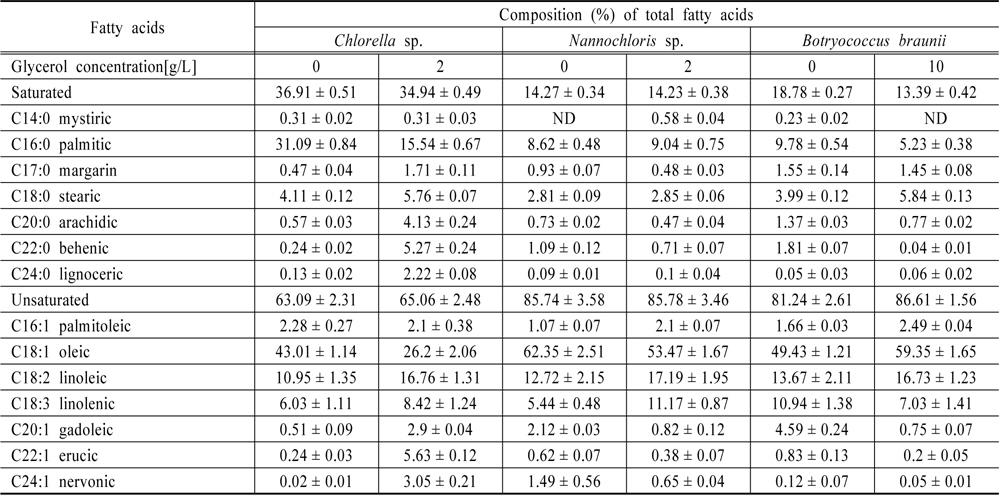
Table 2에서 Total TAG 가 많이 측정된 glycerol 농도와 비교를 위하여 0 g/L glycerol 농도의 포화, 불포화 지방산함유량을 Table 3에 나타내었다. 바이오 디젤의 천연 불포화 지방산(특히 다불포화 지방산)은 활성 메틸렌기를 갖고 있어서 산화반응이 일어나기 쉽다. 이러한 자동산화에 의해 알코올, 케톤 및 알데히드 등 산화물을 생성하여 지질의 열화를 일으킬 것으로 생각된다. 따라서 자동산화는 바이오디젤 연료 성분 중에서 불포화 지방도가 많을수록 빠르게 진행된다. 일반적으로 포화지방산 C18:0 stearic은 안정적이고, C18:1 oleic 보다는 C18:2 linoleic이 산화가 빠르고, C18:2 linoleic 보다 C18:3 linolenic가 산화가 빠르다(Biller et al., 2013; Halim et al., 2012). 불포화 레벨이 증가함에 따라 산화가 약 10배 정도 빠를 것으로 생각된다. 즉, C18:3은 C18:1에 비하여 100배는 빠르게 산화할 수 있다. 본 실험결과 포화지방산은
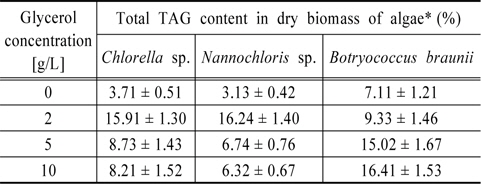
[Table 2.] Total TAG content in dry mass of investigated algae species
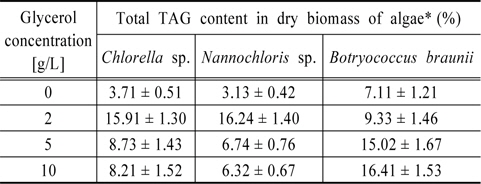
Total TAG content in dry mass of investigated algae species
[Table 3.] Composition of total fatty acid profiles of algae oil
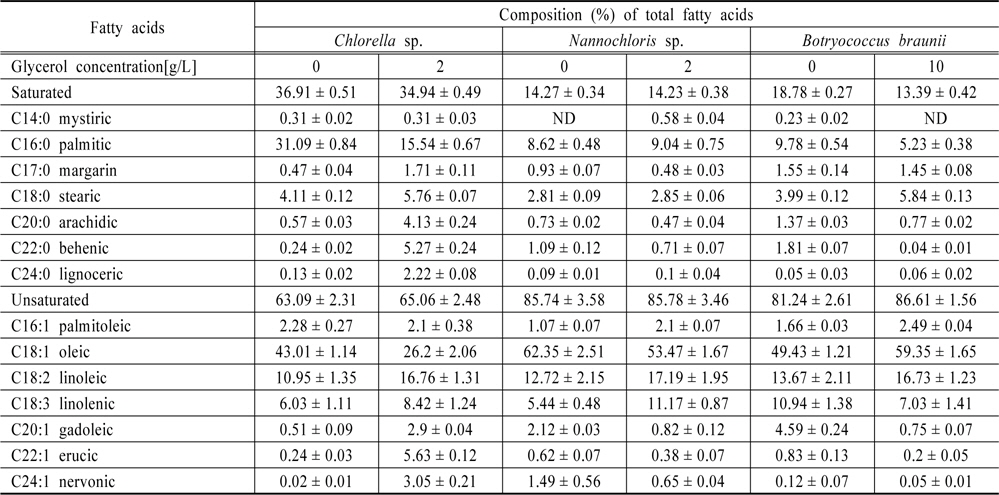
Composition of total fatty acid profiles of algae oil
불포화 지방산 함유량은
다양한 glycerol의 농도가
1) Chlorella sp. 와 Nannochloris sp. 는 5 g/L glycerol에서 그리고 Botryococcus braunii 2 g/L의 glycerol에서 각각 1.91, 1.92 그리고 2.31 g/L의 최대 바이오매스를 나타내었다. Botryococcus braunii 는 2 g/L 와 5 g/L glycerol과의 차이가 미미했다. 그러나 glycerol을 첨가하지 않고 BGII 배지에 증식한 각각의 미세조류와 비교하면 Chlorella sp.는 28.27%, Nannochloris sp.는 37.5% 그리고 Botryococcus braunii 는 36.36%의 높은 최대 바이오매스를 나타내었다. 따라서 바이오매스 증가에 가장 좋은 glycerol의 농도는 5 g/L였다. 2) TAG 함량은 Chlorella sp. 와 Nannochloris sp. 는 2 g/L의 glycerol에서 각각 15.91%와 16.24%, 그리고 Botryococcus braunii 는 10 g/L glycerol에서 16.41%를 나타내어 BGII 배지와 비교하여 12 - 13% 높았다. 3) Glycerol을 복합영양소로 사용했을 때가 glycerol을 사용하지 않았을 때 보다 Chlorella sp. 는 1.97%, Nannochloris sp. 는 0.04% 그리고 Botryococcus braunii 는 5.37% 불포화지방산의 함유량이 높았다. 4) 실험에 사용한 미세조류 중에서 Botryococcus braunii 가 Chlorella sp. 또는 Nannochloris sp.와 비교하여 바이오매스 증식이 빨랐고, 지질함량과 불포화지방산 함량이많았다.