The knowledge on the migration of antimony (Sb) from PET bottles into the water is of greate concern. Antimony in all bottled water marketed in korea and in raw water was analyzed. The detection rate of antimony in total bottled water was 88 % and 100% in PET (Polyethylene terephthalate, PET), 55% in PC (Polycarbonate, PC) bottled water. 55% of raw water contained antimony. The average concentration of Sb in PET bottled water was 0.39 μg/L, higher than PC bottles (0.20 μg/L) and the raw water (0.22 μg/L). The migration of Sb into water that is stored in different conditions (room temperature, 45℃, and direct sunlight exposure) was investigated for 180 days. The migration tendency increased with the storage time and temperature. PET bottles showed a sharp increase of Sb concentration at 45℃, but there was no differences between the room temperature and sunlight exposure. The Sb migration in all simulated solution(deionized water, 4% acetic acid, and 20% ethanol) also increased with storage time and temperature. The Sb migration values ranged from 0.35 to 0.49 μg/L in all simulated solution, which was far below the permissible korean migration level of 40 μg/L. There was a tendency that the number of re-use of a bottle and the amount of leaching were in inverse proportion.
안티몬은 자연유래 무기물질로 지각에 0.3 mg/kg 정도로 존재, 납(15 mg/kg), 비소(1.5 mg/kg)보다 낮은 함량을 보이는 희귀원소이며 대부분 불용성인 황화합물 형태로 존재한다(Shotyk et al., 2006). 안티몬은 섬유와 플라스틱의 난연제, 납축전지, 금속접합제 등 여러 용도로 사용되며 음료수 용기인 PET 제조 시 촉매제, 구충제 등의 의약품에도 사용된다. 호흡을 통한 인체 노출 시 폐암을 일으키는 발암물질로 국제암협회(IARC)에서 2B물질로 지정하고 있고, 과량의 경구 노출시 구토, 설사 등의 급성독성을 일으킨다고 알려져 있다(IARC, 1989; WHO, 2008). 먹는샘물 용기 재질인 Polyethylene terephthalate(PET)는 테레프탈산(terephthalic acid)과 에틸렌글리콜(ethylene glycol)을 원료로 에스테르반응과 중합공정을 통해 생산되며 중합공정에서 안티 몬, 티타늄, 게르마늄이 촉매제로 사용되는데, 가격경쟁력, 용기의 색과 투명성 등 여러 이유로 전 세계 PET의 90%이상이 안티몬을 촉매로 제조되고 있다(MacDonald, 2002 ; Westerhoff et al., 2008). Nishioka et al. (2002)의 페트용기에서의 안티몬 함량조사 결과에 따르면, 중합공정에서 안티몬 촉매의 사용 여부에 따라 용기의 안티몬 함량이 170 ~ 220 mg/kg 또는 불검출로 큰 차이를 보이는데, 안티몬대신 게르마늄, 또는 티타늄을 사용하는 경우 용기의 안티몬 함량은 검출한계 이하로 나타난다.
유럽연합 등에서는 안티몬을 자연유래 유해물질로서 먹는샘물(Natural mineral water)의 수질기준으로 운영하고 있으며, 동시에 PET의 이행기준을 설정하여 관리하고 있다(EU, 2003, 2011). 세계보건기구(WHO)는 안티몬의 권고기준을 20 μg/L로 제시하고 있으며, 유럽연합(EU) 5 μg/L, 미국과 캐나다가 6 μg/L 등 국외 대부분의 국가에서 수돗물 및 먹는샘물의 수질기준으로 관리하고 있다(EU, 2003; U.S. EPA, 2009; U.S. FDA, 2012; WHO, 2011). 우리나라는 수돗물에서만 감시항목으로 설정하여 권고기준 20 μg/L로 관리하고 있으며, 먹는샘물에서는 식약처 규정에 따른 용기에만 용출기준이 설정되어 있다. 안티몬처럼 용기 제조시 의도적으로 첨가되는 물질들은(intentionally-added substance) 대부분의 국가에서 규격기준을 만들어 관리하고 있으며, 우리나라와 일본은 용출기준(extraction limit)으로 각각 40 μg/L, 50 μg/L, 유럽은 이행기준(migration limit)으로 40 μg/L를 정해 관리하고 있다.
용기로부터의 안티몬 침출영향은 그동안 국외에서 많은 연구가 진행되어, 보관되는 기간과 온도가 증가함에 따라 PET 용기로부터의 침출량이 증가하는 것으로 알려져 있다(Bach et al., 2013; Reimann et al., 2012; Shotyk and Krachler, 2007; Welle and Franz, 2011; Westerhoff et al., 2008). 반면 국내의 경우 PET 용기로부터 안티몬의 용출영향 조사는 거의 수행된 예가 없으며 특히 먹는샘물에 대해서는 Park et al. (2011), Lee et al. (2010)의 연구가 거의 유일하다. 또한 먹는샘물의 원수로 사용되는 국내 지하수에서 자연적으로 존재하는 안티몬의 함량이 파악되지 않아 안티몬의 관리를 위한 기초자료도 확보되지 못한 상태이다.
본 연구에서는 먹는샘물 중 안티몬의 관리 필요성 검토를 위해 국내에서 생산되는 모든 먹는샘물(제품수)과 샘물(먹는샘물의 원수)중의 안티몬 함량과 보관조건에 따른 용기로부터의 침출 영향을 조사하였다. 또한 먹는샘물 PET 용기의 재사용에 따른 안전성 확인을 위해 용도별 재사용 형태을 모사하여 안티몬의 침출 특성을 조사하였다.
샘물은 2013년 1월 기준으로 등록된 67개 먹는샘물 제조업체 중 휴업 등의 사유로 취수가 불가능한 업체를 제외하고, 상반기(3~5월)에 58개 제조업체 171개 취수공, 하반기(7~9월)에 56개 제조업체 164개 취수공에 대해 각각 안티몬 함량을 조사하였다. 먹는샘물은 국내 제조업체별 대표브랜드 1품목에 대해 상반기 68개(PET 46개, PC 22개), 하반기 63개(PET 44개, PC 19개)의 안티몬 함량을 측정하였고, 수입 유통중인 먹는샘물은 상반기에 21개 PET제품에 대해 조사하였다.
보관온도, 보관기간 등 먹는샘물의 유통조건에 따른 안티몬의 함량변화를 알아보기 위한 침출량 조사는 국내 먹는 샘물용 PET용기 시장점유율 상위권의 3개사 용기(500mL 용량)를 대상으로 용기에 정제수를 채우고 다양한 환경조건(노천, 실온, 45℃)에서 180일간 보관하면서 안티몬 함량을 측정하였다.
용기 재사용 실험은 먹는샘물 음용 후 먹는샘물 용기를 매실액 등 액체식품의 저장용기로 사용하는 형태를 모사하고자 모사용액으로 정제수, 4% 아세트산, 20% 에탄올을 사용하여 용출실험을 수행하였다. 용출실험은 「기구 및 용기포장의 기준 및 규격(식약처 고시 제2012-115호)」에 따라 60℃로 가열한 용출액(모사체)을 용기에 채워 온도를 유지하고 30분 후 모사체를 따라내고 이를 시험용액으로 하였다. 또 모사체를 채운 용기를 다양한 온도조건(4℃, 실온, 45℃)에서 5일, 10일, 20일 보관 후 안티몬 함량을 측정하였다. 재사용 횟수에 따른 안티몬 함량변화 실험은 유럽연합(EU) 규정의 용기 이행실험 방법에 따라 모사체를 채우고 10일 후 용기를 비워 시험용액으로 하고, 다시 동일한 용기에 모사체를 채우는 방식으로 3회 반복하여 측정하였다.
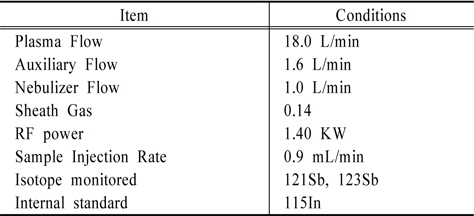
샘물은 0.45 μm 멤브레인 필터로 여과하여 질산을 첨가 하였고, 먹는샘물은 여과없이 바로 질산을 첨가하여 분석하였다. 샘물의 경우 전처리로 여과없이 질산 첨가, 질산 첨가 후 마이크로웨이브 분해도 병행하였으며, 전처리 방법에 따른 안티몬의 함량 차이는 보이지 않았다. 용기 재사용 실험에 사용된 용출액과 모사용액은 시료 100 ml에 질산(유해금속측정용) 1 ml를 가해 50 ml로 농축하여 분석하였다. 시약의 조제, 용출액의 희석 등 실험에 사용된 정제수는 ELGA water purification system (18.2 mΩ) 을 사용하여 제조하였으며, 실험에 사용된 모사용액은 Sigma Aldrich 사의 아세트산(99.7%), 에탄올(99.5%)을 정제수로 희석하여 각각 4%, 20%로 조제하였다. 안티몬 분석을 위해 Bruker사의 820-MS유도결합플라즈마-질량분석기(ICP-MS)를 사용하였으며, 분석 검출한계는 0.017 μg/L, 정량한계 0.05 μg/L, 정확도는 97.3%, 정밀도는 2% 이내였다. 기기분석을 위한 ICP-MS의 작동조건은 Table 1로 정리하였다.
[Table 1.] Instrument operating conditions for Antimony determination by ICP-MS
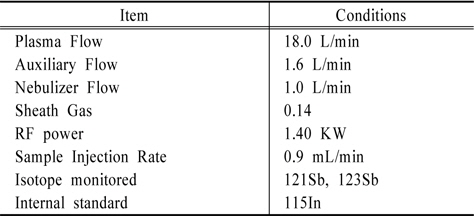
Instrument operating conditions for Antimony determination by ICP-MS
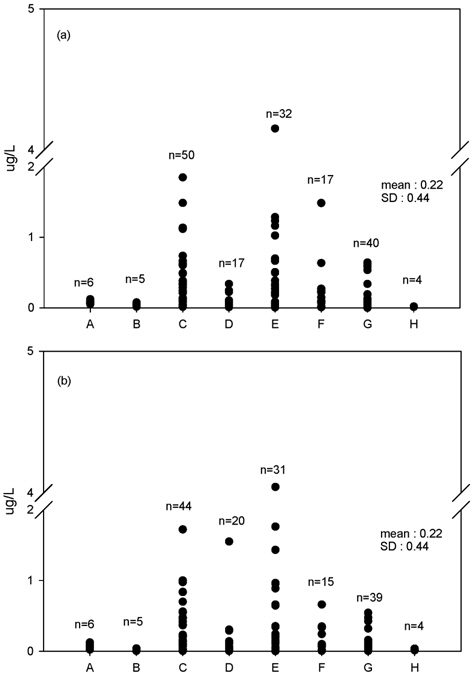
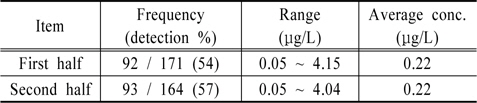
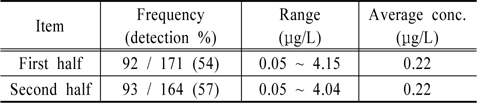
전국 샘물의 안티몬 함량을 상하반기 취수공별로 2회 측정하고 그 결과를 행정구역에 따라 8개 지역으로 구분하였으며(Fig. 1), 일부는 다른 지역에 비해 샘물에서의 함량이 다소 높은 수준을 보였다. 상반기 취수공 171개 중 정량한계인 0.05 μg/L 이상 검출된 취수공이 92개, 하반기는 164개 중 93개로 평균 55%의 취수공에서 안티몬이 검출되었다. 평균 검출농도는 상하반기 모두 0.22 μg/L, 농도범위는 0.05~4.15 μg/L로 1개 취수공에서 상하반기 모두 최대 4.0 μ g/L 이상 검출되었으며(Table 2) 이는 유럽 먹는샘물 수질 기준인 5 μg/L의 80%를 상회하는 수준이다. 통상 오염되지 않은 지하수에서 안티몬 평균농도는 0.2 μg/L 이하로 알려져 있어(Jeong, 2008), 향후 지질학적인 영향이나 주변오염원의 영향 여부에 대한 정밀한 조사가 필요하다. 다만 이 최고농도는 A제조업체가 보유한 4개 취수공 중 1개 취수공의 측정 결과이며, 먹는샘물은 여러 취수공의 물이 혼합되어 제품으로 생산되므로 먹는샘물에서 국외 수질기준에 근접한 수준으로 검출될 가능성은 없는 것으로 판단되었다.
[Table 2.] Determined concentration of Antimony in source water
Determined concentration of Antimony in source water
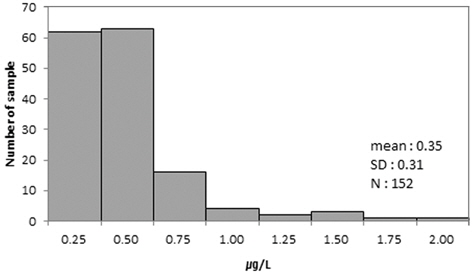
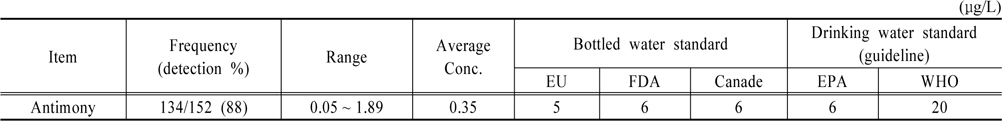
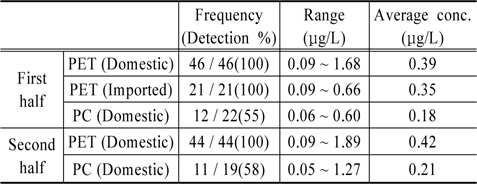
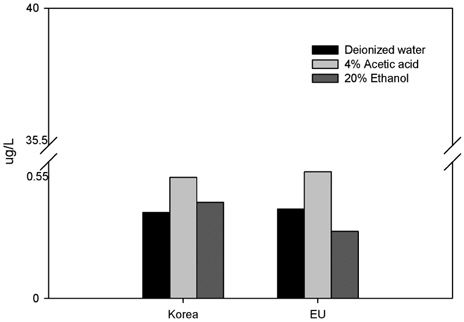
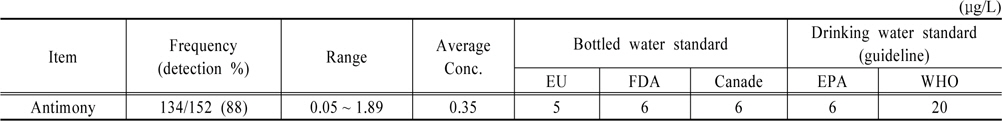
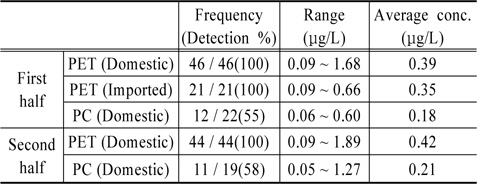
먹는샘물에서의 안티몬 측정결과를 Fig. 2와 Table 3에 나타냈다. 먹는샘물에서 안티몬 검출률은 88%, 검출 농도 범위는 0.05~1.89 μg/L, 평균 0.39 μg/L로 조사되었다. 검출률과 평균 검출농도는 샘물에 비해 증가하였으며, 최대 검출농도는 감소하였다. 용기재질에 따른 차이를 보기 위해 전체 먹는샘물의 안티몬 검출률 88%를 용기별로 구분하면, PC 용기 55% PET용기 100%로, PC용기의 경우 평균농도와 검출빈도가 샘물과 유사하여 용기로부터의 안티몬 영향은 거의 없는 것으로 판단되었다. 반면, PET용기는 검출률이 샘물에 비해 2배정도 증가하고, 검출 평균 농도도 2배 증가하는 것으로 조사되었다. PET용기 먹는샘물의 최고농도 1.89 μg/L는 취수공별 조사에서 최고농도 4.15 μg/L의 취수공을 보유한 제조업체 생산 제품으로, 취수공의 고장 등 사유로 혼합생산이 불가능할 경우에는 먹는샘물에서 안티몬이 이보다 더 높은 농도로 함유될 가능성이 있다. 따라서 안티몬 농도가 높은 취수공을 보유한 제조업체에서의 주기적인 모니터링과 적절한 생산관리가 필요하다.
[Table 3.] Determined concentration of Antimony in bottled water and water quality standards
Determined concentration of Antimony in bottled water and water quality standards
[Table 4.] Antimony in PET and PC bottled water
Antimony in PET and PC bottled water
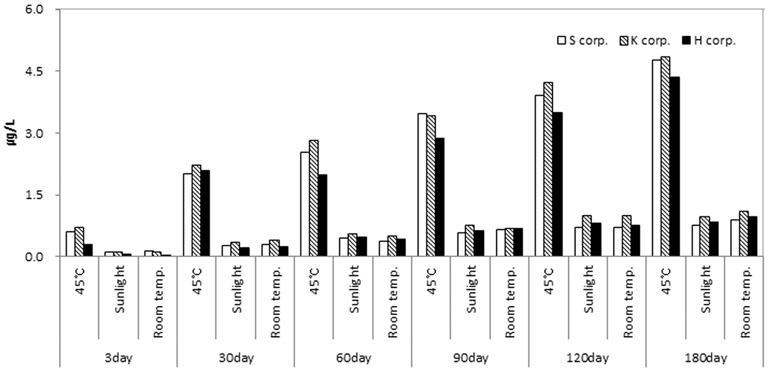
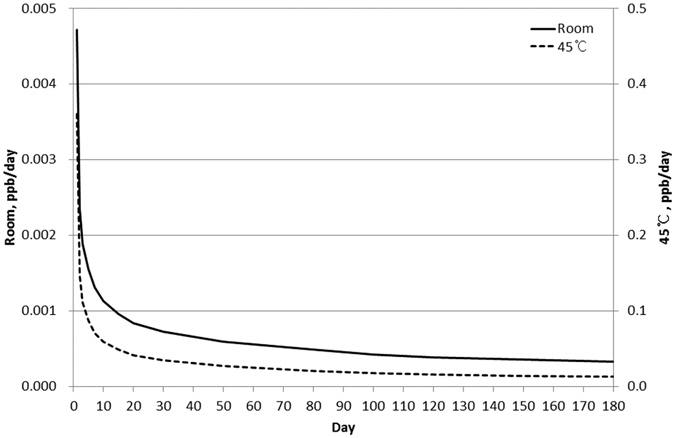
3개 PET제조사의 용량 500mL 용기에 정제수를 채우고 환경조건을 실온, 노천, 45℃로 달리하여 180일간 보관하면서 용기로부터 이행되는 안티몬의 함량을 측정하였다(Fig. 3). 조사결과 용기로부터의 안티몬 이행량은 보관기간과 온도에 비례하여 증가하였으며, 이는 국내외 여러 연구결과와 동일하였다(Bach et al., 2013; Hansen et al., 2006; Reimann et al., 2012; Shotyk and Krachler, 2007; Welle and Franz, 2011; Westerhoff et al., 2008). 보관실험 결과 45℃에서 180일 경과시 안티몬 농도는 4.87 ~ 4.85 μg/L로 유럽의 먹는샘물 기준인 5.0 μg/L에 근접하였다. 그러나 실온에서는 90일 경과시 0.67 ~ 0.69 μg/L, 180일 경과 시 0.90 ~ 1.09 μg/L로 낮은 이행량을 보였으며, 실제 먹는샘물이 실온에서 유통되고 제조 후 3개월 이내에 거의 소비되는 점을 고려하면 안티몬에 의한 위해도는 없는 것으로 판단되었다. Takahashi et al. (2008)의 연구결과에 의하면 PET 에서의 안티몬 이행량은 용기 각각의 품질과 용기의 안티몬 함량에 따라 차이를 보인다. 본 조사에 사용된 국내 먹는샘물용 PET용기 시장점유율 상위권의 세 종류 용기는 이행량에 차이가 거의 없어, 적어도 안티몬의 침출영향 면에서는 동일한 품질을 유지하는 것으로 간주할 수 있었다. Wegelin et al. (2001)은 PET 재질의 변화에 미치는 햇빛의 영향을 조사한 연구에서 햇빛에 의한 용기의 변화는 내부가 아닌 용기 표면에서 일어나기 때문에 먹는샘물로의 안티몬 이행 영향은 크지 않은 것으로 제시하였다. 또 Westerhoff et al. (2008)은 햇빛노출 실험에서 aluminium foil로 감싼 PET과 노출시킨 PET의 비교실험결과 햇빛노출이 안티몬의 용기침출에 미치는 영향은 매우 제한적인 것으로 결론지었다. 이번 실험에서도 햇빛의 영향을 직접 받는 노천보관시료에서의 이행량이 실온에 비해 증가하는 경향은 나타나지 않았다. 그러나, 노천에서의 실험이 다른 주요 요인인 온도를 일정하게 유지할 수 없어, 햇빛에 의한 정량적인 영향 정도는 햇빛외 다른 요인을 동일하게 유지한 추가 조사가 더 필요하다. 현행 먹는샘물 관련 규정에 따르면(환경부 고시 2013-184) 국내생산 먹는샘물의 유통기한은 6개월이며, 제조업체에 따라 최고 2년까지 연장하기도 한다. 먹는샘물이 제조에서 소비까지 3개월 이상 소요되는 경우는 드물지만, 유통기한이 최고 2년까지 연장 가능하고 또 이번 조사에서 안티몬 이행량이 180일까지 계속 증가하는 경향을 보여 향후 180일 이상 보관실험을 통한 추가 조사도 필요할 것으로 판단되었다. 다만, Westerhoff et al. (2008)이 조사에서 밝혔듯이 용기의 안티몬 함량 중 아주 작은 일부만이 물로 이행되며, 이번 조사에서도 단위기간당 이행량은 초기 20일까지가 크고 이후 완만한 경향을 보여 통상의 유통조건에서는 180일 이후에도 안티몬의 총이행량이 우려할 만한 수준까지 증가 하지는 않을 것으로 예상되었다. 45℃와 실온에서의 안티몬 이행속도를 Fig. 4에 나타냈다.
먹는물관리법에 따르면 먹는샘물 용기는 식약처 규정에 의한 용출규격에 적합한 것을 사용토록 규정되어 있고, 용기 규격실험에서 pH 5이상의 음료를 담는 용기는 용출액으로 정제수를 사용하여 실험한다. 국내 먹는샘물 소비자들은 먹는샘물 소비 후 용기를 다양한 용도로 재활용하고 있으며, 특히 매실 액기스, 과실주 등의 보관용도로도 사용하고 있다. 먹는샘물 소비 후 용기의 재사용 형태에 따른 안티몬 침출 영향을 조사하기위해 모사체로 정제수, 4% 초산, 20% 에탄올을 사용하여 실험하였다. 용출실험을 위한 용출원액은 모두 정량한계 이하로 불검출이었으며, 식약처 규정에 따라 60℃에서 30분간 용출시킨 후 농도는 정제수 0.35 μg/L, 4% 초산 0.49 μg/L, 20% 에탄올이 0.39 μg/L로 모두 용기 용출 규격인 40 μg/L의 10% 이내로 안전하였다. EU규정에 의한 migration limit test (45℃, 10일)에서도 이와 유사한 결과를 보였다(Fig. 5).
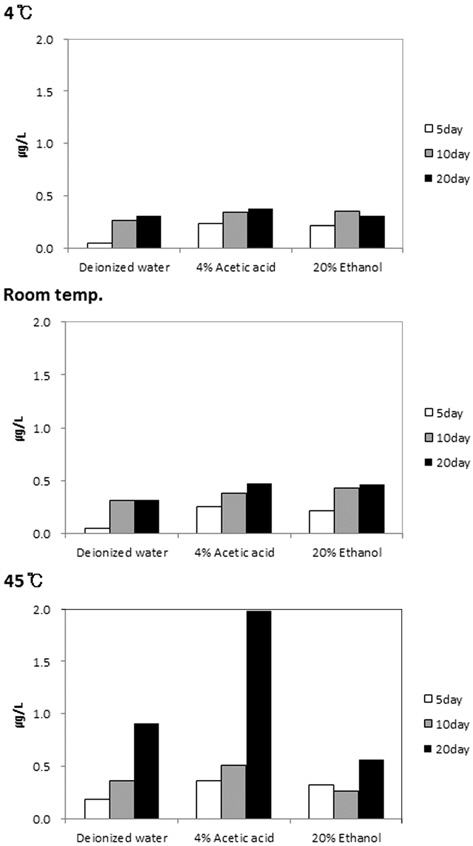
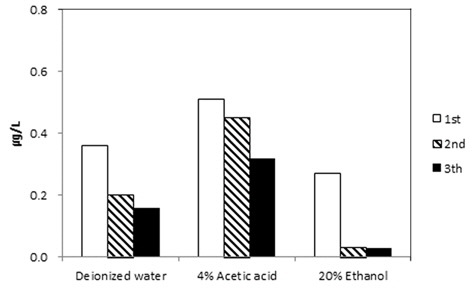
모사체 종류와 보관조건에 따른 안티몬 이행농도를 Fig. 6에 나타냈다. 보관온도 및 기간의 증가에 따라 안티몬 이행량은 증가하였으며, 4% 초산에서 20% 에탄올과 정제수 보다 이행농도가 높았다. Sachez-Martinez et al. (2013)은 EU 규정의 식품모사체인 정제수, 3% 초산, 20% 에탄올을 사용하여 40℃에서 10일간 보관실험을 하고 그 결과 0.56 ~ 1.30 μg/L의 안티몬 이행농도를 보고하였는데 이번 조사(45℃ 10일 보관)에서는 0.27 ~ 0.35 μg/L로 더 낮은 결과를 얻었다. 모사체의 종류에 따른 이행량은 초산에서 가장 높은 결과를 보여 Rungchang et al. (2013)의 40℃ 10일 보관실험과 동일하였으나, 20% 에탄올에서 가장 높은 이행량을 보인 Sachez-Martinez et al. (2013)의 실험과는 다른 결과이다. Takahashi et al. (2008)은 용기로부터의 안티몬 침출은 모사체의 pH나 유기용매로서의 침투력보다는 PET 각각의 고유한 분해특성에 더 영향을 받기 때문에 PET의 품질에 따라 상반된 결과를 보이기도 한다고 제시하였다. Reimann et al. (2010)의 연구에서도 pH에 따른 안티몬등 미량원소들의 용출 경향을 파악하기위해 pH 6.5와 pH 3.5에서 각각 이행량을 측정하였으나, 낮은 pH에서 유의한 증가경향을 보이지 않았다. 다만, PET 품질에 따라 영향정도가 달리 나타날 수도 있으므로, 국내 유통 PET용기를 대상으로 다양한 pH조건에서의 추가실험은 필요할 것으로 판단되었다. 용기의 재사용 횟수에 따른 이행 농도를 Fig. 7에 나타냈다. 실험결과 표본수가 충분하지 않았으나, 대체적으로 사용 횟수의 증가에 따라 PET 용기로부터의 이행량이 감소하는 경향을 보였다. 이를 통해 용기로부터의 이행은 초기 용출의 영향이 큰 것을 알 수 있었다.
전국 먹는샘물 제조업체 전수조사결과 55%의 원수와 88%의 제품수에서 안티몬이 검출되었으며 제품수(국내생산 131개, 수입 21개)의 평균 검출농도는 0.35 μg/L, 검출범위는 0.05 ~ 1.89 μg/L로 조사되었다. 제품수 평균농도는 국외 수질기준의 10% 수준으로 안전하였으나, 일부 원수 취수공과 제품수의 최대검출농도는 각각 국외 수질기준의 80%, 40% 수준이었다. 제품수를 용기 재질에 따라 분류하면 PC용기 제품수는 검출률과 평균 검출농도가 원수와 유사하였으며, PET 용기 제품수는 검출률, 검출 평균농도가 원수에 비해 각각 2배씩 증가하여, 먹는샘물 제품수의 안티몬은 자연유래 뿐 아니라 PET 용기로부터도 유래되는 결과를 보였다.
PET용기 보관실험 결과, 안티몬의 침출영향은 보관기간 및 온도에 비례하여 증가하고, 180일 45℃ 조건에서 가장 높은 이행량을 보였으며 실온과 노천에서의 이행량은 큰 차이가 없었다. 규정된 유통기한 6개월 이후 2년까지 안티몬 총 이행량은 계속 증가될 것으로 예상되나, 기간 증가에 따른 이행속도는 크게 감소하여 우려할 수준은 아닌 것으로 판단되며, 통상의 실제 유통조건인 실온 3개월에서 안티몬 농도는 국외 수질기준의 10% 수준으로 안전하였다.
용기 재사용 형태에 따른 모사체 실험결과 4% 초산에서 용출 농도가 가장 높았으며 모사체 보관실험에서도 기간과 온도에 비례하여 이행량은 증가하였다. 모사체를 이용한 식약처 규격 용출실험 및 EU 규격 이행실험 결과, 검출농도는 모두 기준치 40 μg/L에 훨씬 못 미치는 안전한 수준이었으며, 용기 재사용을 위한 반복실험결과 재사용 횟수가 증가할수록 이행량은 감소하는 결과를 보였다.
안티몬은 유해성과 PET에서의 침출가능성 등으로 대부분의 국가에서 먹는샘물의 수질기준으로 설정하고 있다. 국내 원수 및 제품수 조사결과에서도 안티몬의 검출률이 높고, 고온 등 특이 보관조건에서 용기로부터의 이행가능성도 매우 높은 것으로 나타나 상시 모니터링을 통한 수질감시가 필요한 것으로 판단된다. 특히 일부 안티몬 함량이 높은 취수공의 경우는 지질영향, 인위적인 오염원 등에 대한 조사를 통해 안전관리 방안도 마련되어야 한다.