In order to remove both nitrate and sulfate present in the concentrate of RO(reverse osmosis) process, a combined bio-regeneration and ion-exchange(IX) system was studied. For this purpose, both denitrifying bacteria(DNB) and sulfate reducing bacteria(SRB) were simultaneously cultivated in a bio-reactor under anaerobic conditions. When the IX column containing a nitrate-selective A520E resin was fully exhausted by nitrate and sulfate, the IX column was bio-regenerated by pumping the supernatant of the bio-reactor, which contains MLSS concentration of 125±25 mg/L, at the flowrate of 360 BV/hr. Even though the nitrate-selective A520E resin was used, the breakthrough curves of ionic species showed that sulfate was exhausted earlier than nitrate. The reason for this result is due to the fact that the concentration of sulfate in RO concentrate was 36 to 48 times higher than nitrate. The bio-reactor was successfully operated at a volumetric loading rate of 0.6 g COD/l・d, nitrate-N loading rate of 0.13 g NO3--N/1・d, and sulfate loading rate of 0.08 g SO42-/1・d. The removal rate of SCOD, nitrate-N, sulfate was 90, 100, and 85%, respectively. When the virgin resin was fully exhausted and consecutively bio-regenerated for 2 days, 81% of nitrate and 93% of sulfate were reduced. When the virgin resin was repeatedly used up to 4 cycles of service and bio-regeneration, the ion-exchange capacity of bio-regenerated resin decreased to 95, 91, 88, and 81% of virgin resin.
이온교환공정은 수중에 존재하는 이온성 오염물질을 제거하는데 효과적인 기술이다. 이온교환수지는 이온교환공정에서 핵심적인 요소로서, 수중에 존재하는 질산성질소(NO3--N)와 황산염(SO42-)은 음이온교환수지에 의해 제거된다. 파과된 음이온교환수지는 일반적으로 염(NaCl)으로 재생되지만, 이때 발생하는 폐액에는 재생과정에서 사용되지 않은 NaCl이 고농도로 존재하기 때문에 폐액에 존재하는 질산성질소와 황산염을 최종적으로 처분하는 것이 기술적으로 쉽지않다(Bae et al, 2004; Clifford and Liu 1993; Van der Hoek and Klapwijk, 1987).
최근에 역삼투(Reverse Osmosis, RO) 막공정이 물 재이용 분야에서 널리 보급되고 있다. 특히, 하수처리수나 하천수로부터 공업용수를 생산하는 분야에서 RO 막이 활발하게 적용되고 있다. RO 공정에서는 난분해성 유기물, 질산성질소, 황산염, 그리고 염분 등이 농축된 농축폐액이 발생하는데, 이 농축폐액의 처리가 새로운 이슈로 대두되고 있다(Kim and Kang, 2012).
한편, 질산성질소 제거용 이온교환수지의 재생폐액과 관련된 문제를 해결하기 위하여, 파과된 이온교환수지를 탈질균(Denitrifying Bacteria, DNB)과 직접 반응시켜 생물학적으로 직접 재생(Direct Bio-regeneration)하는 기술이 발표된 바 있다(Nam and Bae, 2013). 본 연구에서는 음이온교환수지를 이용하여 RO 농축폐액에 존재하는 질산성질소와 황산염을 흡착한 후, DNB와 황산염환원균(Sulfate Reducing Bacteria, SRB)을 이용하여 생물학적으로 재생하는 방법을 연구하였다. 즉, 파과된 이온교환수지의 작용기(functional group)에 결합된 질산성질소는 N2 가스로, 그리고 황산염은 H2S로 직접 환원시키는 기술을 연구하였다. 이를 위하여 이온교환컬럼과 결합된 생물반응조를 운전하였으며, 반복적인 파과실험으로 생물재생 효율을 평가하였다.
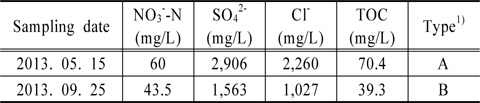
본 연구에서는 충청남도 서산시의 대산정수장의 RO 농축폐액를 채취하였다. 대산정수장은 아산호 원수를 취수하는 아산정수장으로부터 침전수를 공급받아, RO 막(Hydranautics, Nitto Denko Co.)으로 공업용수를 생산하는 정수장이다. 본 연구에서는 이온성 오염물질의 농도가 상대적으로 높은 2단막에서 배출되는 농축폐액을 채취하여 실험에 사용하였다. Table 1에는 실험에 사용한 RO 농축폐액의 특성을 정리하였다.
[Table 1.] Characteristics of RO concentrates used in this study
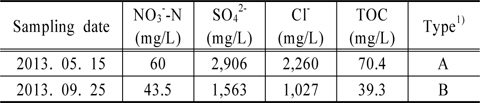
Characteristics of RO concentrates used in this study
본 연구에서는 질산성질소 선택수지(Nitrate Selective Resin)인 A520E(Purolite Co.)를 선정하여 이온교환 및 생물학적 재생실험을 수행하였다(Bae et al, 2004). A520E 수지는 chloride-form의 macroporous-type이며, 입자의 크기는 300~1,200 μm이다(Samatya et al., 2006). 본 연구에서는 생물재생 장치와 연결된 이온교환컬럼이 슬러지 입자에 의해 막히는 현상을 방지하기 위하여, 30번 체(sieve)로 수지를 거른후 직경이 600 μm 이상인 수지 입자만을 이온교환컬럼에 충진하여 실험을 수행하였다.
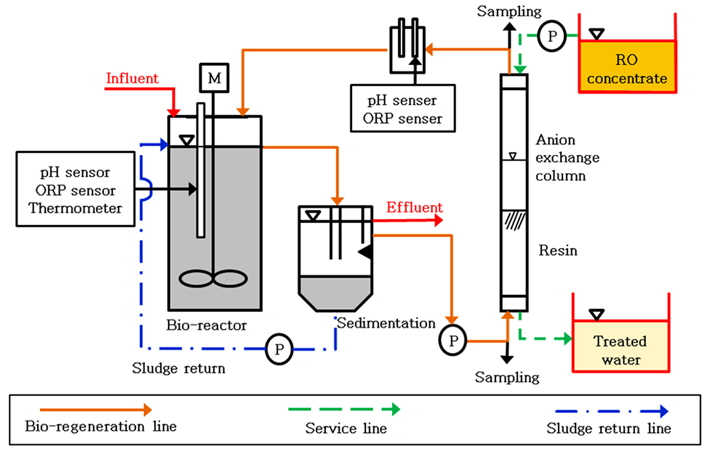
RO 농축폐액에 파과된 이온교환수지의 생물학적 재생을 위해 Fig. 1과 같은 실험장치를 구성하였다. Fig. 1의 왼쪽은 DNB와 SRB를 동시에 배양한 생물반응조이고, 오른쪽은 이온교환컬럼이다. RO 농축폐액에 의해 이온교환수지가 파과되면, 생물반응조 내 미생물을 이온교환컬럼으로 이송하여 파과된 이온교환수지와 직접 반응시켰다. 생물반응조와 침전조, 그리고 이온교환컬럼은 워터자켓을 이용하여 온도를 30°C로 일정하게 유지하였다.
본 연구에서는 황산염과 질산성질소에 의해 파과된 A520E 수지를 생물재생하기 위하여 DNB와 SRB를 동시에 배양하 였다. 이를 위해 유효용량 20 L의 완전혼합형 반응조(직경 25 cm, 높이 50 cm)와 8 L의 침전조(가로 15 cm, 세로 15 cm, 높이 40 cm)를 운전하였다. 반응조의 Mixed Liquor Suspended Solids(MLSS)를 일정수준(2,000 ~ 2,200 mg/L)으로 유지하기 위해 침전조에 침전된 미생물을 주기적으로 반송하였다.
먼저, 생물반응조는 대전하수처리장 무산소조에서 채취한 탈질미생물로 식종된 후 장기간 운전되었다. 이후, 수리학적 체류시간 1일, COD/NO3--N(g/g) 비 3.8, 그리고 Nitrate-N Loading Rate 0.14 g NO3--N/1・day의 운전조건에서 45일 동안 정상적으로 운전되었다. 이렇게 배양된 DNB를 이용하여 질산성질소에 파과된 A520E 수지를 생물재생하는 실험을 수행하였고, 그 결과를 선행논문에서 발표한 바 있다(Nam and Bae, 2013). 본 연구에서는 RO 농축폐액에 존재하는 황산염과 질산성질소에 파과된 A520E 수지를 생물재생하기 위하여 Na2SO4를 추가로 투입하여 SRB를 DNB와 동시에 배양하였다. 외부탄소원으로는 에탄올(ethanol)을 사용하였으며, 영양염류와 미량원소를 공급하였다. 영양용액은 Shelton and Tiedje (1984)의 방법에 따라 제조하였다.
본 논문에서 제시한 실험결과는 DNB와 SRB을 동시에 배양한 생물반응조로부터 얻은 것이다. 생물반응조는 수리학적 체류시간 1일에서 약 130일간 운전되었으며, Volumetric Loading Rate는 0.6 g COD/1・d, Nitrate-N Loading Rate는 0.13 g NO3--N/l・d, 그리고 Sulfate Loading Rate는 0.08 g SO42-/1・d로 실험기간 동안 일정하게 운전되었다. 즉, 파과된 이온교환수지를 생물재생하는 동안에도 탄소원, NaNO3, 그리고 Na2SO4를 일정하게 첨가하였다.
아크릴로 제작된 이온교환컬럼(직경 2.5 cm, 길이 50 cm)에 virgin A520E 수지 50 mL를 충진한 후, RO 농축폐액을 하향류 방식으로 공급(service)하였다. Table 2에 생물재생이 결합된 이온교환컬럼의 운전조건을 단계별로 정리하였다. RO 농축폐액 A로 실험을 수행한 Cycle 1에서 2까지는 공급유량을 30 BV(bed volume)/hr로 하였으나, Cycle 3동안에는 공급유량을 20 BV/hr 낮추어 운전하였다.
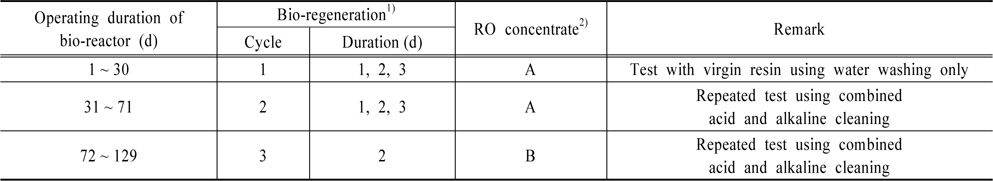
[Table 2.] Operation of combined bio-reactor and ion-exchange column
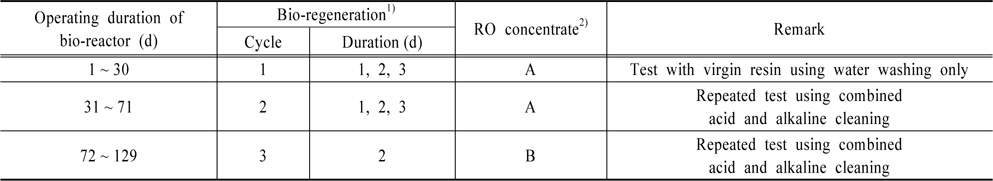
Operation of combined bio-reactor and ion-exchange column
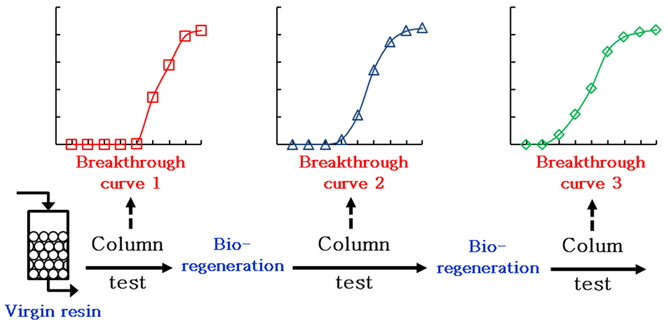
수지가 완전히 파과된 것을 확인한 후, 이온교환컬럼을 생물반응조와 연결하여 생물재생 실험을 수행하였다. Table 2에 요약된 바와 같이, 생물재생 동안에는 MLSS가 125±25 mg/L인 침전조 상등액을 360 BV/hr의 유량으로 이온교환 컬럼으로 공급하였다. 일정한 기간 동안 생물재생을 수행한 후, 증류수로 세척한 후 산・알카리 세정을 수행하였다. 산세정은 0.2 M HCl 용액 500 mL로, 그리고 알카리세정은 0.2 M NaOH 용액 500 mL으로 20분간 세정하였다. 화학세정 후 한 번 더 수세정을 실시하였으며, 이렇게 생물재생된 수지에 다시 RO 농축폐액을 공급하여 파과실험을 수행하였다. Virgin 수지로부터 구한 파과곡선과 생물재생된 수지로부터 구한 파과곡선을 비교하여 수지의 이온교환용량이 얼마만큼 회복되는지를 평가하였다. 전체적인 실험순서를 Fig. 2에 나타내었다.
Table 2에 생물재생이 결합된 이온교환컬럼의 운전 조건을 Cycle 별로 구분하였다. Cycle 1에서는 생물재생 기간에 따른 재생효율을 평가하기 위하여 virgin 수지를 RO 농축폐액으로 파과시킨 후, 일정 기간(1, 2, 그리고 3일) 동안 생물재생 하였다. 이 실험에서는 매번 virgin 수지를 사용하였다. Cycle 2 동안에는 한번 충진한 virgin 수지를 반복적으로 파과・재생 하면서 재생기간에 따른 재생효율을 평가하였고, 산과 알카리를 이용하여 생물재생된 수지를 화학세정하였다. Cycle 3 동안에는 생물재생 기간을 2일간 고정한 후, 파과와 생물재생을 4회 반복하면서 반복적인 생물재생이 재생효율에 미치는 영향을 조사하였다.
생물재생 동안에 이온교환수지로부터 용출되는 이온의 농도를 분석하기 위하여 침전조에서 이온교환컬럼으로 유입되는 지점과 이온교환컬럼에서 생물반응조로 되돌아가는 지점에서 시료를 채취하여 질산성질소와 황산염 농도를 분석하였다. 이를 위해 서프레서(ASRS 300, Dionex)가 장착된 이온크로마토그래피(ICS 900, Dionex)를 사용하였다. 생물반응조의 내부와 이온교환컬럼 유출수의 pH(ath250v(L), Samsan) 및 산화환원전위(oxidation reduction potential, aorp 450v, Samsan)를 10분 간격으로 측정하였다. TOC(total organic carbon)는 TOC 분석기(VCPH, Shimadzu)를 사용하여 분석하였다.
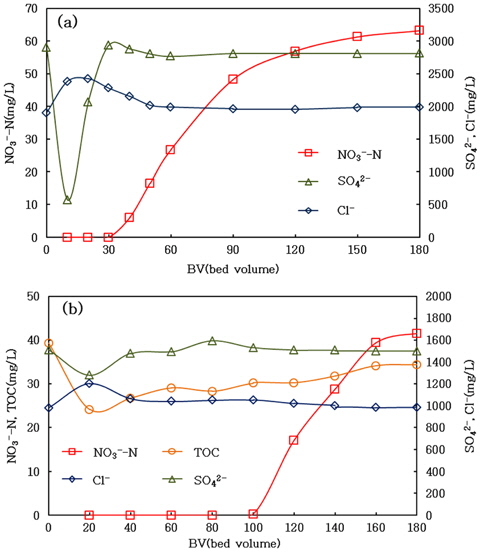
Fig. 3은 A520E 수지로 RO 농축폐액 A와 B를 각각 30과 20 BV/hr의 유량으로 처리하면서 180 BV까지 운전한 결과이다. Fig. 3(a)는 Table 2의 Cycle 1과 Cycle 2 동안에 RO 농축폐액 A를 처리한 파과곡선으로서, 질산성질소는 30 BV 이후부터 파과되었고 황산염이온은 10 BV부터 파과되기 시작하였다. Fig. 3(b)는 Table 2의 Cycle 3 동안에 RO 농축폐액 B를 처리한 파과곡선으로서, 질산성질소는 100 BV 이후부터 파과되었고 황산염이온은 20 BV부터 파과되었다. Fig. 3(a)에서 질산성질소와 황산염의 파과가 더 빨리 발생한 이유는 농축폐액 A에서 이들 이온의 농도가 상대적으로 높았을 뿐만 아니라, 이온교환컬럼 통과유속이 1.5배 더 컸기 때문이다. A520E 수지가 질산성질소 선택수지임에도 불구하고 황산염 이온이 상대적으로 빨리 파과에 도달한 것은 RO 농축폐액 A와 B에서 황산염의 농도가 질산성질소에 비해 각각 48 및 36배 높았기 때문이다.
한편, Fig. 3(b)에서는 RO 농축폐액에 존재하는 TOC 농도에도 변화가 있었는데, 이는 음이온으로 하전된 유기물이 A520E에 흡착되었기 때문이다(Cornelissen et al., 2008). Fig. 3의 RO 농축폐액 A와 B의 파과곡선으로부터 virgin A520E 수지의 이온교환능을 계산한 결과, RO 농축폐액 A는 질산성질소와 황산염이온이 각각 0.43 및 0.26 meq/mL씩 제거되었고, RO 농축폐액 B는 각각 0.41 및 0.23 meq/mL씩 제거되어 RO 농축폐액의 농도와 관계없이 비슷한 교환능을 나타내었다. 그리고 RO 농축폐액 B의 경우, 수지 1mL 당 2 mg의 TOC가 흡착되었다.
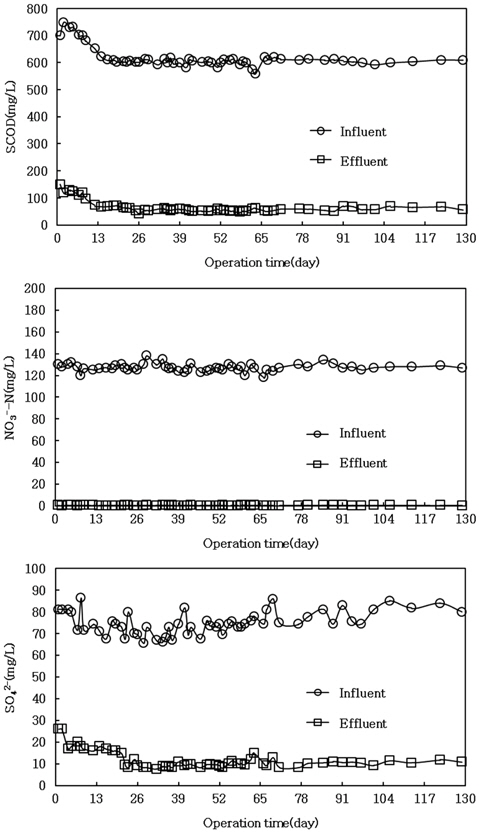
Fig. 4는 130일간 운전한 생물반응조의 운전결과로서 유입 및 유출수의 SCOD, 질산성질소, 그리고 황산염 농도를 나타내었다. SCOD 제거율은 90% 이상을 유지하였으며, 황산염에 적응되지 않았음에도 불구하고 황산염을 투입한 직후부터 65% 이상의 황산염 환원율을 보였다. 이후, 운전25일 후에는 85%의 황산염 환원율을 보였고, 탈질율은 거의 100%를 보였다.
3.3. 단독 및 반복실험을 통한 이온교환수지의 생물학적 재생효율
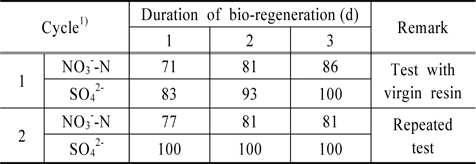
Table 3은 생물재생 기간(1, 2, 그리고 3일)이 재생효율에 미치는 영향을 조사한 결과이다. Table 3의 Cycle 1 동안에는 매번 virgin 수지를 이용하여 파과와 생물재생 실험을 수행하였다. 생물재생 기간이 1, 2, 그리고 3일일 때 질산성질소의 재생효율은 각각 71, 81, 그리고 86%로 나타났고, 황산염이온의 재생효율은 각각 83, 93, 그리고 100%로 측정되었다.
[Table 3.] Bio-regeneration efficiency according to the duration of bio-regeneration
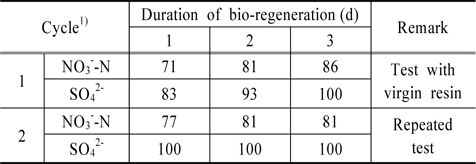
Bio-regeneration efficiency according to the duration of bio-regeneration
Table 3의 Cycle 2는 한번 충진한 virgin 수지를 반복적으로 파과・재생하면서 재생기간에 따른 재생효율을 측정한 결과이다. Cycle 2에서 처음 충진한 virgin 수지를 1일간 생물 재생하였을 때 질산성질소의 재생효율이 77%로 Cycle 1에서의 1일간 생물재생 하였을 때보다 높게 측정되었다. 이는 생물재생 후 파과실험을 수행하기 전에 산・알카리 세정을 수행하였기 때문인 것으로 판단된다. 2일간 생물재생된 수지의 질산성질소의 재생효율은 단독실험의 2일 생물재생 효율과 같은 81%를 나타냈으며, 3일간 생물재생된 수지의 질산성질소의 재생효율도 81%로 일정하게 측정되었다. 한편, Cycle 2 동안에 황산염은 모두 100% 환원되었다.
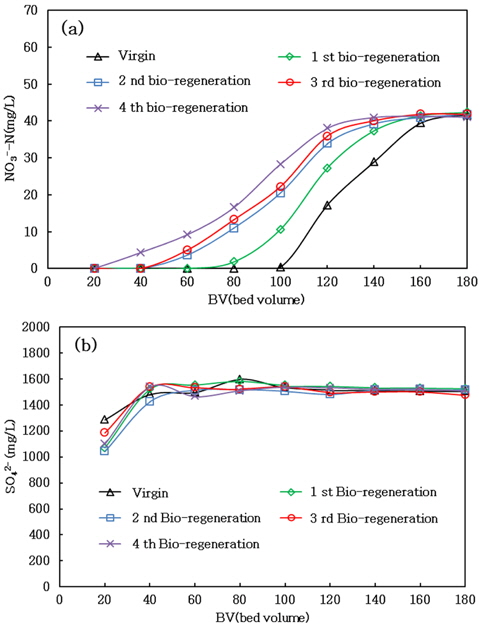
Table 3의 Cycle 2에서 얻은 결과에 근거하여 생물재생 기간을 2일로 고정한 후, 반복적인 파과와 재생이 재생효율에 미치는 영향을 조사하였다(Cycle 3). Fig. 5는 Table 1의 재생폐액 B를 이용하여 4회 파과와 재생을 반복한 결과이다. Fig. 5(a)의 질산성질소 파과곡선은 반복사용 횟수가 증가할수록 초기 유출이 빠르게 나타났고, 질산성질소의 재생효율은 각각 85, 77, 73, 그리고 58%로 감소하였다. 황산염 파과곡선의 경우, 반복적인 파과와 재생에도 불구하고 virgin 수지와 비교할 때 거의 차이가 없었고, 흡작된 양을 기준으로 평가할 때 생물재생 효율은 100%로 측정되었다.
3.5. 생물재생용 이온교환컬럼 유입?유출수의 질산성질소 및 황산염의 농도
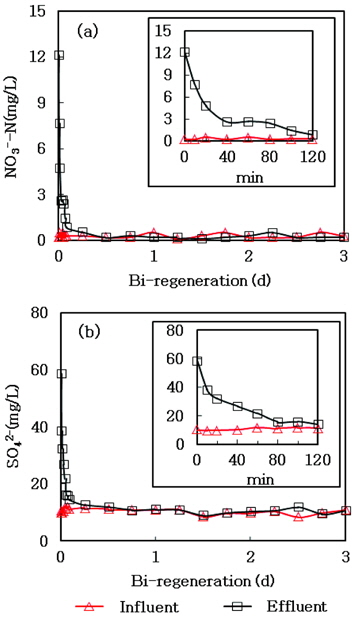
Fig. 6은 Table 2의 Cycle 1 동안에 생물재생이 진행되고 있는 이온교환컬럼의 유입 및 유출수를 채취하여 질산성질소와 황산염의 농도를 측정한 결과이다. Fig. 6(a)의 질산성질소는 생물재생 직후에 이온교환컬럼 유출수에서 최대 12mg/L로 증가하였다가 약 2시간 이후에 유입수 수준으로 감소하였다. 한편, Fig. 6(b)의 황산염은 생물재생 직후에 이온교환컬럼 유출수에서 최대 59 mg/L로 증가하였다가 약 80분 이후에 유입수 수준으로 감소하였다. 황산염은 질산성질소보다 40분 먼저 탈착되었는데, 이는 실험에 사용된 A520E 수지가 질산성질소 선택수지이기 때문에 결합력이 상대적으로 약한 황산염이 먼저 탈착된 것으로 판단된다.
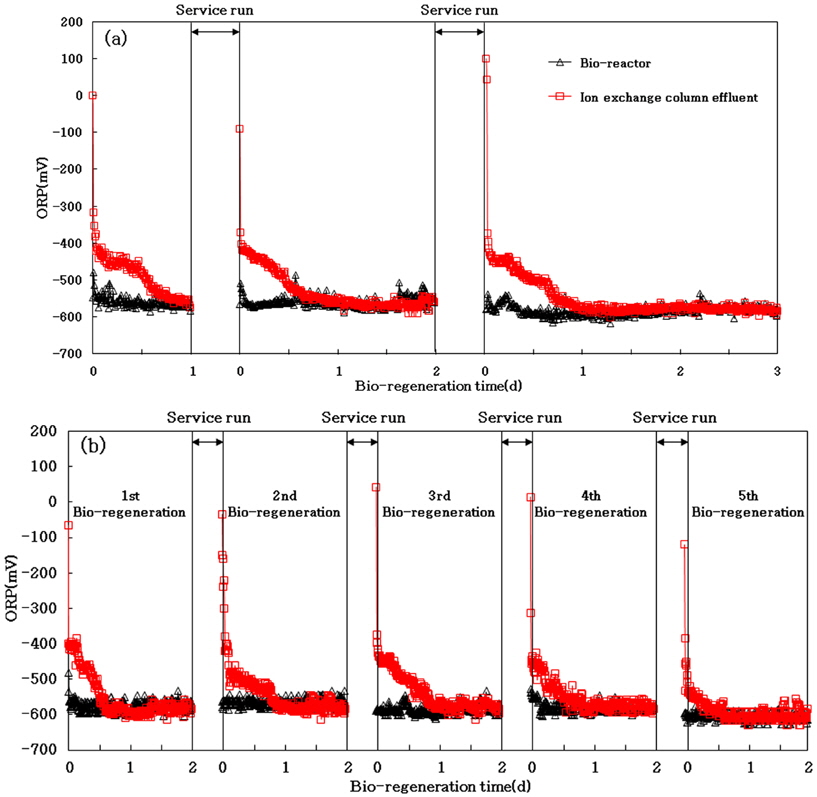
Fig. 7은 생물재생 동안에 생물반응조 내부와 이온교환컬럼 유출수를 대상으로 측정한 ORP 결과이다. Fig. 7(a)와 (b)는 Table 2의 Cycle 2와 Cycle 3에서 생물재생을 수행할때 측정한 ORP 값의 변화로서, 생물반응조는 -580 ~ -600mV의 수준으로 유지되었다. 생물반응조에 이온교환컬럼을 연결하고 생물재생을 수행한 직후에는 이온교환컬럼 유출수의 ORP 값은 -400 mV 이상이었으나, 생물재생 18시간 이후에 생물반응조의 ORP 값과 비슷하게 유지되었다. Cycle 3 실험 동안에 측정한 Fig. 7(b)에 의하면, 반복적으로 재생하는 횟수가 많아질수록 이온교환컬럼 유출수와 생물반응조의 ORP 값이 유사하게 나타나는 시점이 처음 18시간에서 6시간으로 줄어들었다. 한편, DNB만을 배양하여 이온교환수지에 흡착된 질산성질소를 생물재생한 Nam and Bae(2013)의 연구에서 탈질반응조의 ORP 값은 -450 ~ -500mV이었다.
음이온교환수지를 이용하여 RO 농축폐액에 존재하는 질산성질소와 황산염을 흡착한 후, DNB와 SRB를 이용하여 생물학적으로 재생하는 방법을 연구하였다. 본 연구에서 얻은 결론은 다음과 같다.
1) 단일 생물반응조에서 DNB와 SRB를 동시에 배양하였다. 생물반응조는 COD 용적부하 0.6 g COD/1・d, 질산성질소 부하 0.13 g NO3--N/1・d, 그리고 황산염 부하 0.08 g SO42-/1・d에서 SCOD 제거율 90%, 질산성질소 제거율 100%, 그리고 황산염 제거율 85%의 성능을 보였다. 2) 생물재생 기간이 증가함에 따라 파과된 수지의 생물재생 효율이 증가함을 확인하였다. 즉, 수지에 존재하던 질산성질소와 황산염이 환원되는 비율이 증가하였다. 또한, 생물재생 후 수행한 산・알카리 세정은 생물재생된 수지의 이온교환능 회복에 도움이 되었다. 3) 생물재생 기간을 2일로 고정하고 반복적으로 파과와 재생을 수행한 결과, 반복사용 횟수가 증가할수록 질산성질소는 초기 유출이 빨라졌으며 재생효율도 감소하였다. 그러나, 황산염의 경우, 반복적인 파과와 재생에도 불구하고 생물재생 효율이 100%로 측정되었다. 4) 생물재생이 진행되고 있는 이온교환컬럼 유출수를 대상으로 이온의 농도를 측정한 결과, 황산염이 질산성질소보다 먼저 탈착되었다. 이는 실험에 사용된 A520E 수지가 질산성질소 선택수지이기 때문에 결합력이 상대적으로 약한 황산염이 먼저 탈착된 것으로 판단된다. 5) 파과된 이온교환수지를 생물학적으로 직접 재생하는 기술은 이온교환공정이 갖고 있던 재생과 관련된 문제를 극복함으로써 오염된 대수층의 복원과 RO 농축액(concentrate)과 같은 특정 산업폐수 분야에 성공적으로 적용할 수 있을 것으로 기대된다.