Overall studies for the N-nitrosodimethylamine (NDMA) formation and treatment methods were conducted. In this study, occurrence in several countries and emerging treatment technologies of NDMA were generally reviewed. The NDMA formation was dependent on pH, contact time, and molar ratio (monochloramine/dimethylamine). The formation was rapidly increased when the molar ratio was greater than 1. It was likely that monochloramine could be related to stimulate NDMA formation. NDMA concentrations in water supply and wastewater plants after disinfection were approximately 10 ng/L and 100 ng/L, respectively. UV oxidation and adsorption processes are regarded as effective technologies for the NDMA removal. It is suggested that the UV oxidation with proper lamps is applied in water supply system.
1990년대에 캐나다 온타리오주의 음용수인 상수원에서 N-nitrosodimethylamine (NDMA)가 처음으로 검출되었으며, 미국 캘리포니아 상수원의 경우 1998년 이후 지속적으로 NDMA가 존재하는 것으로 조사되어 새로운 소독부산물 유해물질로 관심받기 시작하였다(Ontario MOE, 2000; Mitch and Sedlak, 2004). 미국 환경청에서는 다양한 종류의 상수와 하수의 염소화합물에 의한 살균 처리 후에 존재하는 것으로 발표하였으며 백만분의 일 확률로 암을 발생시킬 수 있는 NDMA 농도를 0.7 ng/L로 규정하였다(U.S.EPA, 2004). 초기에는 캐나다와 미국에서 연구가 가장 활발히 진행되었으나 현재는 여러 나라에서 조사가 이루어져 살균 후 일부 상수 및 하수에서 이 화합물 농도가 1,000 ng/L 이상 발생되는 사례도 보고되고 있다(Ontario MOE, 2000; Krauss et al., 2009).
NDMA생성 과정은 크게 두 가지로 구분할 수 있다(Choi and Valentine, 2002a; Mitch and Sedlak, 2002; Mitch and Sedlak, 2004). 첫째는 염소나 모노클로라민이 NDMA 전구 물질인 디메칠아민과 반응하여 중간 생성물인 1.1-dimethyl-hydrazine(DMH)로 산화되어 생성되는 것이다. 둘째는 디메칠아민이 아질산과 반응하는 니트로소화이다. 상수원에서는 미량이지만 디메칠아민과 아질산염을 포함한 여러 종류의 전구물질이 있어 생성이 가능하며, Choi (2002)의 연구에 따르면 상수에서 브롬(Br) 및 염소이온이 NDMA의 생성을 촉진시키는 촉매역할을 한다고 발표하였다. NDMA 전구물질로서 자연적으로 존재하는 유기물, 아민류에서도 NDMA가 생성되지만 농도는 낮다고 여러 연구에서 보고되었다(Gerecke and Sedlak, 2003; Mitch and Sedlak, 2004; Chen and Valentine, 2007; Shen and Andrews, 2013). 또한, 여러 연구에서 아민 관련 의약품들 및 살충제(Shen and Andrews, 2013), 아민 관련 폴리머나 레진(Najm and Trussell, 2001; Mitch and Sedlak, 2004)에도 전구물질이 존재한다고 지적하였다. Shen and Andrews (2013)는 의약품 성분인 ranitidine과 sumatriptan을, Najm and Trussell (2001)은 4종류의 음이온 레진을 전구물질로서 미처리 지하수 또는 증류수에 반응시킨 결과, NDMA 생성과 연관이 있는 것을 조사하였다. Lee and Yoon (2007)은 아질산, 디메칠아민, 용존산소가 존재하는 조건에서 광화학 반응에 의한 NDMA 생성에 대해서 발표하였다. 이와 같이, 염소나 모노클로라민을 이용한 상수 및 하수 살균처리 과정에서 NDMA가 형성되는데, 생성된 NDMA의 농도는 모노클로라민농도와 직접적인 관련이 있으며 Gerecke and Sedlak (2003)은 자연수에서 소독제인 염소나 모노클로라민이 디메칠아민과 반응하여 약 0.6% NDMA가 생성된다고 발표하였다.
수처리 공정 후에 존재하는 NDMA로 인해, 많은 상・하수처리 시설에서 NDMA는 새로운 이슈가 되고 있는데, 특히 처리수를 지하대수층으로 주입하는 남부 캘리포니아의 여러 재이용 시설들에서 더욱 큰 문제로 부각되었다(Barrett et al., 2003; Patterson, 2012; US Orange County Sanitation District, 2002). 이 화합물은 고분자 폴리머를 사용한 응집침전과 이온교환을 이용한 상수처리 과정에서도 발견되는 것으로 조사되어 그 심각성은 높아지고, 트리할로메탄 보다 독성이 몇 배 강하여 외국에서는 엄격한 환경기준으로 규제하고 있다. NDMA 처리법으로는 여러 가지 방법이 연구되었으나 UV 산화법과 흡착법이 일반적으로 효율적 처리법인 것으로 알려져 있다(Webster et al., 2013). 실리카나 제오라이트와 같은 흡착제에는 흡착이 잘 되지 않는데 이는 NDMA가 친수성 성질을 나타내기 때문이다. Lee et al. (2007)에 따르면, 전통적인 오존 처리는 NDMA 제거율이 낮았으나, 오존/과산화수소를 사용할 경우 산화제 농도와 비율에 따라 높은 제거율을 보였다. Hatzinger et al. (2011)은 R. ruber ENV425를 주입한 멤브레인 생물 반응조에서 99.95% 이상 제거된 것으로 조사하였다. 하지만 지하수에 고농도 트리클로로에틸렌이 존재 할 경우 처리효율은 감소 하였고, 생물학적 처리법이 대두되고 있으나 너무 느린 반응성 때문에 다른 대안을 찾고 있다.
본 연구에서는 국내외 상・하수에 존재하는 NDMA 생성농도를 조사 또는 측정하였으며 pH 변화에 따른 발생을 검토하였다. 그리고 이 화합물의 가장 효율적인 처리법을 고찰하여 우리나라에 실정에 맞는 제거방법의 제시와 상수와 하수처리장의 염소 살균 전후의 NDMA 검출 가능성을 분석하였다.
본 연구에 사용된 재료인 N-nitrosodimethylamine (100 ug/mL)은 Ultra Scientific NS-100(USA), NDMA-d6 (1 mg/mL)은 Cambridge Isotope Laboratory (USA), 차아염소산 나트륨용액은 Fisher Scientific (USA), 디메칠아민은 Alfa Aesar (USA)에서 각각 구입하였다.
디메칠아민 농도를 일정하게 유지하고 모노클로라민 농도에 따른 NDMA 생성농도를 24 시간 후에 측정 분석하였다. 이를 위하여 1 리터 갈색병에 증류수를 넣고 온도가 조절되는 어두운 장소에서 화학반응에 의한 NDMA 생성농도를 측정하였다. 모노클로라민 농도는 0.001 ~ 5 mM로 변화시켰으며, 내부 표준물질인 NDMA-d6을 주입하여 250 rpm으로 1시간 동안 흔들어 주었다. 흡착물질(Ambersorb 348F)은 여과장치에 의해 회수한 후 후드에서 1 ~ 2 시간동안 건조시킨 후 디크로로메탄으로 추출하였다. 모노클로라민은 실험 바로 전에 DPD-FAS 방법에 의해 제조하였으며, pH 조절은 완충용액을 사용하였다(APHA, WWA, and WEF, 1998).
분석은 Restek Rtx-Vrx 칼럼(60 m, 0.32 mm ID, 1.8 um film, USA)이 설치되고 질량분석기는 EI 모드에 의해 이온화가 되는 GC/MS (Shimadzu QP5050, Japan)을 사용하였다. 자동 시료기에 의해 디크로로메탄으로 추출된 4 uL 시료를 채취하여 주입하였고, 분석조건은 오븐, 주입, 검출온도가 각각 35℃, 200℃, 200℃로 하고 초기에 오븐온도에서 4분간 유지한 후 10℃/min되게 상승시켰다. 운반 기체는 헬륨이며 유량은 1.2 mL/min이고 splitless 조건으로 분석하였다. 분석 장비의 NDMA 검출한계는 1 ug/L이다.
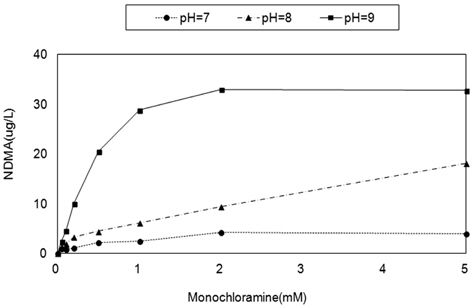
상수에서의 NDMA 생성 경로는 염소살균에 의한 모노클로라민과 전구물질인 디메칠아민에 의해 발생하는데 pH가 중요한 역할을 한다. Fig. 1은 본 연구결과로서, pH 7 ~ 9에서 모노클로라민 농도에 따른 NDMA 생성을 보여주고 있다. pH 9에서 높은 NDMA가 생성되고 있으나 모노클로라민 농도가 1 mM 이상에서는 발생이 정체되는 모습을 보이고 있으며 pH 8에서는 지속적으로 증가하는 경향을 나타내고 있다. 모노클로라민 농도가 5 mM일 경우 pH 8과 9에서 NDMA 생성 최대농도는 각각 18.1 ug/L, 32.7 ug/L로 측정되어 모노클로라민 증가와 밀접한 연관이 있었다.
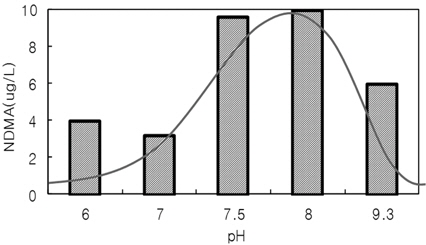
Mitch and Sedlak (2002)의 연구에 따르면 NDMA 발생이 pH에 따라 변하는데 pH 8에서 NDMA농도가 최고가 되는 것을 발견하였다. 낮은 pH에서는 수소이온, 높은 pH에서는 수산화이온이 NDMA 발생에 방해 작용하는 것으로 추측된다. Shen and Andrews (2013)에 의하면 pH 8에서 최대의 NDMA가 생성되고 pH 7이하에서는 비양성화된(non-protonated) 아민과 수소이온에 의해서, 높은 pH의 경우는 비양성화된 아민이 증가하지만 디클로라민의 부족 때문에 이 화합물 생성이 한정된다고 하였다. 즉 pH 9이상에서는 낮은 디클로라민 농도로 인하여 NDMA 생성도 감소한다고 설명하였다. pH는 NDMA 생성에 중요한 역할을하므로 이를 예측하는 연구가 발표되기도 했다(Choi and Valentine, 2002b; Kim and Clevenger, 2007). Hatt et al.(2013)은 하수 처리장에서 NDMA 생성을 줄이기 위해서는 pH을 6 이하로 유지하는 것과 염소살균 접촉시간을 줄일 것을 제안했다. Fig. 2는 기존 연구를 비교 해석한 것으로 모노클로라민과 디메칠아민 농도가 같은 조건인 0.1 mM에서 NDMA 발생을 나타낸 것이다(Choi, 2002; Kim, 2008). pH가 7.5 ~ 8에서 최고 농도를 보이다가 점차 감소하는 것을 보여주고 있다. 현장에서 pH 조정은 쉽지 않지만 pH 7 ~ 8을 피하여 살균할 것을 제안하고자 한다.
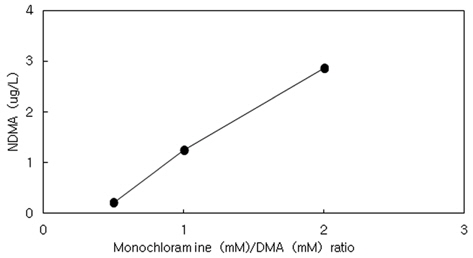
NDMA 생성에 주는 다른 인자로는 온도, 디메칠아민 농도, 접촉시간을 들 수 있다. Farré et al. (2011)은 상수처리장에서 NDMA 생성에 미치는 영향에 대하여 종합적으로 비교 발표하였다. 온도가 증가 할수록 주로 NDMA 발생은 증가하는 것으로 조사 되었는데 이는 반응속도상수가 온도에 비례하기 때문이다. 상・하수에서의 주요 NDMA 생성경로는 염소 또는 오존살균과 전구물질인 디메칠아민 농도에 의해 발생하고 있다. Choi와 Valentine (2002b)의 연구결과에 의하면 모노클로라민/디메칠아민 비율이 1 근처에서 NDMA 생성 농도의 변화를 보이는데, 비율이 1보다 클 경우 NDMA 생성이 높게 나타났다(Fig. 3). 앞에서 언급했듯이, 모노클로라민/디메칠아민 비율이 1보다 클 경우 중간 생성물인 1.1-DMH를 산화시키기 위하여 모노클로라민이 급속도로 소모되면서 NDMA 생성을 증가시키는 것으로 여겨진다.
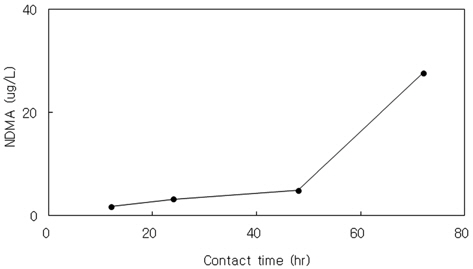
Mitch and Sedlak (2004)의 연구에서는 475 시간 동안 NDMA 생성에 관하여 조사하였는데 초기 150 시간까지 생성이 급속하게 증가하다가 그 이후는 점차 둔화되는 경향을 보였고 염소이온 농도도 이 시간까지 급속하게 감소하여 NDMA 생성에 연관이 있음을 발표하였다. Fig. 4에서도(Kim, 2008), 일정 디메칠아민과 모노클로라민 농도에서 반응시간을 변화시킨 결과 48 시간까지는 일정하게 증가하다가 72 시간에 급속하게 증가하는 것을 볼 수 있다. 특히 정수장에서 접촉시간과 초기 디메칠농도를 고려할 경우 염소 소독시 접촉시간 증가와 함께 고농도 NDMA 생성을 촉진할 수 있음을 보여 주는 결과이었다.
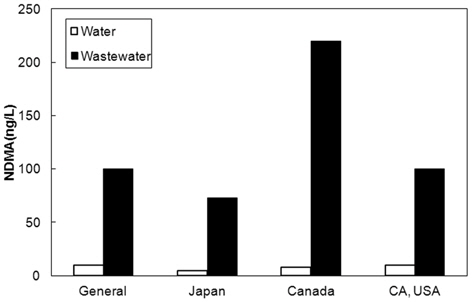
인체에 매우 위해한 발암물질로 분류되고 있는 NDMA가 최근 상수원에서도 검출되고 있는데 위해성은 트리할로메탄보다 훨씬 심각한 것으로 알려지고 있다. 상수와 하수에서의 NDMA 모니터링은 캐나다가 가장 많은 자료를 확보하고 있으므로 캐나다 온타리오 정부의 자료를 중심으로 상수에서 발생되는 NDMA 농도를 살펴보았다. Fig. 5는 여러 국가에서 조사한 기존 연구로서, 상・하수 처리수에서 검출된 최고 NDMA 농도를 요약한 것이다(Asami et al. 2009; Ontario MOE, 2000; US Orange County Sanitation District, 2002). 1990년과 1998년 사이 지표수를 원수로 사용하는 정수장 101개를 대상으로 조사한 결과에 의하면, 37개 정수장의 원수에서 1 ng/L 이상의 NDMA가 검출되었다. NDMA는 원수뿐만 아니라 정수에서도 발견되었다. 온타리오 주 내에 위치한 100개 정수장에서 시료를 분석한 결과에 의하면, 45%에 해당하는 시료에서 1 ng/L 이상의 NDMA가 검출되었고 최고 8 ng/L 이었다(Ontario MOE, 2000).
상수와 마찬가지로 재이용수에서도 NDMA가 발견되었다. 미국 캘리포니아 오렌지카운티의 상수도국에 있는 Water Factory 21(WF 21)은 하수처리장 2차 처리수를 원수로 이용해서 3차 처리한 후 지하 대수층에 주입하고 있다 (US Orange County Sanitation District, 2002). 이 지하수는 인근 정수장에서 원수로 사용하는데, WF 21의 처리공정은 소석회를 이용한 화학적 침전, 이산화탄소를 이용한 pH조정, 여과 그리고 역삼투 공정으로 구성되어 있다. 비공식적으로 측정된 자료에 의하면, 66 ng/L의 NDMA가 WF 21에 유입되어서 152 ng/L로 유출되었다. 이러한 결과는 NDMA가 처리공정을 거치면서 제거되는 대신 생성되는 것을 나타내고 있다. 비록 정확한 이유는 밝혀지고 있지 않으나 WF 21은 처리공정 중 주입되는 염소로 인해서 NDMA가 생성되는 것으로 추측하고 있다. Asami et al. (2009)의 연구에서는 일본의 상수 원수에서 NDMA가 2.6 ~ 4.3 ng/L 검출되었고, 오존 살균 처리 후 농도는 10 ng/L까지 증가하다가 생물활성탄 처리 후는 점차 감소하는 것으로 조사하였다. Huy et al. (2011)은 일본의 23개 지하수와 18개 강에서 시료를 분석한 결과 NDMA 농도가 지하수와 강에서 각각 0.5 ~ 5.2 ng/L, 0.5 ~ 3.4 ng/L로 발표하였다.
여러 나라에서 연구한 결과, NDMA는 상수원의 염소, 모노클로라민, 오존 살균처리 과정에서 증가하는 것으로 보인다. Mitch et al. (2003)은 염소 또는 클로라민 살균 때에 미량의 질소함유 유기화합물이 있어도 서로 화학 반응을 하여 NDMA, 즉 소독부산물이 생성된다고 하였다. Dai and Mitch (2013)는 클로라민으로 살균된 미국 상수 시료의 34%에서 NDMA가 존재하는 것을 확인하였고 새로운 분석법이 이 화합물 농도를 정확하게 나타내지 못하는 문제점을 제시하고 NDMA 생성의 중요성을 강조하였다. 상대적으로 오존 살균 과정에서는 이 화합물의 발생 농도가 낮은 것으로 보여 우리나라에서 상수원 살균방법에 도움이 되는 결과로 이용될 것으로 여겨진다. 미국 캘리포니아는 3 ng/L, 캐나다 온타리오는 9 ng/L, 캐나다 연방정부는 40 ng/L, 세계보건기구는 100 ng/L로 음용수 기준치를 잠정적으로 제시하고 있다(Sakai et al., 2012). 상수에서 세계보건기구 기준치를 초과하는 경우는 없었으나 캘리포니아와 같이 엄격한 기준을 초과 하는 경우가 있어 이에 대한 대책이 필요하다.
초기에 하수에서의 NDMA 모니터링도 캐나다가 가장 많은 자료를 확보하고 있으며, 상수보다 하수에서 NDMA가 더 높은 농도로 검출되었다. Fig. 5에서와 같이, 하수처리장 처리수 39개의 시료를 분석한 결과에 의하면 27개의 시료에서 NDMA가 검출되었고 최고 검출농도는 220 ng/L에 이르렀다(Ontario MOE, 2000). 미국 캘리포니아 주내에 위치한 하수처리장 방류수의 NDMA농도를 조사한 결과에 의하면, 일부 처리장에서는 100 ng/L를 초과하는 고농도의 NDMA가 검출되었다. 미국 내 14개 하수처리장에서 발생한 건조 슬러지에 포함된 NDMA 농도를 조사한 결과에 의하면 하수 슬러지에서는 0.6 ~ 45 ug/L에 이르는 고농도의 NDMA를 함유하고 있었다(Mumma et al., 1984). 일본의 12개 하수처리장에서 유입수 NDMA는 1 ~ 80 ng/L이고 하수처리 후 유출수는 1 ~ 73 ng/L로 큰 차이가 없었다(Yoon et al., 2011). 스위스 21개 하수처리장에서 NDMA농도는 대개 5 ~ 20 ng/L이었으나 최고 1 ug/L까지도 검출되었다(Krauss et al., 2009).
일반적으로 하수에서 NDMA 발생 농도는 상수보다 높게 검출되었는데 이는 유기물을 포함한 많은 전구물질이 존재하기 때문으로 생각된다. 아직 하수 배출허용기준은 시행되고 있지 않으나 최고 1 ug/L 이상 검출되고 있고 지하수나 다른 지표수에 유입될 수 있어 이에 대한 대책도 필요하다. 앞에서 언급하였듯이 살균 경로에서 증가 하므로 염소 농도조절, pH 조절 등을 통하여 발생 억제를 유도할 것을 제안한다.
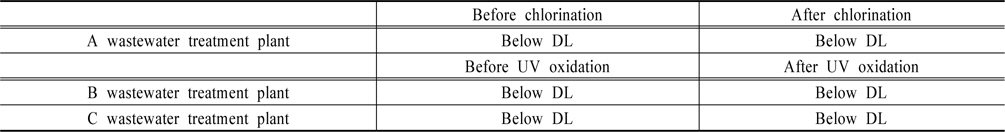
국내에서 NDMA의 발생 농도를 알아보고자 전라남도 상・하수 처리장 몇 곳을 선정하여 실험을 실시하였다. 먼저 정수장의 경우 대상 시료는 염소처리 전과 염소처리 후에 채수하였다. 하수처리장은 염소 또는 자외선 살균처리를 하는 곳을 각각 선정하였으며, 채수 장소는 염소나 자외선 처리전과 처리 후이며 분석 결과는 Table 1과 같다.
[Table 1.] NDMA concentration at wastewater treatment plant
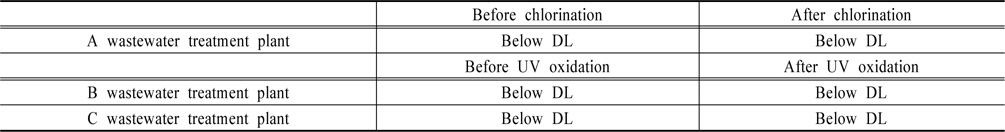
NDMA concentration at wastewater treatment plant
실험결과, 상수와 하수의 모든 시료에서 NDMA는 검출한계농도(1 ug/L) 이하로 조사되었다. 앞에서 언급하였듯이 상수의 경우는 NDMA가 낮은 농도로 존재하여 국내 시료에서도 무시할 정도로 존재할 것으로 여겨진다. 외국의 하수 시료에서는 1 ug/L이상 검출되는 경우가 자주 있었는데 다행히 국내 하수시료에서는 NDMA가 존재하지 않았거나, 존재하더라도 그 농도가 극미량 존재 할 것으로 추측된다. 분석기기의 검출농도 한계로 인하여 그 이하로 존재할 경우 앞으로 추가적인 연구가 필요한 실정이다.
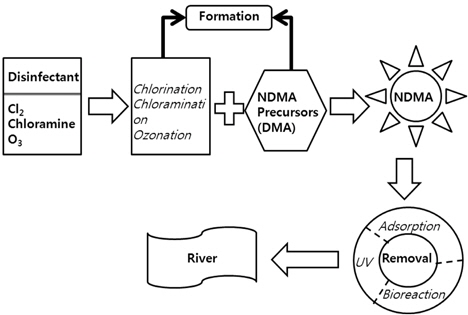
Fig. 6은 NDMA 발생과 처리를 종합적으로 나타낸 설명이다. 앞에서 언급하였듯이, NDMA 처리법으로는 UV 산화법과 흡착법이 일반적이고 효율적 방법으로 인식하고 있다(Kommineni, 2003). Sakai et al.(2012)의 연구에서는 UV 파장에 따른 NDMA 광분해에 대해서 발표했는데 222-nm이 254-nm 보다 4 배 정도 효율이 증가 하는 것으로 조사하였으며 파장과 램프 종류에 의해서도 효율이 변한 것으로 발표하였다. 하지만 고농도 유기물이 존재 할 경우 광화학에 의한 반응이 더욱 느려져 처리가 어려워지는 것과 고비용 처리라는 단점이 있어 다른 대체 연구가 발표되고 있다. 활성탄 흡착이 효과적인 방법으로 알려져 있지만, 실리카겔은 낮은 처리율을 나타내고 있고 고비용이 문제점이 되고 있다.
대안으로 생물학적 처리가 대두되고 있는데 처리에 시간이 걸리는 것과 적합한 미생물 선정이 중요한 요소가 된다. Hatzinger et al. (2011)은 R. ruber ENV425를 주입한 멤브레인 생물 반응조에서 유입 NDMA 7.4 ug/L에서 0.0023 ug/L로 감소하여 99.95% 이상 제거되었다. 하지만 지하수에 고농도 트리클로로에틸렌이 존재할 경우 처리효율은 감소하였다. 지하수의 경우 여러 가지 휘발성 유기화합물이 존재 할 가능성이 높아 생물학적 처리에 한계가 있을 것으 로 생각된다. Webster et al. (2013)은 R. ruber ENV425를 주입한 유동상 장치를 이용하여 30분 체류시간에서 지하수에 존재하는 NDMA 농도가 0.01 ug/L이하로 조사되어 UV의 대체 기술로 적합하다고 보고하였다. 이와 같이, 생물 반응조를 적용한 NDMA 처리 시도가 있으나 체류시간이 긴 단점이 있어 해결할 과제로 여겨진다. Pisarenko et al.(2012)는 오존/과산화수소 산화 및 역삼투압을 적용한 파일럿 크기의 장치를 이용한 상수와 하수를 처리할 경우 NDMA 농도가 상수에서는 약간 감소하였으나 하수는 0.006 ~ 0.033 ug/L 생성되는 결과를 얻었다. Chen and Valentine (2008)은 유기물이 존재하는 지표수에 염소, 과산화수소, 오존과 반응시킨 후 광화학 처리를 한 결과 NDMA가 감소한 것을 밝혔다.
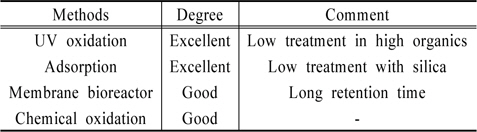
Table 2에 요약하였듯이, 여러 가지 NDMA 처리법이 연구되고 있는 상황에서 단시간에 효율적으로 사용 가능한 처리법은 UV 산화법으로 여겨진다. 효율을 증대하기 위해서는 UV 램프의 파장과 종류를 선택적으로 사용할 경우 도움이 될 것으로 생각된다. 상수 처리장에서는 염소나 오존 살균 후 UV 또는 활성탄과 같은 흡착제로 최종 처리할 경우 NDMA의 문제는 크게 감소할 것으로 판단된다.
[Table 2.] Comparison of NDMA Treatment Methods
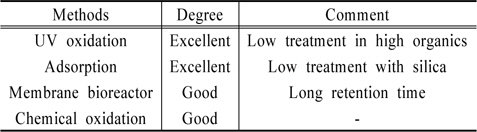
Comparison of NDMA Treatment Methods
상・하수에서의 주요 NDMA 생성 경로는 전구물질인 디메칠아민과 염소살균 이후에 발생하는 결합잔류염소인 모노클로라민과 오존살균에 의해 발생되고 있다. 많은 연구결과에서 모노클로라민 농도에 비례하여 NDMA의 생성도 증가함을 알 수 있었다. 이는 염소살균 처리에 발생하는 잔류성 결합염소인 모노클로라민과 유기물에 포함된 디메칠아민과의 상관성이 있기 때문이다. 그리고 pH와 접촉시간이 생성에 중요한 역할을 하여 이를 조정하는 방법도 생성감소에 도움을 준다. 우리나라가 물 부족 국가로 분류된 실정에서 하수의 재사용을 위해 염소 살균 및 상수원의 염소살균처리 과정에서 발생 가능한 NDMA의 생성에 대한 주의가 요구되며, 이에 따른 대책 마련도 필요할 것으로 예상된다. 단시간에 효율적으로 사용 가능한 NDMA 처리법은 UV 산화법으로 여겨지며 처리효율을 증대하기 위해서는 알맞은 UV 램프의 파장과 종류를 선택할 것을 제안한다. 상수 처리장에서는 염소나 오존 살균 후 UV 또는 활성탄과 같은 흡착제로 최종 처리할 경우 NDMA의 문제는 크게 감소할 것으로 판단된다.