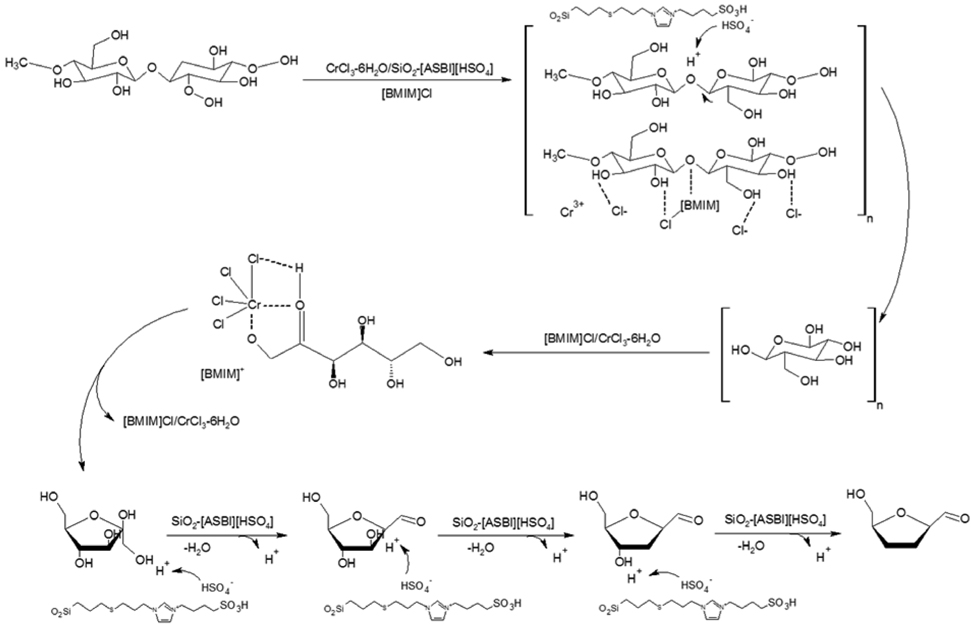
Various metal chlorides and acid catalysts in ionic liquid solvent were investigated to directly convert cellulose into 5-hydroxymethylfurfural (5-HMF). Metal chlorides containing Sn(II), Zn(II), Al(III), Fe(III), Cu(II), and Cr(III) were used and acidic ionic liquid immobilized on silica gel as an acid catalyst and commercial acid catalysts (sulfuric acid, chloric acid, Amberlyst-15,DOWEX50x8) were used for comparison studies. The acid strength and amount of acid catalysts were probed with Hammett indicator. The selectivity and yield of 5-HMF were determined with reaction temperature, reaction time and catalyst ratio. A catalyst containing CrCl3-6H2O and SiO2-[ASBI]HSO4 showed the highest selectivity and it was found that this catalyst had higher activity than commercial solid acid catalysts such as Amberlyst-15 and DOWEX50x8. The selectivity of 5-HMF appeared to be mainly dependent on the acid strength and catalyst ratio, it was found that levulinic acid was produced from 5-HMF by rehydration.
화석자원의 고갈과 화석연료 사용에 따른 환경오염이 중요시 됨에 따라 바이오매스를 원료로 하는 바이오에너지가 대두 되고 있다. 바이오매스(biomass)는 화석자원과 달리 이산화탄소, 빛과 물을 흡수하여 생성될 수 있는 생물을 의미하며 에너지로 전환될 수 있는 가능성과 더불어 이산화탄소의 저감효과, 원료 공급의 지속 가능성 장점 등을 지니고 있다[1-3] . 바이오매스를 이용한 바이오에너지 생산 사례 중, 가장 대표적인 것은 사탕수수나 옥수수를 이용하여 바이오에탄올을 생산한 연구가 있다. 그러나 사탕수수나 옥수수 등의 농작물은 인류를 위한 식량이므로 목재, 간벌재, 건축과 공장폐재, 혹은 볏짚과 보릿짚 등 식량과 경쟁하지 않는 폐기물계 바이오매스를 에너지 자원으로 이용하는 것이 더 바람직하다고 할 수 있다[4]. 이러한 점에서 셀룰로우스는 2세대 바이오매스인 목질계의 주요 구성성분으로써 매우 풍부하고 인류의 식량으로 바로 이용할 수 없는 물질이기 때문에 에너지, 연료 및 화학 물질로 전환하기에 바람직한 물질이다[5]. 셀룰로우스는 단위체인 글루코오스가 1,4-글리코시딕 결합(1,4-glyosidic bond)과 수소결합으로 이루어진 안정한 고분자 물질로써 생물학적 또는 열화학적 방법을 통한 기초화학원료로의 전환이 어려우며, 셀룰로우스의 분해도 어렵게 한다. 이러한 문제점을 해결하기 위하여 분쇄, 용해, 산, 알칼리 처리 등과 같은 다양한 전처리 방법이 연구되고 있다. 이러한 셀룰로우스의 전처리 공정은 대상물질에 대한 높은 수율을 얻을 수 있지만, 공정의 경제성 문제로 상업화에 어려움이 있다. 따라서 셀룰로우스의 전처리 공정 없이 기초화학원료를 직접 전환하는 공정의 연구가 필요하다[6].
5-HMF는 수산화 작용기를 지니고 있는 친수성 성질의 케톤계 고리화합물 구조로 화학중간체로써, 우수한 활용성을 보이고 있다. 5-HMF의 유도체로써 2,5-디메틸푸란(2,5-dimethylfuran, DMF)은 에탄올에 비하여 에너지 밀도가 40% 정도 높아 바이오연료로 사용할 수 있으며, 다른 유도체인 5-hydroxymethylfuric acid, 2,5-furandicarboxyaldehyde와 레불린산(levulinic acid) 등은 중합반응을 통하여 플라스틱 및 고분자 물질로 활용 가능 하다[7].
5-HMF는 일반적으로 단당류 프룩토오스(fructose)로부터 탈수화 반응에 의하여 생성된다. 그러나 프룩토오스는 자연적으로 존재하지 않기 때문에, 셀룰로우스(cellulose)의 가수분해를 통해 생성된 글루코오스의 이성질화 반응으로 얻을 수 있게 된다[8]. 즉 셀룰로우스로부터 5-HMF로 직접 전환하기 위해서는 가수분해, 이성질화 및 탈수화 반응이 이루어져야 하고, 이에 관한 연구가 보고되고 있다[9-14] . 반응에 관여하는 주요 인자는 반응용매와 반응촉매이다. 하지만, 셀룰로우스의 안정한 구조이므로 일반 유기용매에 용해되지 않는다. 2002년 Rogers가 발표한 이후, 염화 1-에틸-3-메틸 이미다졸리움(1-ethyl-3-methylimidazolium chloride, [EMIM]Cl)이라는 이온성 액체가 반응용매로 많이 사용되고 있다[9]. 반응촉매는 크게 금속염화물 촉매를 기반으로 많이 알려져 있는데, 이는 금속염화물의 금속이온이 글루코오스를 5-HMF로 전환 하는데 주요한 역할을 하기 때문이다. 염화이온(Cl-)을 지니는 이온성 액체 용매하에서, 염화(III)크롬 육수화물(CrCl3-6H2O) [10], 염화(II)크롬(CrCl2)과 염화(II)구리(CuCl2)[11], 염화(II)크롬(CrCl2)과 염화루테늄(RuCl)[12]과 같은 금속염화물 촉매들이 사용되고 있다. 이 외에도 염화(II)크롬(CrCl2)/염산(HCl) [13]을 사용하여 셀룰로우스의 가수분해를 증가시키거나 3-allyl- 1-(4-sulfobutyl) imidazolium hydrogen sulfate ([ASBI]HSO4)의 산성 이온성 액체 용매에서 황산코발트(CoSO4)를 사용한 사례[14]가 최근 제시되었다. 그러나 이러한 반응계는 30~50%의 5-HMF 수율을 보이지만 반응 후, 균일하게 섞여있는 혼합액에서 5-HMF의 분리가 어렵고 촉매의 재사용이 힘든 단점을 보인다. 더욱이 산 촉매의 경우 반응기를 부식시키거나 폐수를 발생시킨다는 문제점도 지니고 있다. 이 연구에서는 친환경적이고 촉매를 재사용하기 위하여 불균일계 산 촉매인 Amberlyst-15, DOWEX50x8과 산성 이온성 액체를 고정화한 촉매를 제조 및 사용하여 셀룰로우스의 5-HMF로의 직접 전환반응을 수행하여 보였다. 이온성 액체는 거대 양이온과 음이온으로 이루어진 액체로 양이온과 음이온에 따른 다양한 특성(산성, 염기성, 소수성, 친수성, 선택적 반응의 가능성)과 넓은 응용성(반응용매, 반응촉매 등)으로 인해 다양한 반응에 활용 할 수 있는 물질이다[15]. 본 연구에서는 다양한 산성 작용기 와 음이온이 포함된 고정화산성 이온성 액체 촉매를 제조하고, 이 촉매가 셀룰로우스의 5-HMF 직접전환에 미치는 영향을 평가하였다. 또한, 무기산 H2SO4, HCl와 상용화 고체산 Amberlyst-15, DOWEX50x8를 대조군으로 선정하여 촉매 성능을 비교하였다.
고정화 산성 이온성 액체 촉매 제조를 위해 사용된 시약으로는 Merck사의 실리카겔 60 (0.063~0.200 mm)과 Sigma-Aldrich의 순도 95%의 3-멜캄토프로필-트리메톡시실란(3-mercaptopropyl trimethoxysilane, 3-MPS), 99% 1,4-부탄술톤(1,4-butane sultone), Alfa사의 순도 99% 1-알릴이미다졸(1-allylimidazole), 삼전화학의 순도 99% 염화티오닐(thionyl chloride), 99.7% 아세톤, 99.5% 디에틸에테르(diethylether), JUNSEI사의 순도98% 진한황산, 99.5% 톨루엔(toluene), 98% 아조비스이소부틸니트릴(azobisobutyronitrile, AIBN)를 사용하였다. 5-HMF 전환을 위한 반응물질과 반응용매는 Sigma-Aldrich사에서 99% 셀룰로우스와 98% [BMIM]Cl을 구입하였으며, 금속염화물 촉매로는 98%의 염화(II)주석(SnCl2), 염화(II)아연(ZnCl2), 염화(II)구리(CuCl2)와 95%의 염화(III)알루미늄(AlCl3), 97%의 염화(III)철(FeCl3)은 JUNSEI에서 구입하였으며, 99%의 염화(III)인듐(InCl3), 염화(II)크롬(CrCl2), 염화(III)크롬(CrCl3)과 염화(III)크롬 육수화물(CrCl3-6H2O)은 Sigma-Aldrich에서 구입하였다.
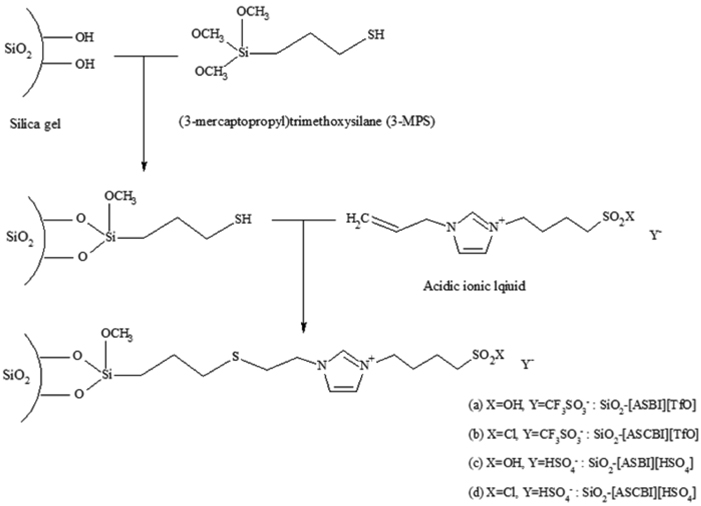
반응에 사용된 촉매인 산성 이온성 액체 촉매는 이온성 액체를 이루고 있는 양이온의 작용기와 음이온에 따라 각각 3- allyl-1-(4-sulfobutyl)imidazolium hydogen sulfate ([ASBI]HSO4), 3-allyl-1-(4-sulfobutyl)imidazolium trifluoromethanesulfonate([ASBI]TfO), 3-allyl-1-((4-sulfurylchloride)butyl)imidazolium hydrogen sulfate ([ASCBI]HSO4), 3-allyl-1-(4-sulfurylchloride) butyl)imidazolium trifuloromethanesulfonate ([ASCBI]TfO)라 명명하였다. 이후, 실리카겔에 제조한 산성 이온성 액체를 고정화하여 SiO2-[ASBI]HSO4, SiO2-[ASBI]TfO, SiO2-[ASCBI] HSO4, SiO2-[ASCBI]TfO라 명명하였다. 각 촉매의 구조는 Figure 1에 나타내었다[16].
제조된 고정화 산성 이온성 액체 촉매가 지니는 산도 및 산밀도는 Hammett indicator를 통하여 결정하였다. 본 실험에 사용한 Hammett indicator 지시약의 종류는 2-nitroaniline(pKa = -0.2), 4-nitrophenylamine(pKa = -2.4), 2,4-dichloro-6-nitroaniline (pKa = -3.2), 2,4-dinitroaniline(pKa = -5.6)과 chalcone(pKa = 5.6)을 사용하였다. Hammett indicator 지시약 0.035 g을 벤젠 40mL에 용해시킨 용액에 촉매 0.1 g을 넣어 분산시킨 후 색 변화를 관찰하여 촉매의 산도인 pKa 값의 범위를 선정하였다.
각 촉매의 산 밀도는 Hammett indicator 지시약 1.5 mL와 벤젠 유기용매 4.5 mL를 혼합한 용액에 촉매 0.1 g을 분산시켰으며 2.6 N n-부틸아민(n-butylamine)으로 적정하였다. 촉매가 분산된 용액의 색이 Hammett indicator 지시약의 염기성으로 변할 때까지 적정하였으며 하기식으로부터 제조 촉매의 산밀도를 계산하였다[17].
Bc는 n-부틸아민 농도(mmol/mL)이며, Bv는 n-부틸아민 적정량(mL), Xa는 촉매 질량(g)이다.
5-HMF로의 직접 전환 반응을 위한 반응장치는 Radleys사 에서 제조한 carousel 12 plus reaction station의 45 mL 용량의 유리 튜브 반응기에서 수행하였다. 반응기 내부에 반응용매 1.96 g, 셀룰로우스 0.10 g, 금속염화물 촉매와 산 촉매 각각 0.02, 0.01 g을 넣고 반응시간과 반응온도에 따라서 마그네틱바로 교반하여 실험을 수행하였다. 반응기의 온도가 목표 온도에 도달하였을 때부터 반응을 시작하는 시점이라 설정하였다. 반응 후에는 반응기를 상온으로 냉각하였으며 얻어진 반응물을 고성능 액체크로마토그래피(high performance liquid chromatography, HPLC, Shimadzu LC-20A)에 주입하여 5-HMF 및 부생성물의 수율을 분석하였다. 반응 후의 고체 잔여물은 증류수로 여러 번 세척 및 건조시킨 후 셀룰로우스의 전환율을 계산하였다. 셀룰로우스로부터 생성되는 수율, 셀룰로우스의 전환율, 생성물의 선택도는 하기식으로부터 계산하였다.
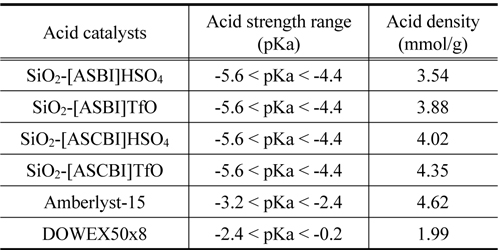
Table 1은 Hammett indicator를 사용하여 얻어진 고정화 산성 이온성 액체 촉매와 상용화 촉매인 Amberlyst-15와 DOWEX50x8에 대한 산도 및 산 밀도의 결과값을 나타내고 있다. 고정화 산성 이온성 액체 촉매 4종류는 약 -5.6 < pKa < -4.4 사이의 값을 나타내었으며, 4종류 모두 유사한 범위의 pKa값을 나타내었다. 상용화 촉매인 Amberlyst-15는 -3.2 < pKa < -2.4의 범위에서, DOWEX50x8은 -2.4 < pKa< -0.2 범위의 pKa값을 확인할 수 있었다. 각 촉매의 산 밀도를 계산한 결과, 고정화 산성 이온성 액체 촉매는 4종류 모두 3.54~4.35 mmol/g 범위의 산 밀도를 확인할 수 있었다. Amberlyst-15 촉매는 4.62 mmol/g, DOWEX50x8은 1.99 mmol/g의 산 밀도를 확인하였으며, 제조 촉매가 Amberlyst-15와 DOWEX50x8보다 높은 산도를 지니고 있음을 확인할 수 있었다.
[Table 1.] Acid strength and density of acid catalysts by Hammett indicator
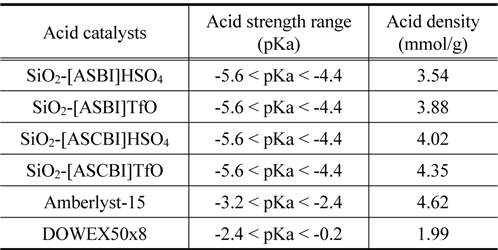
Acid strength and density of acid catalysts by Hammett indicator
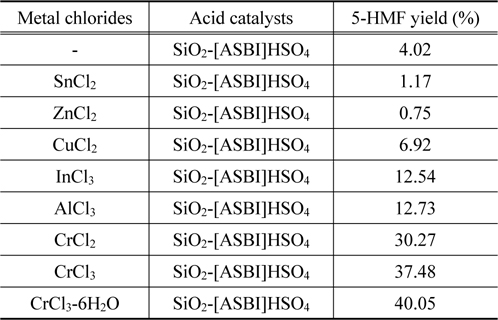
셀룰로우스의 5-HMF 직접 전환에서 다양한 산 촉매와 금속염화물 촉매를 사용하여 5-HMF의 수율에 미치는 영향을 평가하였다. Table 2에서는 전이금속을 포함하는 금속염화물과 SiO2-[ASBI]HSO4을 함께 사용하여 5-HMF의 수율 결과 이다.
[Table 2] The effect of different metal chlorides on 5-HMF produc- tion from cellulose
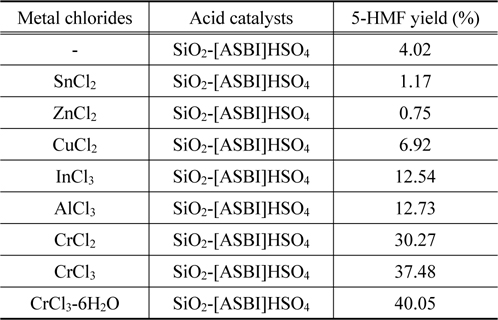
The effect of different metal chlorides on 5-HMF produc- tion from cellulose
반응실험 결과, Cr(III), Cr(II), Al(III), In(III), Cu(II), Sn(II), Zn(II)의 금속이온을 포함한 촉매순서로 5-HMF 수율이 높다는 것을 확인하였으며, 그 중 크롬을 포함하는 염화물에서 가장 높은 활성을 보였다. 이는 크롬 이온이 피라노스(pyranose) 형태의 글루코오스를 퓨라노스(furanose) 형태의 프룩토오스로 전환시키는데 가장 낮은 활성화 에너지를 지닌다는 사실과 부합한다[18]. 또한, [BMIM]Cl 이온성 액체 용매에 대하여 5mol%의 범위 내에 수화물을 포함할 경우, 셀룰로우스의 전환율이 더 증가한다는 결과와 부합하여 수화물 형태인 CrCl3-6H2O를 사용할 경우 무수화물인 CrCl3보다 높은 5-HMF 수율을 보였다[19].
Figure 2는 다양한 산 촉매에 따른 생성물의 수율의 결과이다. 제조한 고정화 산성 이온성 액체 촉매 4종에 대하여 모두 63.2~64.4%의 전환율과 55.6~60.9%의 5-HMF 선택도를 확인 할 수 있다. 고정화 산성 이온성 액체 촉매를 각각 비교하면 HSO4 음이온이 TfO 음이온보다 높은 활성을 보였으며, 브뢴스테드 산을 보이는 SO3H 작용기가 루이스 산을 나타내는 SO2Cl 작용기보다 높은 활성을 나타냈다. 무기산인 염산을 사용할 경우 불균일계 산 촉매에 비하여 셀룰로우스의 전환율은 높게 나타난 반면에 5-HMF의 선택도는 낮게 나타났다. 염산과 같은 균일계 산 촉매는 반응계 내에서 분자 수준에서 반응이 일어나기 때문에 셀룰로우스의 전환율은 높으나 선택적으로 5-HMF를 전환하기에는 어려움이 있다. 상용으로 사용되는 불균일계 산 촉매인 Amberlyst-15는 고정화 산성 이온성 액체촉매에 비하여 낮은 5-HMF의 선택도를 보였으나, 레불린산의 선택도가 높은 것으로 보아 5-HMF의 재수화 반응에 영향을 끼치는 것으로 판단된다. DOWEX50x8은 약 57.1%로 고정화 산성 이온성 액체 촉매를 사용할 경우와 비슷한 5-HMF 선택도를 나타냈으나 셀룰로우스의 전환율이 52.0%로 낮음을 보였다. 이를 통해 셀룰로우스로부터 5-HMF가 선택적으로 높게 전환되기 위해서는 사용되는 산 촉매의 적절한 산도 범위가 중요하다고 사료된다.
셀룰로우스의 5-HMF 직접 전환 반응은 가수분해, 이성질화와 탈수화 반응이 연속적으로 일어나야 한다. 3단계의 복잡한 반응은 각각 필요한 촉매가 다르며 사용되는 촉매에 따라서 생성물들이 변화될 수 있다. Figure 3은 셀룰로우스의 5-HMF 직접 전환 반응에서 4가지 형태의 촉매종류가 생성물에 어떠한 영향을 미치는지에 대한 결과를 나타내고 있다. 반응에 사 용한 촉매의 종류는 먼저 이온성 액체 용매인 [BMIM]Cl를 단독으로 사용한 경우, [BMIM]Cl와CrCl3-6H2O를 동시에 사용 한 경우, [BMIM]Cl와 SiO2-[ASBI]HSO4를 동시에 사용한 경우 및 [BMIM]Cl, CrCl3-6H2O와 SiO2-[ASBI]HSO4를 동시에 사 용한 형태로 나누었다. 첫 번째로 [BMIM]Cl 이온성 액체만을 사용할 때, 셀룰로우스의 전환율은 33.0%였고 글루코오스와 5-HMF가 각각 10.6, 4.0%로 낮게 생성되었다. 이는 [BMIM]Cl 가 반응의 촉매적 기능보다 셀룰로우스를 용해시키는 용매로서의 기능으로만 작용한다는 것을 알 수 있다. [BMIM]Cl는 셀룰로우스의 단위체인 글루코오스의 C3 와 C6에 위치한 수산 기와 결합을 이루면서 구조를 깨어지게 한다. [BMIM]+은 전자쌍주개로 작용하는 산소원자와 결합하며, Cl-은 전자쌍받개로 작용하는 수소원자와 공유결합을 형성한다. 그 결과 셀룰로우스의 고분자 구조가 점차 깨어지면서 용해도가 증가하게 된다 [20,21]. 즉 반응에 사용한 [BMIM]Cl은 셀룰로우스의 단위체인 글루코오스의 수산기 결합을 분해하여 셀룰로우스의 용해도를 증가시키는 반응용매로 작용함을 알 수 있다.
반응용매 [BMIM]Cl 하에서 금속염화물계 촉매인 CrCl3-6H2O를 첨가하여 사용하였을 때, 셀룰로우스의 전환율은 46.0%로 증가하였으며 그와 동시에 5-HMF의 수율도 17.2%로 증가하는 경향을 보였다. 이는CrCl3-6H2O가 셀룰로우스로부터 5- HMF를 직접 전환하는 데 촉매로 작용하는 것으로 판단된다. 먼저 CrCl3-6H2O가 지니는 수화물(H2O)의 proton으로 인해 셀룰로우스의 1,4-글리코시딕 결합이 분해되면서 글루코오스가 생성된다. 가수분해 이후 생성된 글루코오스는 pyranose 구조를 띄게 되는데 이 때 크롬 이온을 통하여 furanose 구조의 프룩토오스로 전환된다. 이후 탈수화 반응을 통해 5-HMF로 전환되어진다[22].
그러나 SiO2-[ASBI]HSO4를 첨가하여 사용하였을 때, 셀룰로우스의 전환율이 증가함과 동시에 글루코오스의 수율이 증가하였다. 이는 SiO2-[ASBI]HSO4가 지니고 있는 술폰산(SO3H)의 작용기와 HSO4 음이온의 proton으로 인해 가수분해 효율이 증가한다고 사료된다[23]. 제조 촉매의 산도는 Hammtt indicator 적정을 통하여 측정하였는데 pKa 범위는 -5.6 < pKa <-4.4로 확인하였다. 그러나 -5.1 이하의 pKa 값에서 셀룰로우스의 전환율이 증가함과 동시에 글루코오스의 수율이 증가한다는 결과를 고려하면 제조촉매의 산도 범위는 -5.6 < pKa < -5.1이라 사료된다[24].
마지막으로, 두 촉매를 동시에 사용할 경우 5-HMF의 수율은 40%로써 단독으로 사용한 경우보다 크게 증가하였다. 이는 SiO2-[ASBI]HSO4를 사용함으로써 셀룰로우스의 전환율과 글루코오스의 수율이 증가하고 그와 동시에 CrCl3-6H2O를 통해 생성된 글루코오스가 5-HMF로 전환되어 수율이 증가하는 것으로 판단된다. 하지만 5-HMF의 수율이 증가하면서 레불린산의 수율도 증가하였다. 이는 레불린산은 산 촉매하에서 5- HMF의 재수화 반응에 의하여 생성되며, 이 반응계의 산 촉매인SiO2-[ASBI]HSO4가 지니는 산 성질로 인해 5-HMF의 부반응인 재수화 반응이 일어나 레불린산이 생성된다는 것을 알 수 있다.
3.2. CrCl3-6H2O/SiO2-[ASBI]HSO4 촉매하에서의 생성 물 변화
Figure 4는 셀룰로우스의 5-HMF 직접 전환반응에서 가장 우수한 활성을 보인 CrCl3-6H2O/SiO2-[ASBI]HSO4의 촉매하에서의 반응온도에 따른 셀룰로우스의 전환율 및 생성물의 변화를 나타내고 있다. 반응온도가 증가할수록 셀룰로우스의 전환율이 31.0에서 74.0%로 증가하였고 5-HMF의 선택도도 373에서 403 K까지 11.6에서 60.9%로 증가하였다. 그러나 413K 의 반응온도에서는 5-HMF의 선택도가 47.4%로 감소하는 경향을 알 수 있는데 이는 레불린산의 선택도가 22.3에서 38.7%만큼 급격한 증가에 의한 것으로 판단되며, 403 K보다 높은 반응온도에서는 셀룰로우스의 5-HMF로 직접 전환보다 5-HMF의 재수화 반응의 활성이 높아져 레불린산으로 전환되는 것 이라 사료된다.
Figure 5는 CrCl3-6H2O, acid : SiO2-[ASBI]HSO4촉매하에서의 반응시간에 따른 셀룰로우스의 전환율 및 생성물의 변화 결과이다. 반응시간이 증가할수록 셀룰로우스의 전환율이 57.0에서 78.0%로 증가하는 경향을 보이나 5-HMF의 선택도는 2시간 에서 60.9%로 나타난 후 2시간 이후부터 44.1%로 감소한다는 것을 알 수 있었다. 그와 동시에 레불린산의 선택도는 18.6 에서 38.6%까지 지속적으로 증가하는 경향을 보였다. 이는 셀룰로우스의 5-HMF 직접전환 반응이 연속적으로 일어나는 반응이므로 반응시간이 증가할수록 연속반응의 최종산물인 레불린산의 선택도가 증가하였다고 사료되며, 셀루로우스로부터 5-HMF의 높은 선택도를 얻기 위해서는 적정한 반응시간이 필요하다는 것을 알 수 있다.
Figure 6은 셀룰로우스에서 5-HMF 직접 전환반응에서CrCl3-6H2O 와 SiO2-[ASBI]HSO4의 중량비에 따른 전환율 및 생성물의 변화 결과이다. 먼저 CrCl3-6H2O 와 SiO2-[ASBI]HSO4 중량비 50 : 50 비율일 때 5-HMF의 선택도가 60.9%로 가장 높게 나타났다. 또한 단독으로 CrCl3-6H2O 와 SiO2-[ASBI]HSO4를 사용한 경우보다 동시에 사용하였을 때 5-HMF의 선택도가 높다는 것을 알 수 있다. 그러나 SiO2-[ASBI]HSO4의 촉매 중량비가 50 이상일 때 레불린산의 선택도가 증가하였으며, 이는 SiO2-[ASBI]HSO4가 지니는 강산성으로 인해 5-HMF가 레불린산으로 전환되는 것이라 판단된다.
3.3. SiO2-[ASBI]HSO4 촉매의 재사용성 평가
반응 후, SiO2-[ASBI]HSO4촉매의 재사용성 평가 결과는 Table 3에 나타내었다. 반응 이후 반응용매에 불균일계로 존재하는 SiO2-[ASBI]HSO4 촉매는 필터링을 통하여 회수하고 건조시킨 후 재사용하였다. 5회까지 사용한 결과 촉매의 활성이 약 17.5% 감소되었으며 이는 술폰산(SO3H) 작용기를 지닌 고정화 산성 이온성 액체 촉매의 반응활성이 크게 감소되지않고 유지될 수 있으며, 재사용이 가능하다는 것을 알 수 있다. 더욱이 이와 같은 특성을 지닌 고정화 산성 이온성 액체 촉매가 다양한 반응에서 활용될 수 있음을 보인다[25,28].
[Table 3.] The reusability of SiO2-[ASBI]HSO4 on direct conversion from cellulose to 5-HMF
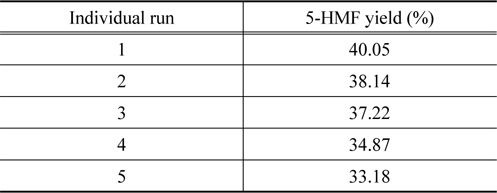
The reusability of SiO2-[ASBI]HSO4 on direct conversion from cellulose to 5-HMF
Figure 7에서는 본 연구에서 사용된 각각의 용매 및 촉매가 셀룰로우스의 5-HMF 직접 전환반응 메커니즘을 나타내었다. 가수분해 반응에 의해 셀룰로우스가 지니는 1,4-글리코시드 결합이 깨지게 된다. 이 때 SiO2-[ASBI]HSO4 촉매의 수소이온이 글리코시드 결합의 산소원자와 결합하고 동시에CrCl3-6H2O의 염화이온이 수산화작용기의 수소원자와 결합하게 된다. 또한, 용매로 사용된 이온성 액체 [BMIM]Cl에서 1-butyl- 3-methylimidazolium 양이온이 글리코시드 결합의 산소원자와 공유결합을 이루게 된다. 이와 같은 용매와 촉매의 영향을 통해 글리코시드 결합이 끊어지게 되면서 단당류인 글루코오스로 전환되는 것으로 판단된다. 이후, CrCl3-6H2O의 크롬 이온이 생성된 글루코오스의 일반적 고리형 구조인 파이라노스를 개환시켜 프룩토오스로 전환시키는 주요한 역할을 한다. 프룩토오스는 다시 SiO2-[ASBI]HSO4 촉매의 수소이온이 수산화작용기와 결합되어 단계적으로 3개의 물분자가 빠지게 되고 최종적으로 5-HMF가 생성된다. 그러나 반응 중, SiO2-[ASBI]HSO4 촉매의 수소이온이 과량으로 존재하여 재수화 반응을 통한 레불린산으로 전환되기 때문에 5-HMF의 선택도가 감소되는 것이라 사료된다[29].
실리카겔에 담지된 산성 이온성 액체와 금속염화물 촉매를 이용하여 셀룰로우스의 5-HMF 직접 전환반응을 수행한 결과 다음과 같은 결론을 얻었다. CrCl3-6H2O와 SiO2-[ASBI]HSO4촉매를 동시에 사용하였을 때 높게 나타났으며, 특히 403 k, 2시간 동안 반응시킨 결과, 5-HMF 수율은 40%로 높게 나타내었다. 본 연구에서 사용된 촉매 반응계에서 Cr(III)을 포함한 CrCl3-6H2O 금속염화물에서 가장 높은 활성을 보였으며, 제조한 촉매가 상용화 촉매인 무기산(H2SO4, HCl)과 불균일계 산촉매(Amberlyst-15, DOWEX50x8)에 비하여 선택적으로 높은 활성을 보인다는 것을 알 수 있었다. 산 촉매에 따른 5-HMF의 수율은 촉매가 지니는 산도에 따라서 선택적으로 5-HMF가 전환됨과 동시에 5-HMF의 재수화 반응을 일으켜 레불린산으로 전환되는 것을 확인하였다.
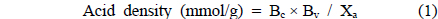

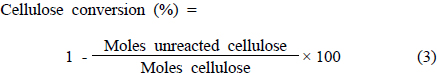
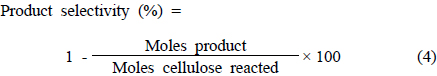
![The correlation between product selectivity and acid catalysts. (conditions : cellulose (0.10 g), solvent (1.96 g), MClx (0.02 g), acid (0.01 g), 2 h) ; solvent : [BMIM]Cl, MClx : CrCl3-6H2O).](http://oak.go.kr/repository/journal/13249/CJGSB2_2014_v20n2_108_f002.jpg)
![Direct conversion of cellulose into 5-HMF using different catalytic process. (conditions : cellulose (0.10 g), solvent (1.96 g), MCl x (0.02 g), acid (0.01 g), 403 K, 2 h) ; solvent : [BMIM]Cl, MCl x : CrCl 3-6H2O, acid : SiO2 -[ASBI]HSO4 ).](http://oak.go.kr/repository/journal/13249/CJGSB2_2014_v20n2_108_f003.jpg)
![The effect of reaction temperature on conversion and selectivity from cellulose. (conditions : cellulose (0.10 g), solvent (1.96 g), MClx (0.02 g), acid (0.01 g), 2 h) ; solvent : [BMIM]Cl, MClx : CrCl3-6H2O, acid : SiO2-[ASBI]HSO4](http://oak.go.kr/repository/journal/13249/CJGSB2_2014_v20n2_108_f004.jpg)
![The effect of reaction time on conversion and selectivity from cellulose. (conditions : cellulose (0.10 g), solvent (1.96 g), MClx (0.02 g), acid (0.01 g), 403 K, ) ; solvent : [BMIM]Cl, MClx : CrCl3-6H2O, acid : SiO2-[ASBI]HSO4).](http://oak.go.kr/repository/journal/13249/CJGSB2_2014_v20n2_108_f005.jpg)
![The effect of catalyst loading on conversion and yield from cellulose. (conditions : cellulose (0.10 g), solvent (1.96 g), 403 K, 2 h) ; solvent : [BMIM]Cl, MClx : CrCl3-6H2O, acid : SiO2-[ASBI]HSO4).](http://oak.go.kr/repository/journal/13249/CJGSB2_2014_v20n2_108_f006.jpg)
![The reusability of SiO2-[ASBI]HSO4 on direct conversion from cellulose to 5-HMF](http://oak.go.kr/repository/journal/13249/CJGSB2_2014_v20n2_108_t003.jpg)