Alkali-surfactant-polymer (ASP) solution was manufactured by using the domestic surfactants for enhanced oil recovery. Domestic surfactants such as linear alkylbenzene sulfonic acid (LAS) and dioctyl sulfosiuccinate (DOSS) were used. This surfactants were purchased from AK chemtech Co., Ltd. (Korea). LAS and DOSS were blended and the ratio of LAS to DOSS are 1:1 and 2:1. Decane was used as a model compound of the crude oil. Surfactant solution and decane were blended to analyze microemulsion. Brine-oil-surfactant are mixed at varying concentration of brine from 0.8 to 3.6 wt.%. Increasing salinity causes the phase transition of microemulsion from water to middle to oil. Also, by measuring the surface tension and interfacial tension using pendent drop tensiometer and Huh’s equation optimal ratio of the ASP solution was determined.
국내산 계면활성제를 이용하여 오일회수증진용 알칼리-계면활성제-폴리머(alkali-surfactant-polymer, ASP)용액을 제조하였다. 계면활성제는 현재 애경에서 사용되고 판매되어지는 리니어알킬벤젠술폰산(linear alkylbenzene sulfonic acid, LAS)과 디옥틸설포석신나트륨(dioctyl sulfosiuccinate, DOSS)을 사용하였으며 LAS와 DOSS를 1:1, 2:1의 비율로 섞어 합성계면활성제를 제조하였다. 염도는 0.8 wt.%에서 3.6 wt.%까지 변화시킨 뒤 계면활성제 용액과 오일모사로 쓰인 데칸(decane)을 섞어서 마이크로에멀젼 형성을 알아보았다. 염도가 변하면서 마이크로에멀젼 층은 증류수에서 오일로 이동하였으며 최적의 염도일 때 가용화 값을 측정하였다. 또한 표면장력 측정기를 이용하여 표면장력을 측정하였으며 Huh 방정식을 이용하여 계면장력을 측정하였다. 이후에 각각의 계면활성제 비율에 대한 마이크로에멀젼의 특성을 비교하였다.
현재 전 세계적으로 오일 수요는 급격히 증가하고 있다. 그 중 중국과 같은 개발도상국의 급격한 경제성장은 전 세계 오일 수요를 지속적으로 증가시키는 원인중 하나이며, 이러한 수요를 책임질만한 신규 유전의 발견은 점점 어려운 실정이다[1]. 과거에는 신규 대형 유전의 발견이 빈번하여 증진 회수로 인한 추가 매장량 확보 비용보다 신규 유전의 탐사 및 발견 비용이 훨씬 저렴했다. 최근에 들어 전 세계적으로 전통형 유전에 대한 신규 발견의 빈도와 양이 점차 감소하여 1999년 이후에는 생산량의 45%만을 신규 발견한데 그치고 있다[2]. 그러나 오일 수요는 매년 1.5% 이상씩 증가하고 있으며 세계주요 100대 유전의 생산량은 정점을 지나 감소하고 있는 추세이다[3].
이러한 수급 불균형 문제의 해결 방안으로 최근 석유회수 증진기술(enhanced oil recovery, EOR)에 대한 관심이 높아지고 있다. EOR기술에는 혼합 가스 또는 용매, 화학물질, 열 에너지 등을 저류층에 주입하여 저류층 내에 존재하고 있는 잔존석유를 회수하는 기법이다. 일반적으로 유전은 저류암 내의 자연 압력에 의해서 석유를 회수하는 방법인 일차회수 후에도 약 70~90% 정도의 잔존석유가 잔존하고 있으므로, 세계적으로 퍼져있는 유전의 확인 매장량을 기준으로 EOR기술을 적용하면 추가적으로 생산할 수 있는 석유의 양은 약 2,417억 배럴정도로 추정할 수 있다[4].
이러한 석유회수증진기술들은 크게 열공법(thermal flooding method), 가스주입법(gas injection method), 화학공법(chemical flooding method) 등으로 분류되며, 유전의 특성이나 적용환경을 고려하여 1차회수 2차회수 후에 저류층에 잔존하는 석유를 추가적으로 회수하기 위한 기술로 사용된다[5].
먼저 열공법은 저류층 내에 열을 공급하여 오일의 점도와 비중을 감소시켜 오일 회수를 증진시키는 방법으로 증기주입법(steam injection), 현장연소법(in-situ combustion, ISC)이 있다. 이 중 증기주입법은 주기적 증기자극법(cyclic steam stimulation, CSS)과 지속적 증기주입법(steam flooding)으로 세분화 할 수 있으며, 현장연소법은 오일의 비중에 따라 중질오일에서 적용되는 고온산화법(500~600 ℃)과 경질오일에 적용되는 저온산화법(150~300 ℃)으로 나눠지며, 저온산화법은 고압 공기주입법(high pressure air injection, HPAI)법으로도 불린다. 이러한 열공법은 증기 주입 시 주입정으로 열이 누출되지 않고 저류층 내에서 대류 및 전도에 의해 열이 효율적으로 전달되는 것이 가장 중요하다[6-8].
가스주입법은 저류층에 탄화수소가스, 이산화탄소, 질소 및 배연가스(flue gas)를 주입시켜 회수를 증진시키는 방법이다. 주입가스는 압력에 따라 혼합상태 혹은 비혼합상태로 유동할 수 있으나 일반적으로 혼합상태에서 회수 효율이 더 높은 것으로 알려져 있다. 수공법이나 계면활성제 주입법과 같은 다른 회수방법과 결합하여 사용할 수 있는 장점이 있다[9,10].
화학공법은 암석의 모세관압과 점착력에 의해 공극 내에 잔류된 오일의 유동성을 증대시키기 위해 사용되며 주로 화학물질을 물과 혼합하여 주입하는 방법이다[11]. 주입되는 화학물질은 계면활성제, 알칼리, 폴리머 등이 있으며, 알칼리-계면활성제(alkali-surfactant, AS), 알칼리-폴리머(alkali-polymer, AP), 알칼리-계면활성제-폴리머(alkali-surfactant-polymer flooding, ASP)를 혼합 또는 순차적으로 주입하는 방법이다[12,13].
본 연구에서는 화학공법중 하나인 ASP공법을 사용하기 위한 기초실험을 진행하였다. ASP공법은 화학공법 중 가장 높은 효율을 갖고 있으나 ASP공법에 사용되는 화학물질들의 가격 경쟁력이 낮아 사용되지 않는 기법으로 분류되었다. 하지만, 석유의 가격이 나날이 높아지는 고유가 시대에 도입하면서 ASP공법의 경쟁력이 확보가 되어 다시금 활발히 연구 되는 기법중 하나이다[14]. ASP공법은 알칼리-계면활성제-폴리머를 혼합하여 저류층에 주입하는 기술로 각각의 화학물질들의 혼합비가 매우 중요하다[15,16]. 본 연구에서는 국내산 계면활성제를 이용하여 알칼리-계면활성제-폴리머의 최적화 된 혼합비를 찾는 연구를 진행하였다[17].
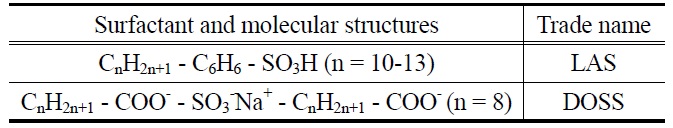
계면활성제는 음이온 계면활성제로 애경에서 구입한 LAS®(linear alkylbenzene sulfonic acid, 99.6%)와 DOSS® (dioctyl sulfosiuccinate, 64.8%)를 사용하였고, 계면활성제의 자세한 분자구조는 Table 1에서 확인할 수 있다. 알칼리물질로 사용된 탄산나트륨(sodium carbonate, Na2CO3)은 삼천에서 구입하여 사용하였으며, 조용매로 사용한 이소부틸알코올(isobutyl alcohol, IBA)과 염도측정 실험에 사용된 염 물질인 염화나트륨(sodium chloride, NaCl) 그리고 오일 모사로 사용된 데칸(decane)은 시그마-알드리치에서 구입하여 본 연구에 사용하였다.
표면장력실험에 사용된 장치는 표면장력 측정기(Dyne Technology Ltd., Model: WS13 7FE)를 사용하였고, 모든 측정은 하나의 시료를 3번 측정하여 평균값을 구하였다. 표준 편차는 ±0.1 mN/m이다.
계면활성제는 두 가지의 계면활성제를 혼합하여 사용하였으며 계면활성제는 각각 한쪽방향의 알킬사슬을 갖는 LAS®와 두 방향의 알킬사슬을 갖는 DOSS®이다. 두 가지의 계면활성제를 사용하는 이유는 LAS®의 경우 최적염도 수치가 매우 높아 현장에 적용하기 어렵기 때문에 염도 수치를 낮출 수 있는 두 방향 알킬체인을 갖는 DOSS®를 혼합하여 사용한 것이다. LAS®는 탄소가 10~13개의 친유성기를 가지고 있고 DOSS®는 탄소 8개의 친유기를 가지고 있다. 혼합계면활성제의 주는
[Table 1.] Surfactant molecular structures
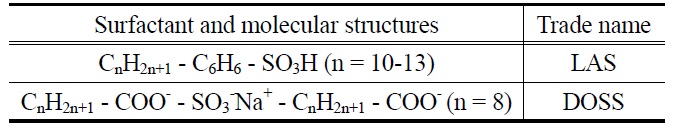
Surfactant molecular structures
[Table 2.] Combinations of LAS® and DOSS® surfactant
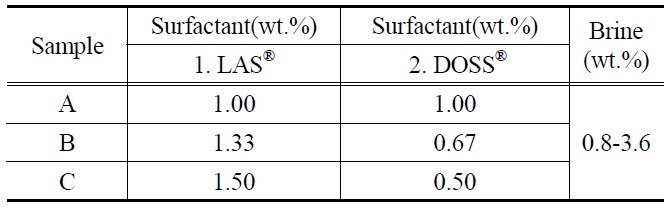
Combinations of LAS® and DOSS® surfactant
LAS®계면활성제를 사용하여 실험이 진행되었고 DOSS®와 1:1, 2:1, 3:1로 배합하여 실험을 진행하였다. 하지만 3:1의 경우 마이크로에멀젼이 생성되지 않아 본 논문에 사용된 결과는 1:1과 2:1로 배합하여 실험한 자료만 첨부하였다. 자세한 내용은 Table 2와 같이 요약할 수 있다.
모든 계면활성제는 4 wt.%의 IBA을 조용매로 사용하여 제조되었다. 제조된 혼합용액과 데칸을 1:1로 혼합시킨 후 염화나트륨을 0.8~3.6 wt.%까지 변화시켜 최적의 염도측정 실험을 진행하였다.
2.3. 국내산 계면활성제의 계면장력 및 표면장력 실험
Huh[18]는 오일과 증류수 사이의 가용화(VO/VS, Vw/VS)와 계면장력(γ)에 대한 이론적인 관계를 정립했다.
VO : 마이크로에멀젼에 대한 오일 부피
VS : 마이크로에멀젼에 대한 계면활성제 부피
Vw : 마이크로에멀젼에 대한 증류수 부피
C 값은 Huh의 상수로 EOR에 사용된 오일과 계면활성제 사이의 대한 값으로 대략 0.3 mN/m이다. 오일과 마이크로에멀젼 또는 증류수와 마이크로에멀젼 사이에 형성된 계면장력은 Huh 방정식으로 정확하게 적용되는 것이 수많은 논문을 통해 보였고, 온도나 염도의 다양한 변화에서도 Huh 방정식의 계면장력 값은 적용된다. 이 방법을 통한 계면장력 측정은 상 거동 실험이 수행된 이후 빠르고 쉽게 계면장력을 측정할 수 있는 장점을 가지고 있다[18,19].
시료의 표면장력은 표면장력 측정기를 이용하여 측정하였으며, 시료 하나당 3회 측정하여 평균값을 구하였다. 표준 편차는 ±0.1 mN/m를 넘지 않았다.
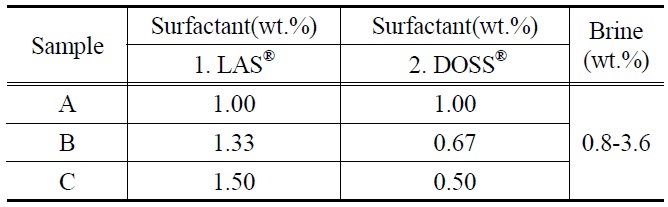
Hearly et al.[20]은 계면활성제 농도 단위당 오일과 물의 용해되는 양을 VO/VS, Vw/VS 같이 정의하였으며, 마이크로에 멀젼 안에 있는 각각의 계면활성제, 오일, 물의 부피를 각각 VS, VO, Vw로 표현하였다. 본 연구에서는 마이크로에멀젼안에 모든 계면활성제가 포함되어 있다는 가정하였고, 이에 대한 결과는 Figure 1을 통해 확인할 수 있다. 오일의 가용화(VO/VS) 측정값은 오일과 계면활성제 용액인 증류수를 적당히 섞은 후 안정화 된 후 측정할 수 있다. 이 값은 마이크로에멀젼에 용해된 오일을 계면활성제의 부피로 나눈 값으로 정한다. 이때 계면활성제의 부피는 모두 마이크로에멀젼 안에 있다고 추정하고 측정하였다. 용해된 오일 값은 처음 오일의 부피에서 마이크로에멀젼에 용해된 오일의 차로 구할 수 있다. 이와 값은 방법으로 증류수의 가용화(Vw/VS) 값은 마이크로에멀젼에 용해된 증류수를 계면활성제의 부피로 나눈 값으로 정의하였다. 마찬가지로 용해된 증류수의 값은 처음 증류수의 부피에서 마이크로에멀젼에 용해된 증류수의 차로 구할 수 있다. 최적의 가용화 값은 오일의 가용화 값과 물의 가용화 값의 그래프를 그렸을 때 만나는 점이 최적의 가용화 값이 된다[21].
염도가 증가하면 증가할수록 마이크로에멀젼은 증류수, 증류수와 오일 중간층 그리고 오일 층 쪽으로 형성이 되는 현상을 보인다. 즉, 마이크로에멀젼의 오일의 가용화(VO/VS) 값은 염도가 증가함에 따라 이 값도 증가하는 증가함수의 형태를 보이며, 증류수의 가용화(Vw/VS) 값은 염도가 감소함에 따라 이 값도 감소하는 감소함수의 형태를 보인다. 이 두 그래프의 교차점을 “optimal salinity” 즉 최적의 염도 값이라고 정의한다[22].
Figure 1(a)에서 최적의 염도 값은 1.9 wt.%가 되고 이때의 가용화 값은 5가 된다. 마찬가지로 Figure 1(b)에서 최적의 염도 값은 2.7 wt.%가 되고 이때의 가용화 값은 5.5가 된다. LAS의 비율이 높아지면 최적의 염도 값과 가용화 값이 동시에 증가하는 경향을 보인다. 따라서 계면활성제의 배합비율을 LAS:DOSS를
2:1로 배합했을 때가 1:1로 배합했을 때보다 더 높은 가용화 값을 갖는다는 것을 확인할 수 있었다.
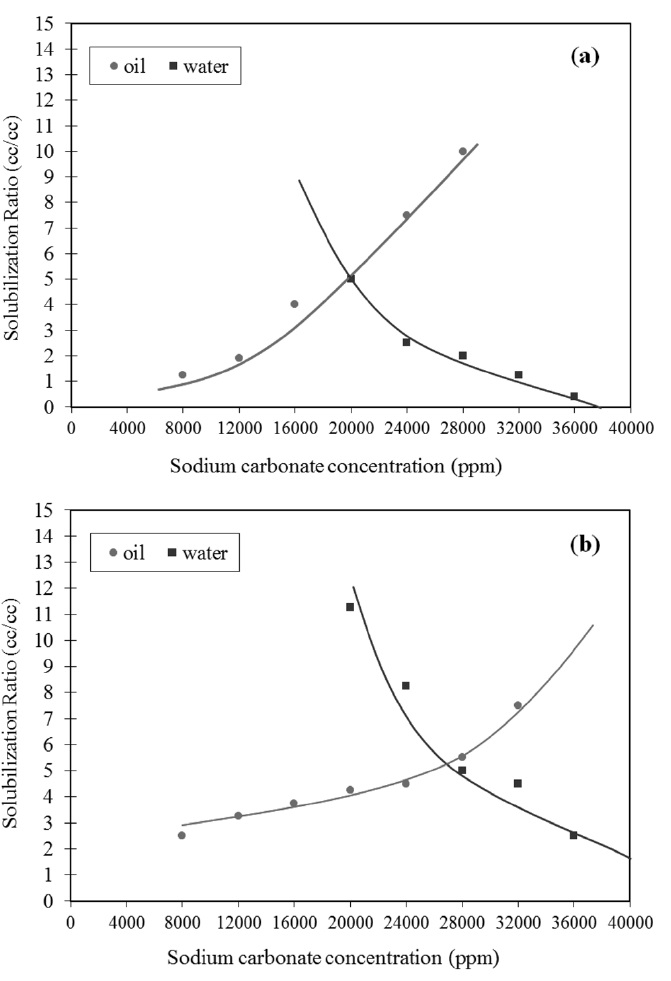
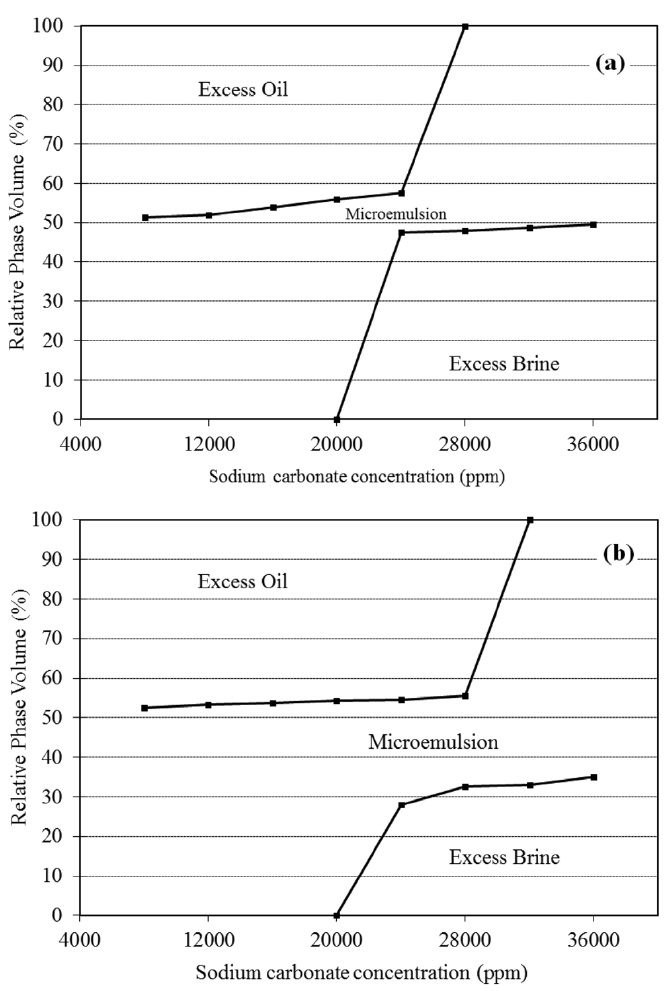
Figure 2(a), (b)는 각각의 계면활성제 비율에 대한 염도변화에 따른 마이크로에멀젼의 변화를 나타낸 실제사진이며, Figure 3(a), (b)는 Figure 2(a), (b)의 가시화된 마이크로에멀젼의 수치를 그래프로 나타낸 값이다. 염도에 변화에 따라 마이크로에멀젼의 위치가 조금씩 이동하는 것을 확인할 수 있었고 LAS:DOSS 2:1의 비율일 때가 1:1의 비율보다 더 높은 가용화된 마이크로에멀젼을 형성하는 것을 결과를 통해 확인할 수 있었다.
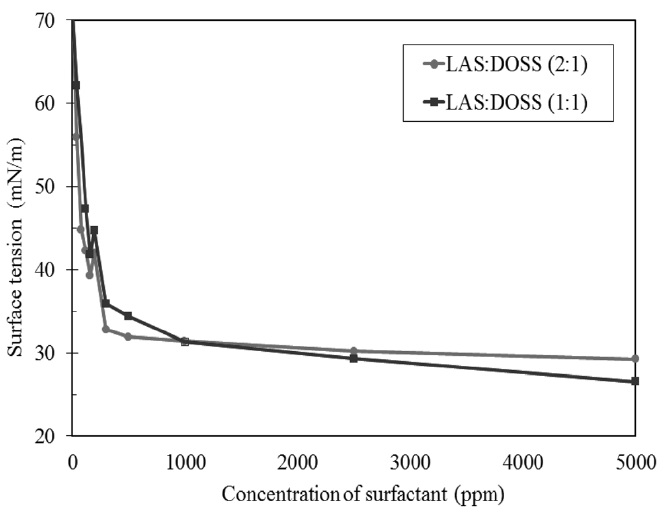
계면활성제는 액체와 기체사이의 계면의 표면장력을 낮추는 물질로 알려져 있다. 임계미셀농도(critical micelle concentration, CMC)는 물에 녹는 계면활성제의 농도가 증가할 때 미셀이 형성되는 시기의 농도로써 계면활성제의 성질을 나타내는 중요한 지표 중의 하나이다. 표면장력의 구배가 크게 변하지 않을 때의 계면활성제의 농도를 임계미셀농도로 정의할 수 있다[23].
Figure 4는 계면활성제의 임계미셀농도를 찾기 위해 계면활성제의 농도를 변화시켜 농도에 따른 계면장력을 나타낸 그래프이다. LAS:DOSS의 비가 1:1인 경우의 임계미셀농도는 0.03 wt.%이고 LAS:DOSS의 비가 2:1인 경우의 임계미셀농도는 0.1 wt.%이다.
마이크로에멀젼의 계면장력은 다양한 염도의 농도, 계면활성제의 종류, 저류층의 온도 등과 같은 복합적인 요인에 의해 결정이 된다. 계면활성제를 넣게 되면 염도에 따라서 마이크로에멀젼이 생기고 그 상이 이동하면서 하나 내지 두 개의 계면이 생기게 된다. 음이온 계면활성제를 통해 생성된 마이크로에멀젼/오일의 계면장력(γ
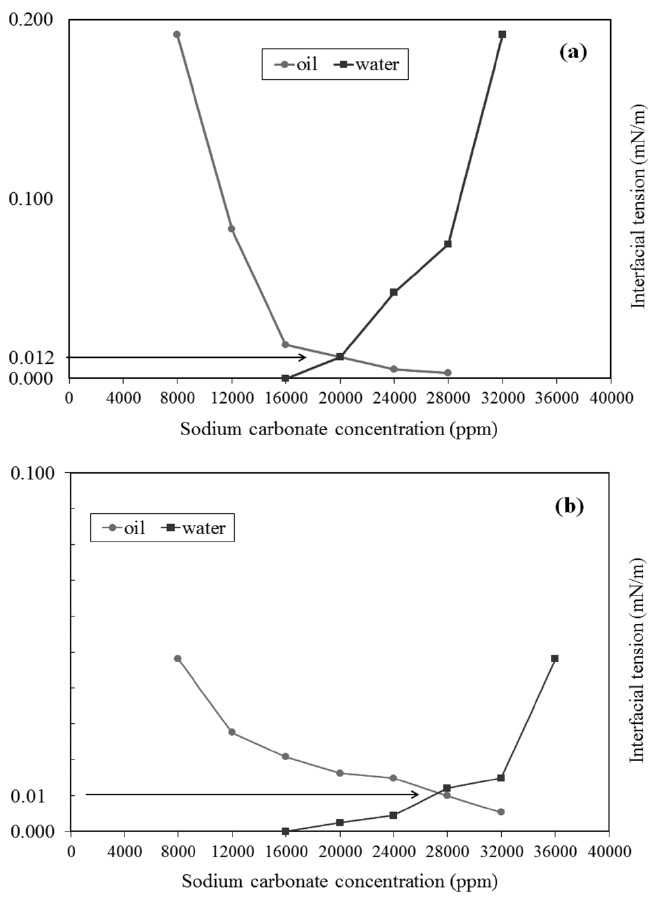
Figure 5는 염도에 대한 계면장력을 나타낸 그래프이다. 염도가 증가하면 γ
γ
LAS:DOSS의 비가 1:1인 Figure 5(a)에서 최적의 염도 일 때 계면장력은 0.012 mN/m이고 LAS:DOSS의 비가 2:1인 Figure 5(b)에서 최적의 염도일 때 계면장력은 0.01 mN/m이다. 현재 ASP용액의 상용화 값을 갖는 울트라 계면장력 값은 (<0.01)이다. 본 연구에서 사용된 국산화 ASP용액은 ASP용 액이 갖추어야 될 울트라 계면장력 값과 근접한 수치를 나타내는 것을 확인할 수 있었다. 이러한 결과는 국산화 ASP용액 의 최적의 배합비율을 찾은 것과 동시에 국산화 ASP용액의 현장 적용 가능성을 확인한 것이라 여겨진다[27-30].
본 논문에서는 국내산 계면활성제인 LAS와 DOSS를 사용하여 국내산 ASP용액을 제조하는 기초실험을 진행하였다. 이러한 기초실험은 실제 ASP용액을 적용하고자하는 저류층의 염도나 온도와 같은 환경 등을 고려해서 진행하는 실험이다. 이러한 기초실험 자료는 실험실 규모 및 파일럿 규모의 저류층 묘사 실험 장치에 적용하기 위한 필수 단계로 다양한 형태로 존재하는 저류층별 데이터베이스를 구축하는데 중요한 실험이다.
먼저 ASP용액의 알칼리, 계면활성제의 배합 비율은 문헌조사를 통해 1.0 wt.%와 2.0 wt.%로 고정을 시켜놓았으며, 현장 적용을 위해 가장 먼저 실시되는 최적의 염도 측정 실험을 진행하였다. 그 결과 2:1의 비율로 섞은 혼합용액이 1:1의 비율로 섞은 혼합용액보다 가용화 값이 높은 것을 확인하였으 며, 최적의 염도 조건은 1:1일 경우는 1.9 wt.%이고 2:1일 경우는 2.7 wt.%인 것을 확인하였으며 이 결과는 LAS의 비율이 높아질수록 최적의 염도 값이 높아지는 것을 확인 할 수 있었다. 이러한 결과를 토대로 다양한 환경을 갖는 현장상황에 맞게 염도조건을 조절할 수 있을 것이라 예상된다.
또한, 울트라 계면장력 값과 본 연구에서 찾은 배합비율을 통해 제조된 국내산 ASP용액이 근접한 계면장력 값을 갖는 것을 확인할 수 있었다. 이러한 결과로부터 국산화 계면활성제의 ASP기법 적용 가능성을 확인하였다.