The aim of this experiment is to provide an objective differentiation of cultivated ginseng, mountain ginseng through component analysis, and to know the change of ginsenoside components in the process of heating and fermentation.
Comparative analyses of ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, Rg1, Rg3, Rh1 and Rh2 from the cultivated ginseng 4 and 6 years, and mountain cultivated ginseng were conducted using HPLC (High Performance Liquid Chromatography, hereafter HPLC). And the same analyses were conducted in the process of heating and fermentation using mixed Lactobacillus rhamnosus, Lactobacillus plantarum, Bifidobacterium lactis for 7 days.
The change of ginsenosides to the process of red ginseng and fermentation, cultivated ginseng and mountain cultivated ginseng were showed another results. Mountain ginseng showed a lot of change compared with cultivated ginsengs. In the 7 days of fermentation, mountain ginseng showed that ginsenoside Rg1, Rb1, Rb2, Rc, and Rd were decreased and increased ginsenoside Re, Rf, Rg3 and Rh1 were increased compared with cultivated ginseng.
It seemed that ginsenosides of mountain cultivated ginseng was better resolved than cultivated ginseng because the difference of structure or distribution of ginsenosides in the condition of fermentation.
인삼(
우리나라의 홍삼 제조 역사는 고려도경(1123년)에 생삼과 오늘날의 홍삼에 해당되는 熟蔘(찐삼)에 대해 문헌적 기록이 있는 것으로 보아 오래 전부터 홍삼이 제조된 것으로 여겨진다. "紅蔘"이란 문자가 처음 기록된 것은 「정조실록」 에서 찾아볼 수 있고, 중국 등에 삼을 수출할 때 부패를 방지하거나 장기 보존의 목적으로 이용하였던 것으로 추정된다.
인삼의 전분은 증숙 과정에서 micelles 구조가 파괴되고 전분입자의 결정성이 점차 상실되며, caramel화에 의해 적갈색을 나타내어 홍삼이란 이름으로 불린다. 이렇게 호화된 홍삼은 ginsenoside Rh2, ginsenoside Rg3 등 다양한 사포닌이 생성될 뿐만 아니라 내용 성분이 잘 우러나오고 복용 후 소화흡수도 잘되는 것으로 알려져 있다.2)
최근 들어 삼에 대한 포제 방법에 따라 효능이 달라질수 있음이 보고되면서 인삼의 새로운 가공방법이 많이 나타나고 있는데, 주로 열처리3), 산(acid)4), 효소처리5) 및 미생물을 이용한 발효처리6) 등에 의해 인삼의 맞춤형 제품들이 출시되고 있다. 특히 미생물 및 효소를 이용한 발효를 이용하여 특정 성분을 강화시킨 가공인삼이 최근 들어 기능성 식품으로 주목을 받고 있다7).
발효는 미생물의 생리활동에 의해 일어나는 화학변화로서 유기물이 산화, 환원 또는 분해에 의하여 인간생활에 유익한 다른 물질로 변화되는 현상을 말하며 발효유나 치츠, 김치, 된장 등의 발효식품은 각 지역의 토착 미생물이 식품원료에 자연 접종되어 생성된 것으로 지역 고유의 식문화를 형성하는데 크게 기여하여왔다. 또한 최근 발효식품의 생리활성 작용이 알려지면서 세계적으로 건강기능성 장수식품으로 인식되고 있다.
이에 저자들은 이미 많은 연구를 통해 암세포의 성장 및 전이억제 효과가 보고8-10)된 ginsenoside Rh2, ginsenoside Rg3를 대량 함유한 삼 가공제품을 개발하기 위한 선행연구로, 인삼과 산양삼의 ginsenoside 함량이 열처리와 발효과정에 의해 어떠한 변화를 나타내며 또한 차이가 있는가를 알아보고자 HPLC(High Performance Liquid Chromatography, 이하 HPLC)를 이용하여 각각의 뿌리에 함유된 10여 종의 ginsenosides를 측정한 후 성분의 변화를 추적하여 분석한 결과, 유의한 결론을 얻었기에 보고하는 바이다.
1) 산양삼 및 인삼
① 산양삼
본 실험에 사용한 산양삼은 충남 서천시에 있는 천방농산에서 재배된 수령 8-9 년생을 36뿌리 무작위로선정하여 사용하였다.
② 인삼
본 실험에 사용한 인삼은 4년 근과 6년 근으로 강화농협에서 구입하여 각각 36 뿌리씩 무작위로 추출하여 실험에 사용하였다.
1) 산양삼 및 인삼의 열처리 및 발효과정에 따른 성분분석
① 실험기기 및 시약
Rotary vacuum evaporator는 Eyela (Tokyo Co.)의 농축기를 사용하였고, 분석용 HPLC로는 Varian 9012 Solvent Delivery System, 검출기는 Varian Variable Wavelength 9050 UV-VIS detector, 그리고 Autos-ampler는 Varian 9300을 사용하였다. AcCN, MeOH 등의 분석시약은 모두 HPLC용 시약을 사용하여 측정하였으며, 추출 및 분획용 용매는 모두 특급시약을 사용하여 실험하였다.
② 추출 및 분석 시료
열처리 및 발효 등 각각의 단계를 홍삼화, 건조, 발효 1일째, 2, 4, 7일로 나누어 각각의 처치에 따라 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, Rg1, Rg3, Rh1 그리고 Rh2의 10종 성분이 어떠한 변화를 나타내는지를 관찰하고자 하였다. 먼저 각각의 공정에서 확보된 삼류에 80% MeOH 100-500 ㎖를 가하여 수욕 상에서 3시간씩 3회 환류 추출하고 여과 후 농축하여 80% MeOH 추출물을 얻었다. 얻어진 80% MeOH 추출물을 증류수에 현탁시켜
③ HPLC의 분석조건
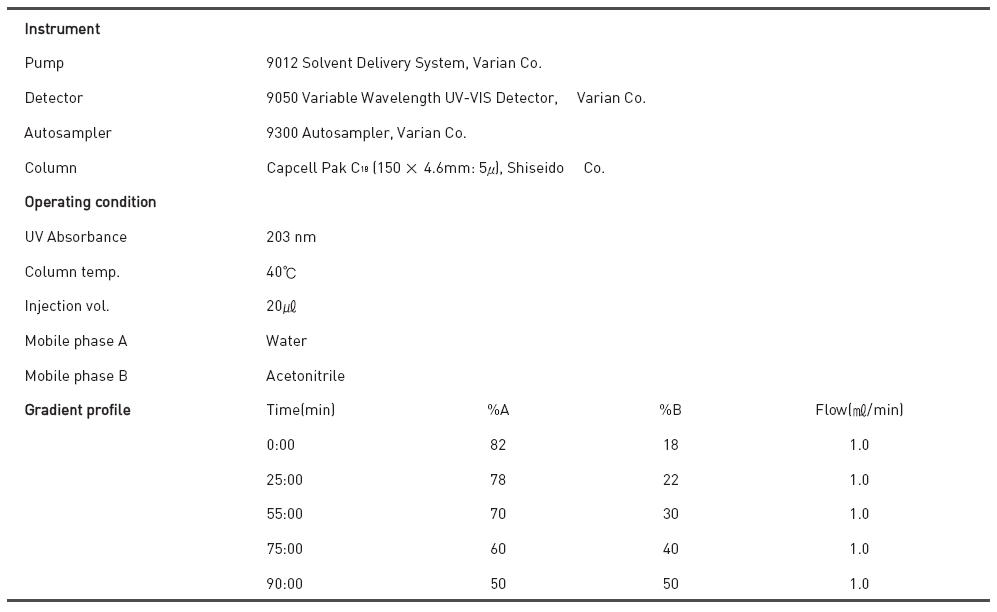
HPLC 조건은 column은 Capcell Pak C18(150 × 4.6mm, 5㎛, Shiseido Co.)이며 유속은 1 ㎖/min, column 온도는 40℃, 시료 주입량은 20 ㎕로 UV 203 nm에서 실험하였다. 분석시의 이동상 조건은 Table 1.에 나타내었다.
④ 표준액 및 검액의 제조
비극성 사포닌류의 패턴 분석을 위한 표준액은 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, Rg1, Rg3, Rh1 그리고 Rh2의 10종 표준품을 각각 100 ㎍/㎖씩 취한 후 MeOH 1 ㎖에 녹인 후 0.45 ㎛ membrane filter로 여과하여 사용하였고, 검액은 얻어진 시료외에
⑤ 검량선의 작성
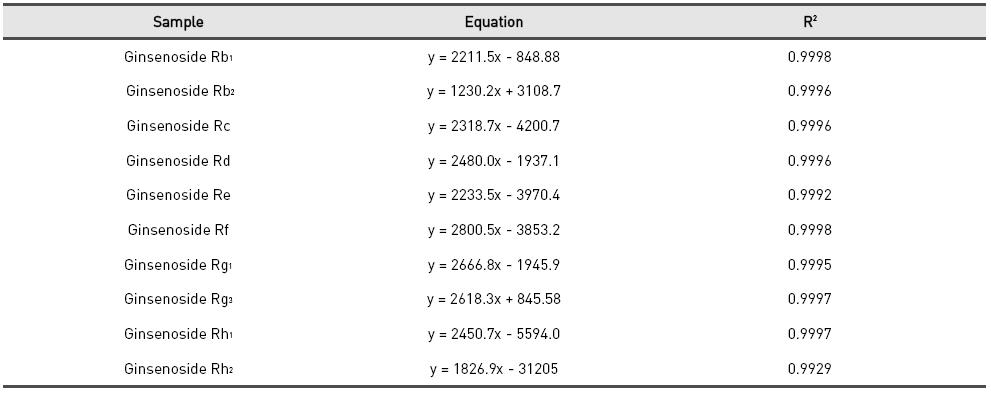
표준품 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, Rg1, Rg3, Rh1 그리고 Rh2의 10종 표준품을 각각 500, 400, 300, 200, 100, 50 ㎍/㎖ 농도로 희석하여 분석하여 얻은 각각의 ginsenoside에 대한 피크 면적비 (X축)와 표준품 농도 (Y축)에 대한 검량선을 각각 작성하였다. 그 결과 각 ginsenoside에 대한 검량선의 함수와 상관계수 R2값은 Table 2.에 제시하였다.
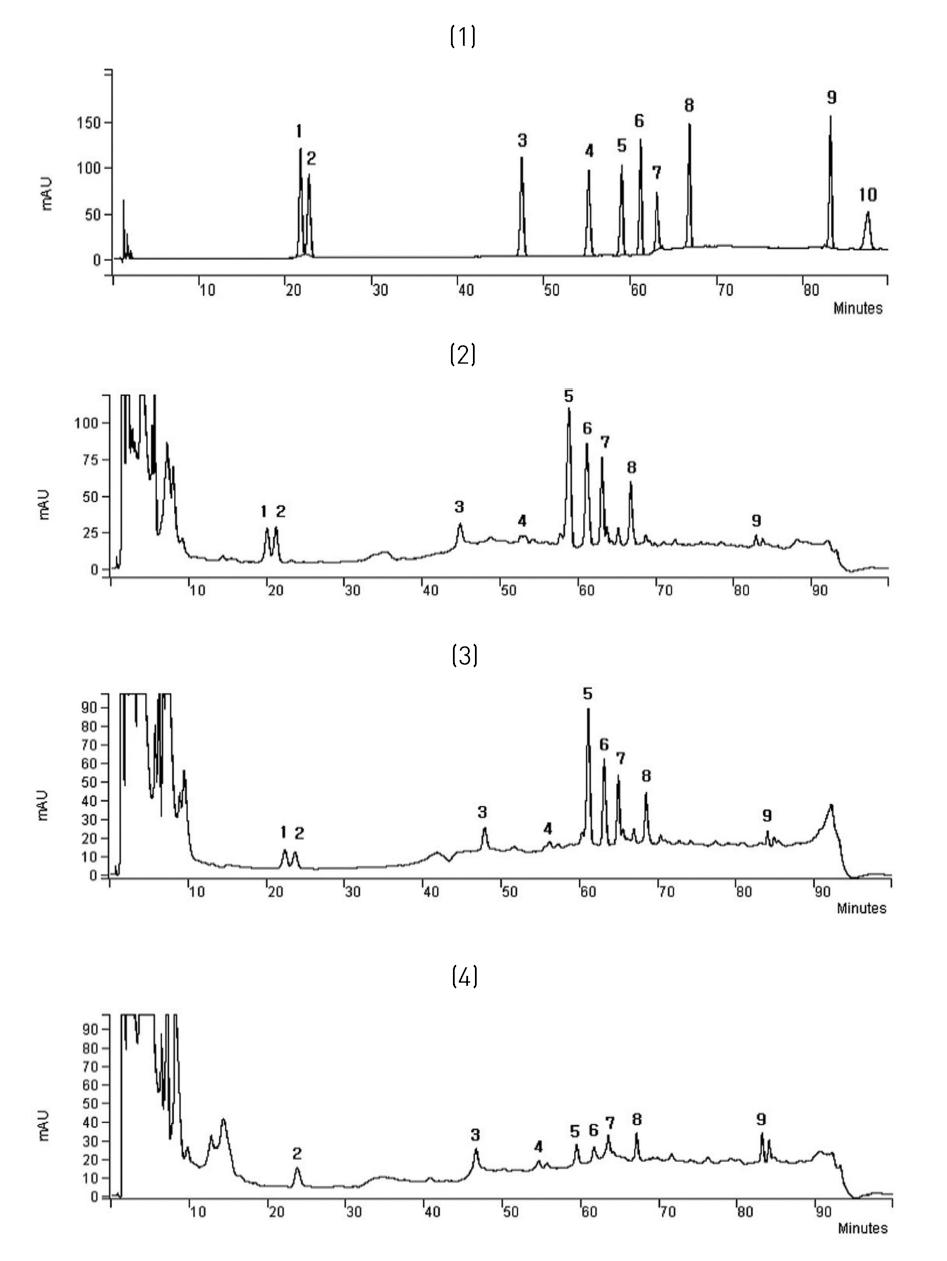
⑥ 10종 표준품의 HPLC chromatogram과 분석시료의 chromatogram 양상
상기에서 제시한 방법에 따라 HPLC로 분석하여 표준품 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, Rg1, Rg3, Rh1 그리고 Rh2와 수종의 삼류에 대한 각각의 chromatogram을 얻은 후 정량 평가하였다.
⑦ 홍삼화 처리과정
인삼 및 산양삼이 홍삼으로 되는 과정에서 나타나는 ginsenoside의 함량 변화를 관찰하기 위하여 모든 시료를 흐르는 물에 깨끗이 세척한 후 고압증숙기 안에 가지런히 세운 후 95-100℃에서 15시간 동안 증숙하였다. 증숙이 끝난 시료들은 다시 건조를 위해 95-100℃에서 72시간 동안 각각의 시료들이 타지 않도록 주의를 기울이면서 건조시켜 실험에 사용하였다.
⑧ 발효과정
건조한 각각의 시료들을 유효 성분의 용출이 용이하도록 이축압축 성형기를 이용하여 각각의 입자 크기가 평균 5 ㎛가 되게 초미세 분말을 만들었다. 그리고 인삼의 발효에 유용하다고 보고11)된 유산균들로 혼합된 (주) cellbiotec (한국)의 ATP 혼합유산균 생균분말(
2) 통계처리
각각의 시료에서 ginsenoside Rg1, Re, Rf, 등 HPLC에서 전방에 위치하고 있는 분자량이 큰 다당체 함유 성분이 분자량이 작은 ginsenoside Rc, Rb2, Rd, Rg3 및 ginsenoside Rh2 성분으로 어떠한 조건으로 이환되는가를 보고자 하는 것이 연구의 목적이므로 통계처리는 시행하지 않았다.
1. 홍삼화 과정에서 각 시료의 ginsenosides 함량 변화
각 종 삼류에 증숙 과정을 통한 열 자극을 준 결과 ginsenoside의 함량에 변화가 나타남을 알 수 있었다(Fig. 3-11).
4년근 삼에서는 홍삼화 과정으로 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, Rg1 그리고 Rh1이 증가하였고, 특히 Re와 Rf는 거의 2배 상승하였으며 Rg3는 큰 변화를 나타내지 않았다.
6년근 삼에서는 홍삼화 과정으로 ginsenoside Rb1, Rb2, Re, 그리고 Rg1 이 소폭 증가하였고, Rc, Rd, Rf, Rg3 그리고 Rh1은 큰 변화를 나타내지 않았다.
산양삼은 홍삼화 과정으로 ginsenoside Re, Rf, Rg1, Rg3 그리고 Rh1이 증가하였고 ginsenoside Rb1, Rb2, Rc는 감소하였다. 그리고 ginsenoside Rd는 큰 변화를 나타내지 않았다.
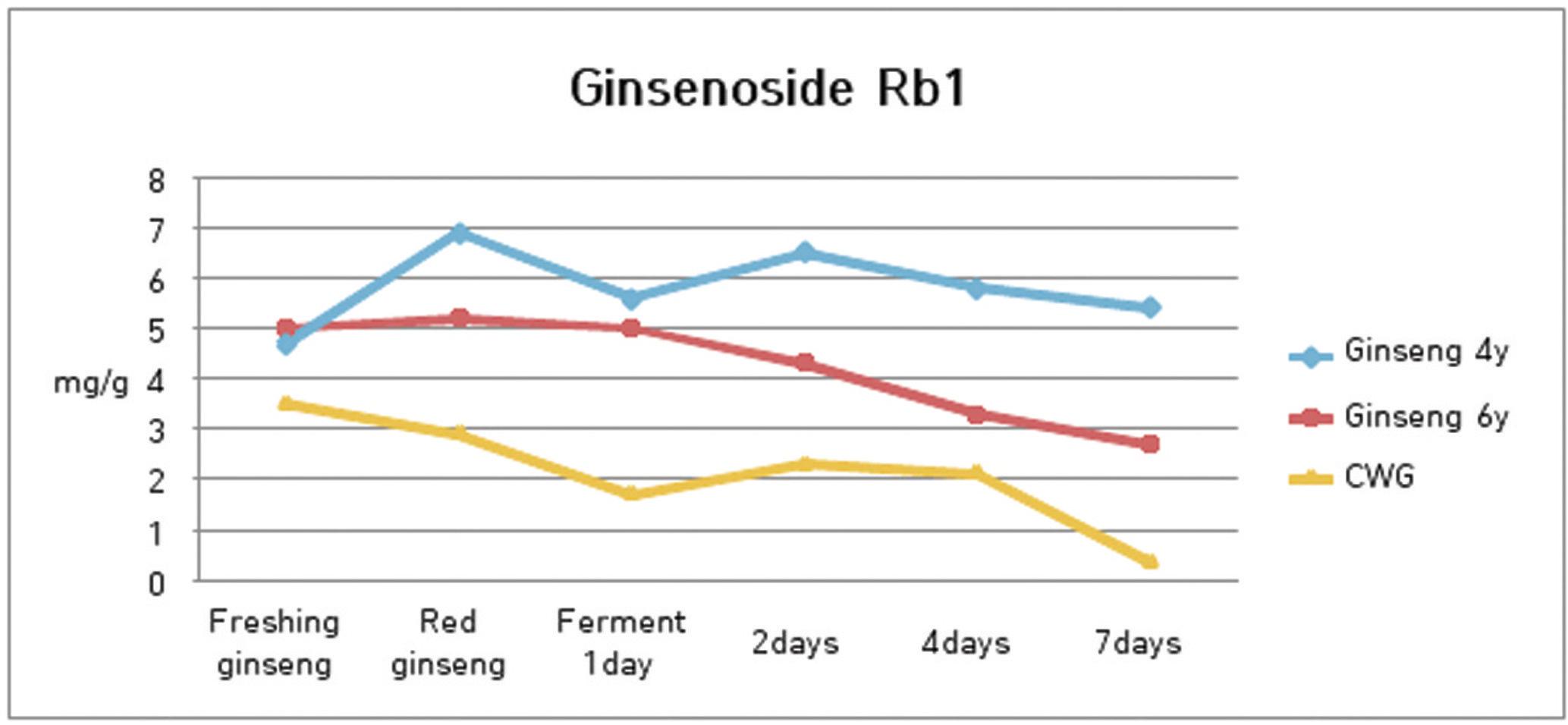
2. 발효과정에서 ginsenoside Rb1의 함량 변화
발효과정에서 수종의 삼류에 대하여 ginsenoside Rb1의 함량 분석을 실시한 결과 4년근 인삼은 6.86 mg/g에서 발효 1일째 5.64 mg/g으로 줄다가 2일째는 6.54 mg/g으로 증가하였고, 4일에는 5.78 mg/g, 7일째에는 5.44 mg/g을 나타내어 소폭 감소하는 경향을 나타내었다.
6년근 인삼은 5.15 mg/g에서 발효 1일째 5.04 mg/g으로, 2일째는 4.27 mg/g, 4일에는 3.27 mg/g, 그리고 7일째에는 2.69 mg/g을 나타내어 지속적으로 감소하는 경향을 나타내었다.
산양삼은 2.85 mg/g에서 발효 1일째 1.69 mg/g으로, 2일째는 2.31 mg/g, 4일에는 2.09 mg/g, 그리고 7일째에는 0.35 mg/g을 나타내었는데 지속적으로 감소하는 경향을 나타내다가 발효 7일째에 급격한 감소를 나타내었다.(Fig. 3)
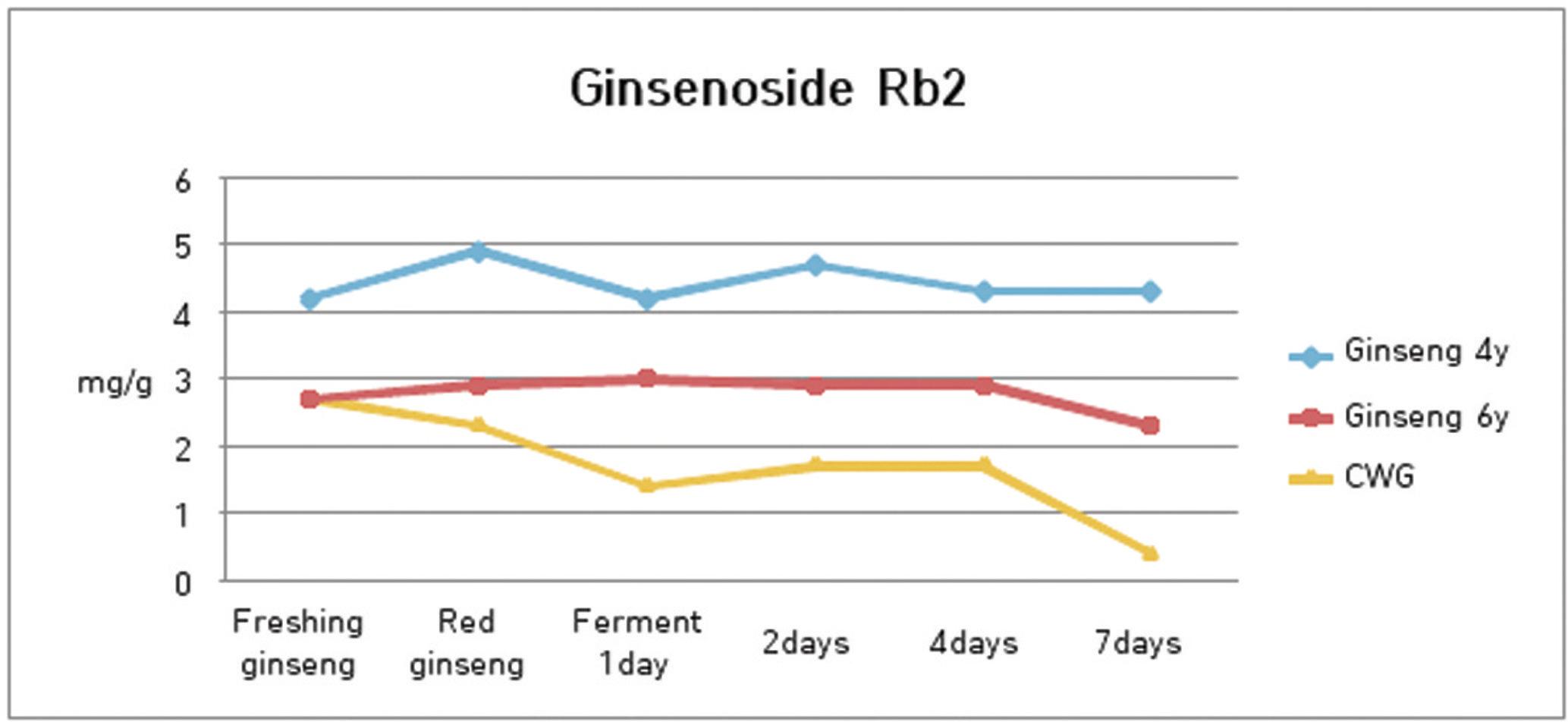
3. 발효과정에서 ginsenoside Rb2의 함량 변화
발효과정에서 수종의 삼류에 대하여 ginsenoside Rb2의 함량 분석을 실시한 결과 4년근 인삼은 4.86 mg/g에서 발효 1일째 4.17 mg/g으로 줄다가 2일째는 4.71 mg/g으로 소폭 증가하였고, 4일에는 4.34 mg/g, 7일째에는 4.27 mg/g을 나타내어 소폭 감소하는 경향을 나타내었으나 그 변화는 크지 않았다.
6년근 인삼은 2.93 mg/g에서 발효 1일째 2.96 mg/g으로, 2일째는 2.93 mg/g, 4일에는 2.89 mg/g, 그리고 7일째에는 2.31 mg/g을 나타내어 변화가 거의 나타나지 않다가 발효 7일째에 감소함을 알 수 있었다.
산양삼은 2.27 mg/g에서 발효 1일째 1.40 mg/g으로, 2일째는 1.79 mg/g, 4일에는 1.69 mg/g, 그리고 7일째에는 0.40 mg/g을 나타내었는데, 지속적으로 감소하는 경향을 나타내다가 발효 7일째에 급격한 감소를 나타내었다. (Fig. 4)
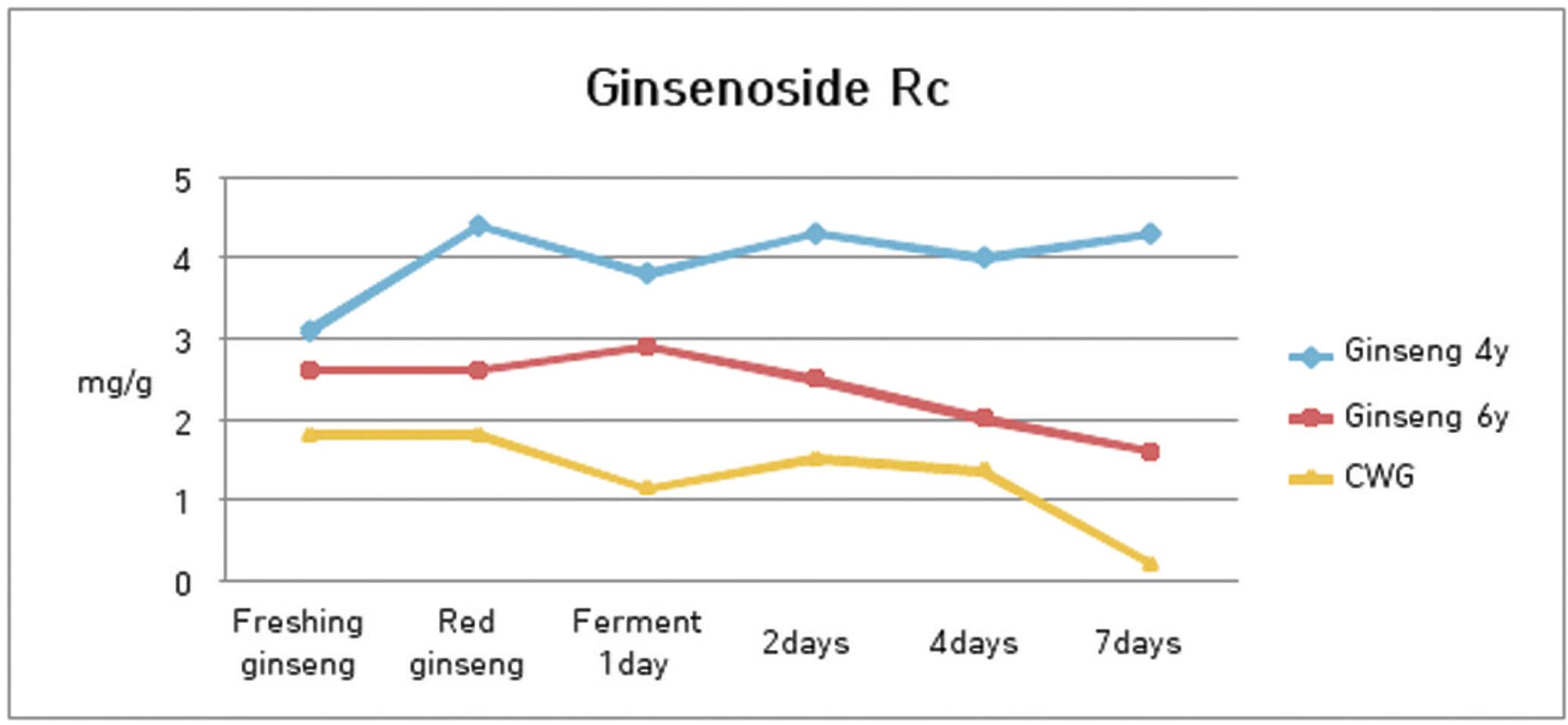
4. 발효과정에서 ginsenoside Rc의 함량 변화
발효과정에서 수종의 삼류에 대하여 ginsenoside Rc의 함량 분석을 실시한 결과 4년근 인삼은 4.42 mg/g에서 발효 1일째 3.82 mg/g으로 줄다가 2일째는 4.30 mg/g으로 소폭 증가하였고, 4일에는 4.00 mg/g, 7일째에는 3.72 mg/g을 나타내어 발효 과정이 진행될수록 소폭 감소하는 경향을 나타내었으나 그 변화는 크지 않았다.
6년근 인삼은 2.61 mg/g에서 발효 1일째 2.87 mg/g으로 소폭 증가하였다가, 2일째는 2.49 mg/g, 4일에는 2.00 mg/g, 그리고 7일째에는 1.63 mg/g을 나타내어 발효가 진행될수록 점차 감소함을 알 수 있었다.
산양삼은 1.78 mg/g에서 발효 1일째 1.14 mg/g으로, 2일째는 1.54 mg/g, 4일에는 1.35 mg/g, 그리고 7일째에는 0.22 mg/g을 나타내었는데, 발효 7일째에 급격한 감소를 나타내었다.(Fig. 5)
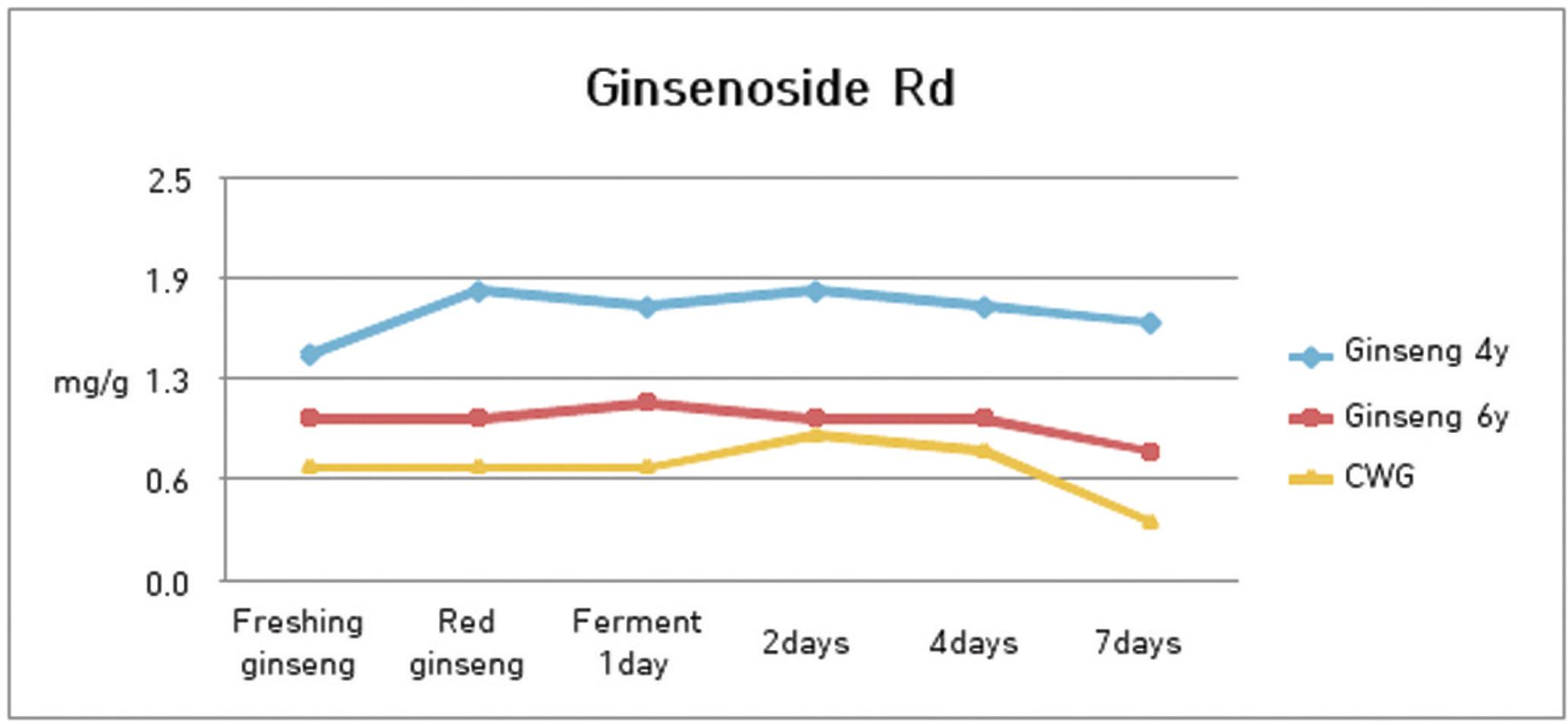
5. 발효과정에서 ginsenoside Rd의 함량 변화
발효과정에서 수종의 삼류에 대하여 ginsenoside Rd의 함량 분석을 실시한 결과 4년근 인삼은 1.79 mg/g에서 발효 1일째 1.69 mg/g으로, 2일째는 1.77 mg/g, 4일에는 1.69 mg/g, 7일째에는 1.55 mg/g을 나타내어 그 변화는 크지 않았다.
6년근 인삼은 0.96 mg/g에서 발효 1일째 1.11 mg/g으로, 2일째는 1.01 mg/g, 4일에는 1.06 mg/g, 그리고 7일째에는 0.77 mg/g을 나타내어 발효과정에서 거의 변화하지 않다가 발효 7일째에 감소함을 알 수 있었다.
산양삼은 0.73 mg/g에서 발효 1일째 0.71 mg/g으로, 2일째는 0.90 mg/g, 4일에는 0.86 mg/g, 그리고 7일째에는 0.36 mg/g을 나타내었는데, 초기에는 증가하는 경향을 나타내다가 발효 7일째에 급격한 감소를 나타내었다.(Fig. 6)
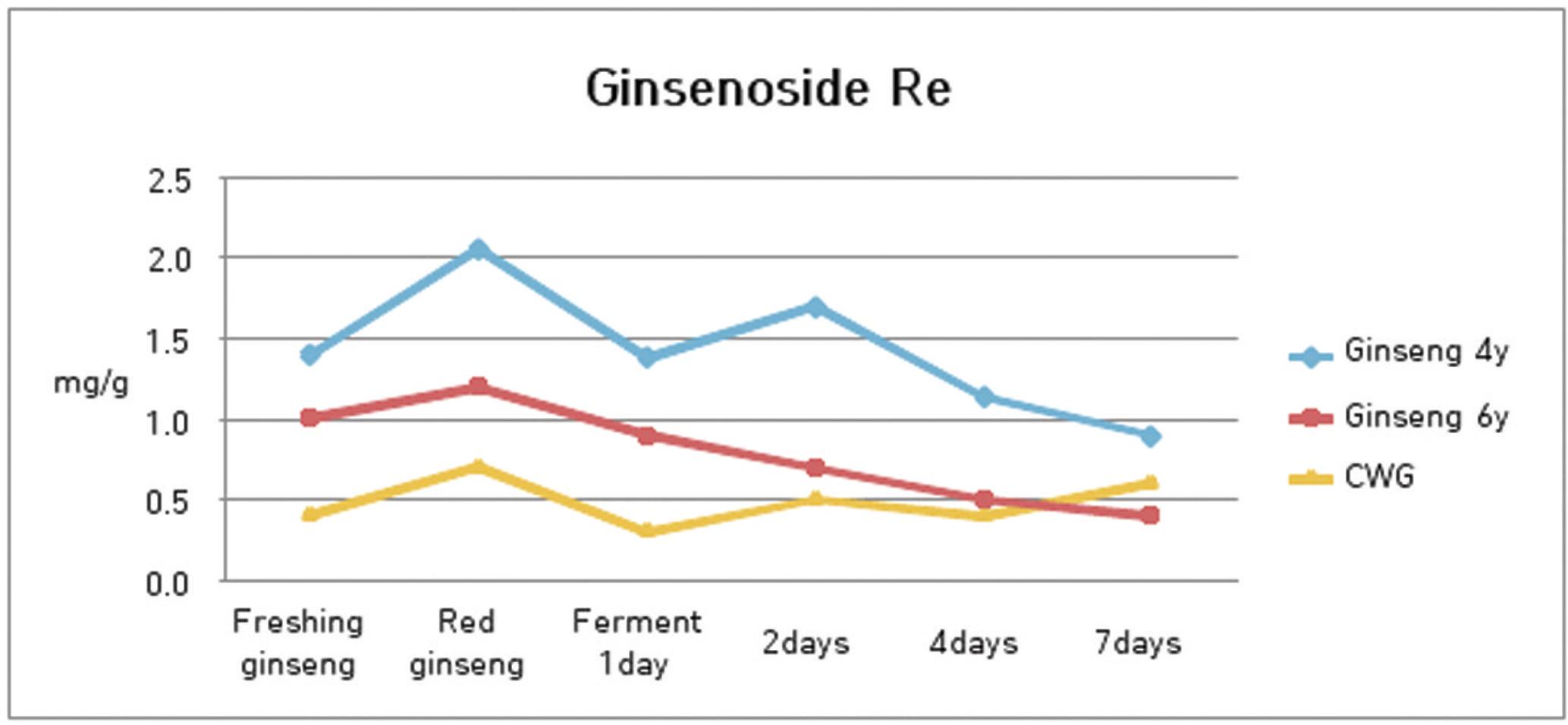
6. 발효과정에서 ginsenoside Re의 함량 변화
발효과정에서 수종의 삼류에 대하여 ginsenoside Re의 함량 분석을 실시한 결과 4년근 인삼은 2.06 mg/g에서 발효 1일째 1.38 mg/g으로 줄다가 2일째는 1.67 mg/g으로 소폭 증가하였고, 4일에는 1.14 mg/g, 7일째에는 0.88 mg/g을 나타내어 발효과정이 진행될수록 점차 감소하는 경향을 나타내었다.
6년근 인삼 역시 1.19 mg/g에서 발효 1일째 0.93 mg/g으로, 2일째는 0.67 mg/g, 4일에는 0.53 mg/g, 그리고 7일째에는 0.42 mg/g을 나타내어 발효과정이 진행될수록 함량이 감소함을 알 수 있었다.
산양삼은 0.66 mg/g에서 발효 1일째 0.27 mg/g으로, 2일째는 0.48 mg/g, 4일에는 0.41 mg/g, 그리고 7일째에는 0.59 mg/g을 나타내어 초기에는 감소하는 경향을 나타내다가 점차 증가하여 전체적으로는 그 변화가 크지 않았다.(Fig. 7)
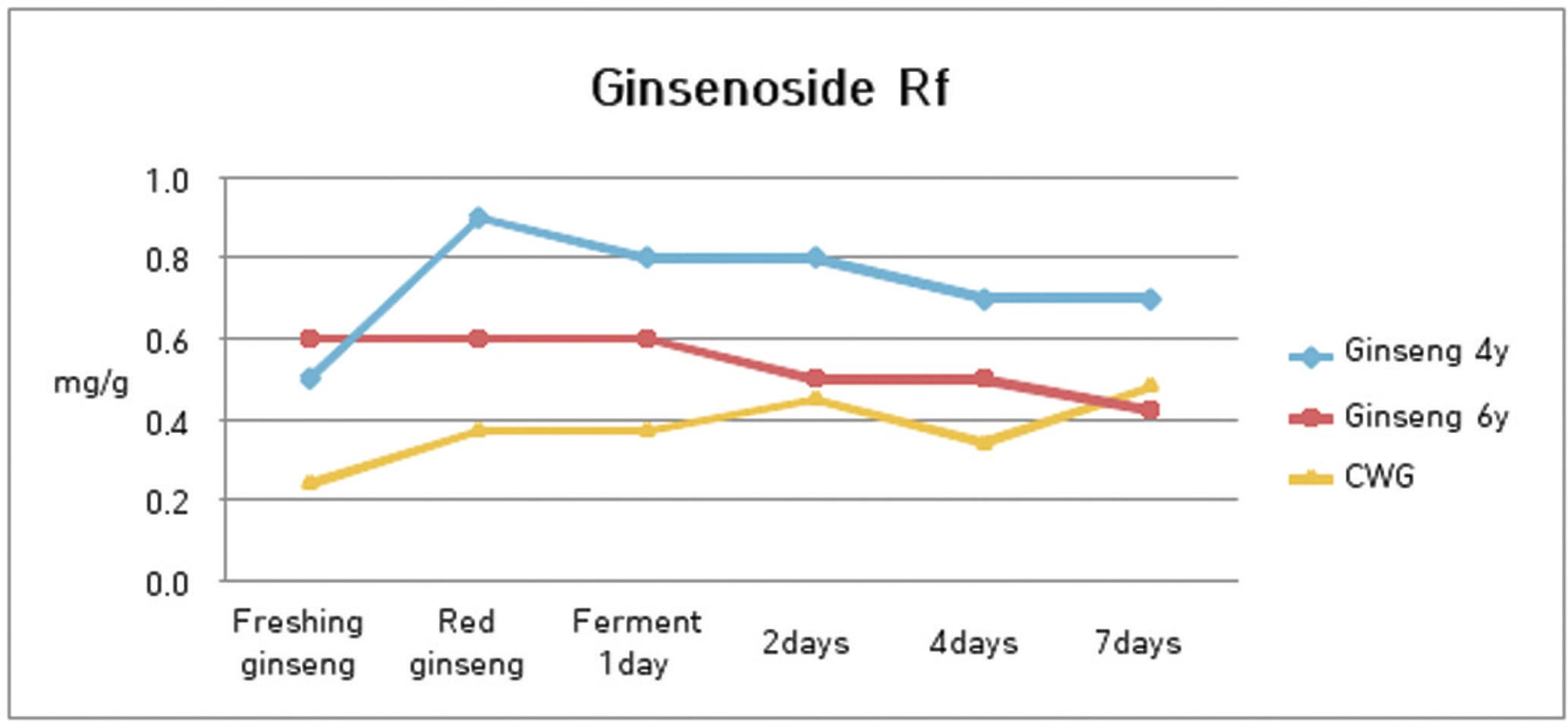
7. 발효과정에서 ginsenoside Rf의 함량 변화
발효과정에서 수종의 삼류에 대하여 ginsenoside Rf의 함량 분석을 실시한 결과 4년근 인삼은 0.48 ㎎/g에서 발효 1일째 0.87 ㎎/g으로 늘다가 2일째는 0.79 ㎎/g으로 소폭 감소하였고, 4일과 7일째에는 0.72 ㎎/g을 나타내어 소폭 증가하였다.
6년근 인삼은 0.64 ㎎/g에서 발효 1일째 0.64 ㎎/g, 2일째는 0.61 ㎎/g, 4일에는 0.52 ㎎/g, 그리고 7일째에는 0.47 ㎎/g을 나타내어 변화가 거의 나타나지 않음을 알 수 있었다.
산양삼은 0.37 mg/g에서 발효 1일째 0.37 mg/g, 2일째는 0.45 mg/g, 4일에는 0.34 mg/g, 그리고 7일째에는 0.48 mg/g을 나타내어 역시 그 변화가 크지 않았다.(Fig. 8)
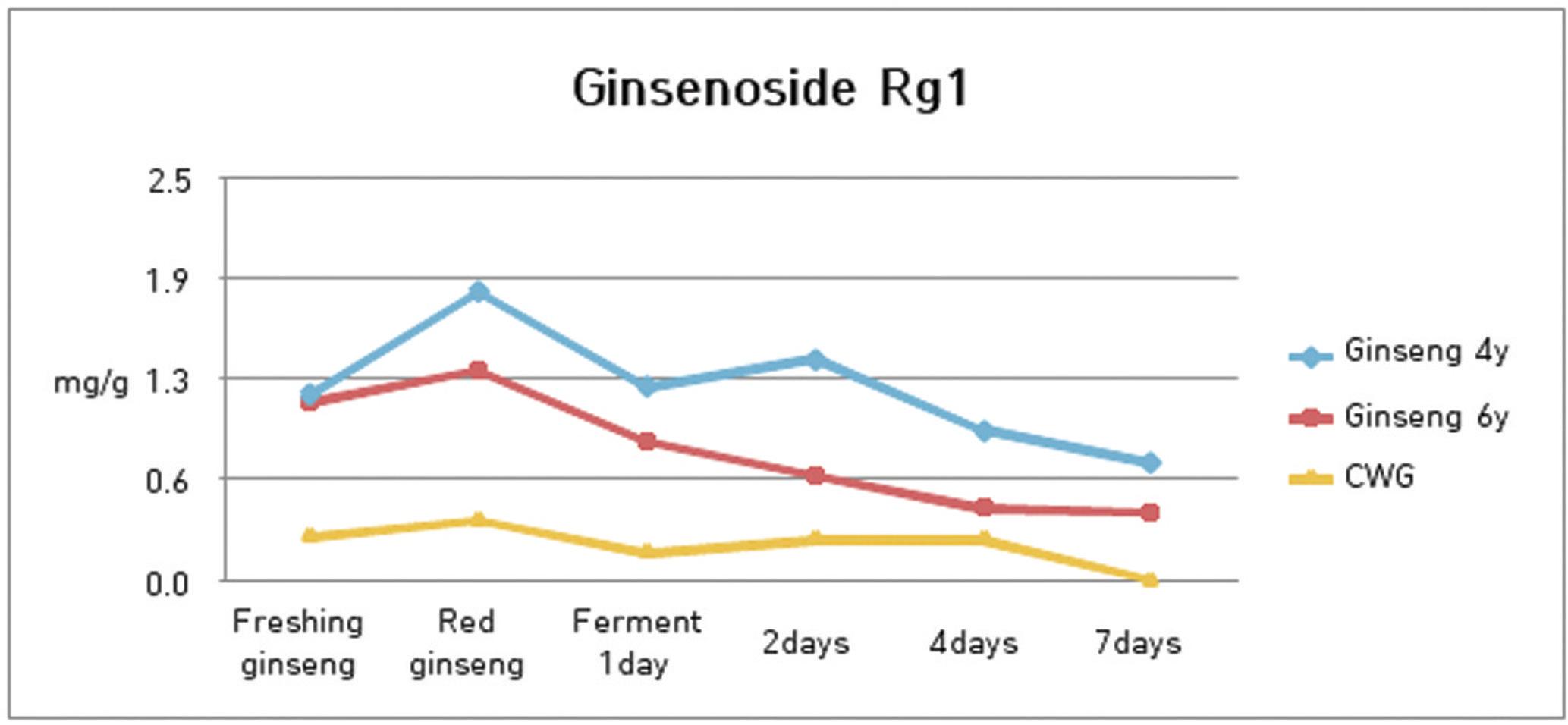
8. 발효과정에서 ginsenoside Rg1의 함량 분석
수종의 삼류에 대하여 ginsenoside Rg1의 함량 분석을 실시한 결과 4년근 인삼은 1.78 ㎎/g에서 발효 1일째 1.20 ㎎/g으로 줄다가 2일째는 1.37 ㎎/g으로 소폭 증가하였고, 4일에는 0.93 ㎎/g, 7일째에는 0.73 ㎎/g을 나타내어 전반적으로 감소하는 경향을 나타내었다.
6년근 인삼은 1.29 ㎎/g에서 발효 1일째 0.86 ㎎/g으로, 2일째는 0.64 ㎎/g, 4일에는 0.47 ㎎/g, 그리고 7일째에는 0.41 ㎎/g을 나타내어 발효 과정에 의해 지속적으로 감소함을 알 수 있었다.
산양삼은 0.38 mg/g에서 발효 1일째 0.17 mg/g으로, 2일째는 0.26 mg/g, 4일에는 0.25 mg/g, 그리고 7일째에는 0.00 mg/g을 나타내었는데, 발효 7일째에 급격한 감소를 나타내어 분해 과정에 의해 완전히 분해됨을 알 수 있었다.(Fig. 9)
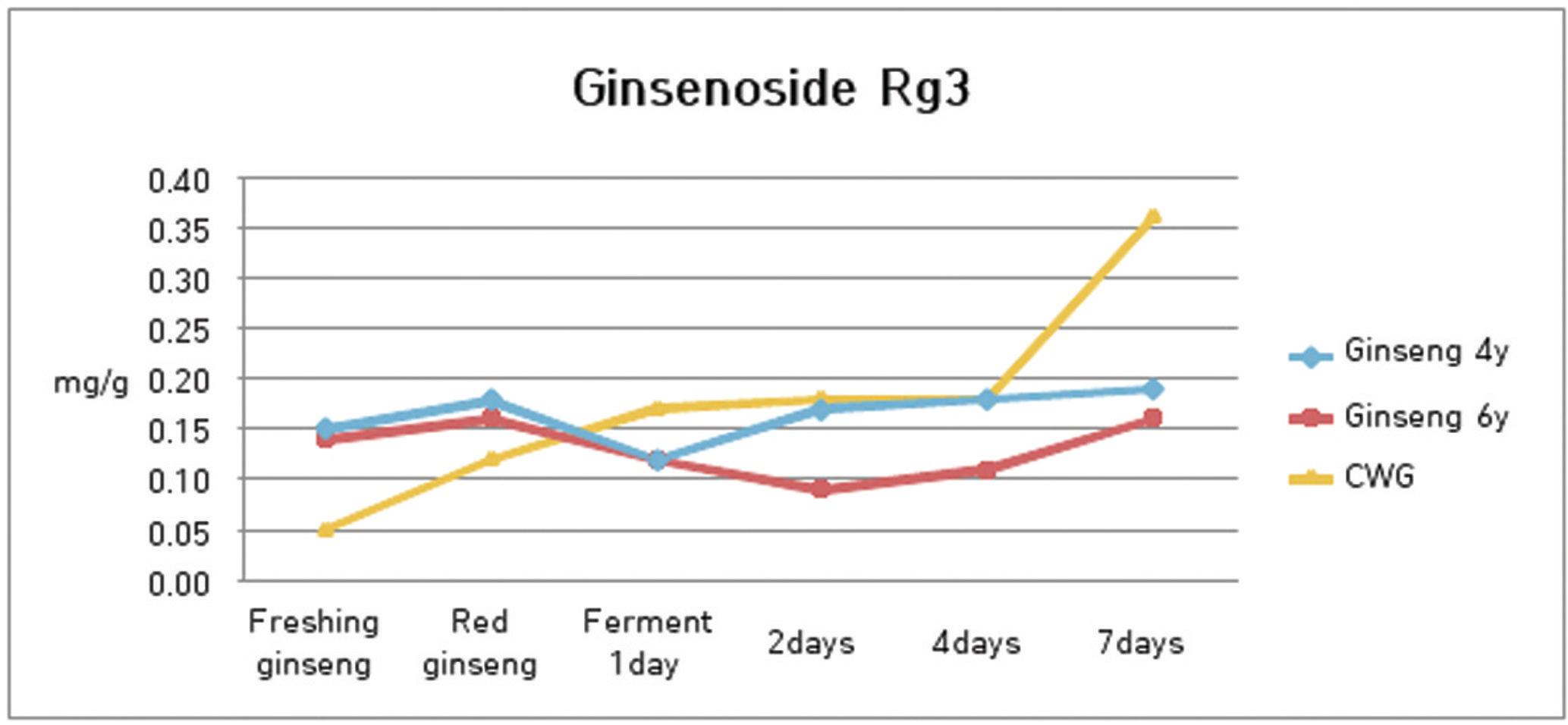
9. 발효과정에서 ginsenoside Rg3의 함량 분석
수종의 삼류에 대하여 ginsenoside Rg3의 함량 분석을 실시한 결과 4년근 인삼은 0.17 ㎎/g에서 발효 1일째 0.13 ㎎/g으로 줄다가 2일째는 0.15 ㎎/g, 4일에는 0.18㎎/g, 그리고 7일째에는 0.19 ㎎/g을 나타내어 그 변화는크지 않았다.
6년근 인삼은 0.16 ㎎/g에서 발효 1일째 0.12 ㎎/g으로, 2일째는 0.09 ㎎/g, 4일에는 0.11 ㎎/g, 그리고 7일째에는 0.16 ㎎/g을 나타내어 감소와 증가의 과정을 나타내었으나 함량에는 큰 영향을 미치지 않았다.
산양삼은 0.12 mg/g에서 발효 1일째 0.16 mg/g으로, 2일째는 0.18 mg/g, 4일에는 0.16 mg/g, 그리고 7일째에는 0.31 mg/g을 나타내어, 발효 7일째에 급격한 함량의 증가를 나타내었다.(Fig. 10)
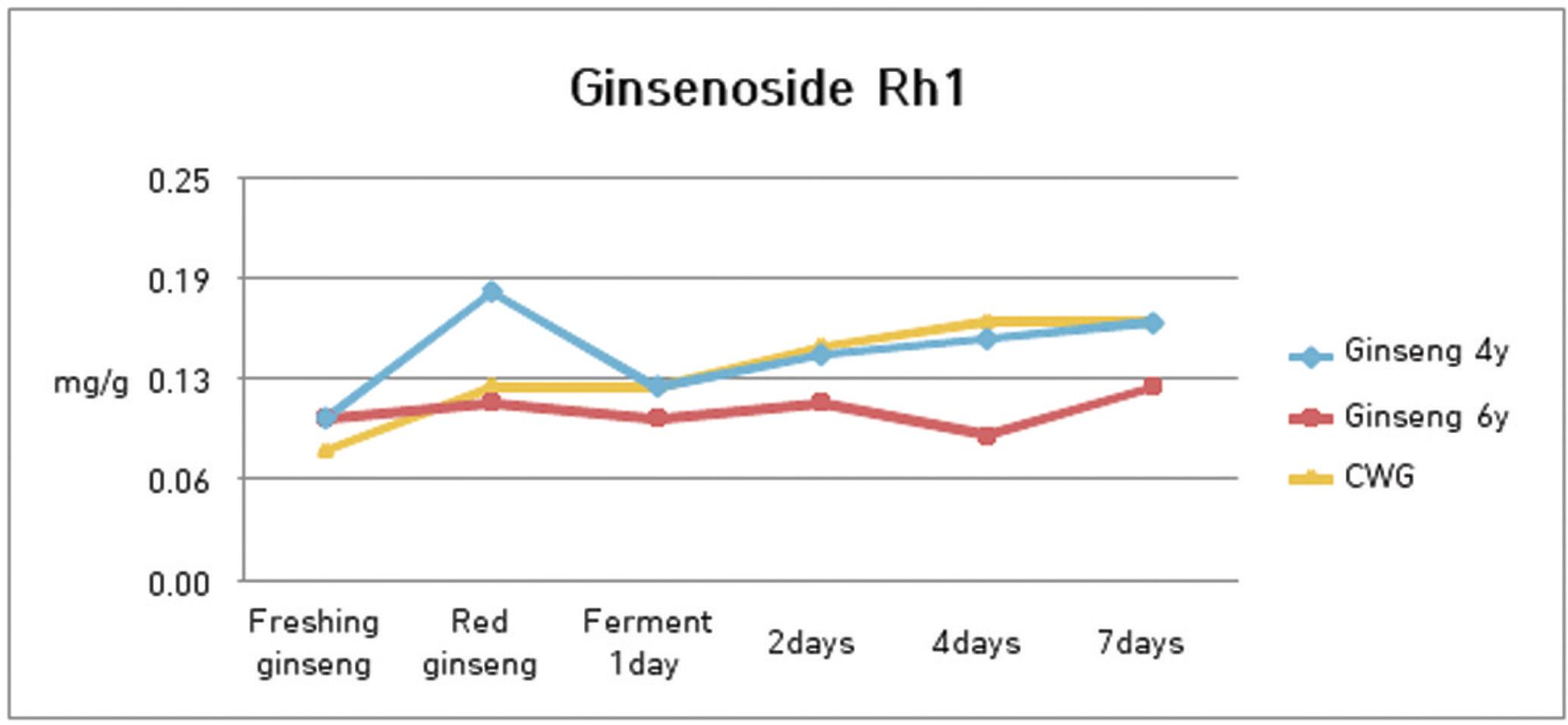
10. 발효과정에서 ginsenoside Rh1의 함량 분석
수종의 삼류에 대하여 ginsenoside Rh1의 함량 분석을 실시한 결과 4년근 인삼은 0.18 ㎎/g에서 발효 1일째 0.12 ㎎/g으로 줄다가 2일째는 0.14 ㎎/g, 4일에는 0.15 ㎎/g, 그리고 7일째에는 0.16 ㎎/g을 나타내어 큰 변화를 나타내지 않았다.
6년근 인삼은 0.11 ㎎/g에서 발효 1일째 0.10 ㎎/g으로, 2일째는 0.12 ㎎/g, 4일에는 0.09 ㎎/g, 그리고 7일째에는 0.12 ㎎/g을 나타내어 변화가 거의 나타나지 않음을 알 수 있었다.
산양삼은 0.11 mg/g에서 발효 1일째 0.11 mg/g, 2일째는 0.14 mg/g, 4일에는 0.15 mg/g, 그리고 7일째에는 0.15 mg/g을 나타내어 약간 증가하는 양상을 보였으나 변화는 크지 않았다.(Fig. 11)
수종의 삼류에 대하여 ginsenoside Rh2의 함량 분석을 실시한 결과 모든 삼류에서 발견되지 않았고, 열처리 과정이나 발효과정에 의해서도 생성되지 않음을 알 수 있었다.
인삼은 파낙스(
인삼의 유효성분으로 알려져 있는 사포닌을 Shibata13)가 인삼에 함유된 배당체라는 뜻으로 ginsenoside라 명명한 이후 현재 약 30여종 이상이 밝혀져 있고, 최근에는 미량의 ginsenoside나 phenol계 화합물, polysaccharide등의 효능이나 기전 연구가 활발하게 진행되고 있다14).
사포닌은 크게 triterpenoid 사포닌과 steroid 사포닌으로 나눌 수 있는데 식물계의 사포닌은 대부분 oleanane 계이다. 일본의 Shibata와 Tanaka 등은 오랜 연구 끝에 인삼의 주요 사포닌은 천연에서 주종을 이루는 oleanane 계가 아닌 dammarane 계열의 triterpenoid 사포닌임을 밝힌 바 있다13). 대부분의 사포닌 즉, ginsenoside 는 구조적으로 triterpenoid dammarane 골격에 glucose, arabinose, xylose, rhamnose 등의 당이 결합되어 생성된 배당체로서 인삼의 가장 중요한 약리활성 성분임은 분명하다.
지금까지 고려인삼에서 추출 분리되어 밝혀진 ginsenoside의 종류를 보면 oleanane계 사포닌인 ginsenoside Ro 1종과 protopanaxadiol계 사포닌인 ginsenoside Ra1, Ra2, Ra3, Rb1, Rb2, Rb3, Rc, Rd, Rg3, 그리고 Rh2 등 총 10종이며, protopanaxatriol계 사포닌인 ginsenoside Re, Rf, 20-gluco-Rf, Rg1, Rg2와 Rh1 등이 있고15), 앞으로도 많은 ginsenoside가 분리 동정될 것으로 기대하고 있다.
인삼 함유 ginsenoside의 효능에 대해서도 많은 연구 보고가 이루어지고 있는데, ginsenoside Rb1은 위염 및 위궤양에 유효하고 항산화 작용이 있으며16), ginsenoside Rb2는 암독소 호르몬에 대한 길항 작용 및 종양혈관 신생 억제작용이 있고17), ginsenoside Rc는 장내 세균에 의한 대사산물을 이용한 항암제 개발 가능성이 보고18)된 바 있다. ginsenoside Rd는 신 기능부전의 치료효과19)와 신경계의 보호 작용20)이 보고된 바 있다. 이 외에도 산삼에서 소량으로 존재하는 것으로 알려진 비극성 사포닌인 ginsenoside-Rg3와 ginsenoside-Rh2의 항암작용 및 항전이작용8-10) 등이 보고되어 있다.
한의학의 생약 중에는 단순히 신선한 재료를 그대로 혹은 건조한 후 사용하는 것 외에도 어떤 가공 처리를 한 다음 사용하는 경우가 많다. 이러한 가공 조제를 修治라고 한다. 인삼 역시 이러한 가공조제 과정을 거쳐 만들어지는 것이 바로 홍삼이다. 홍삼은 수삼을 장기간 저장할 목적으로 증숙하여 인삼의 전분을 호화시켜 건조한 것을말하는데 이때 인삼의 전분이 열에 의해 caramel화 되어적갈색을 나타내므로 홍삼이라고 부른다.
홍삼이 수삼이나 백삼에서 가공 제조 과정을 거치는 동안 홍삼 특유의 미량 사포닌이 만들어지는데 이러한 ginsenoside 류는 홍삼의 제조과정에서 2차적으로 분해, 생성되어 생기는 것으로 알려져 있고15) 중국에서도 항암 효과가 있다고 알려진 ginsenoside Rg3를 대량 생산하는 방법을 개발하여 항암치료제로 사용하고 있다8-9).
최근 들어 삼에 대한 포제 방법에 따라 효능이 달라질 수 있음이 보고되면서 인삼의 새로운 가공방법이 많이 나타나고 있는데, 특히 미생물을 이용한 발효처리6) 등에 의해 인삼의 맞춤형 제품들이 출시되고 있다. 특히 미생물 및 효소를 이용한 발효를 이용하여 특정 성분을 강화시킨 가공인삼이 최근 들어 기능성 식품으로 주목을 받고 있다7).
발효란 미생물의 생리활동에 의해 일어나는 화학변화로서 유기물이 산화, 환원 또는 분해에 의하여 인간생활에 유익한 다른 물질로 변화되는 현상으로, 인류가 기원전 3,000년경부터 각 지역의 토착 미생물이 식품원료에 자연 접종되는 과정을 통해 섭취하면서 고유한 음식문화를 형성하여 왔고, 최근에는 건강기능성 장수식품으로 인식되고 있다21).
특히
본 연구는 인삼과 산양삼의 특이적인 ginsenoside 함량이 열 자극을 통한 홍삼화와
박 등11)의 연구를 통해 상기한 유산균들은 인삼의 발효물 제조 공정에 적합한 것으로 보고된 바 있다. 그리고 시간의 경과에 따른 성분 변화를 확인하기 위하여 접종 후, 배양 1, 2, 4, 7일째에 각각의 샘플을 채취한 후 HPLC를 이용하여 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, Rg1, Rg.3, Rh1 그리고 Rh2의 10종 ginsenoside 함량 분석을 시행하였다.
그 결과 홍삼화 과정에서는 이전의 선행 연구결과23)와 비교하였을 때 인삼 4년근과 6년근은 큰 차이를 나타내지 않았으나 산양삼은 상당한 차이를 나타내었다. 즉 이전의 연구에서는 홍삼화 과정을 통해 ginsenoside Rb1, Rb2, Rc, Rd, Rg3, 그리고 Rh1이 증가하였고, Re와 Rgv 이 감소하였으나 본 연구에서는 ginsenoside Rb1, Rb2 가 감소하였고, Rc, Rd는 거의 변화를 나타내지 않았으며, Re와 Rf, Rg1 Rg3, 그리고 Rh1이 증가하였다.
이러한 결과는 산양삼의 채취 시기나 열의 자극 정도에따라 반응의 차이를 나타내는 것이 아닐까 추정되었다.
발효과정을 통한 ginsenoside의 함량 변화를 관찰한 결과 인삼 4년근은 ginsenoside Re, Rg1이 감소하였고, Rb1, Rd, Rg3, 그리고 Rh1이 증가하였다.
인삼 6년근은 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, 그리고 Rg1이 감소하였고, Rg3가 소폭 증가하였다.
산양삼은 인삼 4년근이나 6년근에 비하여 상당히 큰 변화를 나타내었는데, ginsenoside Rb1, Rb2, Rc, Rd, 그리고 Rg1이 큰 폭으로 감소하였고, Re, Rf, 그리고 Rg3가 증가하였으며, 특히 ginsenoside Rg3는 처음 삼의 상태보다 약 7배 이상으로 상당히 많은 양이 증가하였다.
하지만 본 연구에서 목표로 하였던 암 전이 억제 효능을 지니고 있는 ginsenoside Rh2는 실험 과정에서 생성이 되지 않은 것으로 나타났다.
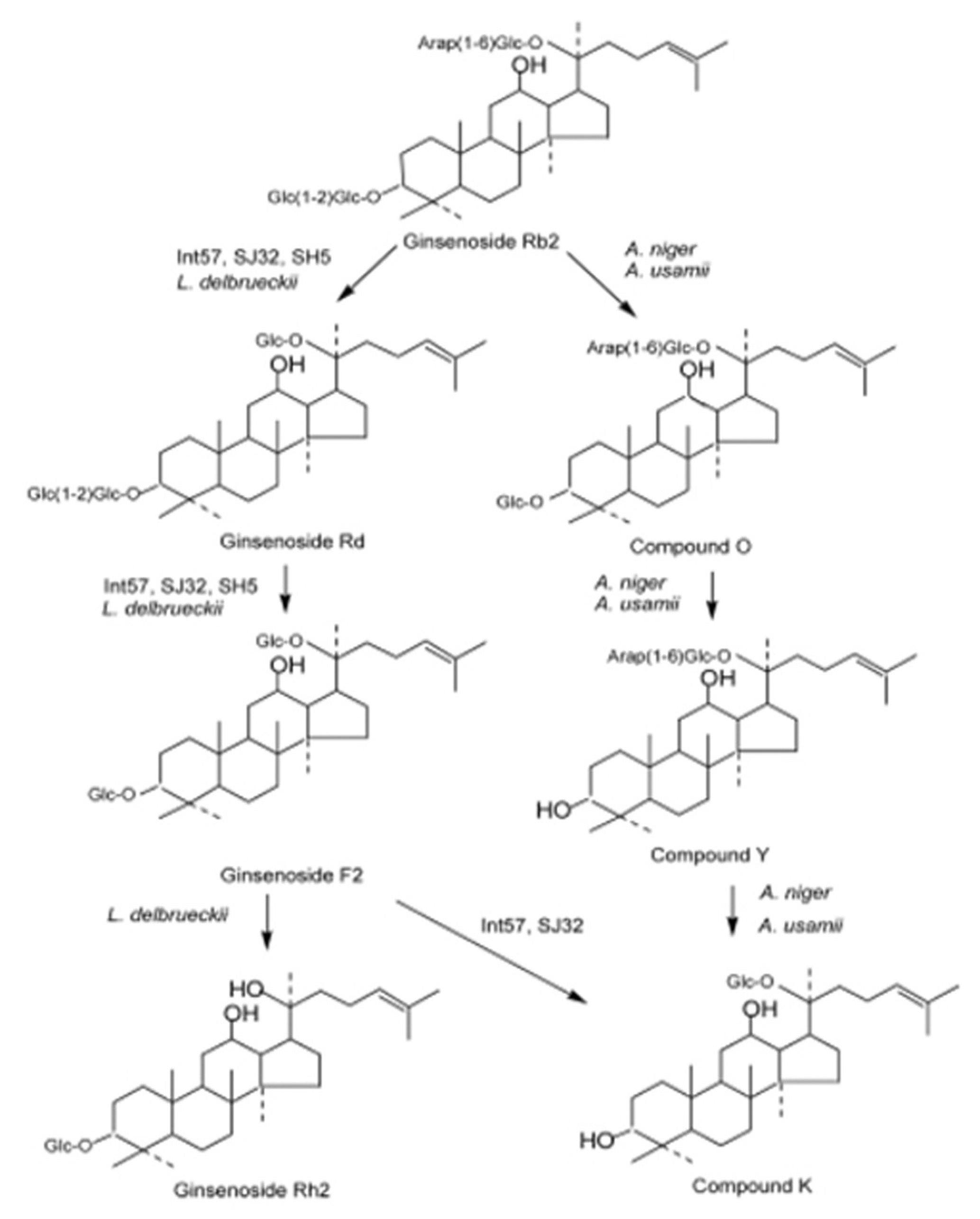
이러한 결과는 체내 미생물의 대사과정을 통해 ginsenosides가 분해되는 일련의 과정, 즉 다수의 당을 가진 구조에서 일정한 자극에 의해 당들이 떨어져 나가면서 분자구조가 작아지는 과정(Fig. 12)을 참조하여 볼 때, 인삼 4년근에 비해서는 6년근이, 6년근보다는 산양삼이 유산균에 의한 배당체의 분해가 더욱 활발히 일어남을 알 수 있었다. 또한 발효 노출 시간이 길어질수록 그 변화는 더욱 뚜렷하게 나타났다.
시료에 따라 특이적으로 차이를 나타낸 원인은 아마도 각각에 함유된 ginsenosides가 용출되어 유산균의 분해에 반응하는 접근성의 환경조건, 즉 각각의 삼에서 ginsenosides의 분포나 세포벽 혹은 세포막 등 용출되어 반응하는 구조의 차이에 의해 이러한 결과를 나타내지 않았을까 추정되었다. 또한 항암작용 및 항 전이작용이 우수 한 ginsenoside-Rg3와 ginsenoside-Rh2의 고용량 함유 제품은 인삼 4년근이나 6년근에 비해 산양삼을 원료로 하였을 때 성공 가능성이 높을 것으로 판단되었으나 본연구에서 목적으로 하였던 항암활성물질을 많이 함유한삼을 얻기에는 만족할만한 성과가 아니었다.
향후 더욱 더 많은 양의 ginsenoside Rg3와 ginsenoside Rh2를 생성할 수 있는 발효의 시간 등 환경설정이나 특정 성분에 반응하는 특정 균주 등 지속적인 연구를 진행해야 할 것으로 생각되었다.
인삼과 산양삼의 특이적인 ginsenoside 함량이 열 자극을 통한 홍삼화와
1. 홍삼화 열 자극에 대하여 이전의 연구와 비교하였을때 인삼 4년근과 6년근은 큰 차이를 나타내지 않았으나, 산양삼은 ginsenoside Rb1, Rb2가 감소하였고, Rc, Rd는 거의 변화를 나타내지 않았으며, Re와 Rf, Rg1 Rg3, 그리고 Rh1이 증가하였다.
2. 발효과정을 통한 ginsenoside의 함량 변화를 관찰한 결과, 인삼 4년근은 ginsenoside Re, Rg1이 감소하였고, Rb1, Rd, Rg3, 그리고 Rh1이 증가하였다.
3. 발효과정을 통한 ginsenoside의 함량 변화를 관찰한 결과, 인삼 6년근은 ginsenoside Rb1, Rb2, Rc, Rd, Re, Rf, 그리고 Rg1이 감소하였고, Rg3가 소폭 증가하였다.
4. 발효과정을 통한 ginsenoside의 함량 변화를 관찰한 결과, 산양삼은 ginsenoside Rb1, Rb2, Rc, Rd, 그리고 Rg1이 큰 폭으로 감소하였고, Re, Rf, 그리고 Rg3가 상당히 증가하였다.
5. 발효과정을 통한 ginsenoside의 함량 변화는 인삼 4년근에 비해서는 6년근이, 6년근보다는 산양삼이 더욱 활발히 일어났고, 발효 노출 시간이 길어질수록 그 변화는 더욱 뚜렷하게 나타났다.
이러한 연구 결과를 바탕으로 향후 보다 더 구체적인 환경 설정을 통하여 특정 성분을 고용량 함유하는 삼 제품이 개발되길 바라는 바이다.
[Table 1.] HPLC condition for analysis of ginsenosides
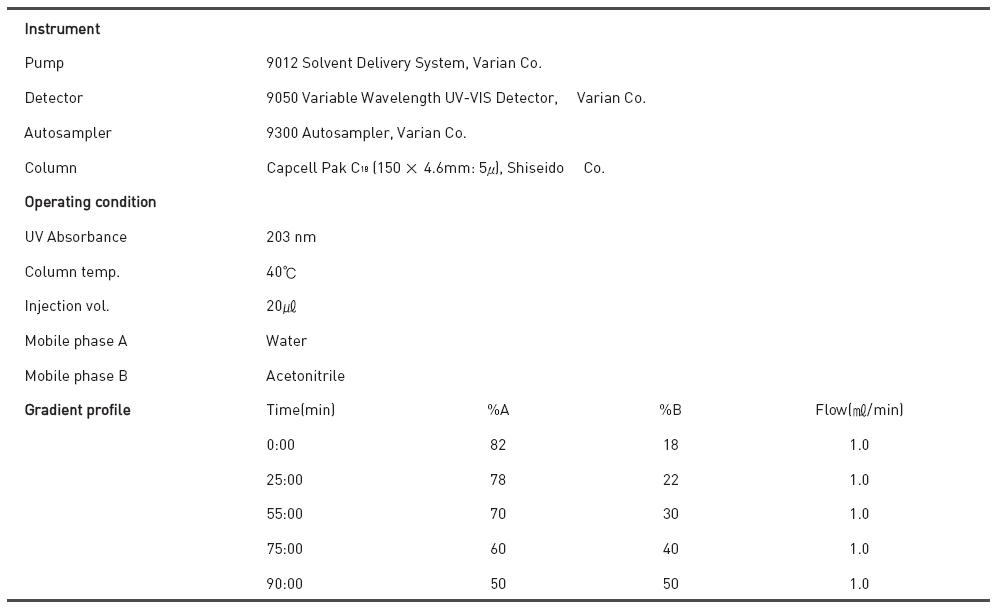
HPLC condition for analysis of ginsenosides
[Table 2.] Equation and R2 value of ginsenosides
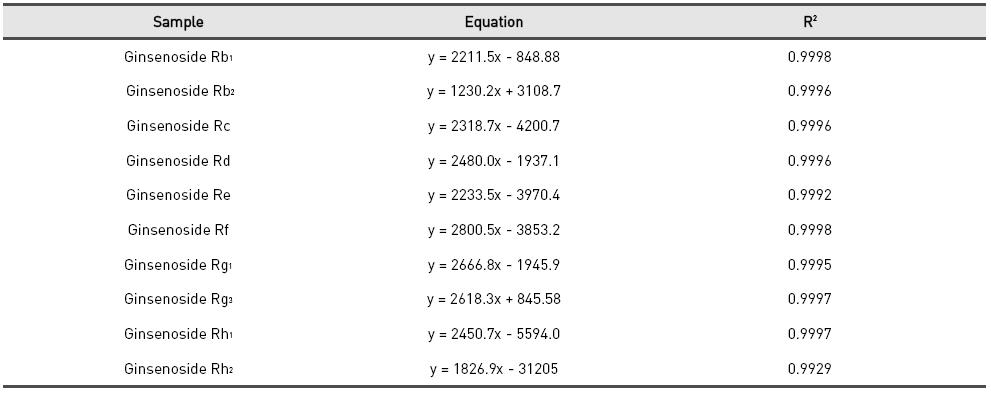
Equation and R2 value of ginsenosides