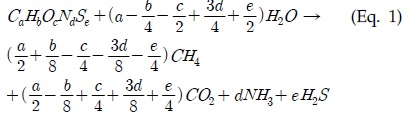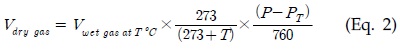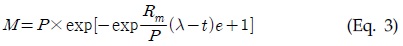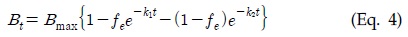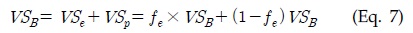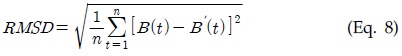Hydrothermal carbonization reaction is the thermo-chemical energy conversion technology for producing the solid fuel of high carbon density from organic wastes. The hydrothermal carbonization reaction is accompanied by the thermal hydrolysis reaction which converse particulate organic matters to soluble forms (hydro-thermal hydrolysate). Recently, hydrothermal carbonization is adopted as a pre-treatment technology to improve anaerobic digestion efficiency. This research was carried out to assess the effects of hydro-thermal reaction temperature on the methane potential and anaerobic biodegradability in the thermal hydrolysate of organic sludge generating from the wastewater treatment plant of poultry slaughterhouse .
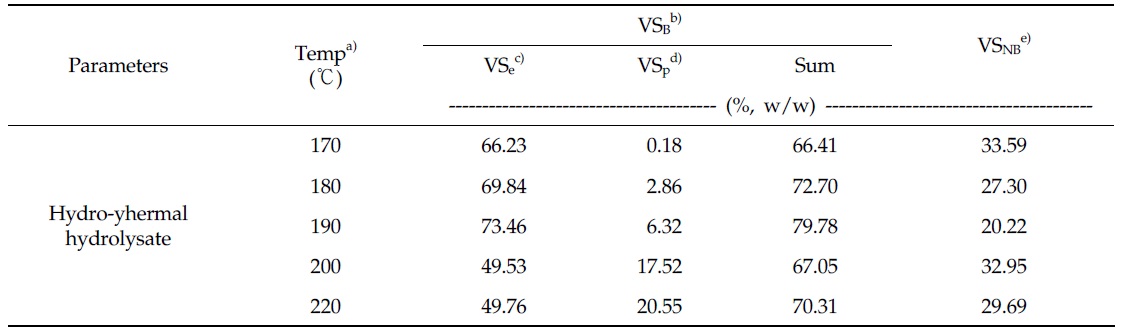
Wastewater treatment sludge cake of poultry slaughterhouse was treated in the different hydro-thermal reaction temperature of 170, 180, 190, 200, and 220℃. Theoretical and experimental methane potential for each hydro-thermal hydrolysate were measured. Then, the organic substance fractions of hydro-thermal hydrolysate were characterized by the optimization of the parallel first order kinetics model. The increase of hydro-thermal reaction temperature from 170℃ to 220℃ caused the enhancement of hydrolysis efficiency. And the methane potential showed the maximum value of 0.381 Nm3 kg-1-VSadded in the hydro-thermal reaction temperature of 190℃. Biodegradable volatile solid(VSB) content have accounted for 66.41% in 170℃, 72.70% in 180℃, 79.78% in 190℃, 67.05% in 200℃, and 70.31% in 220℃, respectively. The persistent VS content increased with hydro-thermal reaction temperature, which occupied 0.18% for 170℃, 2.96% for 180℃, 6.32% for 190℃, 17.52% for 200℃, and 20.55% for 220℃.
Biodegradable volatile solid showed the highest amount in the hydro-thermal reaction temperature of 190℃, and then, the optimum hydro-thermal reaction temperature for organic sludge was assessed as 190℃ in the aspect of the methane production. The rise of hydro-thermal reaction temperature caused increase of persistent organic matter content.
바이오가스의 생산은 산소가 없는 극도의 환원상태에서 혐기미생물의 연속적인 미생물 화학반응에 의해 일어난다. 유기물의 혐기소화는 단계적으로 가수분해(Hydrolysis), 산생성(Acidogenesis), 초산생성(Acetogenesis), 메탄생성(Methanogenesis) 반응으로 구분할 수 있으며, 메탄(CH4)과 이산화탄소(CO2)가 주요한 최종 산물이다(Gerardi, 2003). 따라서 혐기소화에서 유기물의 분해 특성은 최종적으로 생성되는 메탄(CH4) 또는 이산화탄소(CO2)의 발생속도 및 발생량의 분석을 통해 파악할 수 있다(Owen
혐기소화에서 유기물의 분해는 크게 유기 기질의 종류, 입자의 크기, 혐기미생물의 활성, 저해물질의 농도 등에 영향을 받으며, 이중 유기 기질의 종류와 입자의 크기는 유기물 자체의 특성에서 기인하는 유기물 분해의 영향인자이다(Chynoweth
혐기소화에서 유기 기질의 종류에 따른 미생물 반응 특성 연구는 혐기소화의 효율이 일차적으로 유기 기질의 유기물 조성에 의존한다는 점에서 중요하다. 일반적으로 이분해성(Biodegradable) 유기물 함량이 많은 경우 혐기소화의 효율은 증가되고, 난분해성(Non-biodegradable) 유기물과 분해 저항성(Persistent) 유기물의 함량이 많은 경우 혐기소화 효율은 감소한다(Buendía
수열탄화(Hydro-thermal carbonization) 기술은 가축분뇨, 음식물쓰레기, 폐수슬러지 등 다양한 바이오매스의 에너지화를 위한 열화학적 변환기술이다. 수열탄화 반응에서 바이오매스는 고밀도 탄화물로 전환되어 고체연료로 이용하고, 이과정에서 발생하는 열화학적 가수분해액(Hydro-thermal hydrolysate)은 혐기소화를 거쳐 바이오가스로 전환이 가능하다. 수열탄화 기술은 다양한 바이오매스의 효율적인 가용화가 가능한 기술로 현재 하수슬러지 혐기소화 분야에서는 상용화가 진행된 기술이다. 그러나 수열탄화에 의한 혐기소화 증진 사례 보고와 반대로 Bougrier 등(2008)과 Ajandous 등(2008)은 다양한 고상 슬러지의 열화학적 반응 연구에서 반응 온도에 따라 수열탄화액 중에 혐기소화에 분해 저항성을 가지거나 혐기소화를 저해하는 물질이 생성된다는 보고도 있다. 이러한 상반되는 연구결과에도 불구하고 수열탄화 기술은 입자상 유기물의 고체연료화와 가용화를 동시에 달성하는 기술로 바이오매스의 에너지 전환효율을 극대화할 수 있다. 특히 수열탄화액의 혐기소화 측면에서는 바이오매스의 가용화(Solubilization)를 통해 혐기소화조의 유효용적을 감소시키고 메탄의 생산 효율을 증가시켜 혐기소화의 경제성을 크게 향상시킬 수 있다는 장점이 있어 꾸준한 연구가 진행되고 있다. 그러나 지금까지의 수열탄화 연구는 SCOD의 증가 효과에 따른 유기물 가용화를 중심으로 연구되어 왔으며, 유기 기질의 종류와 특성에 따른 혐기소화 미생물 반응특성 연구는 미미한 상황이다. 따라서 본 연구에서는 유기성 슬러지의 수열탄화에서 반응온도가 수열탄화액의 혐기소화 효율에 미치는 영향을 분석하기 위하여 유기 기질의 구성을 난분해성(Non-biodegradable), 분해저항성(Persistent), 이분해성(Biodegradable)의 유기물로 정의하고, 평행 1차 반응속도식(Parallel first order kinetics)을 이용하여 수열탄화 반응 온도별 유기물의 분포 특성을 분석하였다.
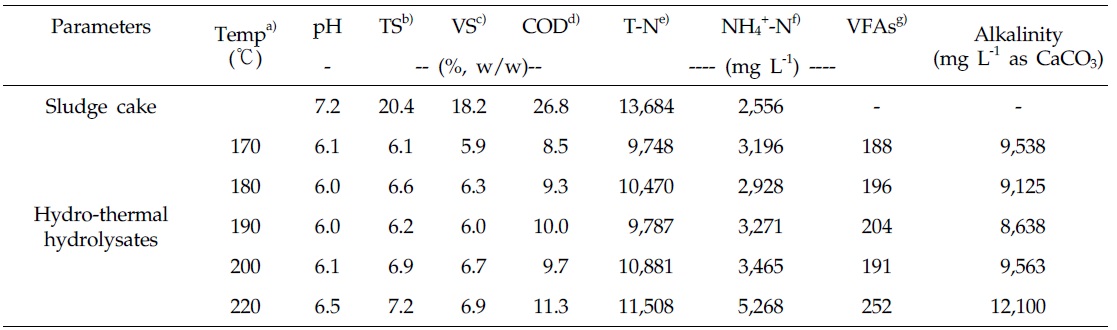
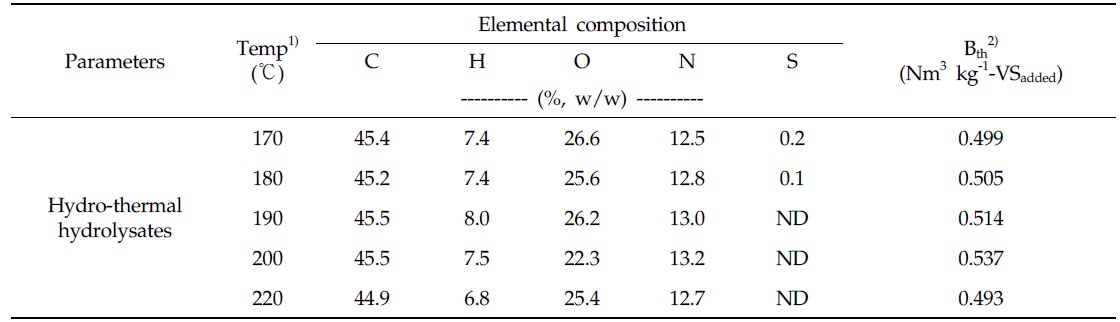
본 연구에서 사용된 시험재료는 충청남도 진천에 위치하는 도계 가공장의 폐수처리 시설에서 발생하는 유기성 슬러지를 사용하였다. 채취한 슬러지의 수열탄화 반응은 외부 전기 히터(Heater)에 의해 열원을 공급하는 2 L용량의 밀폐형 회분식 압력반응기에 1 kg의 시료 원물을 정량 투입 후 170 ∼220℃(170, 180, 190, 200, 220℃) 온도 구간에서 실시하였다. 반응기의 온도는 반응기 내부에 설치한 온도 계측기로 제어하였으며, 운전시간은 승온시간 40분, 반응시간 1시간으로 하였다. 또한 열가수분해 반응기는 반응기 내부온도의 균질화를 위하여 내부에 교반기를 설치하였으며, 반응기의 내부 압력은 반응온도별로 발생하는 내부 포화수증기압 조건으로 유지하였다. 열가수분해 반응을 마친 잉여슬러지 수열탄화액은 정성 여과지(Qualitative filter paper No. 1, Advantec MFS, Inc., Dublin, Califonia, USA)로 여과하여 메탄생산 퍼텐셜(Biochemical methane potential, BMP) 시험에 공시하였다. 실험에 사용한 유기성 슬러지와 반응온도별 수열탄화액의 화학적 성상은 Table 1과 같다.
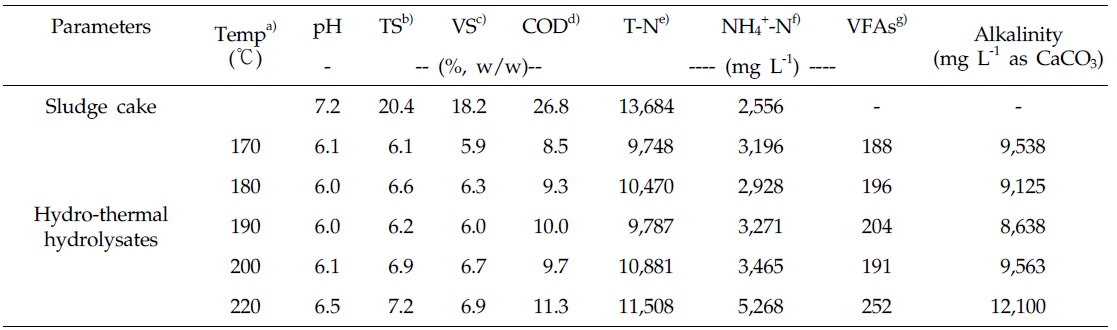
Chemical characteristics of input sludge and hydrolysates by the hydrothermal carbonization reaction
>
이론적 메탄생산퍼텐셜(Theoretical methane potential, Bth) 분석
이론적 메탄생산퍼텐셜은 공시시료의 원소분석 결과를 바탕으로 Boyle(1976)의 유기물 분해 반응식(Eq. 1)을 이용하여 화학양론적으로 산출하였다. 완성된 유기물 분해 반응식을 바탕으로 화학양론식인 Eq. 2을 이용하여 이론적 메탄발생량을 산정하였다.
>
최종 메탄생산퍼텐셜(Biochemical methane potential, Bu) 시험
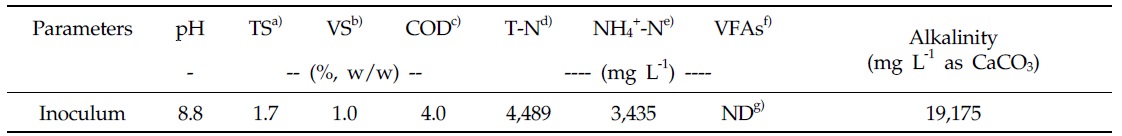
메탄생산퍼텐셜 시험에 사용한 접종액(Inoculum, I)은 경기도 일죽에 위치하는 5 m3 day-1 규모 한경대학교 바이오가스 상용화 연구시설에서 혐기 소화액을 채취하여 사용하였다. 채취한 혐기소화액은 2 mm 체를 통과시킨 후, 38℃ 항온 배양기에서 배양하여 소화액 중의 이분해성의 유기물과 잔여가스를 충분히 제거하여 접종액으로 사용하였다. 회분식 반응기는 처리구당 3반복으로 serum bottle을 이용하였다. 반응기의 용적(Total volume)은 160 mL, 유효용적(Working volume)은 80 mL, 상층부 여유공간(Head space)은 80 mL로 하였다. 여기서 투입기질(Substrate, S)은 기질의 VS 함량과 접종액의 VS 함량의 비율(S/I ratio)이 0.5가 되도록 조절하였으며, 상층부 여유공간은 N2 가스를 충진하여 공기가 없는 상태에서 완전 밀폐시켜 중온(38℃)에서 일일 1회 손으로 반응기를 흔들어 교반하면서 90일간 배양하였다. 또한 접종액에서 발생하는 메탄가스를 보정하기 위하여 접종액 만을 투입한 3반복의 혐기 반응기를 시료와 동일한 조건에서 바탕시험으로 운영하였다. 시험에 사용한 접종액의 성상은 Table 2와 같다.
[Table 2.] Chemical composition of inoculum
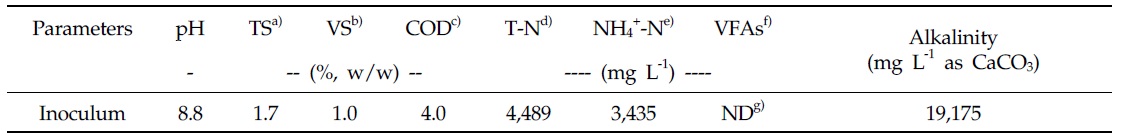
Chemical composition of inoculum
이때, Vdry gas는 표준상태(0℃, 1기압)에서의 건조 가스의 부피, T는 반응기의 운전온도, Vwet gas at T℃는 반응기 운전온도(38℃)에서의 습윤 가스의 부피, P는 가스의 부피측정 당시의 대기압, PT는 T℃에서의 포화수증기압(mmHg)이며, 본 연구에서는 P를 760 mmHg로 간주하고 PT는 38℃서의 포화수증기압으로 계산하였다.
회분식 혐기반응기의 바이오가스 발생량은 반응기운전 10까지는 일일 1회 측정하였으며, 10일 이후 2-5일 간격으로 측정하였다. 바이오가스 발생량의 측정은 2% 황산에 resazurin 0.1%를 함유하는 수주차식 가스량 측정기를 사용하였으며(Beuvink
이때, M은 누적 메탄생산량(mL), t는 혐기배양기간(days), P는 최종메탄생산량(mL), e는 exp(1), Rm은 최대메 탄생산속도(mL day-1), λ는 지체성장시간(lag growth phase time, days)이다.
본 연구에서는 유기성 슬러지 수열탄화액의 반응온도별 유기물의 분포특성을 분석하기 위하여 병렬 1차 반응속도식(Parallel first order kinetics) (Eq. 4)을 적용하였다(Rao
여기서 Bt는 시간 t에서의 메탄생산량(mL), Bu는 최종메탄생산량(Ultimate methane production, mL), fe는 병열 1차 반응 분배계수(g g-1), k1과 k2는 병열 1차 반응속도상수(Kinetic constant)이다.
또한, 본 연구에서는 혐기소화 과정에서 분해되는 기질(Substrate) 중의 유기물(
이때,
이때,
이때,
바이오가스의 가스성분 분석은 TCD(Thermal conductivity detector)가 장착된 Gas chromatography(Clarus 680, PerkinElmer, Waktham, Massachusetts, USA)를 이용하였다. 컬럼은 HayesepQ packed column(3 mm × 3 m, 80~100 mesh size)을 이용하였으며, 고순도 아르곤 (Ar) 가스를 이동상으로 사용하여 flow 30 mL min-1의 운전 상태에서 주입부(Injector) 온도 150℃, 컬럼부(Column oven) 90℃, 검출부(Detector) 150℃에서 분석하였다(Sorensen
유기성 슬러지의 수열탄화액의 누적 메탄생산곡선은 각각 Modified Gompertz model과 Parallel First Order Kinetics를 이용하여 최적화하였으며, 두 수학적 모델에 의한 최적화도는 평균제곱근편차(Root mean square deviation, RMSD) (Eq. 8)를 분석하여 비교하였다.
유기성 슬러지 수열탄화액의 원소분석 결과와 이로부터 Boyle(1976)의 유기물 분해 반응식(Eq. 1)을 이용하여 화학 양론적으로 산출한 이론적 메탄생산퍼텐셜(Bth)은 Table 3과 같다. 유기성 슬러지의 수열탄화액의 탄소 함량은 44.9∼45.5%, 수소 함량은 6.8∼8.0%, 산소 함량은 22.3∼26.6%, 질소 함량은 12.7∼13.2%의 범위를 보였으며, 황 함량은 수열탄화 온도 170℃와 180℃에서 각각 0.2, 0.1%를 나타내었다. 수열탄화액의 이론적 메탄생산퍼텐셜은 수열탄화 반응온도가 170℃에서 200℃까지 상승함에 따라 0.499에서 0.537 Nm3 kg-1-VSadded로 증가하였으며, 수열탄화온도 220℃에서는 0.493 Nm3 kg-1-VSadded으로 감소하였다.
[Table 3.] Elemental composition and theoretical methane potential of hydrothermal hydrolysate
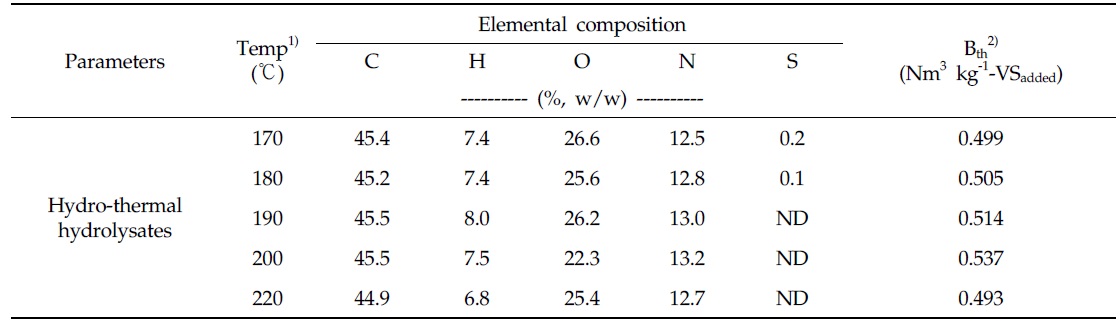
Elemental composition and theoretical methane potential of hydrothermal hydrolysate
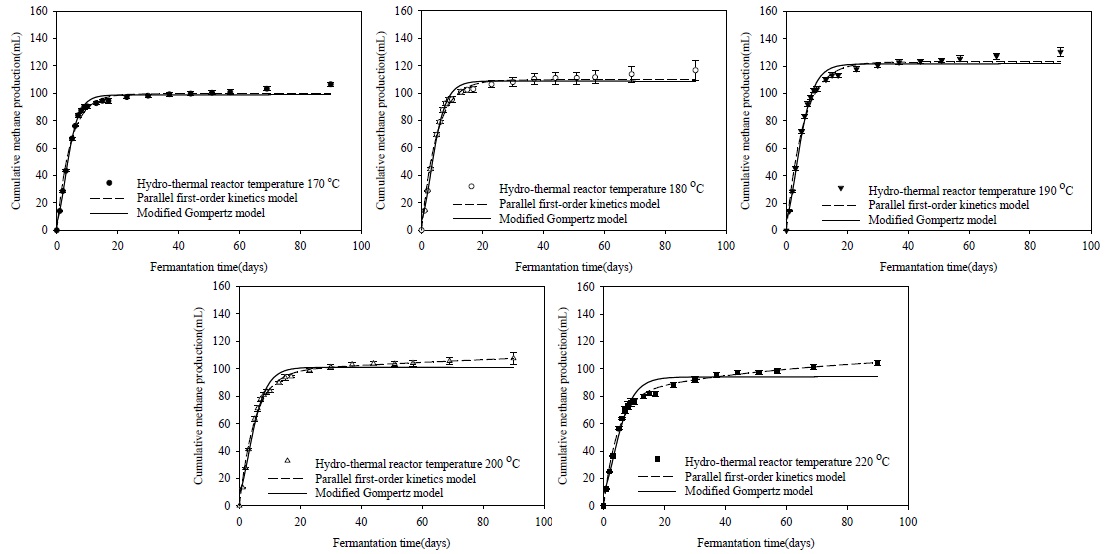
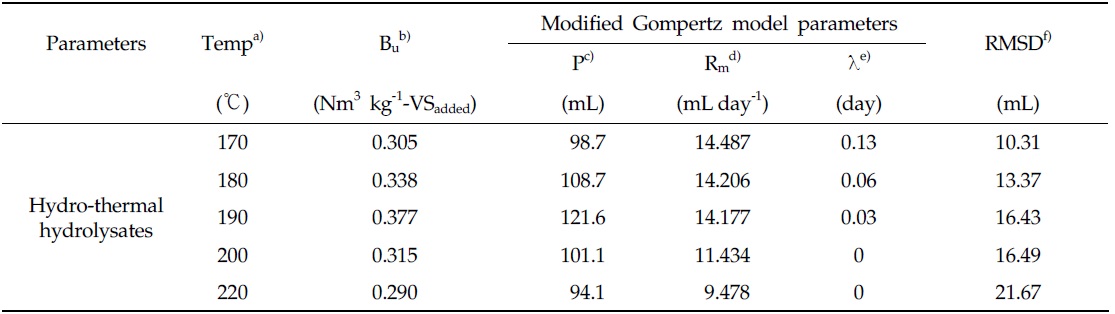
Fig. 1은 유기성 슬러지의 메탄생산퍼텐설 시험을 통해 얻은 수열탄화액의 누적 메탄생산곡선과 Modified Gompertz model, Parallel first order kinetics model을 이용하여 최적화한 곡선을 비교하였다. 또한 Table 4와 Table 5는 각각 유기성 슬러지 수열탄화액의 누적 메탄생산곡선을 각각 Modified Gompertz model과 Parallel first order kinetics model을 이용하여 최적화한 최종 메탄생산퍼텐셜(Bu)과 모델 인자들을 나타내었다.
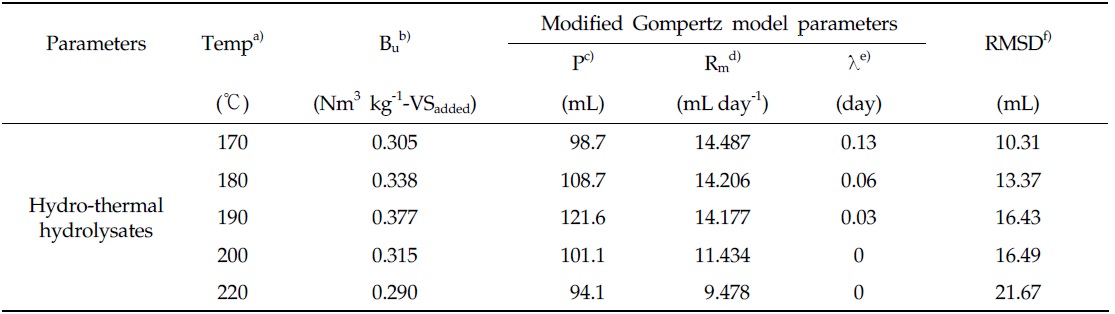
Ultimate methane potential and Modified Gompertz model parameters estimated by the optimization of Modified Gompertz model in the hydro-thermal hydrolysate of organic sludge
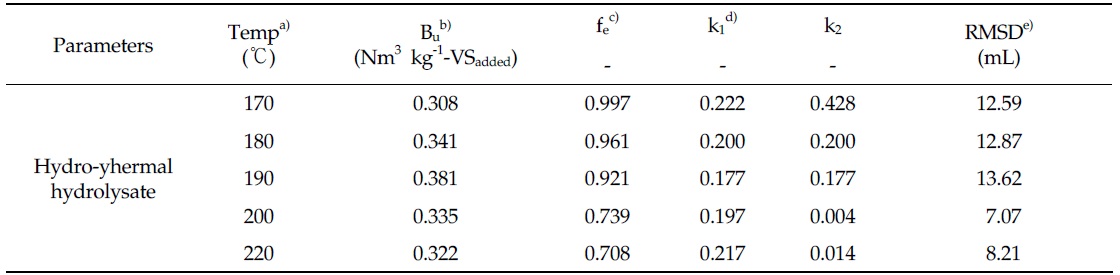
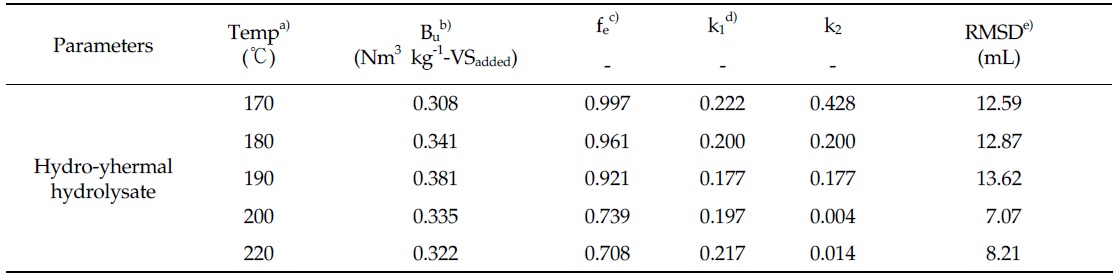
Ultimate methane potential and kinetics model parameters estimated by the optimization of Parallel first-order kinetics model in the hydro-thermal hydrolysate of organic sludge
유기성 슬러지 수열탄화액의 메탄생산퍼텐셜 시험을 통해 얻은 누적 메탄생산곡선에 Modified Gompertz model을 최적화하여 얻은 최종 메탄생산퍼텐셜은 수열탄화 반응온도 170℃에서 190℃까지 0.305에서 0.377 Nm3 kg-1-VSadded로 증가하였으며, 이후 수열탄화 반응온도 200℃와 220℃에서 각각 0.315, 0.290 Nm3 kg-1-VSadded으로 감소하였다. 또한 최대 메탄생산속도(Rm)는 수열탄화 반응온도 170℃에서 14.487 mL day-1로 가장 높았으며, 이후 수열탄화온도가 증가함에 따라 점차 감소하여 수열탄화 반응온도 220℃에서는 9.478 mL day-1를 나타내었다. Parallel first order kinetics model을 최적화하여 얻은 유기성 슬러지 수열탄화액의 최종 메탄생산퍼텐셜은 Modified Gompertz model로부터 얻은 최종 메탄생산퍼텐셜과 비교하여 수열탄화 반응온도에 따라 약 1∼10% 증가하는 것으로 나타났으며, 최종 메탄생산퍼텐셜은 170℃에서 190℃까지 0.308에서 0.381 Nm3 kg-1 -VSadded로 증가하였으며, 수열탄화 반응온도 200℃와 220℃에서 각각 0.335, 0.322 Nm3 kg-1-VSadded으로 감소하여 Modified Gompertz model을 적용하여 얻은 유기성 슬러지 수열탄화액의 최종 메탄생산퍼텐셜과 유사한 경향을 나타내었다. 또한 이분해성 유기물 계수(fe)은 수열탄화 반응온도 170℃에서 0.997을 나타내어 총 생분해성 유기물(VSB)의 99.7%가 이분해성 유기물로 분포하는 것으로 나타났으며, 수열탄화 온도의 증가와 함께 180℃에서 96.1%, 190℃ 에서 92.1%, 200℃에서 73.9%, 그리고 220℃에서 70.8%로 이분해성 유기물의 분포가 감소하였다. 이러한 열화학적 반응에서 반응온도의 증가와 함께 이분해성 유기물의 분포가 감소하는 것은 고온, 고압의 열화학적 반응조건에서 마이야르(Maillard) 반응에 의해 질소 화합물과 탄수화물이 반응하여 멜라노이딘(Melanoidine)이라는 분해저항성을 지니는 물질을 생성하기 때문이라는 보고(Martins
본 연구에서 적용한 Modified Gompertz mode과 Parallel first order kinetics model의 최적화도를 비교하면, 두 개 분석 모델의 최적화 과정에서 얻은 평균제곱근 편차(RMSD)는 수열탄화 반응온도 170℃를 제외하고 Parallel First Order Kinetics model의 적용이 통계적으로 높은 최적화도를 나타내어 Modified Gompertz model보다는 Parallel first order kinetics model이 수열탄화액의 최종 메탄생산퍼텐셜을 예측하는데 더욱 유리한 것으로 판단된다.
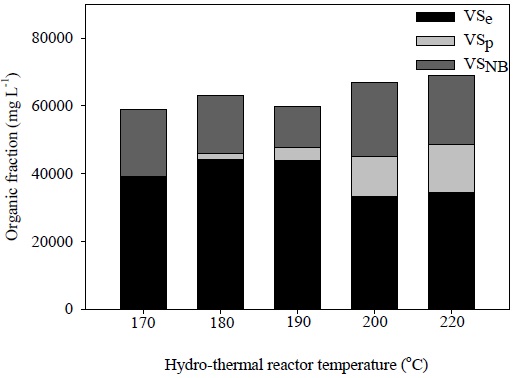
Table 6은 Parallel first order kinetics model을 이용하여 추산한 170℃∼220℃의 수열탄화 반응온도에서 생산 된 수열탄화액의 유기물 분포를 나타내고 있다. 생분해성 유기물(VSB)의 분포는 수열탄화 반응온도 170℃에서 66.41%, 180℃에서 72.70%, 190℃에서 79.78%를 나타내면서 증가하는 경향을 보였으며, 이후 200℃에서는 67.05%로 크게 감소하였다가 220℃에서는 70.31%를 나타내었다. 또한 난분해성 유기물(VSNB)의 분포는 생분해성 유기물(VSB)의 분포와 반대의 경향을 나타내었다. 이분해성 유기물(VSe)의 분포는 수열탄화 반응온도 170℃에서 66.23%를 나타내었으며, 이후 수열탄화 온도의 증가와 함께 지속적으로 감소하여 수열탄화 반응온도 220℃에서 49.76%까지 감소하였다. 또한 분해저항성 유기물(VSp)의 분포는 170℃ 0.18%에서 220℃ 20.55%로 증가하면서 이분해성 유기물(VSe)의 분포와 반대의 경향을 나타내었다. Fig. 2는 유기성 슬러지의 수열탄화액의 유기물(VS) 함량을 기준으로 하여 각각의 반응온도에서 생산된 수열탄화액 중 이분해성 유기물(VSe), 분해저항성 유기물(VSp), 난분해성 유기물(VSNB)의 함량을 나타내었다. 수열탄화액의 유기물(VS) 함량은 Table 1에 나타낸 바와 같이 수열탄화 반응온도 170℃에서 6.1%, 180℃에서 6.3%, 190℃에서 6.0, 200℃에서 6.7, 그리고 220℃에서 6.9%를 나타내었으며, 이때 이분해성 유기물(VSe) 함량은 수열탄화 반응온도 170℃에서 190℃까지는 증가하였으며, 이후 200℃와 220℃에서는 급격한 이분해성 유기물(VSe)함량의 감소를 나타내었다. 이와 함께 분해저항성 유기물(VSp) 함량은 수열탄화 반응 온도의 증가와 함께 지속적으로 증가하는 것으로 나타났다. Parallel first order kinetics model은 기본적으로 서로 다른 반응속도를 가지는 두 가지 종류의 유기물에 대하여 각각의 1차 반응식을 조합하여 해석하는 반응속도식이다. 따라서 이분해성 유기물 계수(fe)는 혐기조건에서 반응속도를 달리하는 두 종류의 기질 특성을 분배하는 계수이다. Rao
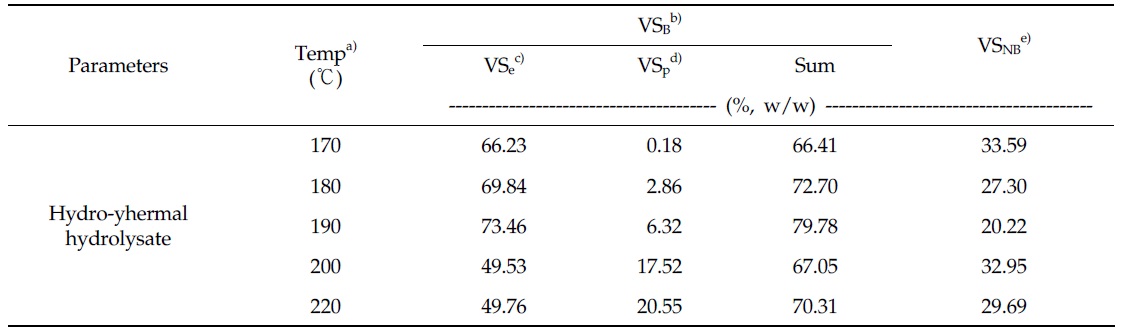
Organic fractions estimated by the optimization of Parallel first-order kinetics model in the hydro-thermal hydrolysate of organic sludge
본 연구는 유기성 슬러지의 수열탄화 전처리가 수열탄화액의 혐기소화와 혐기적 유기물 분해 특성에 미치는 영향을 분석하고자 170∼220℃의 열화학적 반응온도에서 생산된 유기성 슬러지 수열탄화액에 대하여 메탄생산퍼텐셜을 측정하고 평행 1차 반응속도식(Parallel first order kinetics)을 이용하여 유기물의 분포 특성을 분석하였다. 수열탄화액의 이론적 메탄생산퍼텐셜은 200℃에서 0.537 Nm3 kg-1-VSadded로 가장 높게 나타났으며, 실험적 메탄생산퍼텐셜은 190℃에서 0.381 Nm3 kg-1-VSadded로 가장 높게 나타났다. 평행 1차 반응속도을 이용하여 추정한 수열탄화액의 생분해성 유기물(VSB)의 분포는 수열탄화 반응온도 170℃에서 66.41%, 180℃에서 72.70%, 190℃에서 79.78%, 200℃에서 67.05%, 220℃에서 70.31%를 나타내었으며, 이중 이분해성 유기물(VSe)의 분포는 수열탄화 반응온도 170℃에서 66.23%, 180℃에서 69.84%, 190℃에서 73.46%, 200℃에서 49.53%, 220℃에서 49.76%을 나타내었다. 특히 분해저항성 유기물(VSp)은 수열탄화 반응온도의 증가와 함께 증가하여 170℃에서 0.18%, 180℃에서 2.86%, 190℃에서 6.32%, 200℃에서 17.52%, 220℃에서 20.55%로 나타나 수열탄화 반응온도가 상승할수록 분해저항성을 지니는 유기물의 분포가 증가하였다. 따라서 수열탄화 온도의 상승에 따라 메탄생산 효율은 190℃에서 가장 우수하였으며, 190℃ 이상으로 수열탄화 반응온도를 상승시키는 것은 분해저항성 유기물의 생성을 증가시키는 것으로 나타났다.