해조류는 암반 부착생물이며 연안생태계의 일차생산자로서 어패류와 갑각류의 먹이장, 은신장 및 산란장을 제공하는 생태적으로 중요한 기능을 수행하고 있다(Haglund et al., 1996; Tribollet and Vroom, 2007; Whitaker et al, 2010). 또한, 해조류가 생물ㆍ무생물적 환경스트레스(교란, 퇴적, 생활하수 유입)에 노출되면 종다양성, 생물량 및 피도, 그리고 홍조류와 갈조류의 출현종수가 감소되고, 반면에 기회종인 녹조류의 출현종수와 생물량 비율이 증가되는 특성을 보이기 때문에 생물지표자(biological indicator)로 이용되고 있다(Orfanidis et al., 2001; Arévalo et al., 2007; Pinedo et al., 2007; Wells et al., 2007; Scherner et al., 2013).
온대해역에서 서식하는 해조류의 군집구조는 계절변화와 장기간에 일어나는 천이(succession)에 따른 변화가 동시에 발생하므로 장기적인 모니터링을 통한 지속적인 관찰 및 연구가 필요하다(Spellerberg, 1991; Lee et al., 2009). 하지만, 우리나라 연안에서 수행된 해조류 군집구조에 대한 연구는 대부분 1-2년의 단기 연구인데, 장기연구는 해조군집의 변화과정을 파악하고 예상하지 못하는 각종사고(예, 유류오염)가 발생하였을 때 해조군집에 미치는 영향 및 변화를 파악할 수 있다. 해조류 군집구조와 환경을 살펴보면, 교란이 없는 안정된 해역에서는 경쟁종(다년생 해조류)이, 교란(부영양화, 퇴적물 증가 등)이 증가된 곳에서는 스트레스내성종이, 그리고 심각한 환경스트레스 해역에서는 일년생 기회종(갈파래류, 대마디말류, 염주말류등)이 우점하며(Díez et al., 1999; Arévalo et al., 2007; Wells et al., 2007), 환경스트레스 강도와 군집구조의 변화는 밀접한 관련이 있으며(Fujita, 1985; Orfanidis et al., 2001, 2003), 계절에 따른 수온에 따라 갈파래 풍도(abundance)도 영향을 받는다고 하였다(Anderson et al., 1996).
또한, 해조류는 형태, 내부구조, 광합성 및 초식자의 섭식에 대한 생존전략에 따라 다육질형, 유절산호말형, 각상형, 성긴분기형, 엽상형, 사상형의 6개 그룹으로 구분되었으며(Littler and Littler, 1984; Steneck and Dethier, 1994; Padilla and Allen, 2000), 이들 그룹을 다시 생태학적상태그룹(Ecological State Group)인 ESG I(성긴분기형, 다육질형, 유절산호말형, 각상형)과 EGS II (엽상형, 사상형)로 분류하였다(Orfanidis et al., 2003, Arévalo et al., 2007). 어떤 해역의 해조 군집에서 ESG I에 속하는 해조류의 풍도(피도, 생물량)가 높으면 환경스트레스가 낮은 안정된 해역이고, ESG II에 속하는 해조류가 번무하면 오염된 지역으로 판정하였다. 연구기간 중 2007년 12월에 충남 태안군 만리포 북서방 10 km 해안에서 “
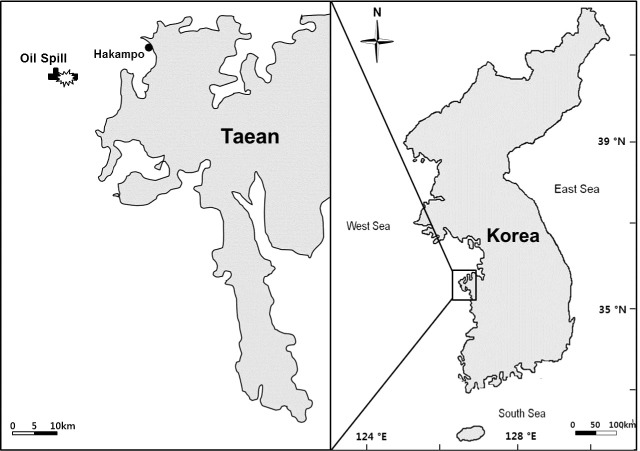
해조류는 충청남도 태안군 원북면에 위치한 학암포 해수욕장 북쪽의 암반 조간대에서(Fig. 1) 2007년 2월부터 2010년 10월까지 계절별로 16회 정량 및 정성 채집되었다. 정량 채집은 간조때 정점을 대표하는 해조상과 생물량을 보이는 곳을 선정하여 방형구(50 cm×50 cm)를 조간대 상, 중부 및 하부 각각 3개씩 무작위로 놓고 방형구내의 모든 해조류를 끌칼로 전량 채집하였다. 해조상을 파악하기 위해서는 정량샘플에 포함되지 않은 해조류까지 정성 채집하였다. 샘플은 현장에서 포르말린-해수 용액(5-10%)으로 고정시켜 실험실로 운반하여 Lee and Kang (2002)의 분류체계를 기준으로 출현종 목록 및 국명을 정리하였다. 해조류의 기능형은 출현종의 형태 및 내부구조에 따라 6개 기능형 그룹으로 구분되었으며(Littler and Littler, 1984; Steneck and Dethier, 1994; Padilla and Allen, 2000), 다시 ESG I과 EGS II로 분류하였다(Orfanidis et al., 2003, Arévalo et al., 2007).
정량 채집된 해조류는 담수로 수회 세척하여 모래 및 불순물을 제거하고 동정한 후 60℃로 세팅된 건조기에서 10일간 건조하여 생물량(g dry wt./m2)으로 환산하였다. 해조류 평균 생물량과 출현종수를 근거로 하여 풍도지수(richness index, R), Shannon's 다양도지수(diversity index, H')와 균등도지수(evenness index, J'), 우점도지수(dominance index, DI)는 이전 연구자와 동일하게 계산하였다(Margalef, 1958; McNaughton, 1967; Fowler and Cohen, 1990; Lee et al., 2007). 군집지수의 산출 및 유사도 분석(Bray and Curtis, 1957)은 PRIMER version 6 (Clarke and Gorley, 2006)을 사용하였으며 유사도 분석에 따른 각 그룹의 유의차는 SIMPROF (similarity profile) tests를 실시하여 검정하였다.
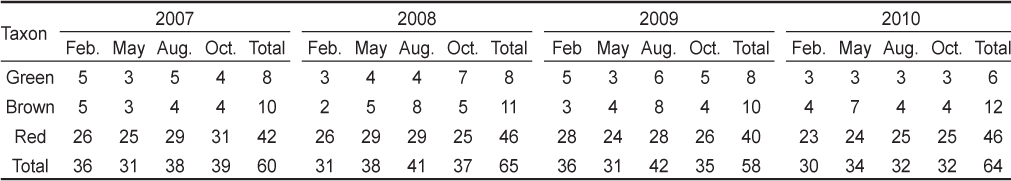
학암포 해안에서 연구기간에 수행된 16회의 계절별 채집에서 해조류 출현종은 101종(녹조 12, 갈조 18, 홍조 71종)이었으며, 구성비는 홍조류(70.30%)가 최대였고 갈조류(17.82%)와 녹조류(11.88%)의 순서였다. 연도별 해조류 출현종수는 58-65종으로 2009년에 최소였고 유류사고 직후인 2008년에 최대였다. 연구기간 계절별 출현종수는 2월(겨울)에 58종이었으며, 5월(봄)에 63종, 8월(여름)에는 59종, 10월(가을)에 65종으로서 가을에 최대였고 겨울에는 최소였다(Table 1).
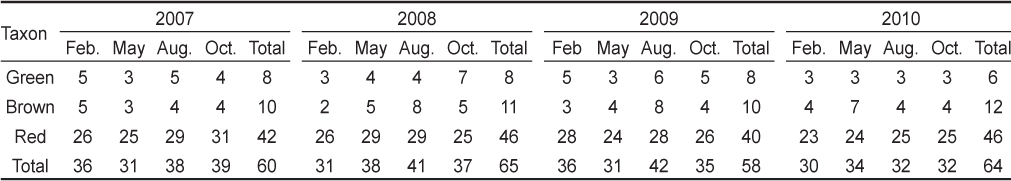
Seasonal variations in the number of macroalgal species occurred at Hakampo, western coast of Korea from February 2007 to October 2010
유류사고 발생(2007년 말)전과 후의 해조류 출현종수를 보면, 사고 이전인 2007년에는 60종(녹조 8, 갈조 10, 홍조 42종)이었고, 2008년에는 65종(녹조 8, 갈조 11, 홍조 46종)으로 유류사고 전에 비해 갈조류와 홍조류가 증가하였다. 연구기간 5년 동안에 수행된 16회의 샘플에서 모두 출현한 종은 7종(지충이, 우뭇가사리, 작은구슬산호말, 까막살, 진두발, 잔금분홍잎, 새빨간검둥이)이었고, 15회 출현한 종은 4종(개지누아리, 비단풀, 누은분홍잎, 참보라색우무)으로 확인되었다.
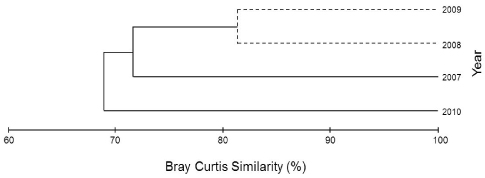
해조류의 연도별 출현종의 유·무로 유사도를 분석하면, 3개 그룹으로 구분되었고(Fig. 2), 그룹A (2007년)와 그룹B (2008·2009년)의 유사도는 71.59%였고 그룹A·B와 그룹C (2010년) 사이의 유사도는 68.83%로 유의차를 보였다(P<0.05).
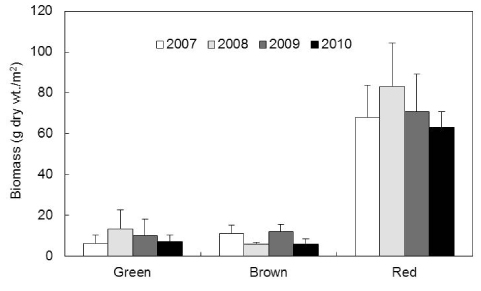
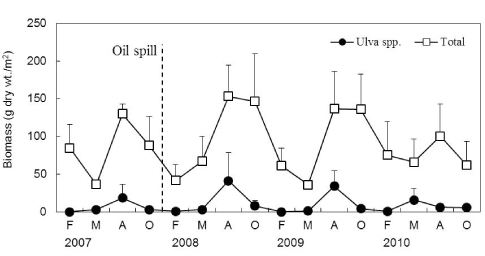
학암포 해안에서 연구기간 동안 해조류의 평균 생물량(g dry wt./m2)은 88.78 g 이었고, 연도별 평균 생물량은 75.81-102.06 g으로 2008년에 최대였고 2010년에 최소였다. 연구기간에 홍조류의 생물량은 63.14-83.06 g으로 녹조류(6.04-13.11 g), 갈조류(5.67-11.82 g)에 비해 높았으며, 평균 생물량은 홍조류가 71.21 g로 최대였고 녹조류(9.00 g)와 갈조류(8.56 g)의 순서를 보였다. 특히, 녹조류의 생물량은 유류사고가 발생 전인 2007년의 6.04 g에서 2008년에는 약 2배 이상 증가한 13.11 g으로 피크(peak)를 보인 후 점진적인 감소를 보였다(Fig. 3). 유류오염 이후 홍조류 진두발과 참보라색우무의 생물량 감소(2007년)와 작은구슬산호말의 생물량 감소(2009, 2010년)는 홍조류의 생물량 급감과 밀접하게 관련되었다(Fig. 3).
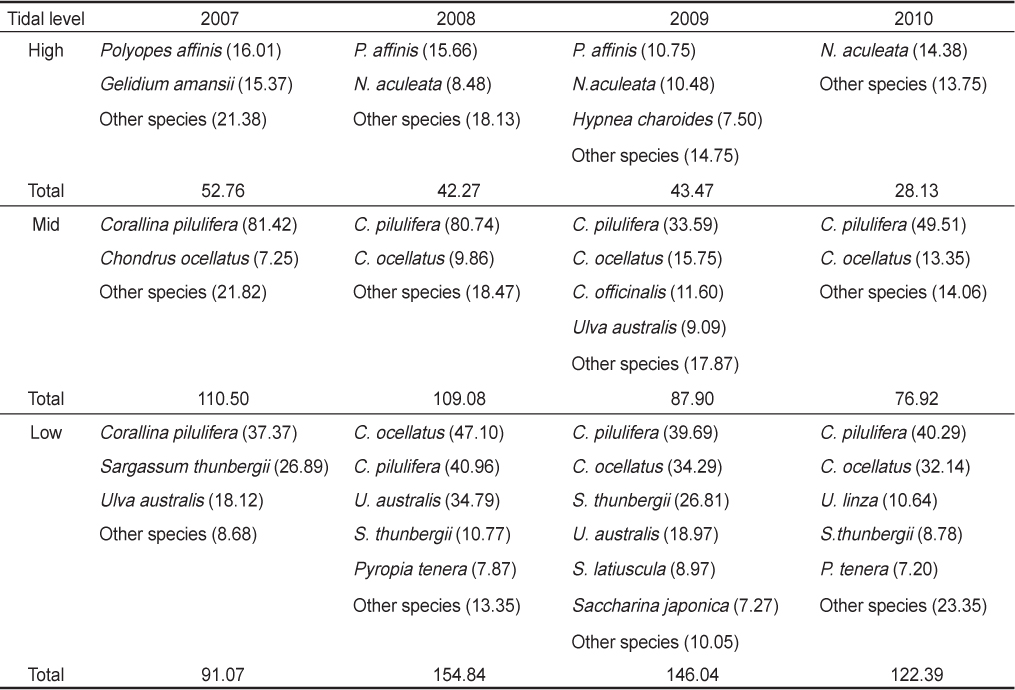
연구기간에 해조류의 조위별 평균 생물량(g dry wt./m2)은 조간대 중부(96.10 g)와 하부(128.59 g)에서 높았으며 조간대 상부(41.66 g)에 비해 2–3배 높은 생물량을 보였다(Table 2). 해조류의 조위별 생물량을 연도별로 보면, 조간대 상부에서 28.13–52.76 g으로 2007년에 최대였으며 2010년에 최소값을 보였다. 중부의 해조류 생물량은 2007년에 최대(110.50 g)였고 2010년에 76.92 g으로 최소였으며 2007년 이후 점차적으로 감소하는 경향을 보였다. 조간대 하부에서 해조류 생물량은 91.07-154.84 g으로 2007년에 최소였고 2008년에 최대를 기록한 후 점차 감소하였다(Table 2).
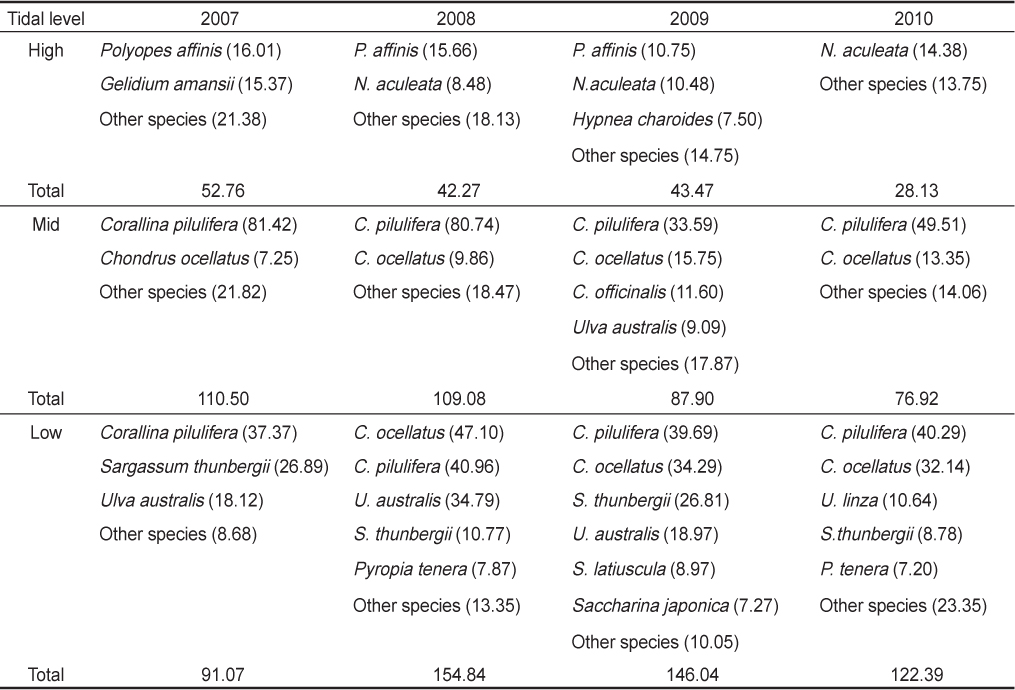
Vertical distribution of dominant species (> 7.00 g in biomass) based on annually-averaged biomass (g dry wt./m2) at Hakampo, western coast of Korea from February 2007 to October 2010
학암포 조간대에 서식하는 해조류 생물량의 수직분포를 보면, 연구기간에 조간대 상부 생물량의 40% 이상은 새빨간검둥이와 까막살이 차지하였고, 중부 생물량의 50% 이상은 작은구슬산호말과 진두발이 차지하였다. 특히, 중부에서 구멍갈파래의 생물량은 2009년에 높게 나타났다. 하부에서는 지충이, 구멍갈파래와 작은구슬산호말이 생물량의 50% 이상을 차지하는 주요종이었으며, 이들의 생물량은 지속적으로 증가하였다(Table 2).
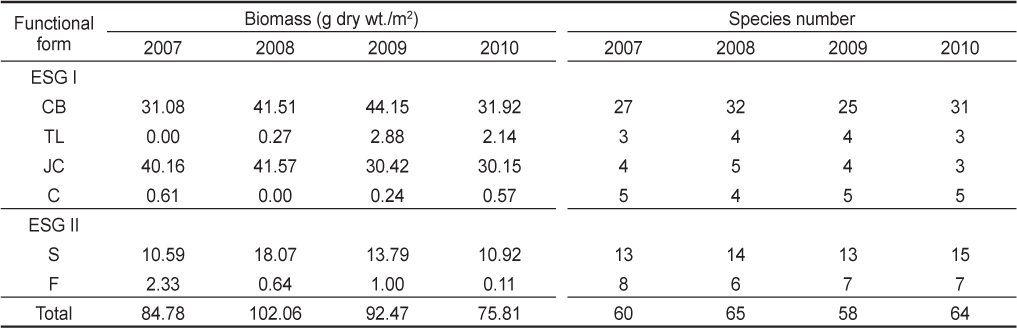
학암포에서 연구기간에 출현한 해조류 101종은, 성긴분기형 47종(46.53%), 사상형 14종(13.86%), 엽상형 21종(20.79%), 다육질형 4종(3.96%), 유절산호말형 7종(6.93%), 각상형 8종(7.92%)으로 성긴분기형이 가장 우점하였고 다육질형이 가장 적었다(Table 3). ESG I에 속하는 해조류가 66종(65.35%)으로 ESG II 해조류(35종, 34.65%)에 비해 많았다. 연구기간 해조류의 평균 생물량(88.78 g dry wt./m2)은 성긴분기형(37.17 g, 41.86 %)과 유절산호말형(35.58 g, 40.07%)이 대부분을 차지하였으며, 엽상형(13.34 g, 15.03 %)이 다음 순서였다. 해조류의 성긴분기형은 많은 출현종으로 인하여 생물량이 높았고, 유절산호말형은 출현종이 적지만 타해조류에 비해 무게가 많은 산호말류이기 때문에 높은 생물량을 보였다.
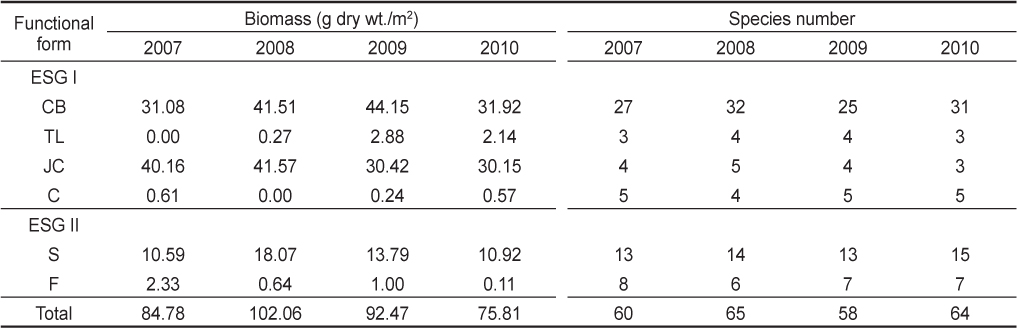
Annual variations in the number of species and biomass (g dry wt./m2) of each functional (F) form seaweed and ecological state group occurred at Hakampo, western coast of Korea during the study period
연구기간에 연도별로 ESG I과 ESG II의 생물량 백분율을 보면, ESG I은 81.67-85.44% (2008년 최소, 2010년 최대)였고 ESG II의 비율은 14.56–18.33%로 2010년에 최소였고 2008년에 최대였다. 해조류의 전체 생물량 중 ESG II의 비율은 2008년을 기준으로 하여 크게 증가하였다가 계속적으로 감소하는 경향을 보였다(Table 3). 해조류 ESG II의 생물량 증가는 엽상형 해조류인 갈파래류의 증가와 정비례적인 관계를 나타냈다.
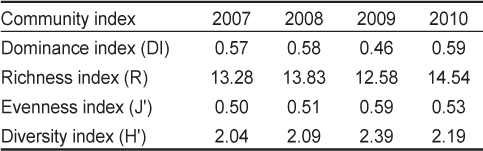
우점도지수(DI)는 2009년에 0.46으로 최소였고 2010년에 0.59로 최대를 보였으며, 2007년에는 제 1, 2우점종이 작은구슬산호말과 지충이였으나, 2008년 이후부터는 작은구슬산호말과 진두발로 바뀌었다. 종다양도지수(H')는 2.04–2.39의 변화를 보였으며, 풍도지수(R)는 58종이 출현한 2009년에 최소(12.58)였고 64종이 동정된 2010년에 14.54로 최대였다(Table 4). 균등도지수(J')는 2007년에 0.50으로 최소였고 2009년에 0.59로 최대를 보였으며 2009년까지 계속적으로 증가하다가 2010년에 감소하였다.
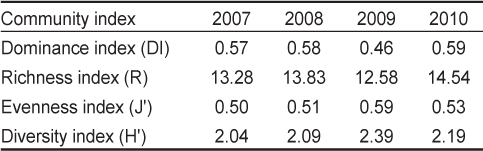
Annual seaweed community indices based on seaweed biomass at Hakampo, western coast of Korea during the study period
태안반도의 학암포에서 4년의 연구기간에 출현한 해조류는 101종(녹조 12종, 갈조 18종, 홍조 71종)이었으며 매년 출현종수는 58–65종으로 변화되었다. 학암포 인근의 해조상은 1987년에 실시된 연구에서 분점도의 91종, 마외에서 75종, 도랑골에서 55종이 기록되었다(Yoo and Kim, 2003a). 이후 1993년에 분점도에서 54종(Yoo and Kim, 2003b), 2006년에 46종(Yoo et al., 2009)이 출현하였고, 본 연구에서의 2007–2010년까지 60종, 65종, 58종, 64종으로 1987년도 이후로는 출현종수가 크게 감소하여 비슷한 양상을 보였다.
본 연구기간에 학암포에서 홍조류 4종(작은구슬산호말, 까막살, 진두발, 새빨간검둥이)과 갈조류 지충이는 16회 채집에서 모두 기록되고 생물량이 많은 대표종이었다. 선행연구에서 갈조류 지충이는 영광(Hwang et al., 1996), 의항(Oh and Lee, 1998), 꽃지(Lee et al., 2007), 주삼도(Heo et al., 2011)에서, 그리고 서해안의 11개 정점(Kim et al., 1995)에서 우점하는 서해안의 대표종이었다. 하지만, 본 연구 정점인 학암포에서 주요종은 작은구슬산호말, 진두발, 지충이와 갈파래류로 나타났다. 특히, 지충이가 주로 서식하는 조간대 하부에서도 진두발, 작은구슬산호말와 갈파래류에 비해 생물량이 낮은 것으로 확인되었다. 학암포 조간대 암반은 참굴(
서해안 해조류의 생물량(건중량, g dry wt./m2)은 1987년에 분점도(144.11 g)와 마외에서 171.10 g을 보였고(Yoo and Kim, 2003a), 1993년에 분점도에서 355.06 g을 기록하였으며(Yoo and Kim, 2003b), 본 연구지역인 학암포에서의 해조류 생물량은 75.81–102.06 g (2010년 최소, 2008년 최대)으로서 선행연구와 비교했을 때 생물량은 많이 감소된 것으로 확인되었다. 선행 연구에서 생물량의 주요 구성종은 산호말류, 지충이, 불등풀가사리로서 이들이 생물량의 50% 이상을 차지하는 것으로 기록되었는데, 본 연구에서도 산호말류의 생물량이 상당히 높았으나, 이전 기록에 비해 감소한 경향을 보였다(Yoo and Kim, 2003a; 2003b). 또한, 지충이와 불등풀가사리가 1993년 연구까지 학암포에서 우점한 것으로 기록되었지만, 본 연구에서 낮은 생물량을 보이는 것은 향후 관심이 갖고 보아야 할 것이다.
해조류가 유류오염에 의해 받는 피해는 조간대 상부에서 최대였고 중부와 하부로 갈수록 감소하였으며, 군집구조의 회복은 하부, 중부, 상부 순서로 일어나는 것으로 알려져 있다(Jones et al., 1998; Shin et al., 2008). 학암포 조간대 중부에서 2008년에는 탄산칼슘의 세포벽을 가진 다년생 작은구슬산호말이 생물량의 80%이상을 차지하였는데, 이러한 결과는 유류오염에 민감한 다른 해조류의 생물량 감소 때문으로 나타났다. 이후 2009년에는 진두발을 비롯한 다양한 해조류가 골고루 분포하였지만 오염지표종인 구멍갈파래의 생물량이 급증하여 생태계 회복을 예단하는 것은 어려울 것으로 판단된다. 조간대 하부에서는 원유유출사고 이후 구멍갈파래 생물량이 급증하였으나 시간이 경과함에 따라 감소되었고 다양한 해조류가 번무함으로써 유류오염 발생 후 3년이 지난 2010년에는 해조류의 군집구조가 점차 안정되고 있는 것으로 사료된다.
Orfanidis et al. (2001)는 ESG I에 속하는 해조류의 피도(혹은 생물량)가 많으면 인간활동으로 인한 환경스트레스가 상대적으로 적은 해역이고 EGS II에 속하는 해조류가 많으면 환경오염이 심각한 해역으로 판정하였다(Yoo et al., 2007; Choi et al., 2008). 유류사고 이후 EGS II에 속하는 해조류 중에서 사상형의 출현종수과 생물량이 감소하였고 반대로 엽상형 해조류의 출현종수과 생물량이 증가하였다. 특히, 갈파래류의 생물량이 급증하였는데, 이는 유류오염으로 인하여 다른 해조류와 동물들의 사망으로 인하여 생성된 새로운 공간에 기회종인 갈파래류가 가입되었거나, 원유제거를 위해 사용되는 유화제로 인한 영양염이 제공되었기 때문으로 사료된다(Chasse, 1978; Felder et al., 2014). 학암포에서 해조상은 계절성을 보였으며 갈파래류는 여름과 가을(8-10월)에 주로 우점하는 것으로 나타났다. 갈파래류의 생물량은 유류사고 전인 2007년 8월에 18.33 g dry wt./m2이었으나, 사고 발생 후 2008년에 크게 증가하여 8월에 41.27 g으로 최대값을 기록한 후 2009-2010년에 점차 감소하여 유류사고 이전과 유사한 생물량을 보였다. Anderson et al. (1996)은 갈파래류는 계절성을 보이고 환경오염이나 부영양화, 혹은 환경스트레스가 심한 해역에서 주로 대발생(bloom)하였다가 안정되면 생물량이 감소하는 것으로 기록하였다. Fujita (1985)는 갈파래류의 번무원인은 다른 해조류에 비해 질소와 인을 빠르게 흡수 및 사용할 수 있기 때문이라고 하였다. 따라서, 갈파래류의 생물량 변화는 유류오염으로 인한 암반생태계의 피해 및 회복 정도를 나타내는 척도라고 볼수 있다.
결론적으로 2007년 “