조피볼락(
최근 어류의 연중 양식으로 인한 질병 발생으로 인한 대량폐사가 빈번하게 발생하여 양식 어민들의 경제적 손실은 아주 심각한 실정이며, 이러한 대량폐사를 감소시키기 위하여 어류용 배합사료내 인위적으로 합성항생제를 사용하고 있는 실정이다. 그러나 합성항생제의 사용은 항생제 내성 증가, 어류내 항생제 잔류 및 환경오염 등의 심각한 문제를 야기시킬 수 있기 때문에 유럽의 몇몇 나라에서는 어류용 배합사료내 합성항생제의 사용을 전면 금지하고 있는 실정이다(Tang et al., 2001). 우리나라에서도 사료회사에서 양어용 배합사료 제품을 생산할 때에는 합성항생제(동물용 의약품)를 사용하지 못하도록 법규로 규정되어 있으며, 항생제는 필요시 양어가가 규정에 준하여 구입하여 사용하도록 규정되어 있다.
따라서 최근에는 이들 합성항생제를 대체할 수 있는 천연 소재의 다양한 소재 개발이나 약용식물(herb)을 개발하여 사료첨가제로 공급함으로서 어류의 성장, 사료 이용성 및 질병 저항성 향상 효과(Turan and Akyurt, 2005; Turan et al., 2007; Galina et al., 2009; Soosean et al., 2010; Dada and Oviawe, 2011; Deng et al., 2011; Cho and Lee, 2012; Kim et al., 2013) 등에 대한 연구가 수행된 바 있다. 따라서 어류의 생산성 향상을 위하여 어류의 성장, 사료의 이용성 및 질병에 대한 내성을 향상시킬 수 있는 다양한 새로운 천연 소재의 사료첨가제 개발은 지속적으로 이루어져야 한다.
함초[Saltwort (SW),
따라서 본 연구에서는 상업용 배합사료내 많이 사용되고 있는 합성항산화제인 ethoxyquin과 비교하여 항산화 기능 사료첨가제(함초, 부추 및 민들레)를 조피볼락용 배합사료내 사용 시 어체의 성장, 체조성, 혈액성상 및 세균 공격성에 미치는 영향을 조사하였다.
실험에서 사용된 조피볼락 치어는 경북 포항에 위치한 개인양어장에서 구입하여 사육실험 환경에 2주간 적응시켰으며, 적응기간 동안에는 1일 2회 충분한 양의 배합사료(상품사료: 단백질 52%, 지질 12%)를 어체의 2-4%가량 공급하여 주었다. 조피볼락 치어[시작시 마리당 평균 무게(Mean±SE: 4.2±0.00 g)] 40마리씩을 8개의 50 L 사각형 유수식 플라스틱 수조(수량: 45 L)에 각각 수용하였다. 각 수조당 환수량은 1.41 L/min이었으며, 각각의 수조에는 충분한 aeration을 시켜주었다.
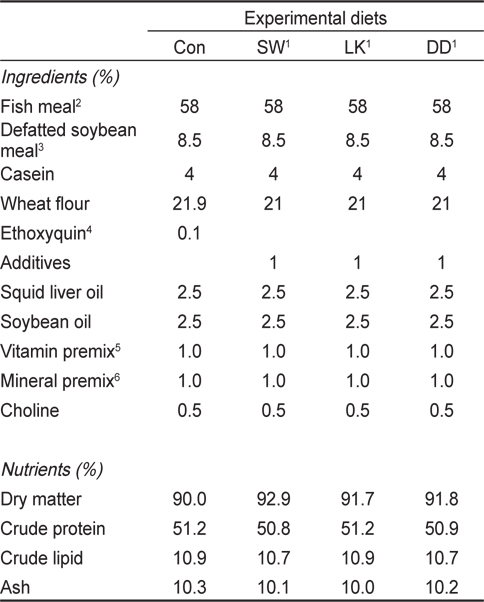
[Table 1.] Ingredients (%, DM basis) and nutrient composition of the experimental diets
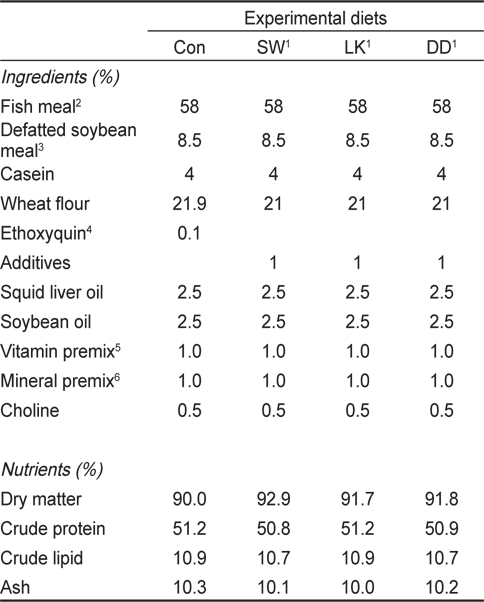
Ingredients (%, DM basis) and nutrient composition of the experimental diets
조피볼락용 실험사료의 사료조성표는 Table 1과 같다. 어분, 대두박과 카제인을 실험용 사료내 주요 단백질원으로 공급하였으며, 소맥분을 주요 탄수화물원으로 공급하였다. 그리고 오징어 간유와 대두유를 실험용 사료내 주요 지질원으로 공급하였다. 0.1% 소맥분 대신에 합성항산화제인 ethoxyquin (천하제일사료, 한국)을 0.1% 첨가한 실험구를 대조구(Con) 사료로 이용하였으며, 1% 소맥분 대신에 시판중인 사료첨가제 SW, LK, DD (토종마을, 서울, 한국)를 각각 1%씩 첨가하여 실험사료로 제조하여 이용하였다. 실험사료 원료는 잘 혼합한 후 물과 3:1의 비율로 섞어서 실험실용 펠렛제조기를 이용하여 실험사료를 제조하였다. 제조한 실험사료는 그늘에서 건조시킨 후 −20℃ 냉동고에 보관하면서 필요시 마다 소량씩 사용하였다. 모든 실험어는 1주일에 7일간 1일 2회(09:00, 17:00)씩 매일 손으로 만복시까지 사료를 공급하여 주었다.
실험사료와 실험어의 일반성분 분석을 위하여 8주간의 사육실험 종료시 각 수조당 생존한 조피볼락 5마리씩을 무작위로 샘플하여 일반성분 분석에 이용하였으며, 수분, 조단백질, 조지방 및 회분을 AOAC 표준방법(1990)에 따라 분석하였다. 조단백질은 Kjeldahl method (Auto Kjeldahl System, Buchi B-324/435/412, Switzerland)과 조지방은 ether-extraction method으로 분석하였으며, 조회분은 550℃ 회화로에서 4시간동안 태운 후 정량하였고, 수분은 105℃ dry oven에서 24시간 건조시킨 후 측정하였다.
8주간의 사육실험 종료시 1일간 절식시킨 이후 각 수조에서 생존한 조피볼락을 무작위로 5마리씩 샘플하여 50 ppm의 아미노안식향산 에틸수용액으로 마취한 후 미부정맥에서 채혈하여 혈청을 분리하였으며, 분리된 혈청을 이용하여 혈액성상 분석에 사용하였다. 조피볼락의 혈액은 Automatic Chemistry System (HITACHI 7180/7600-210, Hitachi, Japan)을 이용하여 총단백질(total protein), glutamic oxaloacetic transaminase (GOT), glutamic pyruvic transaminase (GPT)와 triglyceride 함량을 측정하였다.
8주간의 사육실험 종료시 각각의 사육수조에서 생존한 조피볼락을 무작위로 20마리씩 선별하여 7.9×106 CFU/L 농도의
One-way ANOVA와 Duncan’s multiple range test (Duncan 1955)로서 SPSS program version 19.0 (SPSS Michigan Avenue, Chicago, IL, USA)을 이용하여 각 실험구간의 유의성을 검정하였다.
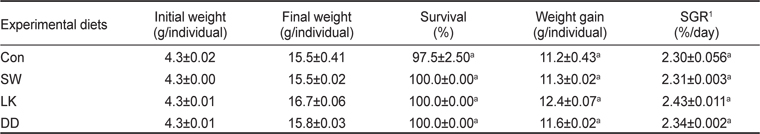
조피볼락용 배합사료내 항산화 기능 사료첨가제를 함유한 실험사료를 8주간 공급시 조피볼락의 생존율(%), 어체중 증가(g/fish) 및 일일성장율(SGR)을 Table 2에 나타내었다. 조피볼락의 생존율은 97.5-100%의 범위로서 항산화 기능 사료첨가제 종류에 따른 유의적인 차이는 없었다(
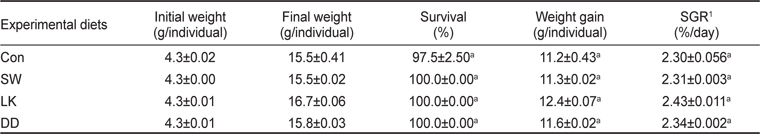
Survival (%), weight gain (g/fish) and specific growth rate (SGR) of rockfish Sebastes schlegelii fed the experimental diets containing various sources of antioxidants for 8 weeks
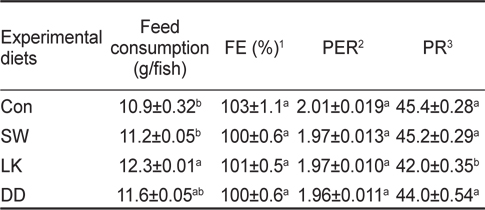
8주간의 사육실험 종료시 조피볼락의 사료섭취량(g/fish), 사료효율(feed efficiency, FE), 단백질전환효율(protein efficiency ratio, PER) 및 단백질축적율(protein retention, PR)을 Table 3에 나타내었다. 마리당 사료섭취량은 부추(LK) 사료 공급구가 대조구(Con)와 함초(SW) 사료 공급구보다 유의적으로 높게 나타났으나(
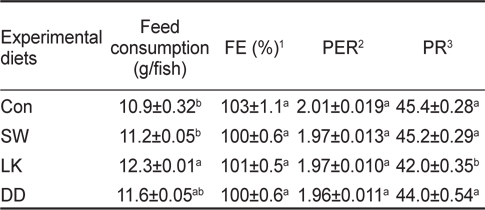
Feed consumption (g/fish), feed efficiency (FE, %), protein efficiency ratio (PER) and protein retention (PR) of rockfish Sebastes schlegelii fed experimental diets containing various sources of antioxidants for 8 weeks
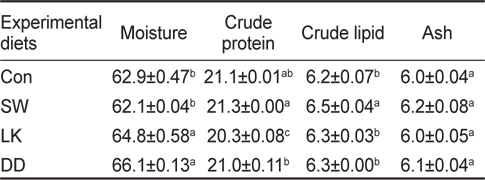
항산화 기능 사료첨가제가 함유된 실험용 배합사료를 8주간 공급받은 조피볼락의 전어체 일반성분 분석 결과를 Table 4에 나타내었다. 전어체의 수분 함량은 LK와 DD 사료를 공급한 실험구가 대조구와 SW 사료를 공급한 실험구보다 유의적으로 높게 나타났다(
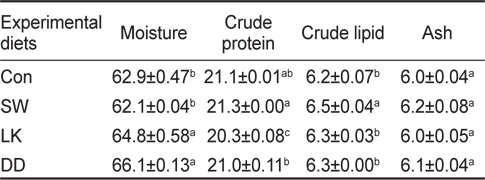
Chemical composition (%) of rockfish Sebastes schlegelii fed experimental diets containing various sources of antioxidants for 8 weeks
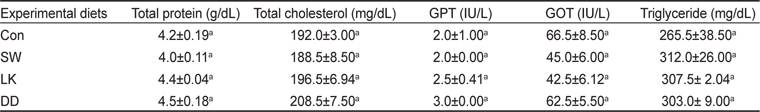
8주간의 사육실험 종료시 조피볼락의 혈청의 total protein, total cholesterol, glutamic pyruvic transaminase (GPT), glutamic oxaloacetic transaminase (GOT) 및 triglyceride의 함량을 Table 5에 나타내었다. 측정된 모든 항목의 함량은 항산화 기능 사료첨가제 종류에 따른 실험구간의 유의적인 차이가 없었다(
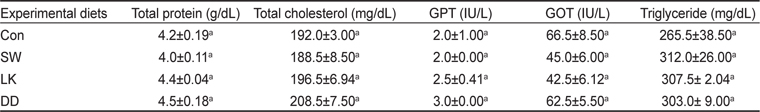
Serum chemistry of rockfish Sebastes schlegelii fed experimental diets containing various sources of antioxidants for 8 weeks
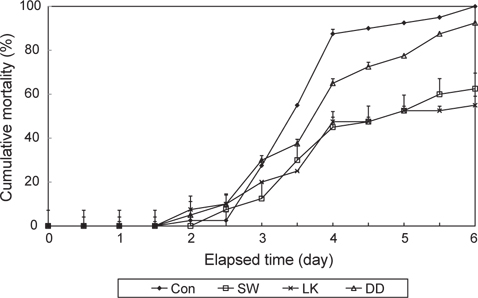
8주간의 조피볼락 사육실험 종료시 생존한 조피볼락 20마리를 무작위로 추출하여
어류에 있어서 다양한 종류나 형태의 사료첨가제가 어류의 면역성 향상이나 내병성에 효과가 있는 것으로 보고되고 있다. 조피볼락용 배합사료내 0.5% 알로에 첨가시
이상의 결과를 고려할 때 항산화 기능을 가진 함초, 부추 및 민들레의 배합사료내 첨가는 조피볼락의 성장과 혈액성상학적 변화에는 효과가 없는 것으로 나타났다. 그러나 함초, 부추 및 민들레의 사료내 첨가는