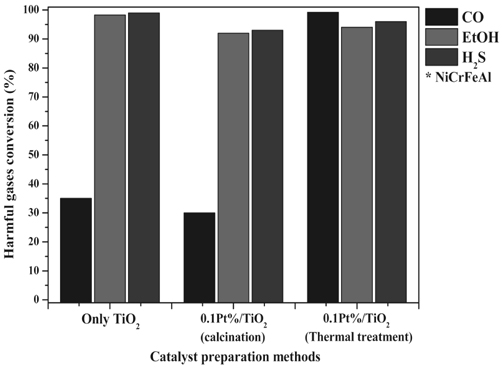
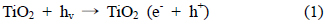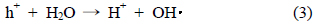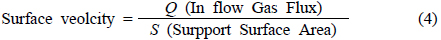This study was performed to study the photocatalyst for controlling the pollutant such as CO, C2H5OH and H2S by the UV light. This was shown in a catalyst having the same volume and the same surface area, that the structure in which the UV light to reach the interior structure exhibits more excellent activity. However, the activity of this activity of this photocatalyst removal of CO was very low. This problem can be solved by performing a reduction process by the addition of the precious metal series of Pt. Particularly, the amount of chemical species Pt0 incerased in the surface of Pt/TiO2 photocatalyst through the reduction process, which make the reaction activity of photocatalyst excellent to the removal of the CO.
오늘날 산업발달과 경제발전으로 인하여 생활수준이 크게 향상됨에 따라, 국민들의 환경에 대한 인식이 향상되었다. 하지만 대기오염의 문제는 심화되어 제어해야 할 오염물질이 증가하였으며, 특히 급격한 산업발전과 도시화 및 에너지 소비의 급증으로 인하여 대기오염물질이 심각한 사회적 문제로 대두되고 있는 실정이다. 이러한 이유로 현대인들의 주 생활공간이 실내의 공기질(IAQ, Indoor Air Quality)에 대한 관심이 높아지고 있다[1].
대기오염의 경우 바람 등에 대한 자연적 희석률이 크고 사회적 인식 확대 및 환경규제 강화로 대기오염 수준이 억제되고 있으나, 실내공기질의 경우는 한정된 공간에서 오염물질이 지속적으로 순환되면서 인체에 영향에 미치는 농도까지 증가될 수 있기 때문에 실내 환경에 대한 인식이 부각되고 있는 실정이다.
실내오염물질로는 외부에서 유입된 먼지, 악취물질(H2S, 메르켑탄, NH3) 등과, 담배연기, 연소가스(CO, NOx, SOx), 라돈, 포름알데히드, VOCs 등의 내부오염물질이 있다. 이러한 실내 오염물질의 경우 실외와 달리 오염될 경우 쉽게 정화되지 않아 하루 중 90% 이상을 실내에서 생활하고 있는 인간에게 단기적으로 또는 장기적으로 인체에 유해한 영향을 끼치고 있다[1]. 이러한 실내오염물질을 제어하는 방법으로는 크게 다섯 가지 방법이 있다. 첫 번째로, 원인물질을 제거 및 교체하는 방법으로 근본적인 제거라는 장점이 있지만 현실적으로 실행이 어려운 단점이 있다. 두 번째로 환기를 하는 경우 오염물질을 제거하기 보단 단순 희석하는 처리방법이다. 세 번째로 짧은 시간에 온도를 증가시켜 흡착된 VOCs 및 오염물질을 탈착시켜 환기시키는 방법으로 Bake out 또한, 단순 환기 일뿐 근본적인 오염물질 제거를 못한다는 단점이 있다. 네 번째로 공지정화시설 설치의 방법이 가장 널리 사용되고 있으나 흡착제의 잦은 교체가 단점으로 부각되고 있다[2]. 마지막 다섯 번째로 백금족 및 전이금속 담지형 촉매를 이용한 저온 산화촉매형 기술들도 제시되었으나 촉매의 비활성화 및 저효율의 문제가 제기되고 있는 실정이다.
이러한 문제로 인하여 최근 앞서 언급한 실내오염물질 처리 방법들의 단점을 보완하기 위하여 높은 제거효율과 경제성 그리고 기존 구조물에 설치가 용이한 제거 기술로 광촉매 기술이 제시되고 있으며 이는 상온, 대기중에서 강한 산화력을 갖고 있고 화학적으로 매우 안정할 뿐만 아니라 경제적인 측면에서도 비교적 저렴한 가격으로, 현재까지 많은 연구가 진행되고 있다.
광촉매는 빛을 받아들여 화학반응을 촉진시키는 물질로써 광에너지를 화학에너지로 변환시키는 TiO2를 반도체 전극으로 사용하여 물을 분해하거나 다른 물질을 산환 · 환원시키는 것을 말한다. 1972년 일본의 Fujishima와 Honda가 물을 수소와 산소로 분해하면서 광촉매 반응의 연구가 시작되었다.
일반적으로 광촉매 반응은 표면상에 반응이 진행되고, 대표적인 TiO2의 광조사에 의한 전자-정공쌍 생성반응을 다음과 같이 나타내었고 일반적인 이론은 아래와 같다.
TiO2 광촉매에 광조사시 Band gap 3.2 eV 이상의 빛에너지를 흡수하여 (1)과 같이 가전자대로부터 전도대로의 전자전이가 일어나게 되어 반응식 (1)의 전자(e−)와 정공(h+)이 생성되며 이렇게 생성된 전자(e−)와 정공(h+)은 산소 및 수분과 반응하여 O2−· (Super Oxide)와 OH· (Hydroxyl Radical)을 생성 한다. 이렇게 생성된 O2−· 와 OH· 에 의하여 오염물질과 반응을 유도하여 2차 오염물질의 발생 없이 완전히 제거할 수 있게 된다[3-7].
이러한 광촉매는 다양한 오염물질에 적용되어 Benzen [8], VOCs [9], NOx [10] 및 악취물질[11] 등 실제 생활에 생성되는 오염물질에 대한 연구가 꾸준히 진행되고 있다.
광촉매를 이용하여 유해가스를 처리하는 경우 상온, 상압에서 조작할 수 있고, 공기를 산화제로 사용할 수 있으며, 최종 생성물이 무해한 물질로 분해되므로 2차 오염의 우려도 없다는 장점이 있다. 또한 수명이 반영구적이고 유지관리가 거의 필요하지 않기 때문에 경제적이다. 이러한 광촉매를 사용할 경우 빛이 조사되는 부분에서만 반응이 이루어지므로, 일반적으로 촉매의 지지체로 사용되는 honeycomb type의 지지체를 사용할 경우 반응이 이루어지는 비표면적이 면에만 해당되기 때문에 반응면적이 낮은 문제점이 제시되고 있다. 따라서 본 연구에서는 상기의 문제점을 보완하고자 다공성 금속촉매 지지체(metal foam) 사용에 대한 연구를 수행하였다. 다 공성 금속촉매 지지체는 3차원 기공구조를 가진 소재로, 넓은 비표면적을 이용하여 광촉매를 분산시키고 동시에 오염물질과 코팅면의 접촉면을 증가시켜 반응성을 향상시키기 위해 사용될 수 있다.
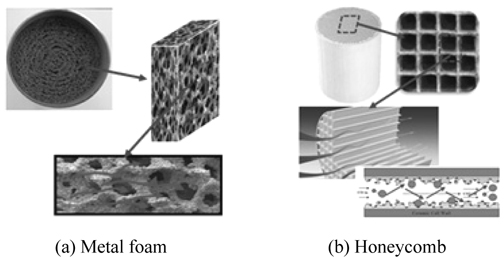
다공체 금속(porous metal)이란 Figure 1에 나타나듯 내부에 수많은 작은 공간(cell)들이 규칙 혹은 불규칙적으로 분산되어 있으며 체적의 50 ~ 95%가 기공으로 이루어진 구조체를 말하며, 기존 재료에 비하여 큰 표면적, 경량성이 우수하며, 열이나 전기의 전도성이 작아 액상이나 공기 투과성이 뛰어난 기능적 특징을 가진다. 또한 metal foam의 기공으로 빛이 조사되어 구조체 내부에 광촉매 반응이 이루어 질 수 있다. 이러한 다공체 금속은 충격흡수제, 여과장치, 열교환기 등 다양한 분야에 사용되고 있으며, 특히 촉매 지지체로써 다공체 금속은 세라믹 허니컴 또는 금속박(metal foil) 허니컴 소재에 비하여 우수한 코팅성 및 넓은 비표면적이 증명되어 SCR, VOCs, 악취처리, 산화촉매 등의 다양한 분야에 적용되고 있다.
광촉매 용액의 제조 및 코팅방법[12]은 다음과 같다. 우선 isopropylalchol (Samchun Co., Ltd), tetraethyl orthosilicate (98%, Acros organic Co.), dimethoxy dimethlsilane (95%, Aldrich Co.)를 일정비율 혼합한 용액에 isopropylalchol과 증류수, 질산 등의 혼합액을 1 h 동안 적하시킨 후 2 h 동안 일정속도로 교반하여 코팅 첨가제 용액을 제조하였다.
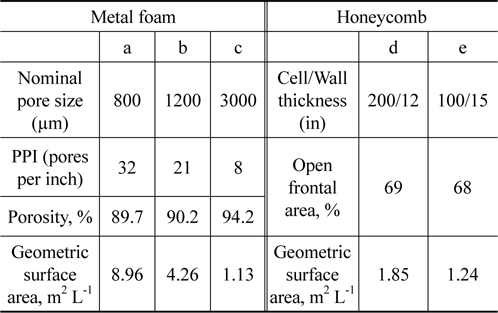
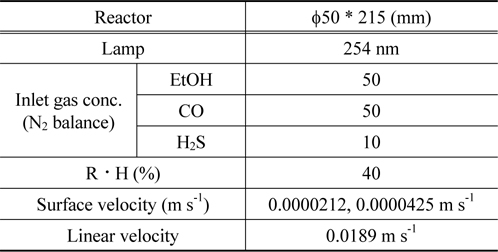
먼저 본 연구에서 사용된 TiO2 및 Pt/TiO2 촉매의 코팅용액 제조 방법은 다음과 같다. 순수 TiO2의 경우 Sol type의 STS-01 (Ishihara Co.)를 사용하였다. Pt/TiO2 촉매의 경우는 담지된 Pt의 함량을 TiO2 담체의 무게를 기준으로 0.1 wt%만큼 담지하였다. Sol type의 STS-01 (Ishihara Co., Ltd.) TiO2의 고형분을 고려하여 활성금속의 함량을 무게비로 결정한 후 계산한다. 계산된 양만큼의 활성금속을 전구체를 제외한 순수 활성금속 의 양만큼을 계산 한 후 증류수에 녹인다. 이때 사용된 활성금속의 전구체는 수산화백금(Pt(OH)2, 16.13%, SNS Co.)을 사용하였다. 백금 전구체가 증류수에 완전히 녹은 수용액은 진한 노란색을 띈다. 다음으로는 정량된 지지체에 천천히 백금수용액을 혼합한다. 앞선 방법으로 준비된 TiO2 및 Pt/TiO2 혼합액을 앞서 제조된 코팅 첨가제와 isopropylalchol, 증류수 혼합액에 적하 및 교반하여 광촉매 용액을 제조하였으며 적하 및 교반 조건은 바인더의 제조법과 같다. 지지체에 광촉매코팅은 pyrex 관내에 지지체를 수직으로 세운 후 하부에 밸브를 연결하여, 제조된 광촉매 용액을 pyrex 관내에 채워 놓은 후 밸브와 연결된 정량펌프를 이용하여 일정량을 펌핑하여 지지체를 코팅하였으며, 하강속도는 약 4 mm min−1으로 하였다. 이때 사용된 지지체는 다음 Table 1과 같은 조건의 지지체를 사용하였다.
[Table 1.] Properties in the honeycomb and the metal foam support
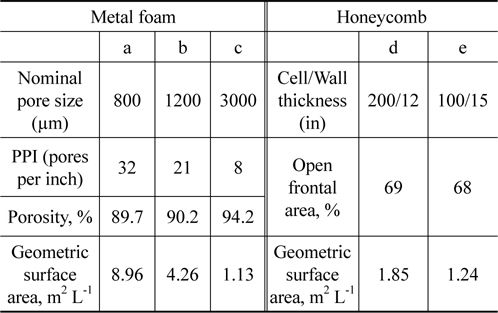
Properties in the honeycomb and the metal foam support
코팅이 완료된 지지체는 1 h 동안 실온 건조하여 먼저 수분 및 기타 휘발물질들을 제거한 후 추가적으로 105 ℃에서 1 h 동안 건조를 수행하였다. 이후 10 ℃ min−1의 승온속도로 관형로(tubular furnace)에서 원하는 온도로 상승시킨 후 그 온도에서 2 h 공기분위기에서 소성하여 소성촉매를 제조하였다. 또한 환원공정이 필요한 촉매의 경우 앞서 설명한 방법으로 코팅, 건조후 소성과정이 진행된 촉매를 다시, 10 ℃ min−1의 승온속도로 관형로(tubular furnace)에서 원하는 온도로 상승시킨 후 그 온도에서 2 h 동안 30% H2/N2 gas를 이용하여 환원시켜 제조하였다.
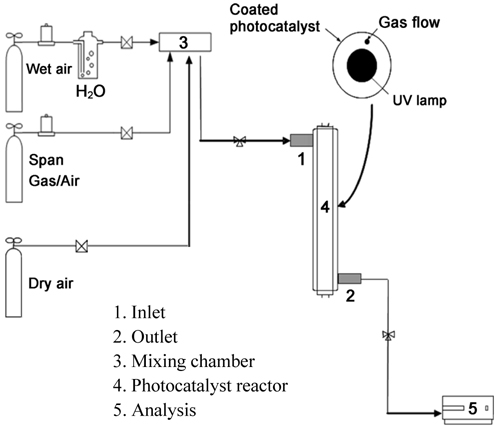
본 연구에서는 photocatalysis 시스템을 비교하기 위하여 Figure 2와 같이 연속식 반응장치를 구성하였다. 반응기 내의 가스의 주입은 MFC (mass flow controller)를 사용하였다. 광촉매 반응에 사용된 lamp는 Table 2에 나타낸 것처럼 주 파장이 254 nm인 lamp로는 GL20 (Sankyo Denki Co.)를 사용하였다. 수분의 경우 2중 jacket 형태의 bubbler에 공급되는 N2를 폭기하여 수분을 함유하게 함으로써 반응기에 수분을 공급되게 하였다. 이때, 공급되는 수분의 양을 일정하게 하기 위해 bubbler 외각에 circulator를 이용하여 일정 온도(45 ℃)의 물을 순환시킴으로써, N2 가스가 bubbler를 통과하여 반응기에 수분을 공급하는 양이 일정하게 하였다.
[Table 2.] Experimental conditions on reaction system
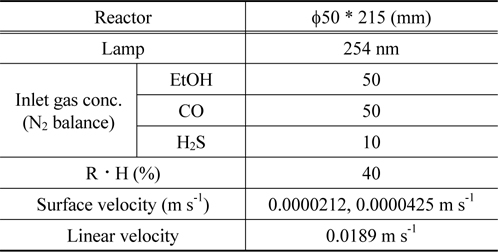
Experimental conditions on reaction system
광촉매 산화 실험은 우선 대상 가스에 대하여 초기농도를 측정하기 위하여 공관에 희석가스(N2)와 유해가스를 주입하여 정상상태에 각 가스의 분석기 또는 검지관을 사용하여 초기농도를 측정하고, 습도계(Center310, G-won Hitech Co.)로 상대습도를 측정하였다.
① 코팅된 지지체 및 lamp를 반응기에 장착한다.
② 건 N2와 습 N2 (bubbler)를 통하여 수분을 함유한 N2를 흘리고 촉매를 활성화하기 위하여 lamp를 키고 30분간 전처리 한다.
③ 전처리 후 유해가스를 주입하여 생성물의 농도가 일정해지면 각 가스의 분석기 또는 검지관을 사용하여 농도를 측정한다.
④ 유량, 상대습도, 농도 등의 변수에 따라서 정상상태에서 농도를 측정한다.
또한, 본 연구에서 실시한 광촉매 산화반응 실험에 관한 운전변수를 Table 2에 나타내었다.
2.3.1. 주사전자현미경(field emission scanning electron microscope, Fe-SEM)
광촉매가 지지체 표면에 고분산된 정도를 조사하기 위하여 JEOL사의 JSM-6599F를 사용하여 Fe-SEM 분석을 수행하였다.
시편으로 입사된 전자가 방전되지 않을 경우를 대비해 시편을 탄소막의 진공 증착시켜 백금으로 전도성 코팅을 하여 측정하였다. 또한 SEM의 전자총, 경통과 시편실의 진공을 유지하기 위해서 9,63 × 10−5 Pa 진공도를 가진 유확산 펌프를 사용하였다.
2.3.2. 광전자분광기(X-ray photoelectron spectroscopy, XPS)
XPS 분석은 Thermo사의 Alpha-K을 사용하였으며, excitation source로써 Al Kα monochlomatic (1486.6 eV)를 사용하였다. 촉매를 약 100 ℃의 온도에서 24 h 건조하여 포함되어 있는 수분을 완전히 제거한 후 XPS 기기의 진공도를 10−6 Pa로 유지하기 위하여 표면 sputtering 및 etching을 하지 않고 하였다. 시료내에 존재하는 Pt, Ti, C, O 원소는 wide scanning spectrum으로 분석하여 binding energy와 intensity를 확인하였다.
2.3.3. 비표면적분석기(brunauer emmett teller, BET)
촉매의 비표면적 및 pore size 측정은 Micromeritics Co.의 ASAP 2010C를 사용하였으며 BET (Brunauer-Emmett-Teller)식을 이용하여 비표면적을 구하였으며, pore size distribution은 Kelvin식을 통해 유체의 meniscus의 평균반경과 상대압력에서의 흡착층의 두께를 이용하여 세공의 크기를 계산하는 방법인 BJH (Barrett-Joyer-Hanlenda)법에 의하여 계산하였다. 이때 각각의 시료는 110 ℃에서 3 ~ 5 h 동안 진공상태로 degassing한 후 분석하였다.
일반적인 광촉매 산화반응은 TiO2가 광원에 의하여 광여기 되어 산화반응을 유도하는 반응(1)과, 250 nm 이하의 자외선 파장을 강하게 흡수하는 VOCs 및 악취 오염물질이 광원에 의하여 직접 광분해되는 반응(2) 두가지 반응이 동시에 진행된다[13]. 이 두 반응을 비교하기 위해서는 광촉매가 있을 때 반응과 광촉매가 없는 반응을 비교함으로써 구분할 수 있다. 또한 직접적인 광분해되는 오염물질의 전환율을 배제함으로써 본 실험에서 사용되는 광촉매의 정확한 반응활성을 구할 수 있다. 이러한 광원의 직접 광분해 영향을 파악하기 위하여 254 nm 파장을 가진 UV lamp를 사용하여 본 실험에서 사용되는 오염물질(C2H5OH (EtOH), H2S, CO)의 분해반응 실험을 실시하였다. 그 방법은 우선 코팅되지 않은 지지체로 직접 광분해 후 배출되는 미반응 물질을 측정하여 반응효율을 측정하였다.
Figure 3에서 알 수 있듯이 광분해에 의한 오염물질의 제거율은 0%를 나타내어 이를 통해 본 실험에서 사용되는 오염물질의 경우 광분해에 의한 분해는 진행되지 않으며, 앞으로 진행될 실험에서 보이는 반응활성은 광촉매에 의한 반응활성임을 확인할 수 있다.
먼저, 동일한 체적을 가지는 기본 세라믹 재질의 촉매 담체인 honeycomb과 metal foam 담체에 광촉매를 코팅하여, 코팅상태를 확인하고자 SEM 분석을 수행하여 Figure 4에 나타내었다. Figure 4에 나타나듯 honeycomb 또는 metal foam의 두가지 지지체에 TiO2의 코팅 표면이 균일하며 결정형을 나타내지 않음을 보이고 있다. 특히 metal foam 지지체의 경우 crack구조를 나타내어 honeycomb 지지체보다 높은 비표면적을 나타낼 것으로 추측된다.
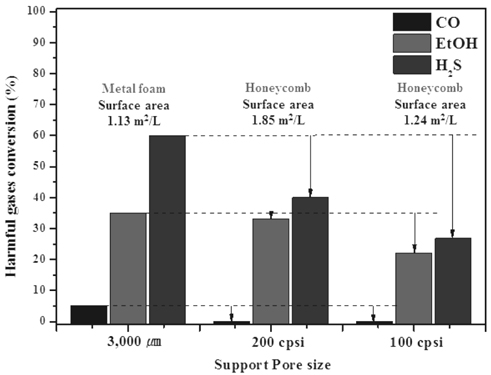
이러한 코팅된 TiO2의 각 오염물질에 대한 전환율을 측정하여 그 결과를 Figure 5에 나타내었다. 실험에 사용된 honeycomb의 경우 100 cell와 200 cell의 honeycomb을 사용하였으며, 금속재질의 공극의 크기가 3,000 µm인 metal foam을 사용하였다. 각각의 코팅촉매의 표면적을 BET를 이용하여 분석하여 그 값을 Table 1에 나타낸 결과, 허니컴의 경우 1.24 m2 L−1, 1.85 m2 L−1의 값이 측정되었으며, metal foam의 경우에는 1.13 m2 L−1의 비표면적을 보였다. 이러한 비표면적에 따른 코팅촉매의 H2S, EtOH 및 CO에 대한 반응활성을 실험을 수행하여 Figure 5에 나타내었다.
먼저, 오염물질에 따른 반응활성을 확인한 결과 H2S가 가장 높은 제거율을 보였으며, 그다음으로 EtOH, CO 순서로 낮은 제거율을 나타내었다. 특히 CO의 경우 모든 촉매에서 10% 미만의 매우 낮은 제거율을 확인할 수 있었다. 특히 100 cell와 200 cell의 honeycomb의 반응활성을 비교하면 200 cell의 honeycomb이 100 cell honeycomb 보다 더 넓은 비표면적을 보였으며 그에 따라 상대적으로 우수한 반응활성을 보였다. 하지만 비표면적이 1.24 m2 L−1을 나타내었던 honeycomb과 상대적으로 낮은 비표면적인 1.13 m2 L−1를 보인 metal foam의 반응활성을 비교해본 결과 상대적으로 적은 비표면적을 보였던 metal foam에서 더 우수한 반응활성을 보였다. 이러한 반응활성의 차이는 앞서 언급했듯이, 일반적인 촉매의 경우 촉매의 비표면적이 커질수록 반응활성이 유리해 지지만, 광촉매를 사용할 경우 기본적으로 빛이 조사되는 부분에서만 반응이 이루어지기 때문에 honeycomb을 지지체로 사용할 경우 반응이 이루어지는 빛이 조사되는 면이 적기 때문에 상대적으로 지지체 내부까지 빛이 조사될 수 있어 빛이 조사되는 면적이 더 넓은 metal foam에서 우수한 반응활성을 보임을 확인하였다. 따라서 광촉매의 경우 honeycomb 지지체 보다 많은 공극구조를 지니고 있는 metal foam 지지체가 반응에 유리함을 확인할 수 있었다.
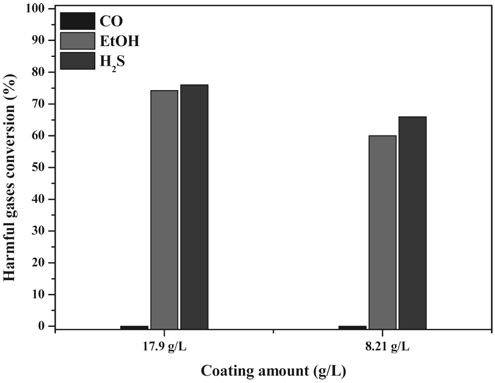
추가적으로 이러한 metal foam 표면에 코팅된 촉매량에 따른 반응활성을 확인하여 Figure 6에 나타내었으며, 촉매량은 코팅횟수의 조절을 통하여, 8.21 g L−1와 17.9 g L−1 두가지 경우에 대하여 수행하였다.
실험 결과 촉매 담지량이 증가할수록 반응활성이 증가하였지만, 촉매 담지량의 증가량에 비하여 반응활성은 미량 증가하였다. 따라서 촉매의 담지량과 반응활성의 선형적인 관계를 확인할 수 없었다.
3.3. metal foam의 구조적 특성에 따른 반응활성
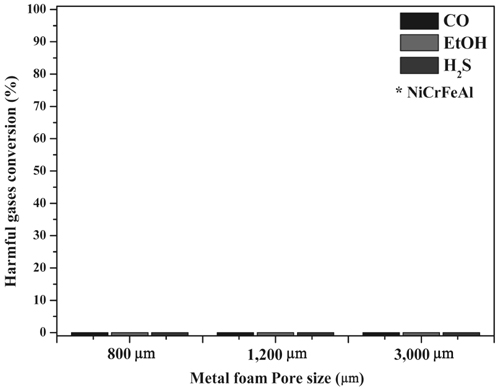
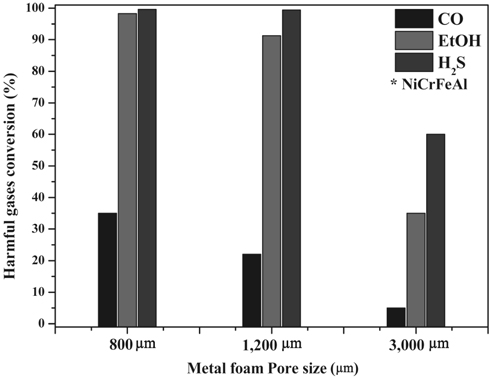
앞 절에서의 실험을 통하여 광촉매의 지지체로 honeycomb보다 metal foam의 형태의 지지체가 더 우수한 반응활성을 보임을 확인하였다. 이에 따라 metal foam의 구조적 특성이 반응활성에 미치는 영향을 확인하고자 metal foam을 Table 1에 나타나듯 공극의 크기가 800 µm, 1,200 µm, 3,000 µm로 각기 다른 공극크기의 metal foam을 지지체로 하는 광촉매를 제조하여 반응활성을 수행결과를 다음 Figure 7에 나타내었다.
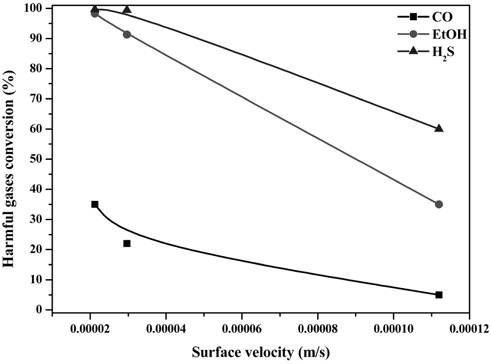
그 결과, 공극크기가 작아질수록 CO, EtOH, H2S 모든 가스에서 반응활성이 증가함을 확인하였다. 특히 800 µm와 1,200 µm의 경우 H2S의 경우 차이가 매우 미미하였으며, EtOH와 CO에서 3 ~ 10%의 활성차이를 보였으나, 3,000 µm의 공극을 지닌 metal foam의 경우 그 반응활성이 크게 감소함을 확인하였다. 이러한 반응활성 실험을 수행하여 각 지지체의 surface velocity에 따른 반응활성을 계산하여 Figure 8에 나타내었다.
여기서 언급된 surface velocity는 다음과 같은 식을 통하여 구할 수 있다.
일반적으로 촉매반응에서는 space velocity가 촉매의 부피당 처리가스의 능력을 나타내는 index로 활용되지만, 광촉매의 경우 촉매의 표면반응이 주반응이기 때문에 촉매의 표면을 기준으로 하여 촉매의 표면적당 처리가스의 능력을 나타내는 surface velocity를 index로 활용하였다. 위와 같은 식을 통하여 Table 1에 나타낸 800 µm, 1,200 µm, 3,000 µm의 표면적을 계산하여 surface velocity를 도출한 결과 0.0000212 ~ 0.000111 m s−1의 조건을 확인하였다. 그에 따른 반응활성은 surface velocity가 증가할수록 반응활성이 감소하였다.
앞선 실험을 통하여 다양한 지지체에 광촉매 TiO2를 코팅하여 그에 따른 반응활성을 확인하였다. 가스별 반응활성을 비교하면, 가장 효율이 우수하였던 800 µm의 metal foam을 기준으로 H2S의 제거효율 100%, EtOH의 제거효율은 95% 이상의 매우 우수한 효율을 보였지만 CO의 경우 40% 미만의 낮은 제거효율을 보였다.
이에 본 절에서는 이러한 CO 제거 효율을 증진시키기 위하여 앞서 실험을 수행한 TiO2 광촉매에 귀금속을 담지하여 촉매를 제조하였으며, 제조된 촉매의 광촉매의 반응활성을 수행하여 Figure 9에 나타내었다.
귀금속의 경우 광촉매의 광활성 과정에서 발생된 전자와 정공을 효과적으로 분리하여 광분해 반응에 사용되도록 하여 전자와 정공의 재결합을 막아주는 역할로 알려져 있는 Pt를 사용하였다[14-16]. Pt의 함량은 TiO2 고형물 기준 0.1 wt%로 고정하여 촉매를 제조하였으며, 앞선 실험에서 사용된 TiO2 광촉매와 동일한 조건에서 열처리를 수행하였다.
Pt를 첨가하여 제조한 촉매에서 H2S 및 EtOH의 경우 모두 90% 이상의 우수한 반응활성을 보였지만, Pt가 첨가되지 않은 순수 TiO2를 코팅한 촉매에 비하여 미량 효율이 감소함을 나타내었다. 또한, CO의 제거율도 증가하지 않음을 보였다. 이후 Pt/TiO2 촉매를 30 vol% H2/N2 가스를 이용한 환원처리를 통하여 촉매를 제조하여 광촉매 반응활성 실험을 수행하였다. 환원촉매의 반응활성은 환원처리를 수행하지 않은 Pt/TiO2 소성촉매에 비하여 H2S와 EtOH의 경우 그 반응활성이 소폭 증가함을 보였으며, 특히 CO의 반응활성은 100%로 크게 증가된 반응활성을 나타냈다. 이러한 반응활성 결과를 통해 Pt/TiO2 소성촉매에 비하여 Pt/TiO2 환원촉매에서 우수한 반응활성을 보임을 확인할 수 있었다.
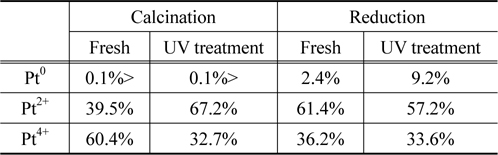
이러한 환원처리의 광촉매 활성증진 인자를 확인하기 위하여 표면 valence state 특성을 XPS 분석으로 확인하여, 그 결과를 Table 3에 나타내었다. 이때, 소성촉매 및 환원촉매뿐만 아니라 광촉매 광반응에 의한 촉매 표면의 valence state의 변화를 확인하기 위하여 UV 조사를 수행한 촉매에 대해서도 XPS 분석을 수행하였다.
[Table 3.] Calcination catalyst and a reduction catalyst surface Pt valence state comparison
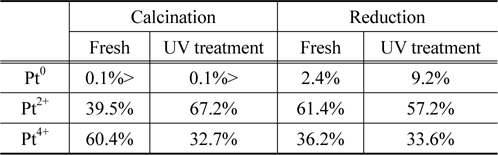
Calcination catalyst and a reduction catalyst surface Pt valence state comparison
먼저, 반응활성의 증진을 보이지 않았던 Pt/TiO2 소성촉매의 경우 촉매의 표면 Pt의 valence state에서 Pt2+의 비율은 39.5% Pt4+의 비율은 60.4%로 나타났으며 Pt0에 해당하는 비율은 0.1% 미만으로 매우 낮은 비율 나타내었다. 또한 광반응에 의한 Pt의 valence state의 변화를 확인한 결과 Pt2+의 비율이 39.5%에서 67.1%로 크게 증가함을 확인할 수 있었으며, 반대로 Pt4+에 해당하는 비율은 60.4%에서 32.8%로 크게 감소함을 확인하였다. 이러한 결과를 통해 광반응에 의하여 촉매 표면의 Pt가 환원됨을 알 수 있었다. 하지만 Pt0에 해당하는 비율은 0.1% 미만으로 큰 변화를 확인할 수 없었다. 반면, 상대적으로 우수한 CO의 반응활성을 보였던 Pt/TiO2 환원촉매의 경우 촉매 표면에 존재하는 Pt의 valence state는 Pt0, Pt2+, Pt4+의 순서로 2.4%, 61.4%, 36.2%의 비율을 나타내었다. 이는 소성촉매와 비교하여 Pt0 및 Pt2+의 비율이 크게 증가한 형태이며, 이러한 결과는 30 vol% H2/N2 가스에 의하여 높은 온도에서 열처리를 통하여 표면 Pt가 환원되었기 때문으로 판단된다. 그리고 Pt/TiO2 환원촉매의 광반응에 의한 표면 Pt valence state의 변화는, Pt0 비율은 9.2%로 크게 증가하였으며, Pt2+의 비율은 57.2%, Pt4+의 비율은 33.6%로 일정량 감소함을 확인하였다. 이러한 결과를 통하여 Pt/TiO2 촉매의 Pt valence state가 반응활성의 영향인자임을 확인할 수 있었으며, 특히 Pt0 형태가 증가할수록 CO의 반응활성이 증진됨을 확인할 수 있었다. 이러한 Pt0는 Seo et al. [17]에 따르면 CO와의 결합력이 Pt2+ 및 Pt4+에 비하여 매우 약한 결합력을 나타내어 CO 반응활성에 있어서 우수한 반응활성을 나타낸다고 보고되고 있다. 또한, 고온에서 환원처리된 촉매의 경우, 일반적으로 환원성 산화물에 담지된 금속 촉매를 높은 온도에서 환원처리 하였을 때 나타나는 강한 금속-지지체 상호작용으로 담지 촉매의 화학흡착 성질과 촉매 성질이 크게 달라지는 현상을 포괄적으로 설명되는 SMSI (strong metal support interaction)에 의하여 금속-지지체 사이 간극점에 새로운 활성 site가 생성된다. 이러한 현상에 의하여 표면의 Pt종의 분산도가 증가하게 되며 표면에 들어나는 Pt종이 증가하여, 상대적 소성촉매에 비하여 표면의 Pt 종이 더 쉽게 환원된 것으로 판단된다[18-20].
실내대기오염물질 처리를 위한 광촉매 실험을 통해 다음과 같은 결론을 도출할 수 있었다.
일반적인 실내오염물질 및 VOCs의 경우 UV광을 이용하여 광분해를 시킬 수 있지만, 일부 오염물질 H2S, EtOH 또는 CO 등의 경우 UV 광에 의한 광분해 반응이 진행되지 않으므로, 광촉매에 의한 광분해가 필요한 물질이다.
다양한 지지체를 이용한 광촉매 코팅 실험결과, 일반적으로 촉매 지지체로 사용되는 honeycomb과 metal foam의 경우, 동일한 조건에서 지지체 내부까지 UV 빛이 조사되는 metal foam에서 우수한 반응활성을 보임을 확인하였다. 따라서, 광촉매의 경우 촉매 표면에 조사되는 빛의 양과, 촉매 지지체 내부까지 빛이 조사될 수 있는 구조가 반응활성에 큰 영향을 미친다.
동일한 조건의 UV 광원과, 지지체 구조 및 재질, 그리고 동일한 체적의 촉매를 이용하여 광촉매 광분해 반응을 수행한 결과, 촉매의 표면적이 더 큰 촉매에서 더욱 우수한 반응활성을 보였으며, 이러한 실험을 통하여 광촉매의 경우 촉매의 체적보다는 반응할 수 있는 표면적에 의하여 반응활성에 큰 영향을 미침을 확인하였다.
다양한 오염물질인 H2S와 EtOH에서는 광촉매 TiO2 코팅만으로도 100%에 가까운 제거효율을 얻을 수 있었지만, CO의 경우 매우 저조한 반응활성을 나타내었으며, 이는 TiO2에 Pt를 첨가하여 환원공정을 거침으로써 해결할 수 있다. 이러한 반응활성의 증진의 영향을 확인하고자 촉매 표면의 valence state분석을 수행한 결과, 표면 Pt의 valence state의 상태가 Pt2+, Pt4+종으로만 존재할 경우 CO의 제거효율의 증진을 확인할 수 없었으며, Pt0 종의 생성 혹은 증가함에 따라 CO 제거효율이 증진됨을 확인하였다. 따라서 Pt0 종이 CO반응 활성증진에 영향을 미치며, 이러한 Pt0의 경우 광촉매 TiO2에 Pt를 담지한 후 환원공정을 통하여 표면 Pt0종을 증가시킬 수 있다.