The nanotoxicity of ZnO nanoparticles used in cosmetics and tire industry is one of emerged issues. Herein, the removal of ZnO nanoparticles dispersed in aqueous phase and its ecotoxicity were investigated. In the short-term exposure for fertilized eggs (
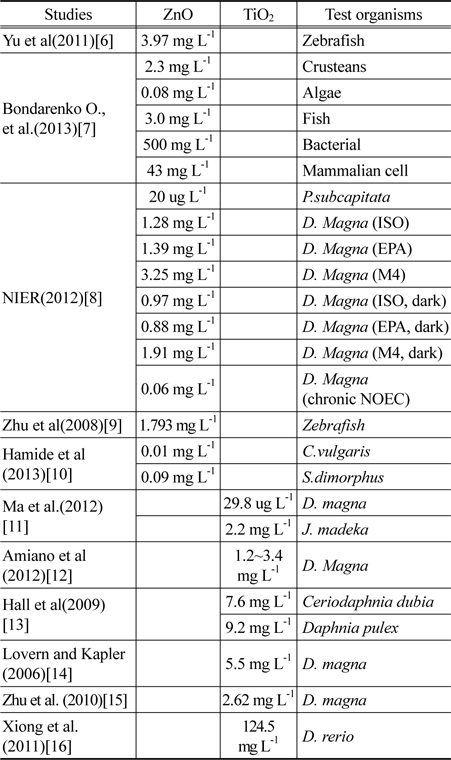
최근 나노물질의 독특한 기능성이 부각되면서 전세계적으로 나노물질의 사용량은 매우 급증하고 있다. Woodrow Wilson Center PEN CPI의 2011년 보고에 따르면 2005년~2010년까지 나노물질 사용량의 연평균 증가율은 468%에 달할 정도이다[1]. 그러나 이러한 나노물질이 어떠한 유해성을 갖는지에 대한 연구는 이제 시작단계이다. 나노 물질의 유해성에 대한 연구는 그동안 주로 Ag에 대해 많이 수행되어져 왔고, 광촉매, 자외선차단제 등으로 TiO2의 사용량이 급증하면서 TiO2 나노입자에 대한 유해성 조사가 수행되었으며, 최근에 ZnO 나노입자에 대한 유해성 조사가 수행되고 있다(Table 1). ZnO 나노입자는 자외선차단효과가 있어 썬크림과 같은 화장품의 원료로 많이 사용되고 있고, 다양한 공업적 용도로 사용되고 있는데 특히 타이어의 내마모제로 타이어 제조시 카본과 혼합하여 사용되고 있다. 화장품에 사용된 ZnO 나노입자는 소비자가 사용 후 세안시에 바로 하수처리장으로 유출되며, 타이어에 사용된 ZnO 나노입자도 타이어 마모시에 카본과 함께 대기중으로 배출되고 지면에 내려앉게 된다. 이후 비가 오면 빗물과 함께 하천으로 유입된다[2,3]. 비의도적 나노물질의 환경배출은 궁극적으로 생태계에 영향을 미칠 수 있는 인자로 작용하며 수서생물에 노출될 경우 다양한 생물에서 독성을 유발시킬 가능성이 높다(Table 1). 따라서 수계상에서 이러한 ZnO 나노입자의 유해성평가와 함께 이를 무해화하는 기술개발이 필요하다.
[Table 1.] Summary of ecotoxicity (EC50s) of ZnO, TiO2
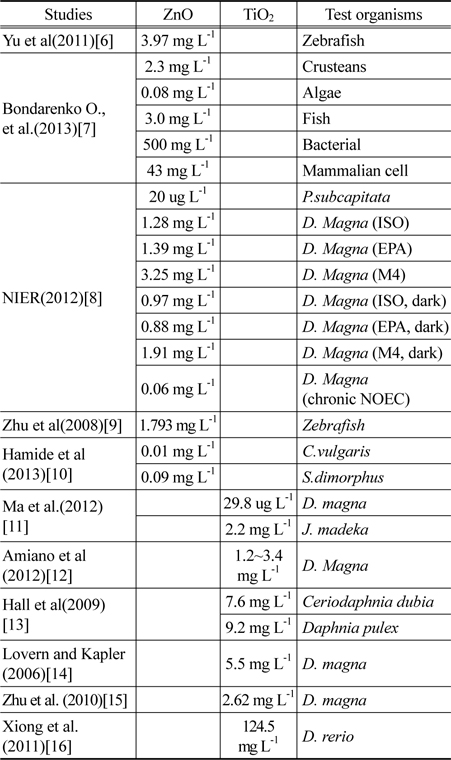
Summary of ecotoxicity (EC50s) of ZnO, TiO2
수계내 존재하는 나노입자를 제거하기 위하여 전기응집법이 적용된 사례가 있다. TiO2 나노입자를 수산화철과 함께 전기응고시켜 높은 제거효율을 보인 경우도 보고되었다[4]. ZnO 나노입자 제거에도 사용할 수 있으나, 추가되는 철염이나 철전극을 사용시 용액내 산화철의 형성으로 탁도가 증가하는 문제가 발생한다. 또한 생성된 철염에 의한 추가적인 생물학적 독성이 발생될 수 있다. 이에 염처리법을 통해 ZnO 나노입자를 용해도가 낮은 입자로 변환시키고자 하는 노력들이 진행되고 있다[5]. ZnO 나노입자의 독성은 주로 Zn2+ 이온에 의한 것으로 해당 이온발생을 억제하면, 수계내 Zn 나노입자가 노출되어도 독성효과를 최소화 시킬 수 있다. 즉 황처리를 통해 용해도 상수값(pKa)이 극히 낮은 ZnS로 변환시켜 독성을 감소시키고자 하였다.
또한, 본 연구에서는 물고기를 이용하여 수계상의 ZnO 나노입자의 유해성 평가 실험을 수행하였고, 유해성을 저감하기 위해 수계상에서의 ZnO 나노입자의 특성을 조사한 후, 이를 이용하여 수계상의 ZnO 나노입자를 화학침전을 통해 제거하는 실험을 수행하였다. 또한, 침전된 물질에 대한 물벼룩 급성독성평가를 수행하여 독성저감을 확인하였다.
수계상에서의 ZnO 나노입자의 유해성을 평가하기 위해 표준시험종인 물벼룩 급성독성시험과 물고기를 이용한 생태독성 실험을 수행하였다. 물벼룩급성독성시험은 부화후 24시간이내의 개체를 이용하였으며 M4 배지를 이용하였다. 노출조건은 21 ± 1 ℃, 명 : 암 = 16 : 8이었으며 노출 24시간 후 치사를 관찰하였다. 독성값은 반수영향농도(EC50)를 사용하였다. 물고기독성시험은 OECD 표준독성 시험종인
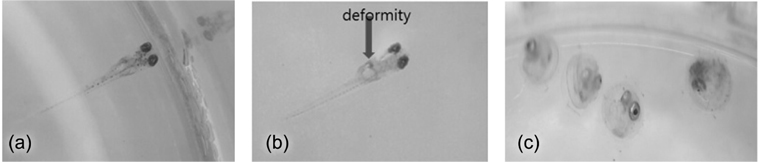
물고기부화실험은 대조군와 ZnO 나노입자의 농도를 2.5, 5, 10 mg L−1로 조절한 실험군을 각각 4set를 준비한 후 각 set 마다 수정란을 5개씩 투입한 후에 챔버에서 25 ℃를 유지하면서 부화율, 기형성 등을 확인하였다.
나노물질은 그 물질이 노출된 매질 및 온습도 등에 따라 다양한 물성 변화를 보이게 된다. 수계 노출된 상태에서도 수계내 존재하는 다양한 염에 의해 대상 나노입자의 표면전하값이 변하게 되어 입자의 응집성이 달라진다. 따라서 수계내 존재하는 ZnO 나노입자를 효율적으로 제거하기 위해서는 우선 대상 나노입자의 수계 노출시 특성 변화를 평가해야 한다. 가장 기본적인 입자의 표면전하와 입도분포, 수동력학적 크기, 전자현미경학적 해석 등이 필요하다. 이를 위하여, 본 연구에서는 수계상에서의 ZnO 나노입자의 특성을 조사하기 위해 elctrophoretic light scattering (ELS) 분석기(ELS-Z. PHOTAL)를 이용하여 hydro dynamic diameter (HDD) 및 제타전위를 조사하였고, mutiful light scattering (MLS) (Turbiscan Lab, Formulation)를 이용하여 침전속도를 조사하였다.
ZnO 나노입자의 농도가 100 mg L−1인 조건에서 Na2S와 Na2HPO4 0.05~0.25 M을 투입하여 혼합한 후 침전을 관찰하였고, 침전체를 투입한 직후에 용액내 입자침전에 의한 색상변화를 UV-vis 분광기(UV-18000, Shimadzu)를 이용하여 분석하였다. 또한 ICP (ICP-AES, Shimadzu ICPQ1000)를 통해 수계상에서의 Zn의 농도변화를 관찰하였고, 이를 기초로 제거율을 계산하였다. 투과전자현미경(TEM, JEOL JSM-6700F) 분석과 EDX (7200-H, Horiba) 분석을 수행하여 침전물의 형태와 침전물의 구성을 확인하였다.
2.4. ZnO 나노입자, ZnS, Zn3(PO4)2의 급성독성평가
ZnO의 유해성을 저감시키기 위해 Zn을 ZnS, Zn3(PO4)2로 합성하여 침전시켰다. 그러나 이 합성물질이 또 다른 유해성을 갖는다면 이 침전법은 아무 의미가 없기 때문에, ZnO 나노입자와 ZnS, Zn3(PO4)2 화합물에 대한 각각의 독성테스트를 수행하여 비교하였다. 실험군으로 사용한 물벼룩은
산화아연은 산화티타늄과는 달리 수계에서 쉽게 이온화하기 때문에 생물독성이 비교적 크게 나타난다. 수계상에서의 ZnO 나노입자의 생태독성 평가를 수행하였고, 그 결과를 Figure 1에 나타내었다. 시험생물종은 송사리(
3.2.1. 분산 안정성
ZnO 나노입자가 수계에 노출되었을 때의 분산안정성을 조사하기 위해 10 mg L−1의 ZnO 나노입자를 OECD TG 303에 의해 제조한 합성하수(Table 2)에 혼합시킨 후 생물시료 교반기로 초당 0.5회 정도로 최대 24시간 동안 교반을 유지한 후 TEM 분석을 수행하였다. 합성하수에서의 ZnO 나노입자는 고분산된 형태이며 초기에는 개별적으로 존재하는 입자형태를 보이지만 24시간이 지나면 입자들간의 응집이 발생하여 뭉친 형태를 보였다(Figure 2).
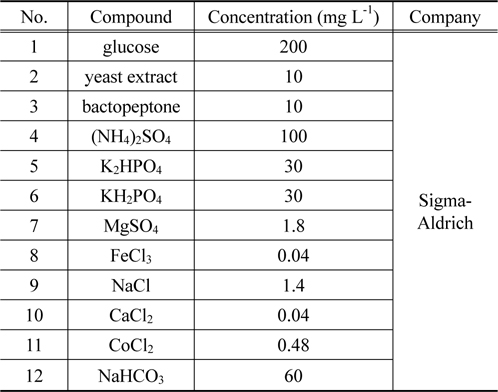
[Table 2.] Composition of synthesized sewage
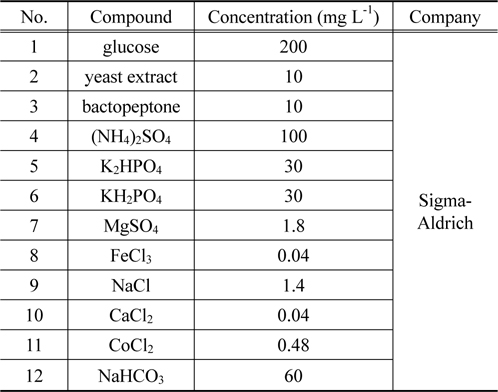
Composition of synthesized sewage
3.2.2. ZnO 나노입자의 HDD, 제타전위 및 침전속도
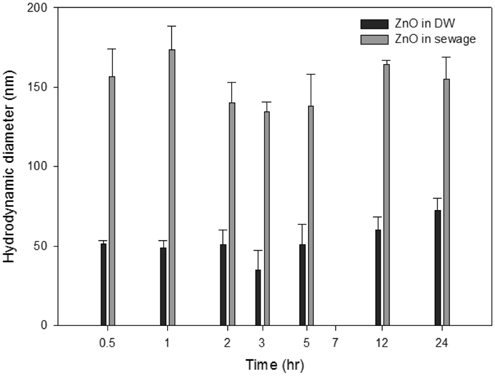
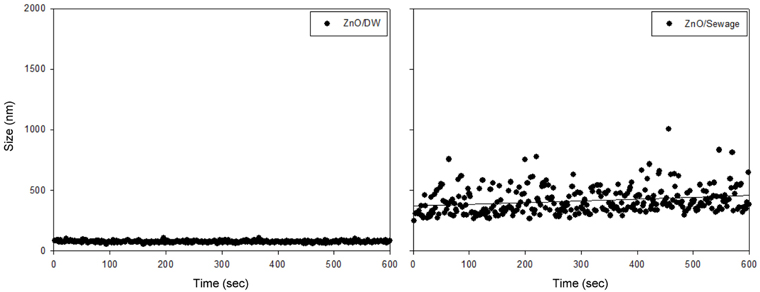
합성하수 및 증류수(distilled water)에 10 mg L−1의 ZnO 나노입자를 분산시킨 후 ELS를 이용하여 시간에 따른 HDD, 제타전위 및 침전속도를 조사하였다. Figure 3은 시간에 따른 HDD의 변화를 나타낸 것이다. 액상 콜로이드 시료라서 증류수에 노출시킨 경우 입자의 분산성이 24시간 이상 유지되어 50~70 nm 크기를 유지했지만, 합성하수에서는 150 nm의 큰 크기를 보여 합성하수에서 입자간의 응집이 더 잘 이루어지는 것을 알 수 있었다.
Figure 4는 시간에 따른 응집속도를 계산하기 위하여 입자의 크기변화를 실시간으로 측정하여 나타낸 것이다. 개별입자 크기가 100 nm 미만인 ZnO 나노입자를 증류수에 분산시 최소 HDD는 60 nm를 보이며, 합성하수에서는 그보다 큰 250 nm를 보였다. 응집속도는 분산 용액의 종류에 의존했으며, 초기 응집속도는 대체로 10−17~10−28을 나타내어 초기에는 고분산성을 유지하였다. 합성하수보다는 증류수에 있을 때 초기 응집속도가 더 작았으며, 합성하수에 존재하는 다양한 유기물에 의해 약간의 응집성이 발생하고 있으나 비교적 안정적인 상태를 유지하고 있었다.
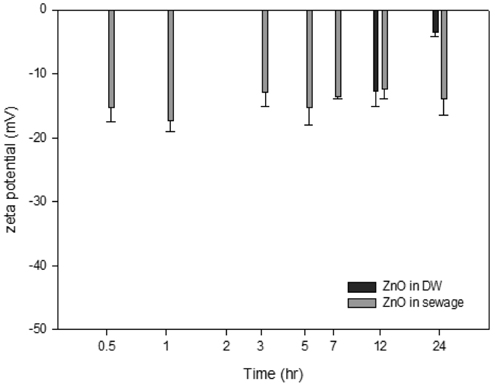
Figure 5는 제타전위 분석 결과를 나타낸 것이다. 제타전위는 분산된 입자의 표면전하를 측정하는데, 액상에 분산된 입자수가 측정한계(105~1012개mL−1) 보다 작게 되면 장치의 한계로 인해 측정되지 않는다. 합성하수에서는 제타전위가 −15 ~ −20 mV를 보였으나 증류수에서는 제대로 측정되지 않았다. 제타전위가 크면 클수록 입자는 불안정하기 때문에 외부와 반응하여 안정한 상태로 가고자 하는 성질을 갖는다[19]. 합성하수에 분산된 ZnO 나노입자는 −15 ~ −20 mV의 제타전위를 나타내고 있어서 비교적 안정적인 분산 안정성을 보이고 있다. 분산성이 높게 되면, 해당 하수내 ZnO 나노입자가 장기간 체류하면서 수생 생물종에게 영향을 미칠 확률을 증대시킬 수 있다.
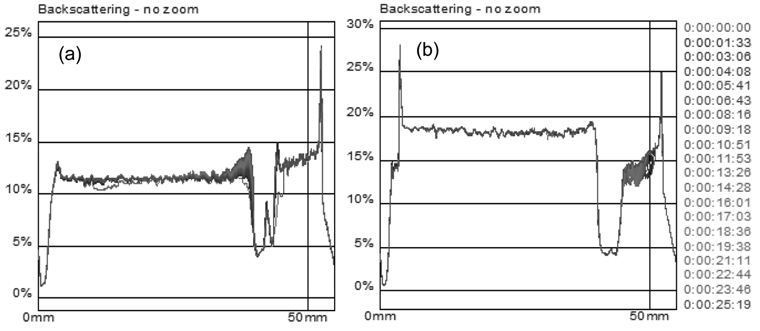
Figure 6은 침전속도를 분석한 결과를 나타낸 것이다. 10 mg L−1의 ZnO 나노입자를 합성하수와 증류수에 분산시킨 후에 바로 MLS 분석을 통해 침강속도를 측정하였다. MLS에서는 분당 침전량을 % min−1으로 계산하고 해당값이 클수록 입자의 안정성이 감소하는 것으로 평가하게 된다. 입자가 안정적으로 분산될 경우에는 침강이 발생하지 않아서 시간에 따른 후방산란 그래프가 일정한 값을 보이며, 그렇지 않고 침강이 발생할 경우에는 후방산란 그래프가 시간에 따라 점점 가라앉는 형태로 나타난다. 1시간 동안 침강속도를 측정한 결과, 합성하수에서의 침강속도가 증류수에서의 침강속도보다 큰 것으로 나타나 상기한(Figure 4) 초기응집속도와 동일한 경향을 나타냈다. 즉, 초기응집이 빠를수록 입자가 커지므로 침강속도가 증가하는 것으로 판단된다. 침강속도는 합성하수에서는 102 µm min-1으로 나타났고, 증류수에서는 43 µm min−1로 침강속도가 감소하여 증류수에서 ZnO 나노입자의 분산성이 더 큰 것으로 나타났다. 분산한 ZnO 나노입자가 모두 침강하기 위해선 합성하수에서는 6시간반, 증류수에서는 15시간이 소요되었다.
제타 전위의 측정에서 수계상에서 ZnO 나노입자가 약한 안정성(−20 ~ −15 mV)을 보이는 것에 착안하여 화학침전법을 통해 ZnO를 제거하는 실험을 수행하였다. ZnO 나노입자 100 mg L−1의 용액에 황과 인의 공급원으로 0.05~0.25 M Na2S와 Na2HPO4를 투입하였다. 100 mg L−1의 ZnO 나노입자가 분산된 용액에 Na2S를 혼합하면 불투명한 상태를 보이며, 염의 농도가 진할수록 침전물의 색이 흰색에서 노랑색으로 변하였다. 동일한 조건에 Na2HPO4를 혼합하면, 저농도에서는 뿌연용액상태를 보이지만 고농도에서는 인산염을 넣자마자 침전되어 용액이 투명하게 변하였다.
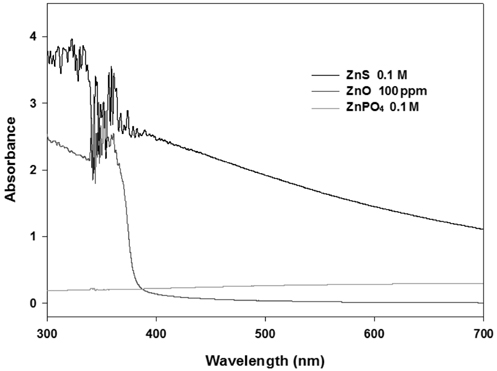
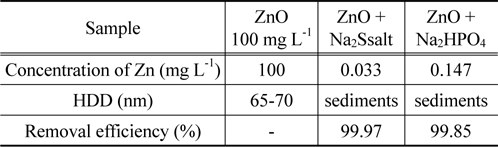
침전제를 투입하고 혼합한 후에 즉시 UV 분석을 한 결과를 Figure 7에 나타내었다. ZnS는 계속 물속에 부유하면서 탁도가 증가하여 UV에 검출되었고, ZnO는 370 nm에서 불규칙한 피크가 나타난 반면, Zn3(PO4)2는 모두 침전되어 UV에서는 피크가 나타나지 않았다. 침전제 투입전의 시료와 투입후 상등액을 채취하여 ICP 분석을 수행하여 해당 농도의 편차를 통해 제거율을 계산하였으며, Zn의 제거율은 두 방법 모두 99% 이상이었다(Table 3).
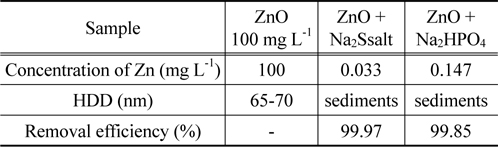
Change of concentration, HDD And removal efficiency before and after precipitating ZnO nanoparticles
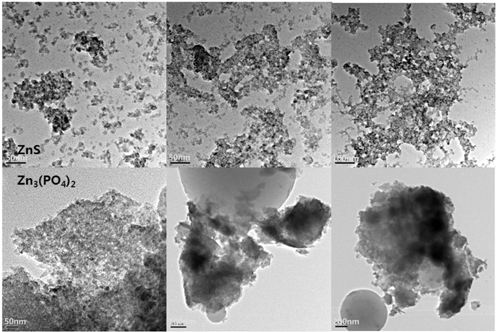
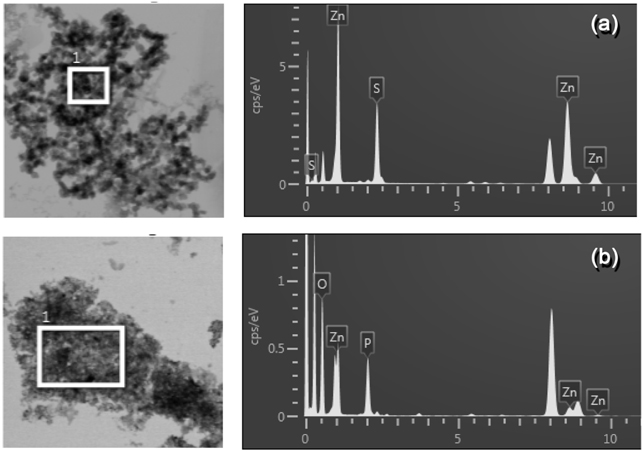
Figure 8은 침전물의 형태를 관찰하기 위해 TEM 분석을 수행한 결과이다. ZnS는 작은 입자들간의 응집을 보이는 polymeric gel network를 보이지만, Zn3(PO4)2는 거대입자가 성장한 aggregated sol 형태를 나타내고 있었다. 이 침전물들의 분자구성을 조사하기 위해 EDX 분석을 수행한 결과를 Figure 9에 나타내었다. ZnS는 비율이 Zn : S = 1 : 1.3으로 거의 1 : 1 결합을 이룬 것을 알 수 있었으며, 이는 Ma Rui의 연구보고와 일치하였다[5]. Zn3(PO4)2는 Zn : PO4 = 1 : 10 정도의 비율로 나타나서 아마도 PO4가 Zn의 표면을 코팅하는 amorphous 형태를 이루거나 Zn3(PO4) 4H2O의 hopeite를 이루는 것으로 판단된다[20]. 의도적으로 pH를 약염기 이상으로 제어하게 되면 ZnO의 표면만 인산으로 대체되는 형태를 보이게 되며, 본 실험에서와 같이 pH 조절없이 침전법을 사용했을 경우는 입자의 전체적인 크기 증가와 함께 입자의 자발적인 침전을 유도하게 된다. 이에 침전에 의한 제거 효율이 증대된다고 할 수 있다.
3.4. ZnO 나노입자, ZnS, Zn3(PO4)2의 급성독성평가
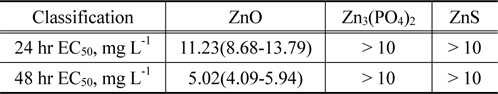
수계상에서 ZnO 나노입자를 제거하기 위해 ZnO를 침전시키면서 발생하는 ZnS와 Zn3(PO4)2 물질에 대한 급성독성 평가를 수행하였고 그 결과를 Table 4에 나타내었다. 물벼룩을 이용하여 급성독성 실험을 수행한 결과, ZnO 나노입자는 11.23 mg L−1에서 24시간만에, 5 mg L−1 (Zn 기준농도)에서는 48시간만에 물벼룩의 50%에서 운동성 소실 등의 독성영향이 관찰된 반면 ZnS와 Zn3(PO4)2는 10 mg L−1 (Zn 기준농도)에서 어떠한 영향도 관찰되지 않아 유해성이 저감된 것을 확인할 수 있었다.
[Table 4.] Acute toxicity evaluation of ZnO, Zn3(PO4)2 and ZnS
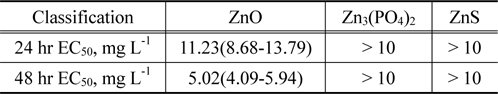
Acute toxicity evaluation of ZnO, Zn3(PO4)2 and ZnS
ZnO 나노입자가 수계상에서 어떠한 유해성을 갖는지를 알아보기 위해 송사리 알을 이용한 생태독성실험 결과, ZnO 5 mg L−1에서 기형이 발생하였고, 10 mg L−1에서는 생장지연 영향을 보였다. 이를 제거하기 위해 Na2S, Na2HPO4를 이용하여 ZnO 나노입자를 침전시킨 결과, 두 방법 모두 제거율은 99% 이상으로 거의 모든 Zn이 수계상에서 침전되어 제거되었다. 침전물은 ZnS 혹은 Zn3(PO4)2였고, ZnS는 Zn과 S가 거의 1:1 로 반응하여 침전한 것과 달리 Zn3(PO4)2는 Zn보다 과량의 PO4가 반응하여 Zn의 표면을 코팅하거나, Zn3(PO4)・4H2O의 HOPEITE로 존재하는 것으로 판단된다. ZnS와 Zn3(PO4)2의 물벼룩 급성독성실험에서는 독성이 발견되지 않아 ZnO 나노입자에 비해 독성이 저감된 것을 확인할 수 있었다.