감태(
그 중에서도 특히, eckol (Fig. 1)은 매우 뛰어난 생리활성을 보이는 물질로서 항산화, 항노화, 항고혈압, 그리고 자외선 보호효과 등에 효과가 있다고 보고되어졌다(Kang et al., 2005; Joe et al., 2006; Jung et al., 2006; Heo et al., 2009). 그러나 감태내의 eckol의 함량은 건조감태분말에서 35.5 mg/kg으로 매우 미량이다(Moon et al., 2008). 감태잎의 70% methanol (MeOH) 추출물의 폴리페놀 함량이 35.5 g/kg (Lee et al., 2006)으로 가장 많은 페놀성 화합물을 함유하고 있는데, 이와 비교 하였을 때 eckol의 함량은 페놀성 화합물의 0.1%에 불과하다.
기존의 eckol의 분리 방법은 건조된 감태분말을 MeOH을 사용하여 추출한 후, 그 추출물로부터 ethyl acetate (EtOAc) 분획물을 획득한다. 획득한 EtOAc 분획물을 유리컬럼을 통하여 diethyl ether 분획물을 얻고, Sephadex LH-20 컬럼크로마토그래피를 사용하여 분획물을 나눈 뒤 최종적으로 TLC 분석을 이용하여 eckol을 분리한다(Moon et al., 2008). 이러한 분리방법은 각 단계별로 시료의 손실이 일어날 수 밖에 없고, 재연성이 불확실하다고 사료되며 시간이 매우 오래 걸린다는 문제점이 있다. 이 연구에서는 이러한 문제점을 해결하기 위해 centrifugal partition chromatography (CPC) 를 사용하였다.
Centrifugal partition chromatography (CPC)는 counter-current chromatography (CCC)의 한 분야의 기술로서 용매시스템을 이용하여 물질이 서로 섞이지 않게 2개의 층으로 분리한 뒤 한 층을 이동상으로, 다른 한 층을 고정상으로 하여 고체지지체 없이도 물질을 분리 정제할 수 있는 시스템이다. CPC를 이용하면 one-step과정으로 순도 90%의 물질을 분리해 낼 수 있으며, 물질을 분리해내는 기존의 과정이 불필요해짐에 따라 빠르게 분리과정을 끝낼 수 있다(Lee et al., 2014).
이 연구에서는 CPC를 이용하여 감태로부터 eckol을 분리하였고, HPLC와 ESI/MS를 통하여 동정을 한 뒤, eckol이 가진 다양한 생리활성 중에서 항염증활성을 쥐의 뇌 대식세포인 BV2 microglial cell line에서 측정하였다.
본 연구에서 사용된 감태(
건조된 감태(20 g)는 Lee et al. (2013)의 방법에 따라 1 L의 70% ethanol (EtOH)로 상온(25℃)에서 초음파 분해에 의해 3시간 동안 추출되어졌고, 3회 반복 추출되어졌다. 추출물은 농축기를 사용하여 농축되어졌고, EtOAc (1:1, v/v of sample)를 사용하여 분획되어졌다. 그리고 나서 건조된 EtOAc 분획물은 CPC분리를 위하여 냉장 보관되어졌다.
Gradient acetonitrile-water 용매 시스템을 사용하여 Atlantis T3 column (3 μm 3.0×150 mm column)에 5 mg/mL의 sample을 5 μL씩 직접적으로 주입하였다. 이동상은 acetonitrile-물로 다음과 같이 비율에 변화를 주었다. 0.1% formic acid가 포함된 acetonitrile과 0.1% formic acid가 포함된 물을 0→40분(10:90→40:60 v/v), 40→50분(40:60→50:50 v/v), 50→60분(50:50→100:0 v/v)으로 흘려주었고, 유속은 0.2 mL/min이었으며 UV 흡광도 290 nm에서 측정하였다(Kim et al., 2014).
HPLC-DAD-ESI/MS 분석은 Hewlett-Packard 1100 series HPLC 시스템을 autosampler, a column oven, a binary pump, a DAD detector, 그리고 a degasser (Hewlett-Packard, Waldbronn, Germany)를 finnigan MAT LCQ ion-trap mass spectrometer와 짝지어서 함께 사용하여 분석하였다. 크로마토그래피의 조건은 HPLC의 조건과 같고, HPLC-DAD-ESI/MS의 조건은 다음과 같다(flow rate 0.2 mL/min; 100-2,000 m/z; source voltage, 4.5 kV; capillary temperature 250℃; capillary voltage, −36.5 V; interoctapole lens voltage, 10 V; sheath gas, 80 psi; auxiliary gas, 20 psi) (Lee et al., 2014).
CPC실험은 n-hexane:EtOAc:MeOH:water (2:8:3:7, v/v/v/v)로 구성된 two-phase 용매시스템을 사용하여 수행되었다 (Delaunay JC et al., 2002). Two phases는 분별깔때기 안의 혼합물이 완전히 균형을 이룬 후에 분리되어지고, 위쪽의 유기상은 고정상으로서 사용되었으며, 아래쪽의 액상은 이동상으로서 사용되었다.
처음 단계에서 CPC column은 유기고정상으로 가득 채워져서 1,000 rpm으로 순환되어졌고, 이동상은 descending mode에서 분리를 위해 같은 유속(2 mL/min)으로 column안으로 유입되어졌다. 이동상이 column 밖으로 나올 때 유체적 평형을 이루었다(배압; 420.5 psi). 감태의 70% EtOH 추출물로부터 획득한 농축된 EtOAc fraction (500 mg)은 two CPC 용매시스템 phases가 1:1 (v/v)으로 혼합된 용매 6 mL에 녹이고 Rheodyne injection valve를 통해 주입되었다. CPC로부터의 배출액은 290 nm 파장의 UV로 관찰되어졌고, 6 mL의 fraction은 fraction collector에 의해 8 mL 튜브에 수집되었다(Kim et al., 2014)
항염증 활성 분석을 위하여 쥐의 대식세포주인 BV2 cell line이 사용되었고, 세포는 American type culture collection (ATCC)에서 분양 받았으며, Dulbecco’s Modified Eagle Medium (DMEM) 배지에 10% fetal bovine serum (FBS)과 1% penicillin-streptomycin을 혼합하여 37℃, 5% CO2 조건에서 배양하였다.
24-well plate에 BV2 cell을 1×105개를 분주하고, 16시간 뒤에 eckol을 10, 25, 50 μg/mL의 농도로 처리한 후 24시간 뒤에 세포생존율을 측정하기 위해 각 well마다 MTT용액[3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide; 0.2 mg/mL]을 첨가하여 37℃에서 3시간 배양한 후 형성된 불용성 결정을 dimethylsulfoxide (DMSO)로 완전히 녹인 후에 ELISA reader를 이용하여 540 nm에서 흡광도를 측정하였다.
>
CPC를 사용하여 분리한 eckol의 항염증 활성 측정
24-well plate에 BV2 cell을 1×105개를 분주하고, 16시간 뒤에 eckol을 10, 25, 50 μg/mL의 농도로 처리한 후 1시간 뒤에 lipopolysaccharide (LPS)를 1 μg/mL의 농도로 처리하였다. 24시간 후에 nitric oxide (NO) 생성량을 측정하기 위해 상층액 100 μL를 Griess 용액(1% sulfanilamide, 0.1% naphthylethylenediamine dihydrochloride in 2.5% phosphoric acid) 100 μL와 혼합하여 10분간 상온에서 반응시킨 뒤 540 nm에서 흡광도를 측정하였다. 세포손상을 측정하기 위해 상층액 50 μL를 LDH kit를 사용하여 빛을 차단한 뒤 상온에서 30분간 반응시키고 490 nm에서 흡광도를 측정하였다. Prostaglandin E2 (PGE2)의 생성량은 상층액을 수거하여 ELISA kit를 사용하여 측정하였다. 각각 측정된 값을 이용하여 nitric oxide (NO) 생성량, 세포손상, PGE2 생성량을 확인하였다.
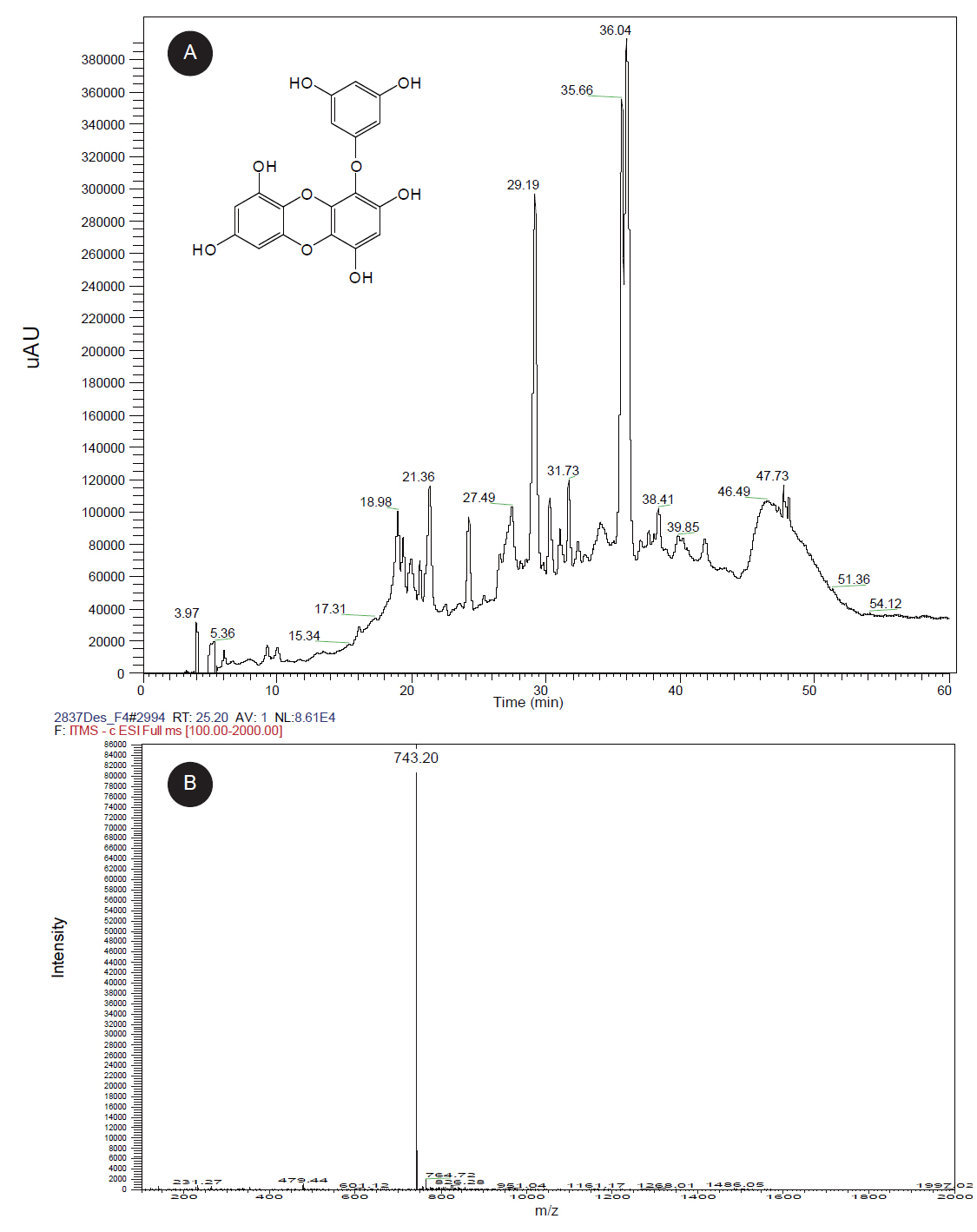
감태에는 fucoxanthin, fucoidans, phlorotanins 등 다양한 생리활성 물질들이 함유되어 있다고 알려져 있다(Balboa et al., 2013). 특히 다른 갈조류에 비해서 phlorotannin 계열 폴리페놀 화합물들이 풍부하게 함유되어 있어 기능성 상품의 원료로서 주목 받고 있다. 감태의 주요 폴리페놀 화합물로는 dieckol, phlorofucofuroeckol A, eckol 등이 알려져 있다. 그러나 eckol 같은 경우에는 생리활성이 매우 뛰어나지만, 감태내 함량이 매우 적고 분리하는 과정이 길고 복잡해서 순도 높은 eckol의 분리가 사실상 매우 어렵다. 이런 이유로 이 연구에서는 분리 과정을 단축시켜 시료의 손실과 시간의 소모를 줄이고, 순도높은 화합물을 분리해 낼 수 있는 CPC를 사용하였다. CPC를 사용하여 eckol의 분리가 가능함을 확인하기 위해 감태의 phlorotannin계열 화합물들을 목적으로 70% EtOH을 사용하여 추출한 감태 추출물을 HPLC를 사용하여 분석한 결과 다양한 물질들이 peak를 나타내었다(Fig. 2A). 다양한 주요 물질들의 peak들을 mass를 통하여 분자량을 확인한 결과, 27-28 retention time의 peak가 eckol로 임의 확인되었다(Fig. 2B).
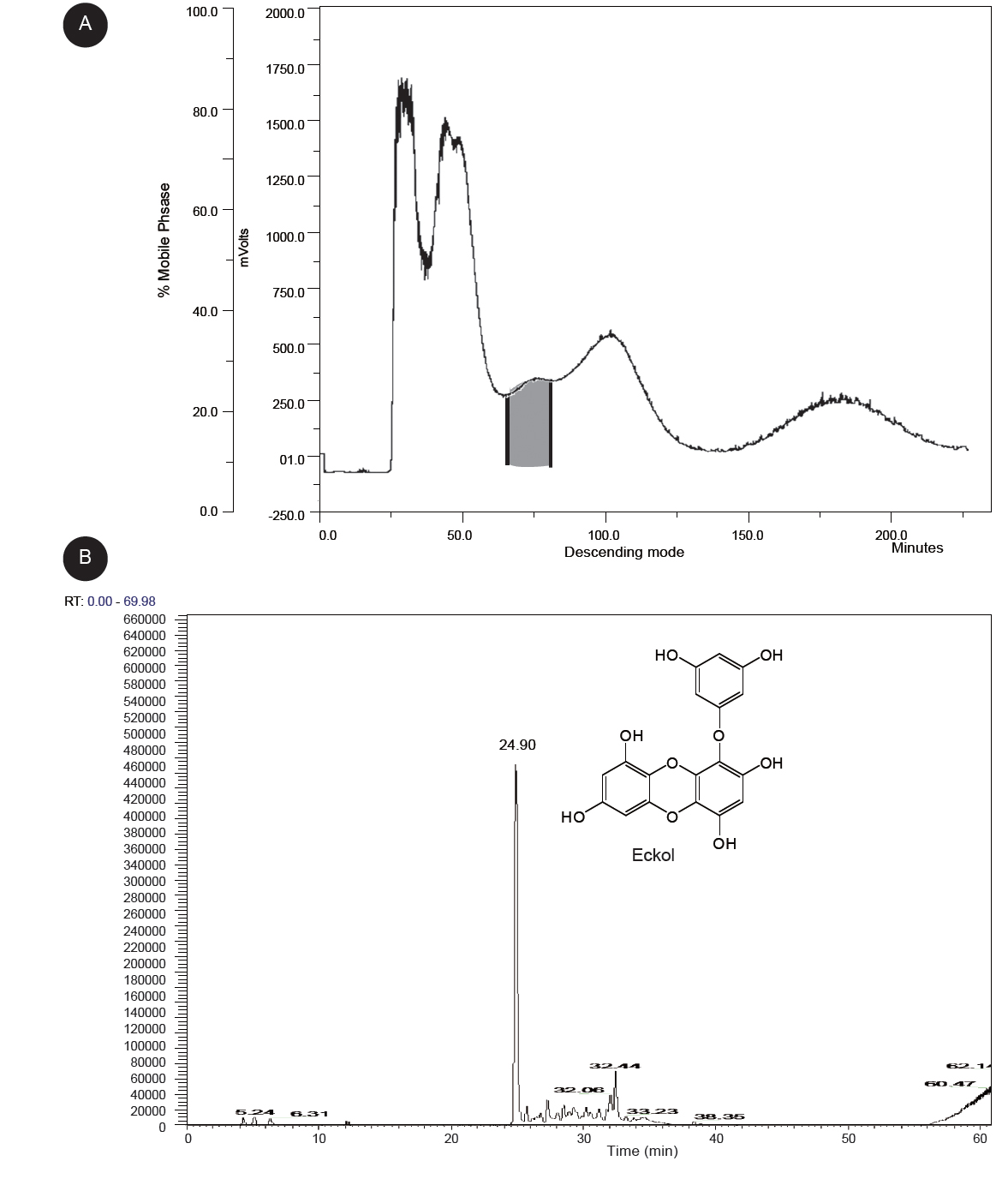
CPC의 최적 가동 조건을 찾기 위해 two-phase 용매시스템의 용매들의 비율을 계산 하였고, K-value의 값을 계산 하였다(Table 1). 다른 물질들과 eckol의 K-value 값을 비교 하였을 때 n-hexane:EtOAc:MeOH:water가 2:8:3:7의 조건이 가장 효율적이라 사료되어 이 조건으로 CPC를 진행하였다. Eckol의 최대 K-value가 1보다 낮은 값을 나타냈으므로, CPC는 descending mode로 작동되었다. CPC가 작동하는 동안 coil안의 고정상은 75%로 유지되었고, 압력은 39 MPa였다. CPC의 chromatogram은 Fig. 3A에 나타내었다. 우리는 어두운 부분이 eckol임을 HPLC 분석을 통하여 확인하였다(Fig. 3B). Fig. 3B에서 다른 peak값에 비해 eckol의 peak값이 독보적으로 높은 것으로 보아 70% EtOH 감태 추출물의 EtOAc 분획물로부터 CPC를 이용하여 90%이상의 순도높은 eckol을 분리하는데 성공하였음을 확인 할 수 있다. 이전연구에 따르면, 감태 유래 EtOAc fraction (24.87 g)으로부터 silica gel chromatography와 Sephadex LH-20 등을 사용하여 58.30 mg의 eckol (수율: 0.234%)이 분리되었으나(Li et al., 2009), 본연구에서 CPC를 사용하여 감태로부터 eckol을 분리 하였을 때, 500 mg의 EtOAc fraction으로부터 3.1 mg의 eckol을 분리 할 수 있었고, 수율은 0.62%을 나타내었다. 이와 같은 이유로 CPC를 사용하여 이전의 물질분리방법보다 간소하며, 순도가 높고, 효율적인 물질의 분리가 가능함을 제시하였다.
[Table 1.] K-values of eckol from Ecklonia cava as solvents for CPC separation

K-values of eckol from Ecklonia cava as solvents for CPC separation
>
CPC로 분리한 eckol의 BV2 cell에서의 염증억제 효과
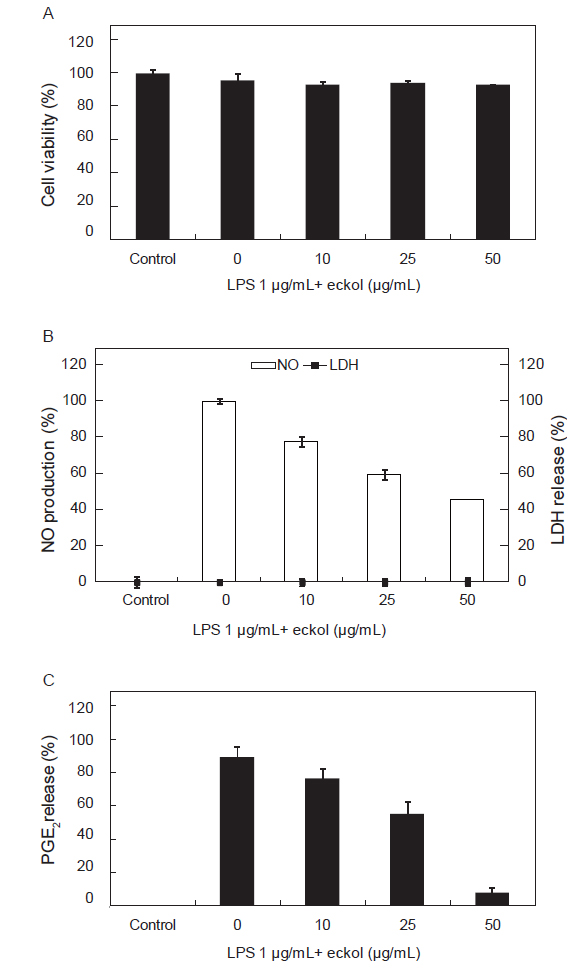
CPC로 분리한 eckol의 염증억제 효과는 Fig. 4A-4C에 나타내었다. MTT assay에서 세포에 대한 독성을 나타내지 않는 농도인 50 μg/mL (Fig. 4A) 이하에서 농도별로 NO 생성 억제활성을 측정하였다. Eckol의 NO 생성 억제활성을 측정하기 위하여 세포에 LPS로 자극을 주고 세포내 염증반응의 지표인 NO와 PGE2에 대한 생성 억제활성을 측정하였다.
NO 생성 억제활성은 10 μg/mL, 25 μg/mL, 50 μg/mL에서 각각 22.3%, 40.6%, 54.4%로 NO의 생성을 억제하여 농도의존적이었으며, 세포손상의 지표인 LDH의 분비는 모든 조건에서 0%로 세포에 대한 손상은 발생하지 않았다(Fig. 4B). PGE2의 생성 억제활성은 10 μg/mL, 25 μg/mL, 50 μg/mL에서 각각 14.2%, 38.4%, 91.2%이었으며, PGE2 생성 억제활성도 농도의존적으로 보였다(Fig. 4C).
LPS로 유도되는 염증반응은 크게 두 가지 메커니즘의 pathway를 통해 일어난다. 이 연구에서 측정한 염증반응의 지표인 NO와 PGE2의 발현은 각각 세포핵 내의 inducible nitric oxide synthase (iNOS)와 cyclooxygenase-2 (COX-2)가 발현됨에 따라 증가하게 된다. iNOS와 COX-2의 발현은 MAPK pathway와 NF-κB pathway 통해 증가된다고 보고되어져 있다(Kim et al., 2010).
결과적으로 이 연구에서는 염증반응의 1차적인 지표인 NO와 PGE2의 발현에 대한 억제활성만을 측정하였지만, CPC로 분리한 eckol이 LPS로 유도되는 MAPK pathway의 JNK, p38, ERK와 NF-κB pathway의 p50, p65와 같은 iNOS와 COX-2의 발현에 관여하는 인자들의 발현을 억제하는 효과적인 활성을 가지고 있다고 기대되나, 확실한 염증발현 메커니즘에 대한 염증억제활성에 대해서는 추가적인 실험이 필요하다.
이 연구에서는 이전의 eckol의 복잡한 분리방법이 아닌 CPC를 사용하여 one-step으로 eckol의 분리를 시도하였다. 그 결과 이전의 분리방법에 비해 많은 시간과 인력을 절약하여 eckol을 분리 할 수 있었고, eckol의 생리활성 중 염증억제 활성 또한 측정하였다. 해조류 혹은 해양생물에서 기존 유용 물질이나 신규 물질을 탐색할 때 분리하는 것에 상당히 많은 시간을 소비하게 된다. 하지만 CPC를 활용하면 이전의 분리방법에 비해 매우 많은 시간을 절약 할 수 있어 연구에 있어 큰 도움이 될 것으로 기대된다.