



In the treatment of spent high energetic materials, the issues such as environmental pollution, safety as well as working capacity should be carefully considered and well examined. In this regard, incineration has been recommended as one of the most promising processes for the disposal of such explosives. Due to the fact that high energetic materials encompass various types and their different characteristics, the technology development dealing with various materials is not an easy task. In this study, rigorous modeling and dynamic simulation was carried out to predict dynamic physico-chemical phenomena for research department explosive (RDX). Plug flow reactor was employed to describe the incinerator with 263 elementary reactions and 43 chemical species. Simulation results showed that safe operations can be achieved mainly by controlling the reactor temperature. At 1,200 K, only thermal decomposition (combustion) occurred, whereas increasing temperature to 1,300 K, caused the reaction rates to increase drastically, which led to ignition. The temperature further increased to 3,000 K which was the maximum temperature recorded for the entire process. Case studies for different operating temperatures were also executed and it was concluded that the modeling approach and simulation results will serve as a basis for the effective design and operation of RDX incinerator.
RDX는 사이클릭나이트라민(cyclic nitramine)계의 고에너지물질로서 급격한 화학반응을 통하여 생성된 고온, 고압의 기체와 이에 수반하는 에너지를 이용하여 화약 및 탄약, 추진제 제조 등 각종 산업 및 무기체계 계발에 이용되는 주요한 물질이다. 또한, 해당물질은 고에너지물질 중에서도 매우 민감한 특성(외부자극에 쉽게 반응하는 특성)을 가지고 있어, 성능이 뛰어나지만 그에 상응하는 위험성도 가지는 물질이기 때문에 해당물질의 정확한 제어방법을 위한 연구는 활발히 진행되고 있다. 이러한 RDX에 대한 연구기술 분야는 설계 및 합성으로부터 시작하여, 제조연구[1], 이를 이용한 복합화약 공정개발, 반응 전후의 물리적-화학적 현상에 대한 실험, 무기체계 및 산업 적용성 연구, 성능 및 안전도 평가, 수명이 지났거나 용도 폐기된 물질의 친환경적 처리방법 등 해당 물질의 생성에서부터 최종 처리까지의 다양한 분야가 연구대상이 되고 있다.
최근 비군사화의 일환으로 수명이 도래한 폐 화약 및 탄약을 환경에 영향을 미치지 않고 안전하게 처리하는 기술이 주목을 받고 있다. 화약 및 추진제에 주원료인 RDX는 복합화약의 성분 중 가장 민감한 물질로서 해당 물질의 특성, 처리할 때 발생하는 화학적, 물리적 영향, 처리방법 및 공정개발에 대한 연구들이 요구되고 있다. 고 에너지물질 처리는 크게 (1)분해공정, (2)회수공정, (3)재활용 및 재사용 공정, (4)폐기공정으로 분류할 수 있다. (1)~(3)처리 방식은 냉동파쇄, 고압 유체에너지를 이용한 절단, 스팀(steam) 혹은 마이크로파(micro wave)를 이용한 용융방법의 기술을 이용하여 화약 및 탄약을 회수 및 파괴시킨다. (4)폐기공정은 소각방법, 초임계산화, 플라스마열분해(plasma thermal decomposition), 용융염 산화, 가수분해 및 산화, 생물학적 처리방법 등이 사용되고 있다[2].
폐기공정에서 소각처리공정은 설계가 간단하고, 운전비용이 낮으며, 후처리 공정을 통해 친환경적으로 고에너지물질의 폐기처리가 가능하다. 그러나 처리대상의 종류가 다양하고 그 특성 또한 매우 다르기 때문에 범용적인 처리 기술이 존재하지 않고 운전시 안전성을 확보할 수 없는 실정이다. 또한 고에너지물질의 특성상 소각처리 시 연소 운전조건을 유지하지 못하면 폭발로 이어져 공정의 안전성을 장담할 수 없다[3]. 이에 각 처리 물질마다 소각로 내부에서 일어나는 변화를 예측하는 연구는 필수적이라 판단되며, 화약성분 중 가장 민감한 RDX의 소각공정 예측은 보편적 화약소각공정 개발에 첫 단계라 될 것이라 사료된다.
RDX를 소각 시에 나타나는 물리-화학적 변화에 대한 연구성과들은 각종 문헌을 통해 확인할 수 있다. RDX에 대한 연소 및 발화의 메커니즘(mechanism)을 확인한 연구성과[4-6]로부터 단계별 경로들이 제시되고 있으며, RDX가 연소하면서부터 발화하는 수많은 반응들에 대한 수식 및 매개변수들을 설명하고 있는 연구성과[7-10]도 있다. 또한 순수 RDX가 연소반응 후에 어떠한 성분들을 생성하는지에 대한 연구결과[11]도 확인할 수 있다. 그러나 위에 언급된 연구들은 실험실 규모에 기초하여 수행되었으며 파일럿 또는 상업 규모 소각 공정에 대한 안정된 적용을 위해 실제 사용되는 반응기 조건에서 모사하는 연구가 필요하다.
실제 소각 공정에서의 적용을 위해 본 연구에서는 복합화약의 주 원료인 RDX를 원통형반응기를 이용하여 소각했을 때, 내부에서 일어나는 화학적, 물리적 변화를 예측하고자 한다. 이를 위해 본 연구는 플러그흐름반응기의 질량-에너지-힘 수지 식을 도입하여 반응기 내부에서의 물리적 거동을 예측하였으며, 고체상의 RDX가 기체로 연소되는 화학적 변화를 모사하기 위해 불균질계(heterogeneous) 및 반응 메커니즘을 적용하였고, 263개의 자세한 기초반응들을 도입하여 총 43가지의 성분들이 참여하는 반응을 모사하였다. 이를 위해 범용 소프트웨어인 gPROMS를 사용하여 동적모사를 실시하였다.
플러그흐름반응기는 폐기물의 연속적인 처리를 위해 널리 사용되는 원통형소각로와 물리적 특성이 가장 흡사한 반응기이다. 본 연구에서는 RDX소각 시 일어나는 동적 특성을 예측하기 위하여 대상 공정을 1차원의 플러그흐름반응기로 채택하였으며 가스상과 고체상이 존재하는 불균질계에 대한 수학적모델링을 수행하였다.
∙ 물질 수지
가스 상
고체 상
∙ 에너지 수지
· 모멘텀 수지
RDX는 1)용융점에서의 RDX 분해반응과 2) 분해반응으로부터 생성된 가스반응, 두 단계로 표현 되며 RDX 분해반응은 아래와 같다[4].
(R1)와 (R3)는 발열반응, (R2)는 흡열반응이며, 각 반응의 반응속도와 반응상수는 아래와 같다.
가스반응을 묘사하기 위해서는 상세한 요소반응이 필요하다. 반응에 참가하는 성분들은 총 43가지(O, O2, H, H2, OH, H2O, HO2, N, N2, N2O, HNO, NH2, NO, NO2, N2H, NH, HCN, NCO, CN, C2N2, HCO, CO, CO2, HOCN, HNCO, HNO2, CH2O, HCNO, CNO, NH3, H2CN, RDX, H2CNNO2, RDXRO, RDXR, H2CNNO, H2CNO, H2CNH, H2O2, NO3, HNO3, HNC, and NCN)이며 관련된 요소반응은 263개이다. 반응속도상수
RDX소각 시, RDX는 가해지는 열원에 의해 온도가 상승하여 용융점에 도달한다. 이후 RDX는 액화가 일어남과 동시에 분해반응이 일어나며, 분해반응이 일어나지 않은 액체RDX는 더 많은 열원을 받아 기화한다. 하지만 액체RDX는 분해반응속도가 기화속도보다 빠르기 때문에 분해반응이 지배적이다. 이후, 분해반응에 의해 생성된 성분들은 상호 가스반응을 일으켜 반응기 내부의 온도를 증가시키며, 온도가 일정수준 이상 올라가면 발화반응이 일어나 급격한 에너지방출을 일으킨다. 때문에 반응기 내부의 초기조건 및 운전조건은 매우 중요하며 이를 이용하여 반응기 내부상태를 일정하게 유지시켜야 한다. 이와 같은 공정특성을 고려하여 본 연구에서는 RDX의 용융점을 유지시킬 정도의 열원(478 K)을 3 m/s로 가하여 내부온도를 유지하였다. RDX는 고정된 상태로 열원을 받아들이기 때문에 반응기 1 m 지점에 고정시켰으며 총 10 kg을 반응시켰다. 세부 모사 조건은 Table 1과 같다.
[Table 1.] Initial & boundary condition to simulate

Initial & boundary condition to simulate
동적모사를 위한 수치 해석 방법으로 편미분 방정식을 시간에 대한 상미분방정식으로 변환하는 선방법(method of lines, MOL)을 사용하였으며, 이 때 전체의 흐름에 대해서는 후방차분법(backward finite difference)이, 압력변화의 계산을 위해서 전방차분법(forward finite difference)이 각각 사용되었다. 본 모사는 CH2O, CO2, H2O 등 비극성 혼합기체에 대한 거동을 다루고 있으며, 이에 대한 열역학적 물성치는 탄화수소 계열의 비극성 가스에 대해 가장 효과적으로 보고되고 있는 펭-로빈슨 상태방정식을[12] 이용하여 계산하였다.
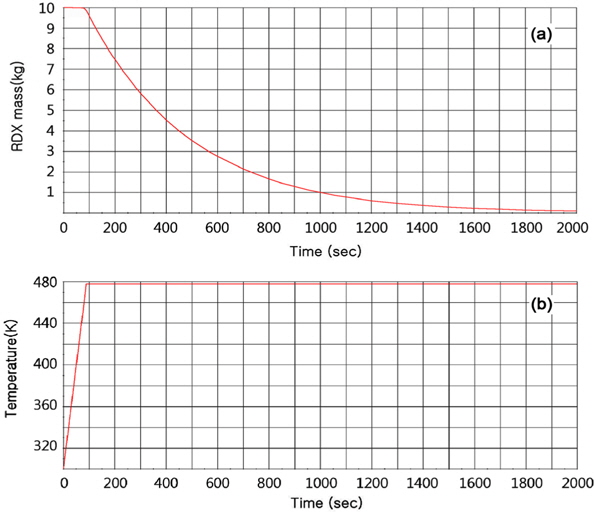
Figure 1에서는 시간에 따른 RDX의 질량 변화와 온도변화를 각각 나타내었다. RDX의 초기 온도(300 K)에서 외부 열 공급에 의해 시간이 80 s에서 온도가 용융점인 478 K까지 올라간다. 이때까지는 RDX의 액화만 일어나며 반응은 수반되지 않는다. RDX의 분해반응은 용융점에 도달한 후 액화된 RDX와 주위에서 분해반응(R-1~R-3)이 주로 일어나며 일부분의 액체 RDX는 기화된다. 분해반응이 진행됨에 따라 RDX의 질량은 2000 s에 다다를 때까지 점차적으로 줄게 된다. 반응에 의해 생성된 열량은 생성된 가스의 온도에 영향을 미치며 따라서 액상 RDX는 온도는 용융점을 계속 유지하고 있다.
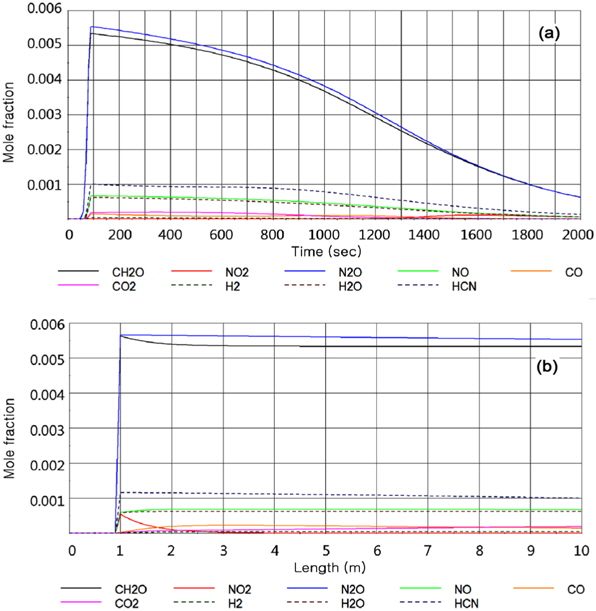
Figure 2(a)는 반응기 출구에서 시간에 따른 성분비율 변화를 나타내며, 최초 RDX가 연소하면서 CH2O, HCN, NO, NO2, N2O, H2O, CO 총 7종의 성분이 생성되는 모습을 확인할 수 있다. 이후 기체반응들에 의해 H2가 생성되며, 1,200 s 이후 전체공정의 온도가 감소하면서 NO2가 추가로 생성되는 것을 확인할 수 있다. 이때, 성분들의 몰분율이 10-2~10-3인 이유는 반응기 입구에서 주입되는 열원의 성분이 순수 N2로 그 비율이 대부분을 차지하기 때문이며, 반응 생성물 중 N2도 상당 비율을 차지하기 때문이다. Figure 2(b)는 RDX분해반응이 가장 활발한 100 s일 때 반응기 내부의 몰분율을 나타내며, 각 성분들이 점차 반응기 끝으로 이동하며 반응하는 모습을 확인할 수 있다. 결국 초기에 RDX분해반응에 의해 생성되는 주요 성분들 중 가스반응에 의하여 NO2는 감소하고, CO2는 증가하는 특징을 확인할 수 있다.
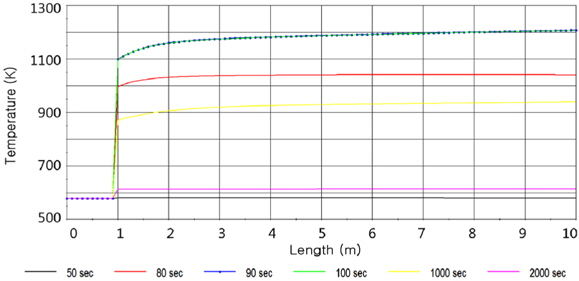
Figure 3은 반응기 내부의 온도변화를 나타내었다. 그림에 나타난 바와 같이 반응기 입구에서는 용융점까지 도달시키기 위한 열원인 N2가 478 K의 온도로 주입되고, RDX가 기화하기 시작하는 1 m 지점에서부터 온도가 상승하는 것을 볼 수 있다. Figure 1(a)와 같이 0~80 s까지 RDX의 온도가 용융점까지 상승하는 단계에서는 RDX의 감소량이 미비한 이유는 반응기 온도상승이 다소 약하다는 것을 확인할 수 있다. 그러나, 80 s 이후부터 급격히 온도가 상승하는데, 이는 RDX가 용융점에 도달하면서부터 급격하게 분해반응하고, 이로 인해 생성되는 발열량이 강한 온도상승의 원인이 된 것으로 분석된다. 또한 90~100 s까지 온도가 더욱 증가하는데 이는 가스반응에 의해 생성되는 열량이 추가적으로 반응기내부 에너지를 상승시킨 것으로 판단된다. 이후 반응기의 끝에 도달할수록 온도가 높은 것을 확인할 수 있는데, 이 또한 반응기 내부에서 가스성분이 기체반응을 일으키며 생성된 열에 의한 것으로 해석될 수 있다.
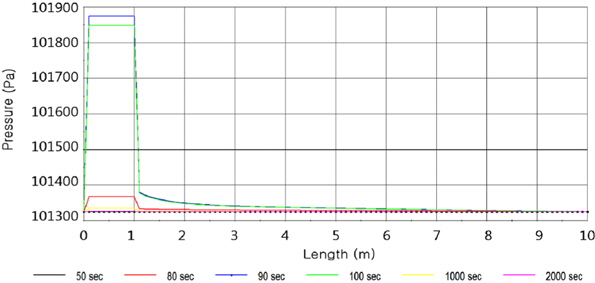
대상공정은 앞뒤가 열린 계로써 반응기의 끝이 대기압으로 유지되고 있다. 이에 Figure 4와 같이 공정은 압력변화가 크지 않다. 90 s 지점에서 순간 발생되는 농도상승과, 온도상승에 따라 순간압력이 101,880 Pa까지 올라가지만 최대 유속 46 m/s 정도의 속도상승으로 인해 압력이 낮아지며 곧 반응기 내부의 압력을 1 기압으로 유지시키고 있다. 결국 압력상승에 의한 반응기 벽면에 가해지는 충격은 적을 것으로 판단된다.
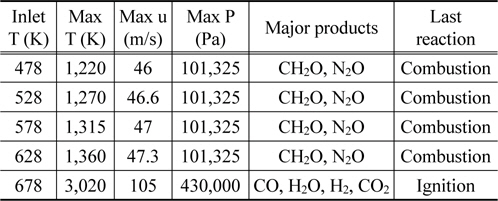
RDX는 주변환경(온도, 압력)에 매우 민감하며 이와 같이 나타나는 물리-화학적 현상 중, 일정 온도 이상에서 급격한 에너지를 생성하는 빠른 반응을 발화반응이라 한다[4]. 본 장에서는 유입온도변화에 따른 반응기 온도상승을 유도하고 이에 따라 RDX반응이 어떻게 일어나는지 확인하였다. 운전조건 변화에 따른 최종반응결과는 Table 2와 같이 나타났다.
[Table 2.] Case study result with varying inlet temperature
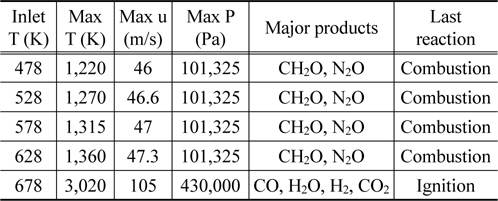
Case study result with varying inlet temperature
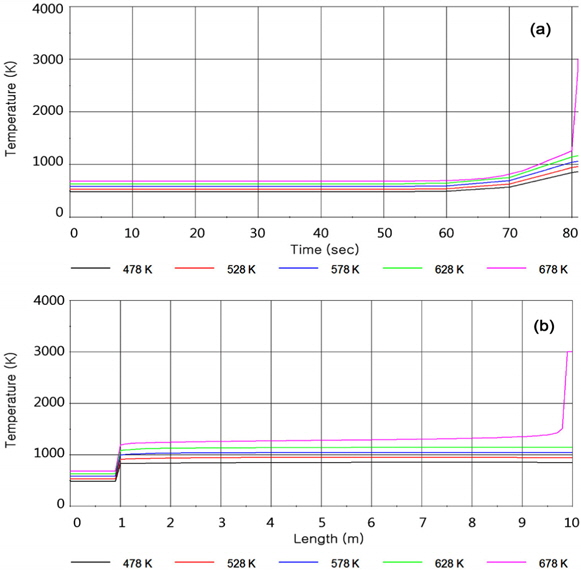
Figure 5는 열원온도변화에 따른 반응기 내부온도변화이다. Figure 5(a)는 반응기 출구에서 678 K의 열원으로 운전시 89.9 s 지점에서 발화반응이 일어나는 것을 확인할 수 있었으며, Figure 5(b)에서는 발화반응이 일어나는 시점인 89.9 s에 반응기 끝 단에서 최초로 발화반응이 시작된 것을 확인할 수 있다. 이는 발화반응이 RDX자체 반응이 아닌 생성된 가스에 의해 일어나는 반응이라는 점을 명증한다. 결국, 열원의 냉각작용이 반응기내부의 온도를 1,300 K 이하로 유지하지 못한다면, 반응기 끝단에서 발화반응이 일어나 반응기에 커다란 충격을 줄 것으로 보여진다.
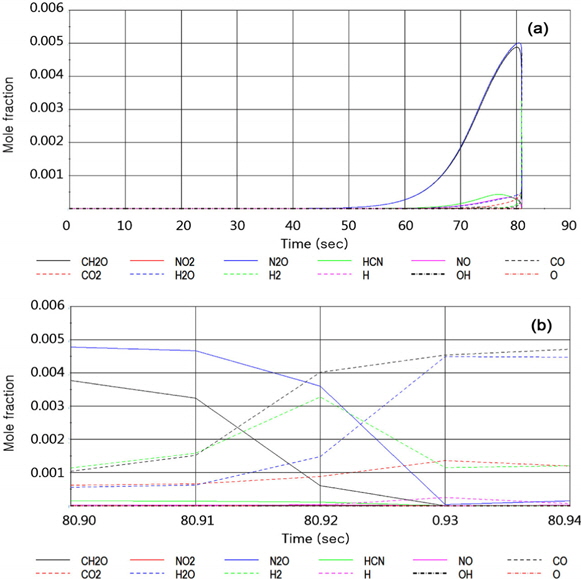
기체성분들의 변화는 Figure 6에 나타냈다. 89 s 지점에서 급격한 반응에 의해 CH2O N2O가 모두 소멸되었고, CO, H2O가 급격히 생성되었으며, 이 후 H2, O, H가 추가적으로 생성되었다. 성분들은 0.04 s에 짧은 시간에 따라 급격히 변화하는 것을 확인할 수 있었으며, 발화반응의 주요인이 된 성분은 CH2O와 N2O라는 것을 알 수 있었다.
최종 생성물의 변화는 아래 Figure 7과 같이 발화반응 시에 나타난 성분결과와 LIAU et al.[5]의 연구결과와 비교 하였다. 그림은 같은 성분 비율로 표준화하여 비교한 결과이다.
대부분의 성분들은 그 오차범위가 5% 미만으로 비슷하였지만, H2O와 O는 큰 차이를 보였다. 이는 본 연구에서 예측한 운전상태의 온도가 평균적으로 낮게 유지되었고, 그 영향으로 H2O를 생성하는 반응이 H를 생성하는 반응보다 더 크게 작용하였기 때문이다. 즉, 운전조건이 낮은 온도에서 오래 유지되어 고온에서 활발한 H생성반응이 많은 관여를 못한 결과라 판단된다.
본 연구에서는 RDX 연소반응을 통한 소각공정의 상세 모델링 및 동적모사를 수행하였다. 소각 공정에서는 RDX액화, 분해반응, 가스반응 등이 온도의 범위에 따라 동시에 일어나며 이를 해석하기 위하여 43가지 화학종과 263개의 반응이 참여하는 반응 메커니즘을 사용하였다.
RDX의 온도를 녹는점으로 유지 시 10 kg의 RDX가 모두 분해되는데 2,000 s 가까이 소요되었다. 분해반응에 의해 생성된 성분들은 가스반응을 일으켰으며 이에 반응기 내부는 1,200 K까지 상승하였다. 주 생성물은 CH2O와 N2O였으며 반응기 내부에서의 성분변화가 미비한 것으로 보아 가스반응이 경미했던 것으로 판단된다. 이때 공급되는 열원의 온도는 478 K였다.
입구에서 열원온도를 678 K까지 상승 시 반응기 내부의 온도는 1,300 K 이상 증가하였으며, 반응기 끝단에서부터 발화 반응이 일어나 급격한 에너지를 방출하였다. 주요 생성물은 CO, CO2, H2O, H2, H, O, OH, N2였으며, 이때 최대 온도는 3,020 K를 보였다. 이는 발화반응에 대한 LIAU et al.[5] 연구와 근사한 결과였다.
결국, 반응기 운전온도를 통제하면 RDX의 민감한 반응을 억제할 수 있기 때문에 통제방법의 선택에 따라 소각공정 및 운전방법이 결정될 것으로 판단되며 이를 이용한 효율적인 공정개발이 가능할 것으로 사료된다.
Uppercase letters
A Pre-exponent factor E Activation energy L length P Pressure(Pa) R Gas constant S Source term T Temperature (K)
Lowercase letters
c Concentration (mol) e Energy (J) i Component k Reaction rate constant m Mass (kg) t time (s) u Velocity (m/s) z Distribution domain
Subscripts & superscripts
Cp heat capacity (J/kg-K) gas Gas phase ini Initial PFR Plug flow reaction rdx RDX phase ρ Density (kg/m3) φ Porosity Reaction rate (mol/m3・s)
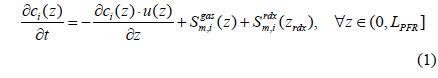
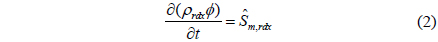
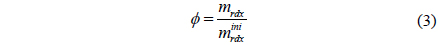
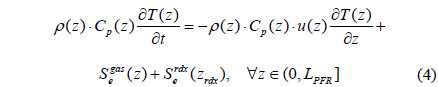
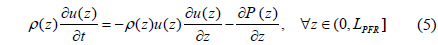
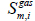
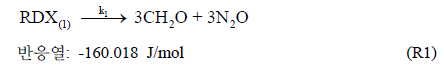
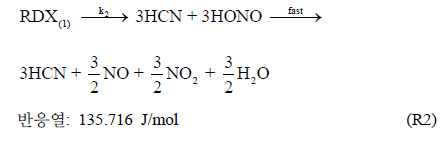
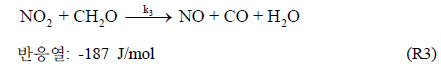
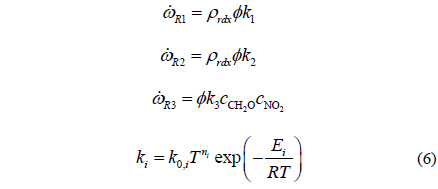
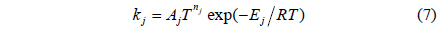

![Graph showing the comparison between components from LIAU et al.[5] and results obtained.](http://oak.go.kr/repository/journal/17035/CJGSB2_2014_v20n4_398_f007.jpg)