수산양식은 빠르게 성장하는 식품 생산 산업의 하나이며 2014년 기준 우리나라 양식수산물 생산량은 약 157만톤으로 전체 어업생산량 대비 3.4%를 차지하며 생산액으로 비교하면 전체 어업생산액 중 13.0%를 차지하고 있다(통계청, 2015). 국내 수산양식 산업 중 새우 양식산업은 1990년대에 보리새우(Marsupenaeus japonicas)를 중심으로 급속히 성장하였으나 흰반점병(White Spot Disease, WSD) 등의 전염병으로 성장이 주춤하다가 2006년부터 상대적으로 질병에 대한 저항성이 좋은 흰다리새우(Litopenaeus vannamei)를 양식하기 시작하여, 현재 새우양식의 대부분을 차지하고 있다(Jang et al., 2007). 전세계적으로도 새우 양식 생산은 매년 16.8%의 성장률을 보이고 있다(Subnutith et al., 2008, Janarthanam et al., 2012). 그러나 세균 또는 바이러스 감염에 의한 질병 발생, 부적절한 사육 환경 등은 새우 양식을 어렵게 하는 주요 요인이며(Pattamarat et al., 2010) 특히, 새우에서 세균 감염증 중 비브리오 감염증은 아시아 국가들의 새우 양식장에서 큰 문제를 유발하고 있으며, 이로 인한 세계 경제적 손실액은 약 3억달러로 추정되고 있다(Janarthanam et al., 2012). 새우양식은 높은 생산성을 확보하기 위하여 밀집양식이 이루어지고 있는데 이는 필연적으로 질병의 발생과 전파를 초래한다. 비브리오균은 다양한 해양생물에서 병원성이 강한 병원체로 인식되고 있으며, 이중 Vibrio harveyi는 toxR gene, haemolysin gene 등의 독력 발현 유전자를 가지고 있으며, 새우의 larva 또는 postlarva 시기에 감염되어 100% 폐사를 유발하고, 새우의 간췌장에서 가장 빈번하게 검출되고 있다(Gopal et al., 2005, Ruwandeepika et al., 2010, Saori et al., 2011, Soto-Rodriguez et al., 2012). Jung et al. (2012)은 2007-2010년 하절기 국내 새우 양식장의 새우 2,413마리에 대하여 세균 및 기생충 감염 현황을 조사한 결과 병원체 감염율이 15.5-61.8%이었으며, Vibrio sp. 감염률은 5.2-30%로 나타났음을 보고하였다. 현재, 새우 양식장에서 비브리오 감염증을 효과적으로 관리하기 위하여 수질 관리, 양성 수조의 염도 저감화, 새우에 대한 스트레스 감소, 항생제 또는 소독제 사용, 프로바이오틱 사용을 행하고 있다(Kulwadee et al., 2011). 소독제로 사용되고 있는 모노퍼설페이트 화합물(monopersulfate compound)은 세균 세포질의 단백질과 다른 구성성분들의 산화를 통한 효소 시스템의 억제와 세포벽 견고성을 손실시켜 살균 작용을 나타내는 산화제 계열 화학물질로 수산양식에서 Vibrio anguillarrum, Pseudomonas aeruginosa, Vibrio splendidus, Vibrio parahaemolyticus Aeromonas hydrophyla sub sp. 등의 세균에 대하여 최소억제농도가 25.6-51.2 mg/L 로서 우수한 항균효과가 있음이 보고되는 등(Wang et al., 2008) 수산양식에서의 유효 소독제로 소개되고 있다. 그러나 비브리오균에 대한 유효 항균농도에서의 모노퍼설페이트 화합물이 새우에 미치는 독성에 대한 자료는 부족한 실정이다. 이에 본 연구에서는 국내 대량으로 양식되는 흰다리새우에서 문제가 되는 Vibrio harveyi에 대한 모노퍼설페이트 화합물의 살균효과와 이의 유효농도에서 흰다리새우에 대한 독성을 확인하고자 수행하였다.
본 연구에 사용 된 흰다리새우는 충남 당진에 위치하고 있는 양식장에서 공급받아 사용하였다. 흰다리새우 사육에 필요한 해수는 자외선 살균 처리 여과수(R/O 수, carbon/micro filter로 1차 정제 후 R/O membrane로 2차 정제하여 자외선 살균 처리한 음수)에 해수염(Red Sea Salt, Red Sea사)으로 염도 18-19psu로 제조하여 만든 해수와 양식장에서 제공받은 해수를 혼합하여 사용하였다. 이렇게 준비한 해수에 2개월령(7-8 g)의 흰다리새우 5마리씩을 산소 발생장치가 장착 된 26×42×18 cm의 사각 사육수조에서 사육하였으며, 사육온도는 26-28℃로 유지하였다.
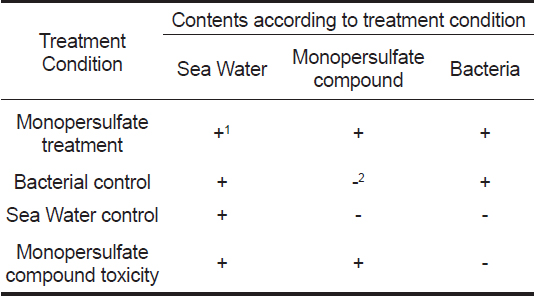
Monopersulfate compound (50.69% w/w)를 함유하는 버콘아쿠아틱(Virkon® Aquatic)제품을 바이엘코리아㈜(서울, 한국)로부터 제공받아 본 연구에 사용하였다. Monopersulfate 화합물의 살균 효과를 확인하기 위한 시험군의 구성은 Table 1과 같이 설정하였다. Monopersulfate 화합물의 희석은 살균 효력시험에 들어가기 1시간 전에 준비하였으며, 10 L 해수에 monopersulfate 화합물 0, 0.15, 0.3, 0.6, 1.2, 2.4 ppm (버콘 아쿠아틱 제품으로서 0, 0.3, 0.6, 1.2, 2.4, 4.8 ppm)이 되도록 첨가하였다.
본 연구에 사용 된 Vibrio harveyi (FP8370)는 국립수산과학원에서 분양 받아 사용하였다. Vibrio harveyi의 증균은 1.5% NaCl이 첨가 된 Trypticase Soy Agar (TSA, Difco)에 접종하여 30℃ 배양기에서 18-24 시간 배양 한 후 4-5개의 단일 콜로니를 취하여 1.5% NaCl이 함유 된 Tryptic soy broth (TSB, Difco)에 넣어 30℃ 진탕배양기(100 rpm)에서 18~24시간 배양하였다. 증균 배양된 세균은 Whatman No 2 filter paper로 여과한 해수를 이용하여 세척하였다. 즉, 증균 배양된 Vibrio harveyi를 원심분리(3,000 rpm, 10 min)한 후 상층액을 제거하고, 균체를 해수로 재부유 시켰으며, 이 과정을 3회 반복하였다. 마지막 세척 후 균체를 해수로 현탁 한 후 Vibrio harveyi의 균수를 MacFarland No 0.5로 조정하였다.
본 연구에서 사용 된 Vibrio harveyi의 virulence gene을 확인하기 위하여 세균 배양 후 DNA 추출 kit (Bioneer, Korea)를 이용하여 Genomic DNA를 추출하였다. toxR gene과 haemolysin gene의 발현을 확인하기 위한 primer는 Table 2에 제시하였다.
Vibrio harveyi로부터 추출한 DNA 2 μL, forward primer 및 reverse primer (20 pmol/μL) 각 1 μL를 16 μL의 PCR 반응액 (H2O 9.8 μL, 10× PCR buffer 2 μL, 10 mM dNTPs 2 μL, 20 mM MgCl2 2 μL, Hotstart polymerase 0.2 μL) (GeneAll Biotechnology, Korea)에 첨가하여 혼합한 후, 94℃에서 10분간 변성시킨 후 94℃에서 1분, 55℃ (haemolysin gene)/53℃ (toxR gene)에서 1분, 72℃에서 1분의 조건으로 30 cycles 수행한 후 72℃에서 10분간 신장하였다.
PCR 증폭산물을 1.5% agarose gel에 전기 영동하여 UV illuminator상에서 특이적인 증폭산물을 확인하였다.
공시하는 Vibrio harveyi 균이 발광성을 띠는 균이지 확인하기 위하여 1.5% NaCl이 첨가 된 TSB 배지에 균을 접종한 후 30℃ 배양기에서 24시간 배양 한 후 균 현탁액을 TSB에 2배 희석하여 96 well plate에 200 μL씩 넣고, TSB 배지를 blank로 하여 Glomax multi detection system (Promega, USA)으로 발광량을 측정하였다.
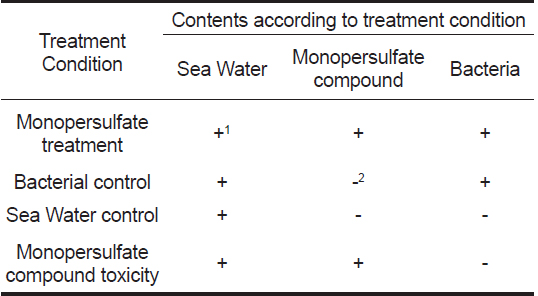
Monopersulfate 화합물의 Vibrio harveyi에 대한 살균효과를 확인하기 위하여 국립수산과학원 고시(제 2013-13호, 2015.05.20) 소독제 효력시험지침을 기본으로 하되 변형하여 살균효능 시험을 실시하였다. 즉, 해수 10 L에 monopersulfate 화합물 0, 0.15, 0.3, 0.6, 1.2, 2.4 ppm (버콘아쿠아틱 제품으로서 각각 0, 0.3, 0.6, 1.2, 2.4, 4.8 ppm) 농도로 처리하고, MacFarland No 0.5로 조정한 Vibrio harveyi를 1×106 CFU/mL이 되도록 첨가한 후 30분간 반응시켰으며, 10분마다 혼합하였다. Monopersufate 화합물과 비브리오균의 반응이 있은 후 30분후에 새우 5마리를 각각의 수조에 넣고 3일간 새우의 상태 및 생존 유무를 확인하였다. 해수 중 Vibrio harveyi의 감소여부를 확인하기 위하여 monopersulfate 화합물 처리 후 1시간, 6시간, 24시간째에 일정량의 해수를 취하여 멸균 PBS로 10배 계단 희석한 후 Thiosulfate Citrate Bile Salt Agar (TCBS agar, Difco)에 도말하여 30℃ 배양기에서 18-24 h 배양한 후 집락수를 측정하였다. 총 세균수 측정은 TSA에 도말하여 측정하였다.
Monopersulfate 화합물의 흰다리새우에 대한 독성을 확인하기 위하여 해수 10 L에 monopersulfate 화합물 0, 0.15, 0.3, 0.6, 1.2, 2.4 ppm (버콘아쿠아틱 제품으로서 각각 0, 0.3, 0.6, 1.2, 2.4, 4.8 ppm) 농도로 처리하고 새우 5마리를 각각의 수조에 넣고 7일간 새우의 상태 및 생존유무를 조사하였다.
실험 결과는 평균과 표준편차(mean±S.D)로 나타내었으며, 각 실험군의 유의성은 STATICSTICA (DELL Software, USA) 프로그램을 이용하여 ANOVA test와 Ducan’s multiple range test (P<0.05)로 분석하였다.
Monopersulfate compound가 새우의 질병 원인체인 Vibrio harveyi에 대한 살균 소독효과 및 흰다리새우에 대한 독성을 확인하기 위하여 시험을 수행하여 다음과 같은 결과를 얻었다.
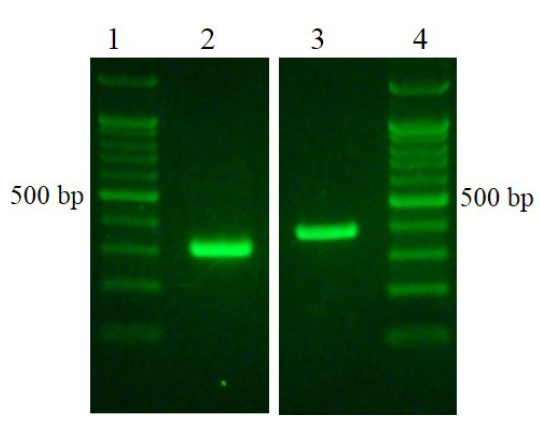
본 연구에 사용 된 Vibrio harveyi는 haemolysin gene과 toxR gene을 모두 함유하는 것으로 확인되었다(Fig. 1). Vibrio harveyi는 다양한 병원성 인자를 가지고 있으며 이에는 caseinase, gelatinase, phospholipase, lipase, haemolysin, cystein protease 등이 보고되어 있다(Liu et al., 1996). 이중 toxR은 transmembrane 전사 조절인자로서 비브리오균에서 다른 병원성 유전자의 조절에 매우 중요한 역할을 하며 Vibrio harveyi 외에 Vibrio cholera, Vibrio paraheamolyticus 등에서도 발현되는 것으로 보고되어 있다(Lin et al., 1993, Miller and Mekalanos, 1988). Haemolysin인자는 용혈과 세포분해를 유발하는 중요한 병원성 인자로서 Vibrio harveyi 외에 Vibrio cholera, Vibrio paraheamolyticus 등에서도 확인되고 있어 수평적 유전자 전달(horizontal gene transfer)이 Vibrio 균속간에 이루어지고 있음을 알 수 있다(Ruwandeepika et al., 2010). 본 연구에서 공시한 Vibrio harveyi는 비브리오 균의 균력을 대표하는 toxR유전자와 haemolysin 유전자가 확인되었으며 이는 새우에서 병원성이 큼을 의미한다.
배양 된 분리 균주를 Glomax multi detection system (Promega, USA)으로 발광량을 측정한 결과, 100-200 cpm 정도로서 균을 접종하지 않은 TSB 배지와 유사한 값을 나타내어 luminescence 가 감지되지 않는 것으로 판정하였다. Defoirdt et al. (2008)는 비록 많은 Vibrio harveyi가 발광성을 띠는 것으로 알려져 있지만 그 발현성 정도는 균주간에 차이가 크고 발광성을 보이지 않는 균주도 있음을 보고하였으며 발광성을 띠지 않는 Vibrio harveyi가 높은 용혈성을 보이는 등 발광성 세기나 발광성을 띠는지 여부와 병원성간에는 상관성이 없음을 보고하였다. 균주별로 발광성에 있어 차이가 나타나는 원인은 아직까지 명확히 규명되지는 않았지만 발광성을 보이지 않는 균주는 lux operon 이나 quorum sensing signal transduction과 같은 발광조절인자 유전자에 결손이 발생한 것으로 추측되고 있다(Defoirdt et al., 2005). 본 연구에 공시한 Vibrio harveyi는 toxR유전자나 haemolysin유전자는 발현되나 발광성이 감지되지 않는 균주이었다.
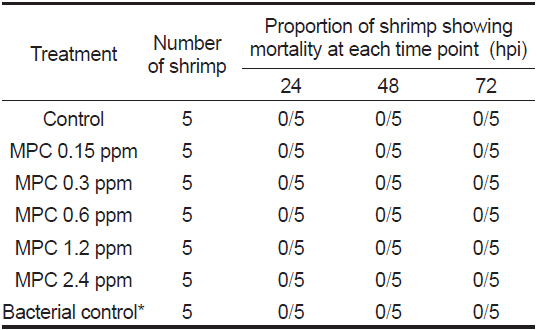
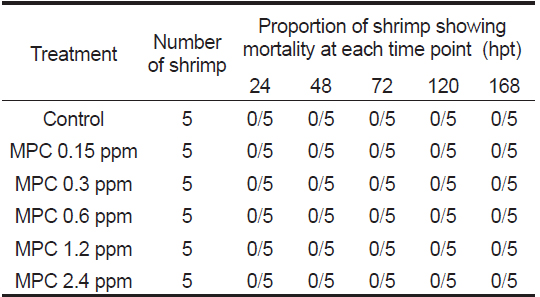
Monopersulfate 화합물이 0, 0.15, 0.3, 0.6, 1.2, 2.4 ppm의 농도로 처리 된 해수에 Vibrio harveyi를 첨가하여 30분간 monopersulfate 화합물과 반응시킨 후 새우 5마리씩을 각각의 수조에 넣고 3일간 생존유무를 관찰한 결과, 모든 시험군에서 폐사한 새우는 관찰되지 않았다. 다만 Vibrio harveyi만 처리 된 병원체 대조군에서는 새우의 활력이 현저히 감소하는 것이 관찰되었다(Table 3). 이를 통하여 monopersulfate 화합물은 최고 2.4 ppm까지 투여하여도 새우에는 이상을 야기하지 않음을 알 수 있으며 Vibrio harveyi를 1×106 CFU/mL의 농도로 해수를 통하여 새우에 3일동안 노출 시 새우의 활력은 저하시키나 폐사까지는 유발시키지 않음을 알 수 있었다.
일반적으로 Vibrio harveyi는 균주별로 병원성이 다양하여 새우 체중 g당 103-107 CFU의 높은 양의 균수에서도 새우에 폐사를 유발하지 않는 균주가 있는가 하면 최근 중국에서 보고되고 있는 Vibrio harveyi HLB0905 균주의 경우와 같이 38 CFU의 양으로도 48시간 이내에 접종된 흰다리새우에서 60%가 폐사하는 고도의 병원력을 지니는 경우도 있다(Zhou et al., 2012). Vibrio harveyi HLB0905 균주는 비발광성의 고병원성을 띠며 HLB0905 균주로 명명되었고 높은 폐사율과 섬유세포와 횡문근의 심각한 괴사가 유발되고 꼬리부분에 탁한 손상이 특징적으로 관찰되어 “세균성 백미병(bacterial white tail disease, WTD)”으로 불리고 있다.
본 연구에서 공시한 Vibrio harveyi는 비발광성의 toxR과 haemolysin 등의 병원성 인자를 띠는 균주로서 1×106 CFU/mL의 양으로 해수에 첨가한 후 흰다리새우를 균이 있는 해수에 넣어 균에 노출시켰다. 이러한 조건에서는 흰다리새우의 단시간내의 폐사는 관찰되지 않으며, 활동성 저하가 관찰되었다.
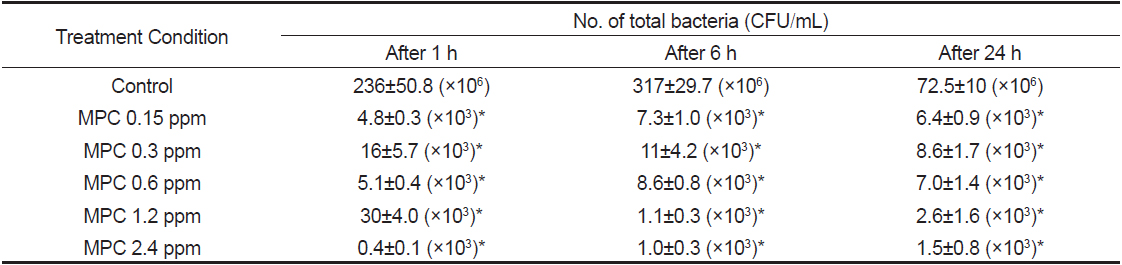
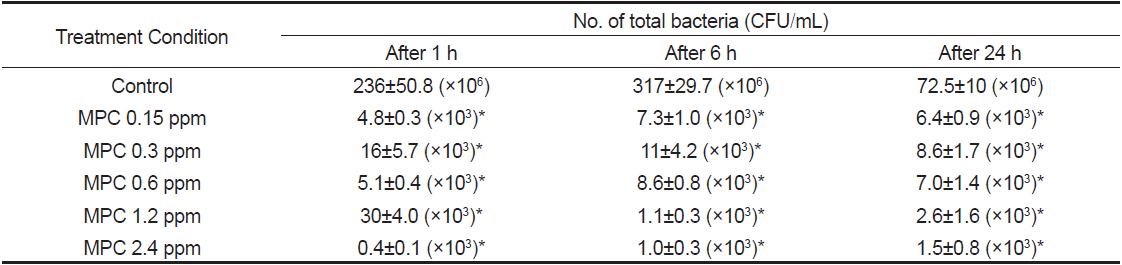
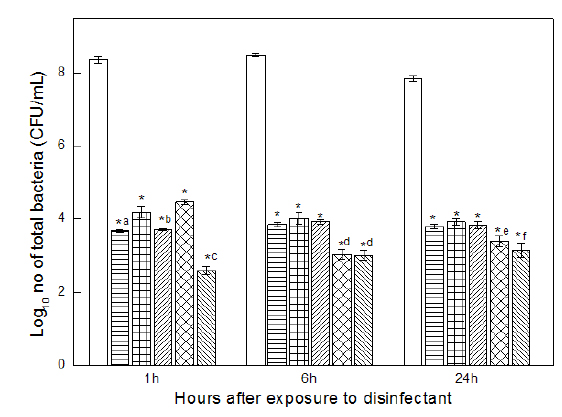
Monopersulfate 화합물 0, 0.15, 0.3, 0.6, 1.2, 2.4 ppm의 농도를 해수에 처리하고 Vibrio harveyi를 첨가하여 30분간 monopersulfate 화합물과 반응시킨 후 새우 5마리씩을 각각의 수조에 넣은후 1시간, 6시간, 24시간째에 총 세균수를 측정한 결과 Table 4와 같이 나타났다. 즉, monopersulfate 화합물에 의하여 1시간째에는 총세균수는 모든 농도의 monopersulfate 화합물 처리농도에서 약 105 CFU/mL의 현저한 감소가 확인되었으며 최고 농도인 1.2 ppm에서는 106 CFU/mL 이상의 균 억제가 확인되었다. 이러한 균 억제는 해수에 monopersulfate 첨가 후 6시간, 24시간째에도 유사하게 나타났으나, 1.2 ppm과 2.4 ppm에서는 다른 농도군에 비해서도 유의한 감소(P<0.001)가 확인되어 농도가 높을수록 총균수 억제효과는 강하게 유지됨을 알 수 있다(Fig. 2). Monopersulfate는 산화 계열 소독제로서 조류제거(algicide) 효과와 살균 효과가 우수하며 농도와 반응시간에 의해 소독력이 결정되며 20분 이상 노출될 경우 효과가 분명히 나타나는 것으로 보고되어 있다 (Wu et al., 2014). 본 연구에서는 monopersulfate 화합물과 균액을 30분간 반응하고 이후 새우에 노출시킨 바 이러한 조건에서 새우에는 영향을 미치지 않으면서 살균효과가 24시간 까지도 유지됨을 알 수 있다.
[Fig. 2.] Inhibition of the growth of bacteria in sea-water after incubation in the presence of various concentration of monopersulfate compound. Results are mean±SD of triplicate data. □, bacterial control; ▤, monopersulfate compound 0.15 ppm; ▦, monopersulfate compound 0.3 ppm; ▨, monopersulfate compound 0.6 ppm ▩, monopersulfate compound 1.2 ppm; ▧, monopersulfate compound 2.4 ppm *Significantly different from bacterial control (P<0.001) a, significantly different from monopersulfate compound 0.3 ppm (P<0.01) and 1.2 ppm (P<0.001) b, significantly different from monopersulfate compound 0.3 ppm and 1.2 ppm (P<0.01) c, significantly different from monopersulfate compound 0.3 ppm and 1.2 ppm (P<0.001) d, significantly different from monopersulfate compound 0.15, 0.3, and 0.6 ppm (P<0.01) e, significantly different from monopersulfate compound 0.15ppm (P<0.01), 0.3ppm (P<0.001) and 0.6ppm (P<0.01)f, significantly different from monopersulfate compound 0.15, 0.3, and 0.6ppm (P<0.001)
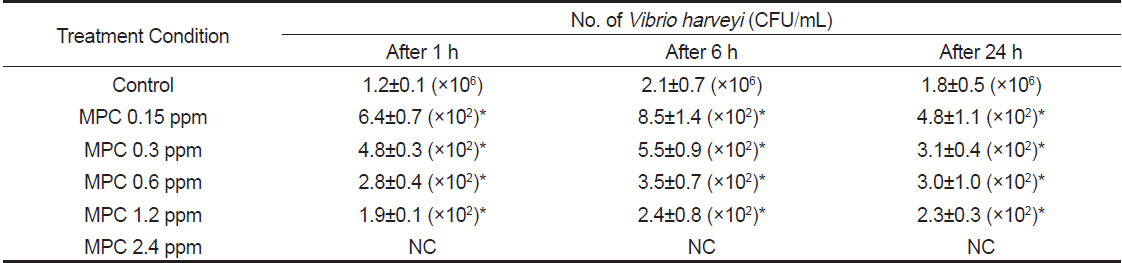
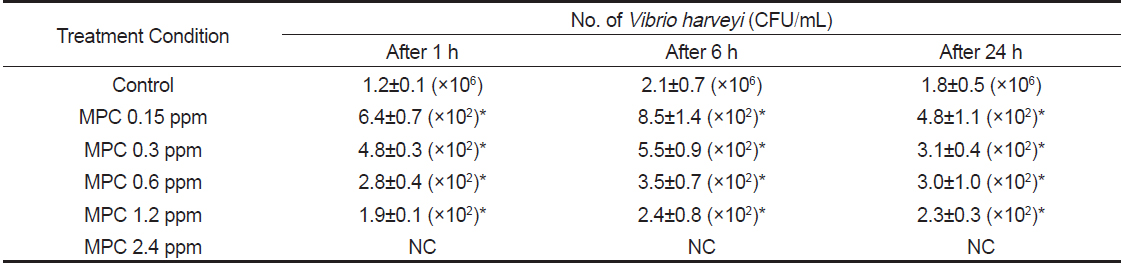
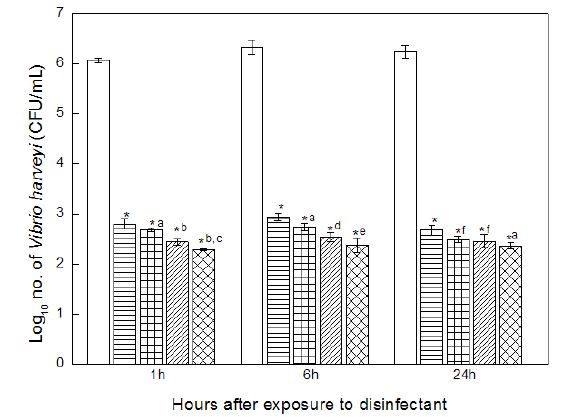
Monopersulfate 화합물 농도에 따른 Vibrio harveyi 균 억제 효과를 확인하기 위하여 0, 0.15, 0.3, 0.6, 1.2, 2.4 ppm의 monopersulfate와 Vibrio harveyi 를 30분간 반응시킨 후 일정량의 해수를 취하여 TCBS 배지에 도말하여 배양 한 후 Vibrio harveyi 균수를 측정한 결과 Table 5와 같은 결과를 얻었다. 즉, 반응 후 1시간, 6시간, 24시간째 병원체 대조군의 Vibrio harveyir는 평균 1.7±0.5×106 CFU/mL로 확인 된 반면, monopersulfate 2.4 ppm에서는 반응 후 1시간째부터 Vibrio harveyi가 검출되지 않았다. 또한, monopersulfate 0.15, 0.3, 0.6, 1.2 ppm에 서는 Vibrio harveyi 균수는 각각 6.6±1.9×102 CFU/mL, 4.5±1.2×102 CFU/mL, 3.1±0.4×102 CFU/mL, 2.2±0.3×102 CFU/mL으로 병원체 대조군에 비하여 약 104배 감소하였으며 균억제 정도는 농도의존적이었다(P<0.001). Monopersulfatedml Vibrio harveyi 균에 대한 살균효과는 노출 후 6시간째 및 24시간 째에도 지속적으로 유지되어 농도의존적으로 살균효과가 나타났고 최고용량인 monopersulfate 2.4 ppm에 의해서는 24시간까지 Vibrio harveyi가 검출되지 않았다. 따라서 monopersulfate 2.4 ppm을 첨가할 경우 해수중의 Vibrio harveyi가 완벽하게 제거됨을 알 수 있다.
[Fig. 3.] Inhibition of the growth of Vibrio harveyi in sea-water after incubation in the presence of various concentration of monopersulfate compound. Results are mean±SD of triplicate data. □, bacterial control; ▤, monopersulfate compound 0.15 ppm; ▦, monopersulfate compound 0.3 ppm; ▨, monopersulfate compound 0.6 ppm ▩, monopersulfate compound 1.2 ppm; ▧, monopersulfate compound 2.4 ppm *Significantly different from the bacterial control group (P<0.001) a, significantly different from monopersulfate compound 0.15 ppm (P<0.01) b, significantly different from monopersulfate compound 0.15 ppm and 0.3 ppm (P<0.001) c, significantly different from monopersulfate compound 0.6 ppm (P<0.05) d, significantly different from monopersulfate compound 0.15 ppm (P<0.001) and 0.3 ppm (P<0.05) e, significantly different from monopersulfate compound 0.15 ppm (P<0.001) and 0.3 ppm (P<0.01) f, significantly different from monopersulfate compound 0.15 ppm (P<0.05)
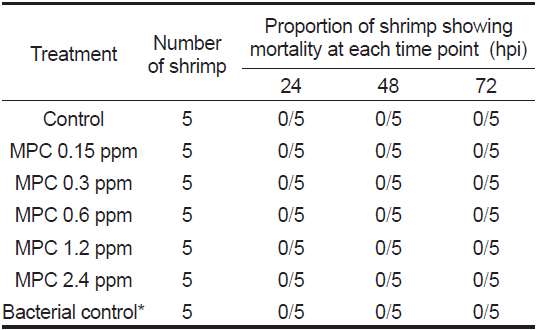
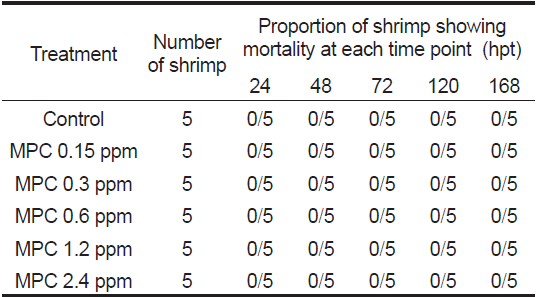
Monopersulfate 화합물이 흰다리새우에 미치는 영향을 조사하기 위하여 수조에 0, 0.15, 0.3, 0.6, 1.2, 2.4 ppm의 monopersulfate을 첨가한 후 흰다리새우를 5마리씩 넣고 7일간 관찰한 결과 새우는 모두 생존하였고 활동력 등에도 대조군과 차이가 없었다(Table 6). 현재까지 monopersulfate 화합물의 흰다리새우에 대한 독성 관련 연구보고는 없다. 본 연구에서는 monopersulfate가 해수에서 Vibrio harveyi를 거의 완벽하게 살균하는 농도인 2.4 ppm에서 7일간의 사육 기간 중 새우의 생존과 활동력에는 영향이 없음이 확인되었는바, monopersulfate 화합물이 새우양식에 있어 새우에는 영향을 미치지 않으면서 비브리오균 제거할 수 있는 유효한 소독제로 쓰일 수 있음을 알 수 있다.
결론적으로, monopersulfate 화합물은 자연적으로 해수 중에 존재하는 세균과 새우 양식업에서 심각한 질병 원인체 중 하나인 Vibrio harveyi를 효과적으로 억제하며 유효성이 확인된 농도에서 새우의 생존과 활동력에 영향을 미치지 않음을 알 수 있었다.