캡슐화 기술은 고체, 액체, 기체상의 물질이 특정 조건하에서 조절된 속도로 방출될 수 있도록 어떤 물질이나 조직 내부에 포장하는 기술을 말하며, 의약품, 공업재료, 향료 및 식품 분야 등에 널리 응용되고 있다(Chan et al., 2011; Gryshkov et al., 2014). 식품 분야에서는 변질 방지, 보존성 향상, 안정화, 이취의 차단, 액상식품의 캡슐화, 향기 보존 및 물성 개선 등의 목적으로 다양하게 이용되고 있다.
어유의 경우, 산화에 의한 어취와 쓴맛의 방지를 위하여 미세 캡슐화가 많이 시도되고 있는데, 직경이 5 mm이상인 macro capsules은 0.5-1.0 mm의 두꺼운 껍질로 둘러싸여 있기 때문에 소화도가 매우 낮아, 수십 μm의 직경을 갖는 micro capsules을 제조하는 방법인 미세 캡슐화(micro encapsulation)가 많이 시도되고 있다(Lim and Jwa, 1999). 이러한 미세 캡슐화 기술은 분사조립법, 분무조립법, 액중조립법, 전동조립법 등 여러 가지 종류가 있으며(Kim et al., 1996), 미세 캡슐화 기술을 이용하여 지방의 산화를 억제하려는 많은 시도가 이루어지고 있다(Katrin and Knut, 1999). Kim et al. (1996)은 n-3계 지방산을 함유하는 어유를 emulsion 방법으로 미세 캡슐화하여 그 특성을 조사하였다. 하지만, emulsion 방법에 의한 n-3계 고도불포화지방산의 미세 캡슐화는 캡슐의 안정성이 낮은 것이 단점으로 지적되어 왔으며(Jang et al., 2000), 분무건조를 이용하여 제조한 미세 캡슐은 액상제품 등에는 첨가가 곤란하며 식품가공과정 중 풍미에도 좋지 않은 영향을 미치는 것으로 알려져 있다(Kim et al., 1996).
한편, 겔(gel)화 기재로 사용되는 알긴산나트륨은 갈조류의 대표적인 다당류로서친수성 염의 형태로 물에서 쉽게 수화되며, 그 수용액에 칼슘이온을 첨가하면 열에 안정한 겔을 형성할 수 있어 캡슐화 재료로 널리 이용되고 있다(Vandenberg et al., 2001; Rousseau et al., 2004). 알긴산 겔을 이용하여 Ji et al. (2007)와 Woo et al. (2007)은 caviar analog를 제조하였고, Jo et al. (2014)은 날치알 analogs 제조 조건을 구명한 바 있다. 또한 수용성인 알긴산은 액체 캡슐을 형성하는 능력이 있으며, 점도가 높은 고지방 식품도 캡슐화 할 수 있는 장점을 지니고 있다(Blandino et al., 1999).
따라서 본 연구에서는 calcium alginate gel을 이용하여 어유를 캡슐화하고, 제조된 캡슐의 특성과 캡슐 내부에 함유된 어유의 산화 안정성을 살펴보았다.
본 실험에서 사용한 어유는 (주) 동원 F&B 창원공장에서 참치 통조림 가공 시 나오는 참치 안와를 자숙할 때 부상하는 기름을 탈검, 탈산, 탈색 및 winterization을 거쳐 제조한 시판 조제유를 사용하였다. 캡슐 제조를 위한 재료로는 알긴산나트륨(Katayama Chemical Co., Ltd., Japan), 무수 염화칼슘(Yakuri Pure Chemicals Co., Ltd., Japan) 및 carboxymethyl cellulose(CMC, Katayama Chemical Co., Ltd., Japan)를 사용하였다.
캡슐의 제조는 Ji et al. (2007)의 방법을 일부 수정하여 단일노즐과 이중노즐의 두 가지 방식을 사용하여 제조하였다. 단일노즐을 이용한 캡슐의 제조는 CMC (1.5%, w/v)와 염화칼슘(1.2%, w/v)을 함유하는 겔화 가교제 용액에 어유를 각각 10, 20, 30, 40 및 50% (w/w) 비율이 되도록 첨가하였고 이중노즐을 이용한 캡슐의 제조는 어유를 30% (w/w) 비율이 되도록 첨가하여 이를 실온에서 10분간 교반하였다. 이 혼합용액을 peristaltic pump (Cassette tube pump SMP-23, Eyela, Japan)를 이용하여 노즐에 연결되어 있는 튜브(내경, 3 mm)를 통하여 흘려 보내면서 알긴산나트륨(0.8% w/v)용액이 담긴 반응조내에 떨어뜨려 반응액을 교반시키면서 캡슐화하였다. 이때 혼합용액을 떨어뜨리는 시간은 1분으로 하였고, 반응조에서의 반응시간은 3분으로 하였으며, 3분 후 체를 이용하여 용액으로부터 캡슐을 분리한 후, 캡슐 외막에 부착한 과잉의 알긴산나트륨을 수세하여 제거하고 2% (w/v) 염화칼슘 용액에 침지시켜20분간 안정화시켰다. 이때 노즐은 내경 1 mm의 것을 사용하였고, 노즐 선단에서 알긴산나트륨 용액 표면까지의 낙하거리를 15 cm로 고정하였으며, peristaltic pump의 유속은 0.05 mL/s, 알긴산나트륨 용액이 담긴 반응조의 교반속도는 280 rpm으로 고정하여 캡슐을 제조하였다.
캡슐의 크기 및 막 두께는 컴퓨터와 연결된 광학현미경(BX-50, Olympus, Japan)을 이용하여 40배의 비율로 관찰하면서 Image-Pro program을 이용하여 측정하였다. 이때 캡슐의 크기는 위의 조건별로 제조된 캡슐을 각각 5개씩 무작위로 골라낸 후 장경과 단경을 재어 그 평균으로 하였으며, 막 두께는 캡슐의 상하좌우의 막 두께를 각각 측정하여 그 평균값으로 하였다.
캡슐의 구형성능은 제조된 캡슐의 각 5개에 대한 캡슐의 장경에 대한 단경의 백분율로 표시하였다.
캡슐의 파열강도 및 변형심도는 각각의 조건 별로 제조된 캡슐을 5개씩 골라내어 Rheometer (Model CR-100D, Sun Scientific Co., Ltd., Japan)를 사용하여 측정하였다. 이때 사용한 plunger는 직경 10 mm의 원판형을 사용하였다.
캡슐당 어유의 양은 각각의 조건 별로 제조된 캡슐을 100개씩 골라내어 조지방 함량을 측정한 후 그 함량을 100으로 나눈 값을 캡슐 1개당 어유의 량으로 하였다. 캡슐화 율은 캡슐 제조를 위해 주입한 어유의 총량에 대해 캡슐제조 후 캡슐화된 어유의 함량을 측정하여 주입 총량에 대한 캡슐화된 어유 함량의 백분율로 나타내었다.
POV의 측정은 Takagi et al. (1977) 방법을 이용하였으며, 저장조건을 동일하게 하기 위하여 어유의 총량이 50 mg이 되도록하여 실험하였다. 즉, 어유 캡슐의 경우 캡슐당 어유량이 약 3.3 mg이므로 50 mg에 해당하는 15개의 캡슐을 Eppendorf tube안에 넣은 후 37℃에서 저장하면서 실험하였고, 캡슐화하지 않은 어유는 마이크로피펫을 이용하여 50 mg을 Eppendorf tube 안에 넣고 저장하였다. 각각의 조건에 대한 실험구는 4개로 하여 그 평균과 표준편차를 구하여 측정값으로 하였다
유의차 검정은 분산분석을 한 후
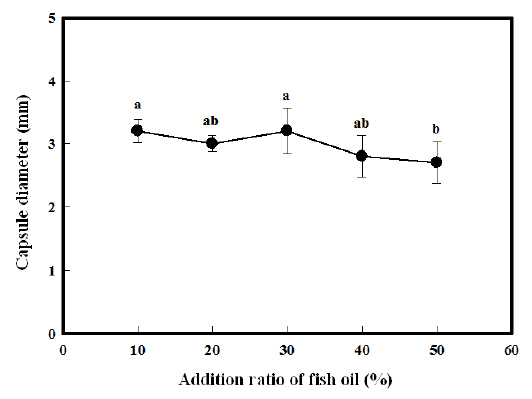
어유의 첨가비율을 달리하여 제조한 캡슐의 크기 변화는 Fig. 1에 나타내었다. 그 결과, 어유를 10-40% 첨가한 경우, 캡슐의 크기는 5% 유의수준에서 큰 차이가 나타나지 않았다. 또한 전체적으로 보았을 때 어유의 농도에 따른 캡슐의 크기가 3 mm 내외에서 큰 폭의 차이를 나타내지 않는 것으로 나타나 어유의 첨가량이 달라진다고 하더라도 캡슐의 크기에는 큰 영향을 미치지 않는 것으로 나타났다.
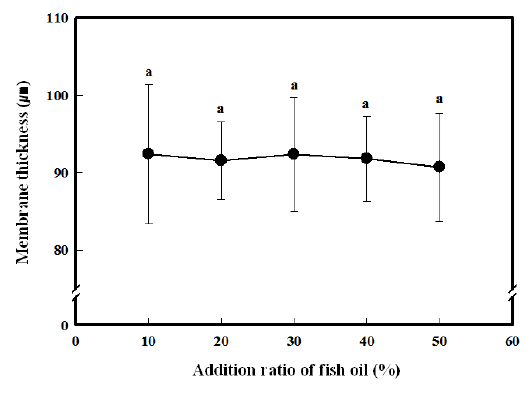
어유의 첨가량에 따른 캡슐의 막 두께 변화는 Fig. 2에 나타내었다. 어유의 농도에 따라 약간의 차이는 있었지만, 약 90 μm 내외의 막 두께를 가지는 것으로 나타났으며, 유의차 검정 결과, 5% 유의 수준에서도 유의차는 없었다.
따라서 어유의 첨가비율은 캡슐의 크기나 막두께에 영향을 거의 미치지 않는다고 볼 수 있는데, 이러한 사실은 Blandino et al. (1999)의 연구에도 밝혀진 바 있다. 즉, calcium alginate gel capsule 제조시 칼슘과 알긴산의 농도에 따라서 캡슐의 막 두께와 크기가 달라지는데, 알긴산의 농도가 낮을수록, 칼슘의 농도가 높을수록 막 두께가 두꺼워지고 캡슐의 크기도 커진다고 하였다. 또한, Blandino et al. (2000)은 칼슘과 알긴산의 농도 뿐만 아니라 겔화 작용이 일어나는 반응시간에 따라서 캡슐의 크기와 막 두께가 달라진다고 하였는데, 알긴산과 칼슘의 농도가 일정할 경우 반응시간이 길어짐에 따라 막 두께가 두꺼워지고, 크기도 커진다고 하였다. 하지만, 본 실험에서는 알긴산의 농도를 0.8%, 칼슘의 농도를 1.2%로, 반응시간을 3분으로 고정하여 실험을 행하였으므로, 어유의 첨가비율에 관계없이 캡슐의 크기와 막 두께가 거의 일정하게 되었다고 볼 수 있다.
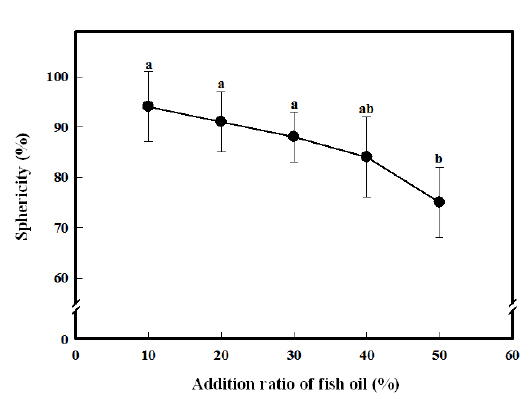
구형성능은 제조된 캡슐이 얼마나 구의 형태에 가까운가를 나타내는 것으로서, 캡슐의 장경과 단경의 길이가 같을 때, 즉 구형성능이 100%가 될 때가 완전한 구의 형태를 나타낸다고 할 수 있다. Fig. 3은 어유의 첨가 비율을 달리하면서 제조한 캡슐의 구형성능을 나타낸 것이다. 그 결과, 어유의 첨가비율이 증가함에 따라 구형성능은 조금씩 감소하는 경향을 나타내었다. 이러한 원인은 Blandino et al. (1999)이 지적하였듯이 CMC는 점성이 강하기 때문에 CMC와 염화칼슘의 혼합용액이 알긴산 용액 속으로 떨어질 때 하나 하나의 액적이 구형을 이루면서 떨어지도록 해주는 역할을 하는데, 혼합 용액 중의 어유의 비율이 높아지게 되면 액적이 떨어질 때 CMC의 비율이 낮아지게 되므로 구형성능이 낮아지게 되는 것이다. 또한 액적이 떨어져 알긴산 용액 속에서 회전하면서 캡슐을 형성할 때에도 점성이 낮아지게 되면 회전력(원심력)의 영향을 많이 받게 되어 캡슐이 구형을 이루지 못하고 타원형에 가까워지게 된다. 따라서 어유의 첨가량이 높아질수록 캡슐의 구형성능은 떨어지게 되므로 어유를 40% 이상 첨가하는 것은 좋은 모양의 캡슐을 얻기는 어려울 것으로 판단된다.
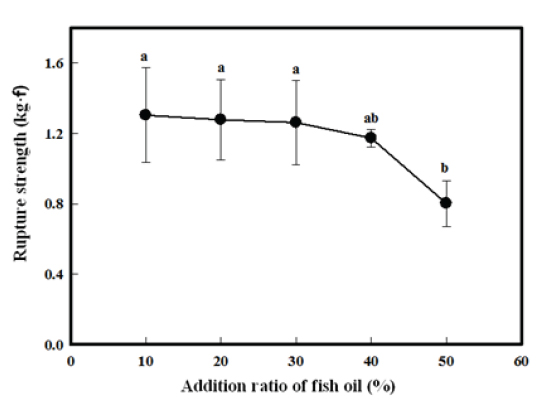
제조된 어유의 첨가비율이 캡슐의 물성에 미치는 영향 중에서 캡슐의 강도와 탄성을 나타내는 척도인 파열강도 및 변형심도를 측정하였다. 캡슐의 파열강도와 변형심도가 크다는 것은 캡슐이 외부의 물리적 자극에 영향을 작게 받는다는 것을 나타내므로 그만큼 캡슐이 안정하다는 의미로 해석할 수 있다. Fig. 4에서 보는 바와 같이 참치 안구유의 첨가비율이 30%까지는 파열강도의 차이를 나타내지 않았으나, 참가비율이 30%를 초과하면서부터는 파열강도가 감소하기 시작하여 50%에서는 급격히 감소하는 경향을 나타내었다.
이러한 파열강도의 감소원인은 캡슐 내부에 포획된 어유의 양이 증가함에 따라 겔을 형성하는 소재인 CaCl2와 점성을 유지하도록 하는 CMC의 양이 감소하게 되고, 그 결과 캡슐의 안정도가 떨어지기 때문인 것으로 판단된다. 특히, CaCl2가 감소하게 되면 캡슐의 막을 이루게 되는 겔의 형성이 감소하게 되므로 막의 구조가 약하게 되어 캡슐의 파열강도가 감소하게 되는 것으로 판단된다. 또한 어유의 첨가비율이 증가하게 되면 앞에서 설명한 바와 같이 캡슐의 구형성능이 떨어지게 되므로 외부의 자극에 대하여 쉽게 변화를 일으키게 되어 캡슐의 안정도가 감소하는 것으로 판단된다.
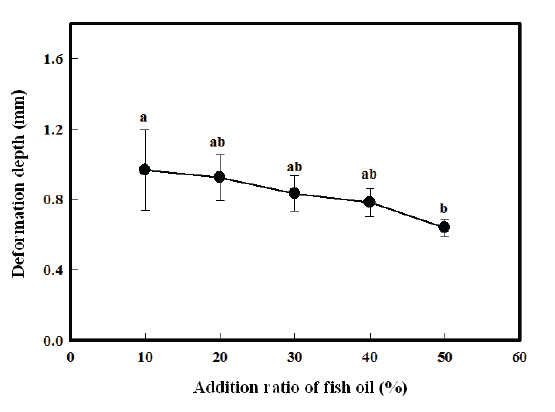
변형심도 역시 어유의 첨가비율이 증가할수록 조금씩 감소하게 되는데(Fig. 5), 이러한 이유는 파열강도의 경우와 마찬가지로 어유의 첨가비율이 증가할수록 캡슐 내부의 CMC의 양이 줄어들고, 캡슐의 구형성능이 감소하기 때문인 것으로 판단된다.
따라서 어유의 첨가비율이 증가하게 되면 캡슐의 안정도가 감소하여 캡슐의 파열강도 및 변형심도가 감소하게 되는 것으로 판단된다.
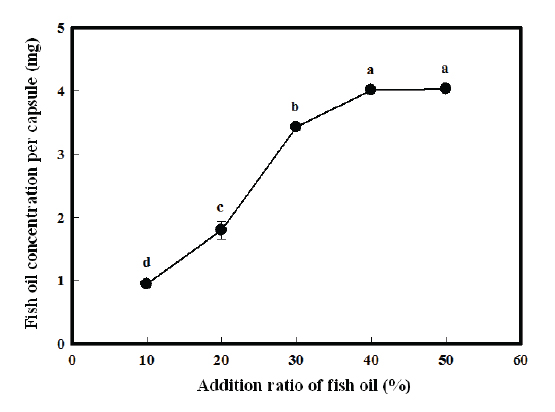
어유의 첨가비율을 달리하여 제조한 각각의 캡슐에 대하여 캡슐당 어유량을 측정한 결과를 Fig. 6에 나타내었다. 그 결과, 어유의 첨가비율이 증가할수록 캡슐당 어유량은 증가하다가 첨가비율이 40% 이상이 되면서부터 캡슐당 어유량은 큰 변화를 나타내지 않았다.
이러한 이유는 캡슐 내부에 포획될 수 있는 어유의 양이 한정되어 있기 때문으로 생각된다. 즉, 어유의 첨가비율이 낮을 경우에는 주입되는 양에 비례하여 캡슐 내부로 포획되는 어유의 양이 증가하지만, 어유의 첨가비율이 너무 높아지게 되면 주입되는 어유의 양에 관계없이 캡슐 내부에 포획될 수 있는 양 만큼만 캡슐화되기 때문인 것으로 판단된다.
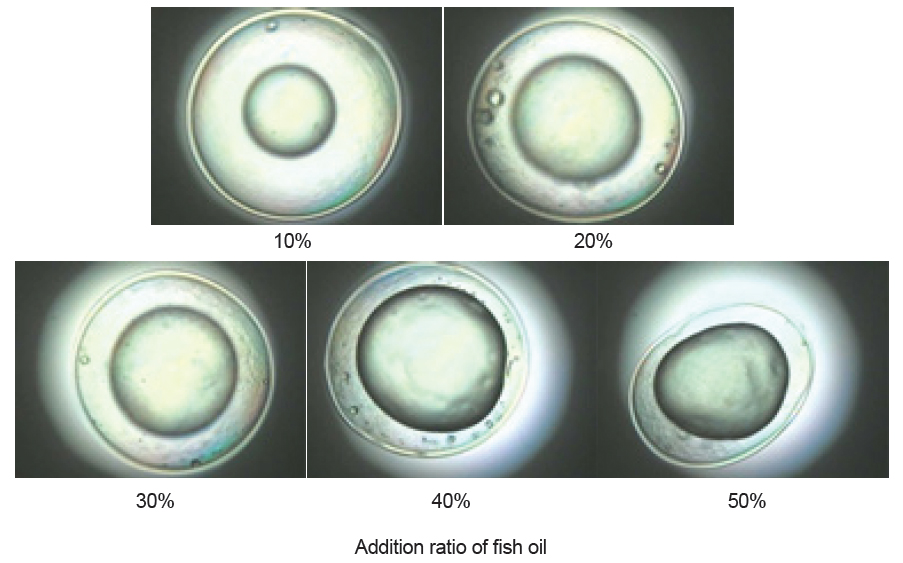
Fig. 7은 어유의 첨가비율을 각기 달리하여 제조한 캡슐의 사진을 나타낸 것이다. 그림에서와 같이 어유의 첨가비율이 증가 할수록 캡슐 내부에 포획된 어유의 양이 조금씩 증가함을 알 수 있다. 하지만, 어유의 첨가비율이 40% 이상이 되면서부터 캡슐의 형태가 일그러지고, 캡슐 내부에 포획된 어유도 구형을 이루지 못한다는 것을 볼 수 있다. 이러한 형태의 일그러짐은 곧 구형성능의 저하를 나타내며, 그에 따라서 캡슐의 파열강도와 변형심도의 저하를 가져온다는 사실을 알 수 있다. 또한 캡슐 내부에 포획될 수 있는 어유의 양에도 한계가 있음을 알 수 있다.
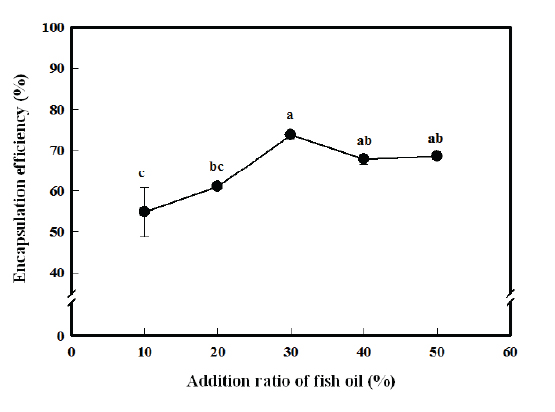
캡슐화 율은 캡슐을 제조하기 위해 주입된 어유의 총량에 대하여 캡슐화된 어유의 비율을 나타낸 것으로서, 그 수치가 높을수록 많은 양이 캡슐화 되었음을 의미한다. Fig. 8에서 보는 바와 같이 어유의 첨가비율이 증가할수록 캡슐화 율은 증가하다가 30% 이후부터는 조금 감소하는 경향을 나타내었다. 이러한 이유는 처음에는 어유의 첨가비율이 증가할수록 캡슐내부로 포획되는 어유의 양 즉, 캡슐당 어유량이 증가하지만, 어유의 첨가비율이 30%를 초과하게 되면 캡슐당 어유량이 일정수준을 유지하기 때문인 것으로 판단된다. 즉, 많은 양의 어유를 주입하여 캡슐을 제조하더라도 캡슐당 어유량에는 한계가 있기 때문에 캡슐화되지 못하는 어유가 다량 발생하게 되어 결국 캡슐화 율이 감소하게 되는 것으로 판단된다. 하지만, 전체적인 캡슐화 율은 약 50-70% 사이의 수준을 유지하는데, 이러한 수치는 일반적인 어유의 미세캡슐화에서 나타난 25-46%의 캡슐화 율보다는 높은 수치이다.
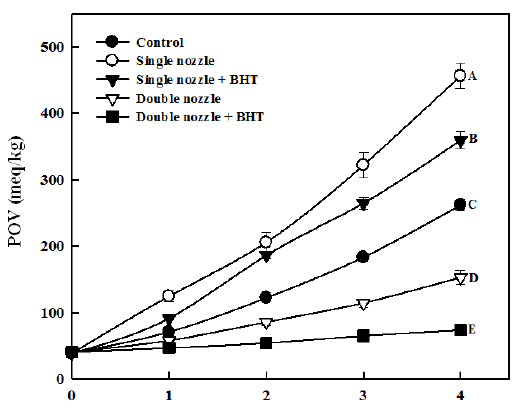
어유 캡슐의 저장 중 산화에 대한 안정성을 구명하고자 단일노즐과 이중노즐을 이용하여 각각의 어유 캡슐을 제조하여 산화안정성을 검토하여 Fig. 9에 나타내었다. 그 결과, 단일노즐로 제조한 캡슐의 경우에는 산화안정성이 아주 나쁜 것으로 나타났다. 단일 노즐의 경우는 산화방지제를 첨가하더라도 대조구에 비해 산화 정도가 높게 나타났다. 단일노즐을 이용하여 캡슐을 제조할 경우 겔화 가교제에 현탁, 분산시킨 어유를 지속적으로 교반하는 과정에서 공기가 유입되는데, 이러한 공기의 유입이 어유의 산화에 영향을 미치게 되어 산화가 더 빨리 일어나는 것으로 판단된다.
한편, 이중노즐을 이용하여 제조한 캡슐의 경우는 산화안정성이 우수한 것으로 나타났다. 특히, BHT를 첨가하여 이중노즐로 캡슐화하였을 경우에는 저장 후 4일이 경과한 시점에서도 거의 산화가 진행되지 않은 것으로 나타났다. 어유에 BHT를 0.01% 첨가한 후 이중노즐을 이용하여 캡슐을 제조할 경우 대조구에 비하여 항산화 능력이 뛰어난 것으로 나타났다. Katrin and Knut (1999)은, 분무건조 등을 통한 어유의 미세 캡슐화는 고온으로 인하여 어유의 산화가 촉진 될 수 있으므로 그 사용에 있어 많은 제약이 따른다고 하였는데, 본 실험에서 이용한 어유의 캡슐화는 저온에도 캡슐화가 가능하기 때문에 분무건조에 의한 방법보다 어유의 산화를 더 억제할 수 있을 것이라 판단된다.
이상의 결과를 종합하여 판단해 볼 때, 단일 노즐을 이용하여 어유를 캡슐화 할 경우에는 공기의 유입으로 인하여 어유의 산화가 촉진되지만, 이중노즐을 이용하여 어유를 캡슐화 할 경우, 캡슐화하지 않은 어유보다 산화안정성이 뛰어난 어유 캡슐을 제조할 수 있으며, 특히 어유에 BHT를 첨가하여 이중노즐을 이용하여 캡슐화 할 경우에는 높은 산화 억제효과를 얻을 수 있는 것으로 나타났다. 따라서 알긴산나트륨의 겔화 특성을 이용한 어유의 캡슐화에 있어서는 이중노즐을 이용하고 산화방지제를 첨가하여 제조하는 경우 캡슐화 어유의 산화안정성을 크게 증강시킬 수 있을 것으로 판단된다.