어분은 어류가 필요로 하는 아미노산을 고르게 갖춘 양질의 단백질원이지만, 가격이 비싸고 수급이 불안정하여 대체 단백질원으로 대두박의 활용도가 매우 높다(Dabrowski et al., 1989). 그러나 대두박은 아미노산의 불균형, protease inhibitor, tannins, lectins, 그리고 non-starch polysaccharides (불용성 탄수화물) 등의 anti-nutritional factors (ANFs)가 어류의 성장을 저해하는 것으로 보고되어 있으며(Francis et al., 2001), 특히 ANFs는 장에서 염증 반응을 일으키고, 장벽의 융모(villi)를 짧게 하거나, 염증 세포의 침윤을 유발하는 등 무지개송어 장의 형태적 변화를 유발하는 것으로 알려져 있다(Mansfield et al., 2010).
그러나 이러한 문제에도 불구하고 탄수화물의 이용성이 큰 온수성 어류를 중심으로 대두박 사료의 이용성이 많이 개선되었고, 경제성을 고려하면 차넬메기 및 틸라피아에서는 완전 대체가 가능한 것으로 알려져 있다(Mohsen and Lovell, 1990). 그러나 육식성어류인 무지개송어에서는 대체적으로 대두박 함량이 높아질수록 성장, 사료효율, 사료섭취량이 뚜렷이 감소하는 경향을 보이며(Gao et al., 2011), 일반적으로 사료 중 10-15% 정도 대두박을 첨가할 수 있는 것으로 알려져 있다(Krogdahl et al., 1994; Refstie et al., 2000).
양어 사료의 생물학적 이용성 평가는 사료에 대한 기호성 평가, 사육을 통한 성장 비교, 사료 및 어체의 일반성분 분석을 통한 영양 성분의 체내 축적 효율, 그리고 표식 물질을 사료에 넣어 영양소의 소화 흡수율을 평가하는 방법 등이 널리 사용되어 왔다. 나아가 사료의 생물학적 이용성을 규명하고자 사료 섭취 후 시간 경과에 따른 위 및 장 소화물의 소화 경향, 소화관 내 소화 효소의 분포 및 활성 등의 생리적인 변화(Dabrowski et al., 1989), 혈액 성분의 조성과 함량 변화, 실험 사료의 영양소의 소화율 및 이용과 흡수 현황 등을 파악하려는 소화 생리학적 연구도 시도된 바 있다(Kaushik and Oliva Teles, 1985; Wilson and Poe, 1985; Yamamoto et al., 2010; Larsen et al., 2012).
어류의 위 및 장 내용물에 관한 연구는 대개 어류의 계절별 먹이 선호도, 조성, 섭취량, 포식자와 피포식자와의 관계를 규명하여 대상 생물의 먹이 특성을 밝히거나, 대상 생물의 feeding history와 종의 생산력을 추정하는 생태학적 연구에 많이 활용되었지만(MacDonald et al., 1982), 어류 양식 분야에서도 사료의 종류와 질에 따른 일일사료공급량과 횟수, 사료의 소화 시간, 사료 섭취 후 경시적인 변화, 소화 효소의 조성과 분비량 등 사료의 질을 평가하는 수단으로도 많이 이용하고 있다(Storebakken, 1985; Jobling, 1986; Bromley, 1987; Rosch, 1987; Larsen et al., 2012).
따라서 본 연구에서는 대두박을 다량 첨가한 실험사료의 성장 지연 원인을 해명하는 수단으로 소화·생리학적 연구를 통한 접근이 매우 유용할 것으로 판단되어, 대두박을 장기간 먹인 무지개송어를 대상으로 사료 공급 후 위(胃) 내용물의 양적 변동, 수분 함량과 pH 변화, 내용물의 가소화(可消化) 정도를 경시적으로 파악함으로써 대두박 사료의 이용성을 평가하고자 하였다.
본 연구는 대두박 사료(Table 1)로 실내 순환여과 시설에서 160일간의 장기사육한 무지개송어(
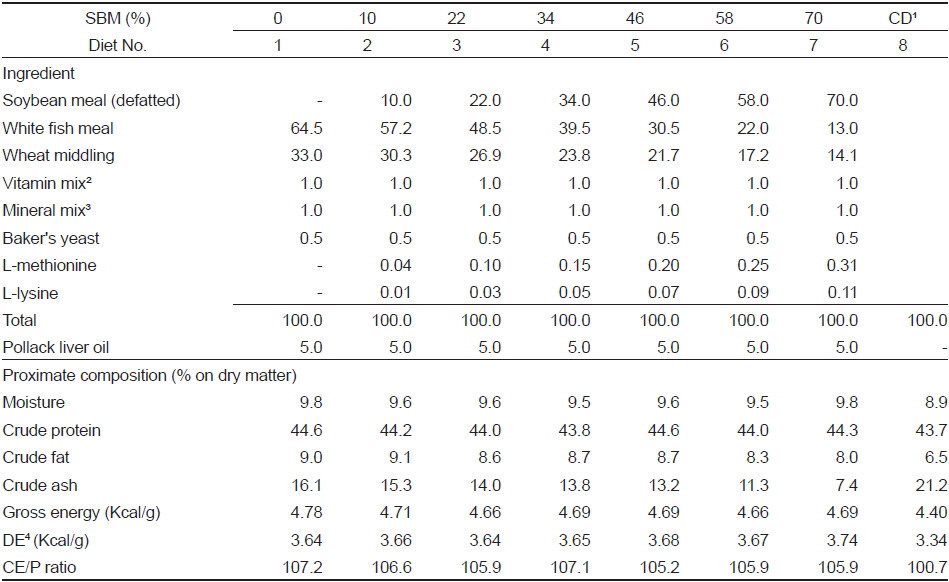
[Table 1.] Ingredient and proximate composition of the test diets for rainbow trout
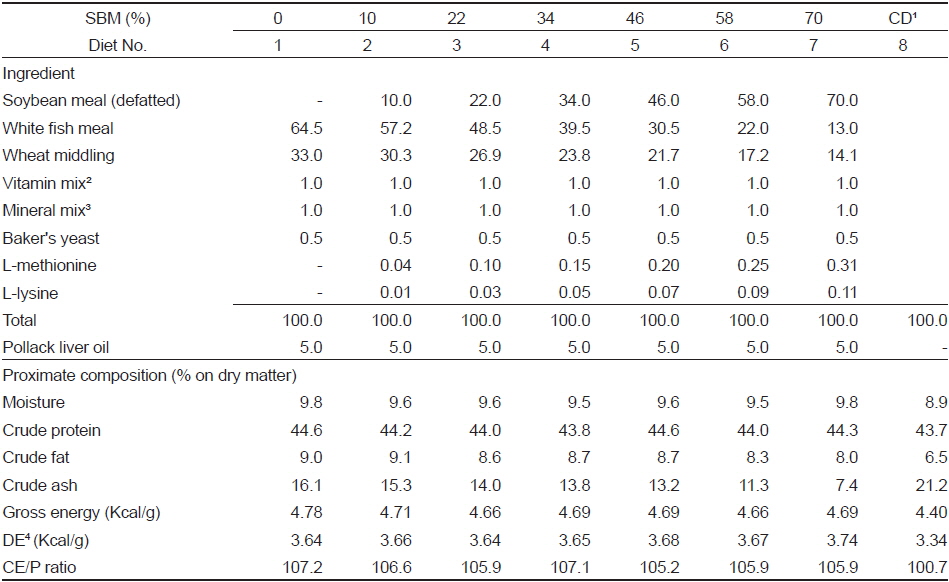
Ingredient and proximate composition of the test diets for rainbow trout
사육시스템은 생물여과조(수량 6 m3)에 4개의 FRP 수조(수량 1 m3)가 연결된 반순환식 여과시스템 2 조를 실험에 이용하였고, 실험어류는 각각의 FRP 수조에 2개의 cage (1.2×0.6×0.5 m)에 수용하였고, 실험구는 무작위로 2반복 배치하였다. 또한, 각 사육 시스템에는 수온자동제어장치(thermo-controller)를 설치하여 실험 기간 동안 17℃를 유지하였다.
실험 사료는 Table 1과 같이 어분을 64.5% 사용한 실험 사료를 대조구(diet No. 1)로 하고, 점차 그 함량을 13%까지 줄이면서 한편으로는 대두박을 10%에서 70%까지 등간격으로 늘린 7종류의 실험 사료(diet No. 2-7)를 사용하였다. 그리고 성장 비교를 위해 시판되는 D 사의 무지개송어용 사료(diet No. 8)를 함께 사용하였다. 사료는 펠렛제조기(AEZ16S, Hiraga CO., Japan)로 제조한 후 공급하기까지 −30℃의 냉동고에 보관하면서 사료 공급 직전에 명태 간유를 5%씩 에탄올에 녹여 실험 사료에 흡착시켰다.
사료 공급 후 1, 3, 6, 9, 12, 18 및 24시간째에 각 실험구로부터 실험 어류를 4-8마리씩 즉살한 후 복부를 절개하고 식도의 최상부와 장 경계부의 위를 절개하고, 위 내용물이 흘러내리지 않도록 내용물을 꺼내어 습중량을 측정하였다(즉, 위 무게 + 내용물 무게). 이것을 건조하여 건중물로 환산하여 수분 함량을 측정하였고, 이들 무게는 체중에 대한 비율로 나타내었다.
사료섭취 후 시간경과에 따른 위 소화물의 변동에 대한 회귀식의 추정은 SPSS 15.0 (Chicago, IL, USA)로 수행하였으며, 위 소화물의 직선적 그리고 지수적 감소경향은 다음과 같이 분석하였고, 회귀식은 r2와 확률로 상호 비교하였다. Linear: y = a + bx + ε, Quadratic: y = a +bx +cx2 +ε 여기에서, y는 어체중에 대한 위 소화물의 양 (%), x는 소화시간(h), a, b, c는 추정변수, ε는 실험오차(residual error)이다. 또한, 대두박 함량과 소화시간에 따른 소화율의 이차회귀식은 다음과 같은 모델을 이용하여 산출하였다. Hyperbolic (decay): y = S·k / (k +x), 여기에서 S는 최대섭취량(%), k는 위 소화물의 50%가 소화하는데 걸리는 시간(h), x는 소화시간(h)이다.
위 중량비(stomach weight/body weight×100)는 위 내용물의 경시적 변화 연구와 동시에 위 무게를 측정하여 어체중에 대한 비율로 환산하였고, 위 내용물의 수소이온농도는 pH 측정기(Orion 502A, U.S.A.)를 사용하였다.
사료 섭취 후 시간 경과에 따른 위(胃) 소화물의 소화 정도를 알아보기 위하여 대조구(사료 1), 사료 3, 5 및 7의 실험 어류를 대상으로 AOAC (1995) 방법에 따라 위 소화물(습중량) 1 g에 삼염화초산(trichloroacetic acid, TCA) 10 mL를 가하여 마쇄한 후 10,000 rpm에서 10분간 원심 분리하여 상등액과 침전 잔사로 나누어 각각 가용성 질소와 불용성 질소로 하여 Kjeldahl법으로 질소를 정량하였다.
모든 측정값은 Statistical Analysis System (SAS) 으로 처리하였고, 실험 구간별 유의성 검정은 Duncun,s Multiple Range Test로 95% 유의 수준에서 하였다. 분석에는 단순회귀(simple regression) 또는 다중회귀(multiple regression) 모델을 사용하였다.
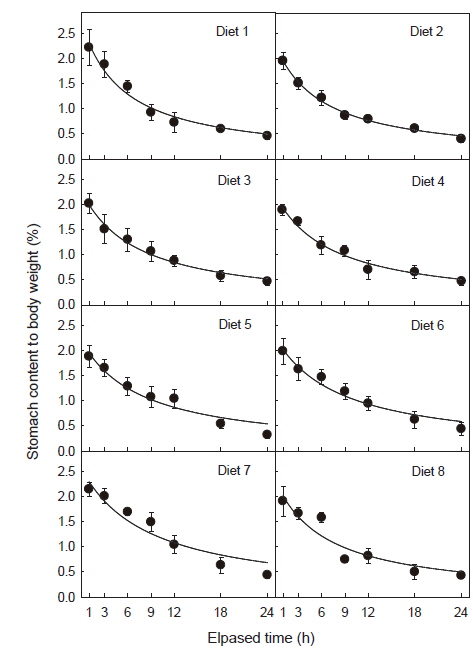
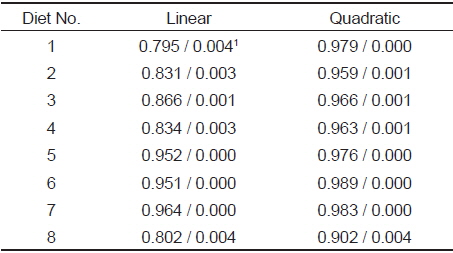
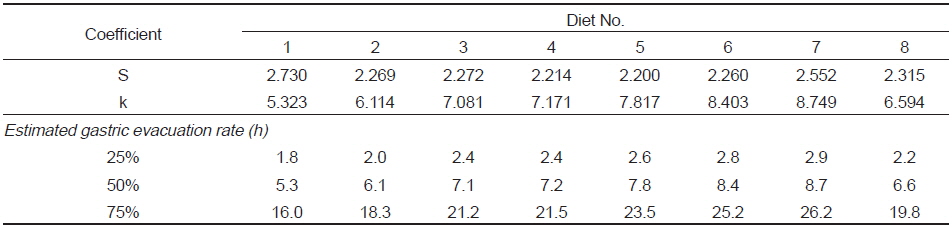
사료 섭취 후 위 내용물(gastric content)의 경시적인 변화는 Fig. 1 및 Table 2와 같이R2값이나 유의수준을 비교하면 사료 섭취 후 24시간까지 직선적 감소보다는 지수적 감소를 하였다. 그리고 위 내용물의 소화 속도(gastric evacuation rate, GER)는 Table 3에 나타내었듯이 위 내용물의 25%가 위를 통과하는 데는 1.8-2.9시간이, 50%가 통과하는 데는 5.3-8.7시간이, 75%가 통과하는 데는 16.0-26.2시간이 소요되어 사료 중 대두박 함량이 증가할수록 위 소화물의 통과시간이 지연되는 것으로 나타났다. 대두박 함량 70%인 사료 7 (diet No. 7) 실험구에서는 대두박이 첨가되지 않은 대조구(diet No. 1)보다 소화시간이 약 1.63배 지연되었으며, 대두박이 첨가되지 않은 대조구와 대두박 10% 첨가(diet No. 2) 실험구에서는 유사한 소화 패턴을 보였다.
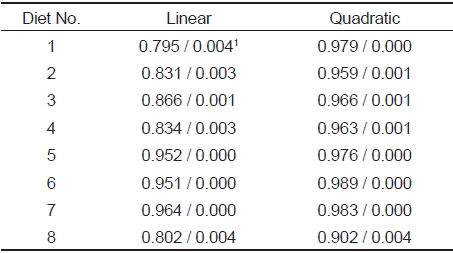
Statistical values of the regression for stomach content of rainbow trout fed with soybean meal diets
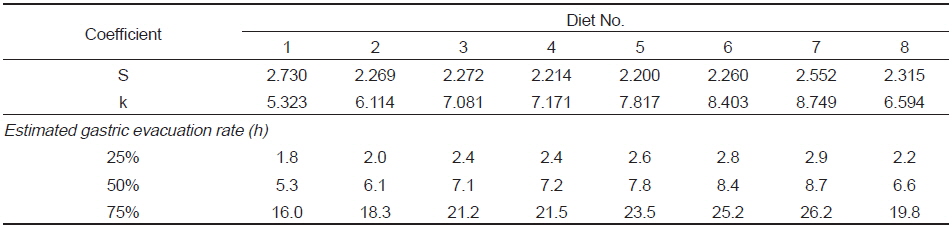
Coefficient of the nonlinear (hyperbolic) regression for gastric content of rainbow trout fed with soybean meal diets
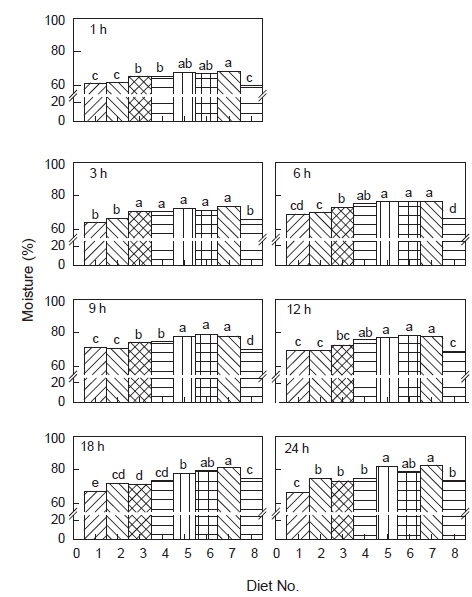
위 내용물의 수분 함량 변화를 Fig. 2에 나타내었다. 수분 함량은 전반적으로 사료 섭취 직후부터 9시간까지는 급격히 증가하고, 그 후 24시간까지 거의 일정한 수준을 유지하였다. 그리고 실험구에 따라서는 유의적인 차이를 보여 대두박 함량이 많아질수록 위 내용물의 수분 함량이 유의적으로 많았다(
한편, 위 내용물의 pH 변화는 전반적으로 사료 섭취 전에는 4.05 수준을 유지하다가 사료 섭취 1시간 후에는 5.12-5.38로 정점을 나타내었으며, 이후 낮아지기 시작하여 9시간 후에는 4.57-4.83 수준으로, 12시간 후에는 4.53-4.80으로, 18시간 후에는 4.46-5.00 수준으로 유지되었으나, 실험 전 48시간 공복시의 수준으로는 도달하지 않았다. 이와 같은 경향은 실험구와 관계없이 거의 비슷하였고, 유의적인 차이는 없었다(
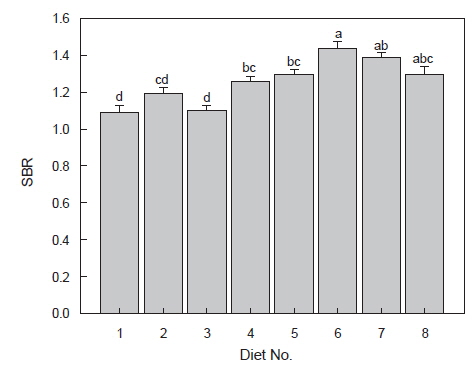
대두박을 장기간 공급한 무지개송어의 위 중량비(SBR: stomach weight/body weight×100)를 비교하면(Fig. 3), 위 내용물의 수분 함량이 많았던 사료 5, 6 및 7 실험구가 1.31-1.44%로 대조구 및 사료2 및 3실험구의 1.10-1.13% 보다 유의적으로 무거웠다(
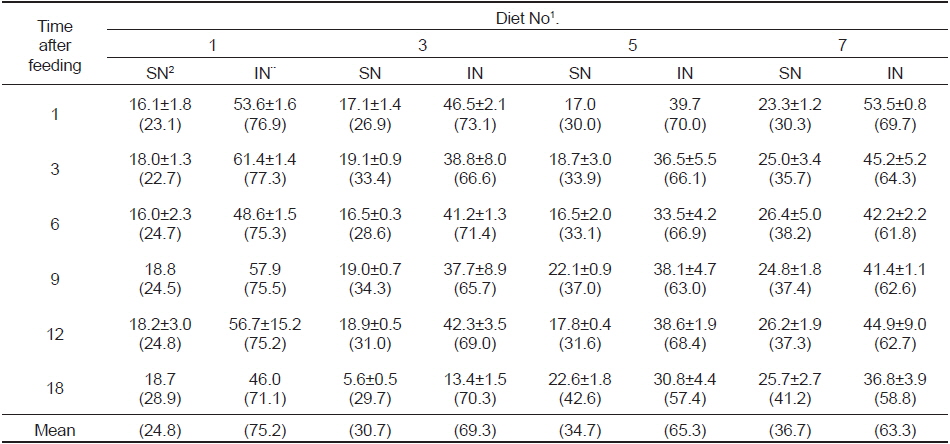
사료 공급 후 경시적으로 위 내용물 중 수용성 질소와 불용성 질소의 양과 비율을 조사하여 소화도를 추정한 결과(Table 4), 사료 섭취 후 시간이 경과함에 따라 수용성 및 불용성 질소의 구성비는 급이한 사료에 따라 다소 차이가 있었고, 대두박 함량이 많은 실험구의 내용물일수록 가용성 질소의 구성비가 컸다. 즉, 대두박을 첨가하지 않은 대조구의 수용성 질소 비율은 평균 24.8%에 지나지 않았으나, 사료 3(대두박 함량 22%) 실험구는 30.7%, 사료 5(대두박 함량 46%) 실험구는 34.7%, 사료 7(대두박 함량 70%) 실험구는 36.7%로 대두박 함량이 많은 실험구일수록 내용물 중 가용성 질소의 비율이 높음을 알 수 있었다.
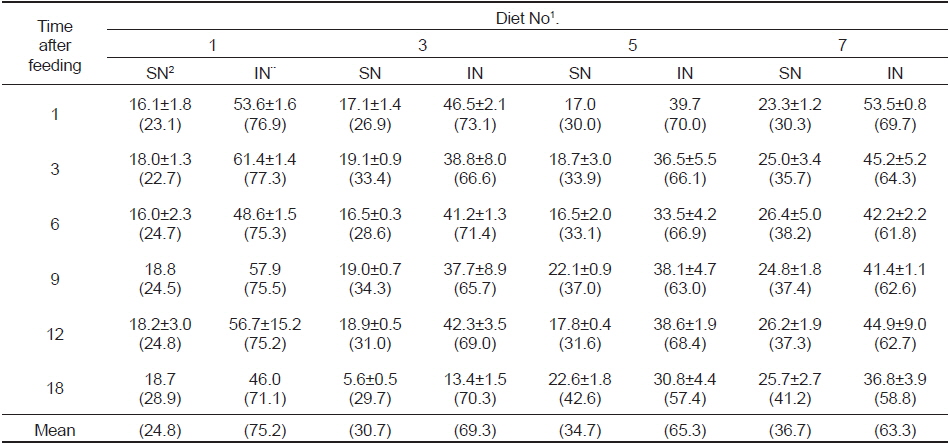
Soluble and insoluble nitrogen in the gastric content of rainbow trout depends on the soybean meal levels and time after feeding
어류에서 위 내용물의 통과 속도는 대상 생물의 크기, 사료 중 수분 함량, 사료의 질(nutritional intensity)과 양, 사료 섭취후 경과 시간 및 사육 수온 등에 따라 크게 달라지는데(Jobling, 1980; Hilton et al., 1981; Lee et al., 2000; Nikolopoulou et al., 2011), 대개는 지수적(exponential), 평방근(square-root), 직선적(linear)인 감소 형태를 나타내는 것으로 알려져 있다(Jobling, 1987). 예를 들어, 극지송어(
한편, Shimeno et al. (1993b)는 위 내용물의 통과 속도(gastric evacuation rate)는 어종에 따라 차이를 보이는데, 온수성 어류인 방어의 경우 위 소화물은 2시간에 1/2, 4 시간에 1/4이 감소하는 것으로 알려져 있으며, Nikolopoulou et al. (2011)는 gilthead sea bream은 섭취한 사료의 1/2이 통과하는데 2.8-3.3시간이, European sea bass는 난분해성의 식물성 사료원료를 사료에 다량 함유할 경우 어분을 단백질원으로 사용한 대조구보다 통과속도가 약 1.35배 증가하지만 대체적으로 6.0-8.1시간이 소요되고, 사료의 질적 차이보다는 종 특이적인 경향(species-specific)을 보이는 것으로 보고하고 있다. 본 연구에서 무지개송어는 소화물의 1/2이 위를 통과하는데 걸리는 시간은 각각 5.3-8.7시간으로 European sea bass의 경우와 유사하였다(Table 3). 또한 Hilton et al. (1981)은 2.9 g의 무지개송어에서는 위 내용물의 1/2이 통과하는데 5.1시간이 걸린다고 하였으나, 300-400 g 크기를 대상으로 한 본 실험에서는 5.3-8.7시간으로 이보다 다소 길었는데, 이것은 같은 어종이라도 어체 크기에 따라, 또는 사료의 질에 따라 위 통과시간에 차이가 있음을 보여준다.
한편, 해양 경골어류의 소화관은 소화 기능뿐만 아니라 삼투압 조절기능을 동시에 수행하기 때문에 먹이 섭취 과정을 통해 피할 수 없이 환경수를 마시게 되고, 그 결과 소화관의 이온 균형에 변화가 오기 때문에 사료섭취 전후에는 피할 수 없이 위 소화물의 수분과 pH가 변동하게 된다(Taylor and Grosell, 2006). 또 소화관 내용물의 pH는 사료의 질, 사료량, 사육 수온, 염분도, 광주기, 스트레스 및 어류의 발달 단계, 사육어종 등에 따라 다를 수 있으며(Kapoor et al., 1975; Fange and Grove, 1979; Nikolopoulou et al. 2011), 틸라피아 같이 위벽이 얇은 어류는 위의 pH가 공복시 1.14 수준으로 매우 낮으나, 사료 섭취 후에는 4.67 수준으로 되어 변화 폭이 크며(Maier and Tullis, 1984; Lobel, 1981), 위가 없는 금붕어는 절식시가 6.67-7.30 수준으로 사료 섭취 후 7.37-8.44과 큰 차이가 없다고 알려져 있다(Kapoor et al., 1975).
본 연구에서 사료 공급 전후에 위 내용물의 pH를 경시적으로 조사한 결과, 실험구와 상관없이 사료 섭취 전 4.05에서 사료 섭취 1 시간 후에 급증하여 정점에 도달하였다가 이후에는 급감하여 6-9 시간 후에 안정하였고, 18시간까지 유지되는 경향을 보였다. 하지만 위 내용물의 수분 함량은 pH 변화 양상과는 반대되는 경향을 보여 pH 급감 시기에 급증하였다. 그리고 수분함량은 대두박 함량이 많은 사료의 실험구일수록 유의적으로 많았는데(Fig. 2), 이것은 사료 섭취 후 lag phase (Jones, 1974) 동안에 위에서 소화 효소가 집중적으로 분비되었기 때문일 것으로 여겨지며, 실험구 사이에 pH의 차이는 없이 수분 함량만 유의적으로 차이가 나는 것으로 보아 환경수가 유입되어서 생긴 증가는 아닌 것으로 생각된다. Nikolopoulou et al. (2011)에 따르면, gilthead sea bream과 European sea bass에게 어분과 carob seed germ meal 기반의 2 종류 사료를 먹였더니 사료 종류에 따른 pH의 차이는 크지 않은 것으로 보고하고 있어 본 연구 결과와 유사하였다. 그러나 이들 어종은 종 특이적으로 위 소화물의 수분함량과 pH의 차이를 보였는데, sea bass는 수분 함량이 59.60-89.01%로 gilthead sea bream의 60.26-76.55%보다 높았음에도 불구하고 pH는 오히려 2.20-5.19 범위로 3.37-6.16보다 훨씬 낮게 유지되어 위 소화물의 수분은 외부로부터 유입된 것이라기 보다 소화효소 등의 분비로 수분 함량이 높아졌을 가능성이 높다. 본 연구에서 위 소화물의 수분함량은 사료섭취 후 1시간부터 증가하기 시작하여 대체적으로 9시간 후 70.1-79.1% 수준으로 정점을 보인 후 24시간까지 지속되는 것으로 보아 gilthead sea bream의 실험 결과와 유사하였다. 또한, 위의 연구 보고와는 달리 본 연구의 무지개송어 위 내용물에서는 사료섭취 전후 18시간까지 pH가 4-5의 좁은 범위를 유지하는 것으로 나타났다.
그리고 사료 섭취 후 시간 경과에 따라 위 내용물의 소화 정도를 조사하기 위하여 위 내용물을 불용성 및 수용성 질소로 나누어 그 함량과 비율을 조사한 결과(Table 4), 대두박 함량이 많은 사료의 실험구일수록 수용성 질소의 비율이 높았는데, 이것은 앞에서도 지적하였듯이 효소의 분비량이 많았기 때문일 것으로 여겨지며, 이들 실험구 어류들의 위 중량이 더 무거웠던 것(Fig. 3)은 위의 효소 분비량이 많아짐으로써 위가 효소적, 형태적 적응을 보인 것으로 여겨진다. 이러한 변화는 Shimeno et al.(1993a)에 의해서도 확인된 바 있는데, 즉, 30%의 대두박을 첨가한 사료로 방어를 12주간 사육하였더니, 배합 사료 실험구의 어류가 생사료의 위(胃) 펩신 활성도가 높아 단백질 소화율이 좋았고, 유문수와 위의 체중비는 커져서 위가 난 분해성 사료에 대하여 형태적, 효소적 적응이 일어난 것으로 보고하고 있어, 본 연구와 같은 현상이 관찰되었다. 그러나 위에서 언급한 바와 동일한 대두박 함량이 많은 공급구에서 많은 양의 소화 효소가 수용성 질소로 계산이 되었다 하더라도 최소한 사료의 단백질 즉, 질소의 소화율은 대조구보다 나쁘지 않았던 것으로 여겨진다.
위 소화물의 경시적 변화 연구에서 대두박 함량이 많은 사료 4, 5, 6번 실험구에서 사료 1, 2, 3번 실험구보다 직선식에 가까운 지수적 감소(Table 2의 R2 값 비교)를 보인 것은 소화 초기에는 lag phase가 길었음을 알 수 있고, 이 시간 동안 소화효소와 같은 소화작용이 위 속에서 더 오랫동안 지속됐을 것으로 추정할 수 있다. 이러한 추정은 위 중량비 값에서 잘 나타내고 있는데, 위의 조직 대부분은 대부분 염산과 펩신 등의 분비세포 위주로 구성되는 점을 고려하면, 대두박 함량이 높은 사료를 장기간 먹인 실험구의 어류 위가 더 비후하다는 점이 이를 입증하고 있다.
비교적 장기간 사육이 이루어진 연구에서는 20-30% 정도의 어분 대체(10-15% 첨가)가 성장에 지장이 없는 것으로 알려져 있다(Oliva Teles et al., 1994; Refstie et al., 2000; Vielma et al., 2000). 본 연구에서도 대두박을 약 22% 정도 사료에 첨가하고 160일간 장기 사육하면 위 중량비의 증가(위의 비대 증상)가 관찰되고, 위 소화물의 수분함량이 증가(대두박 함량이 높은 실험구의 수분 함량의 증가는 소화효소의 증가로 추정)하는 등으로 미루어 대두 단백질의 소화에 어느 정도 소화생리학적으로 적응하는 것으로 추정되었다.