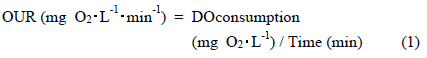20세기 이후 생물학적 처리공정이 확립되면서, 전 세계적으로 생물학적 처리공정은 하수 및 폐수처리 공정에서 하나의 근간이 되어 왔다. 생물학적 처리공정은 포기조(aeration tank) 내에서 자연적으로 발생하는 고농도의 미생물을 이용하는 것으로, 박테리아 및 원생동물을 모두 포함하는 이러한 미생물을 일반적으로 활성슬러지라 부른다. 활성슬러지를 구성하는 미생물은 폐수에 함유된 유기물을 이용하여 자신을 성장시키고, 그 결과 미생물은 폐수에 함유되어 있는 유기물 및 영양염류 등의 오염물질을 정화하게 된다. 그러나 폐수처리 공정에 영향을 미치는 많은 변수들(미생물에 의해 쉽게 분해되지 않는 난분해성 물질 및 미생물의 활성을 저해시키거나 혹은 미생물의 사멸을 초래할 수도 있는 독성물질의 유입 등)로 인해 오늘날 생물학적 처리공정의 운영은 점차 다양하고 복잡해지고 있는 실정이다(Hartmann et al., 2013).
과밀한 인구 및 산업 활동의 증가에 기인하여 중금속과 같은 독성물질의 발생은 갈수록 증가되고 있으며, 이러한 독성물질의 유입은 유기물의 제거효율을 감소시킬 뿐만 아니라, 활성슬러지의 침전성을 악화시키는 등 생물학적 처리공정 전반에 어려움을 주는 것으로 알려져 있다. 게다가 산업폐수와 가정하수를 동시에 병합 처리하는 근래의 경향에 비추어볼 때, 생물학적 처리공정에 장애를 일으키는 독성물질의 유입 가능성은 계속 증가되고 있는 실정이다. 비록 독성물질이 생물학적 처리공정에 미치는 영향에 대해서는 아직 완전히 규명되지 못하고 있지만, 다양한 금속물질은 일정 농도 이상으로 유입되면 미생물의 활성을 저해하거나 처리공정에 장애를 유발하는 것으로 보고되고 있다(Cokgor et al., 2007).
대부분의 중금속은 독성물질 또는 발암물질로 이미 잘 알려져 있는데, 폐수에 함유된 중금속이 적절하게 처리되지 못한 채 수계로 배출되면 먹이사슬(food chain)을 통해 지속적으로 생물농축(bioaccumulation)되어 사람뿐만 아니라 수계에 있는 동 · 식물 및 생태계 전반에 큰 위협이 될 수 있다. Zn, Cu, Ni 등의 금속물질은 낮은 농도에서도 독성을 가지는 것으로 알려져 있는데, 갈수록 강화되는 환경규제를 준수하기 위해서도 폐수로부터 중금속을 제거하는 것은 생물학적 처리공정에서 또 하나의 주요 관심사가 되고 있다(Dhokpande and Kaware, 2013).
국내의 실정을 살펴보면 2008년 기준으로 산업폐수 발생량의 약 45%가 공공하수처리시설에 유입되는 것으로 보고되고 있다. 또한 일부 공공하수처리시설에서는 다량의 산업폐수가 유입되고 있음에도, 이중투자방지 등의 이유로 별도의 배출허용기준을 적용하여 고농도의 산업폐수를 하수처리시설에 유입시키고 있는 실정이다(Yu et al., 2013). 그러나 공공하수처리시설로 유입되는 산업폐수의 유량, 수질 등에 대한 전반적인 실태조사 및 통계 자료는 아직 미흡하다고 할 수 있다. 만일 다량의 중금속을 함유하고 있는 산업폐수가 적절히 처리되지 못하고 공공하수처리시설로 유입될 경우에는 생물학적 처리공정의 정상적인 운영에 악영향을 미칠 수도 있기에, 중금속이 미생물에 미치는 독성에 대한 연구들은 점점 중요한 이슈가 되고 있다.
따라서 본 연구에서는 산업계에서 많이 발생되는 대표적인 금속물질이라고 할 수 있는 Cu, Al, Zn이 생물학적 처리공정에서 미생물에 미치는 독성 영향을 조사하였으며, 이를 통해 생물학적 처리공정에서 안정적인 운전을 위한 대상물질의 적정허용농도를 도출하고자 하였다. 또한 생물학적 활성슬러지에 의한 대상물질의 제거 가능성을 함께 검토하였다.
2.1.1. 산소소모율(oxygen uptake rate)
미생물의 호흡은 호기성 미생물의 활성에 필수적인 요소로, 다양한 독성물질에 대한 생물학적 독성평가에 있어서 하나의 중요한 요소가 되고 있다. 미생물에 대한 독성평가에는 다양한 방법들이 이용되고 있는데, 미생물의 성장저해를 직접 측정하는 방법 및 미생물의 생체발광을 이용하거나 미생물의 호흡률을 측정하는 간접적인 방법 등이 이용되고 있다. 이 중에서 호흡률을 측정하는 방법은 활성슬러지(종속영양 미생물 또는 질산화 미생물)에 대한 폐수의 독성평가에 일반적으로 많이 사용되는 방법으로, 독성물질이 존재할 경우 미생물의 호흡률이 감소될 수 있음에 기초하고 있다. 호흡률 측정에는 Oxygen Uptake Rate(OUR)를 측정하는 방법이 일반적으로 이용되고 있다. 산소소모율(OUR)은 아래의 식 (1)과 같이 표현될 수 있으며, 시간경과에 따라 DO(dissolved oxygen)의 변화를 측정하고, 이를 활용하여 DO 감소곡선을 구하게 된다(Cokgor et al., 2007; Dalzell et al., 2002; El-Bestawy et al., 2013; Hartmann et al., 2013; Ong et al., 2010).
2.1.2. 호흡저해도(respiration inhibition)
호흡저해도(respiration inhibition)은 활성슬러지 미생물의 호흡을 이용하여 독성물질의 저해능을 평가하는 방법이라고 할 수 있으며, 이에 대한 표준화된 방법으로는 ISO 8192, OECD 209 등이 있다. 호흡저해도는 독성물질이 함유된 시료와 비교를 위한 대조시료에 대해 각각 미생물에 의한 산소소모율을 측정하고, 독성물질에 의해 야기되는 미생물의 상대적인 저해정도를 평가하는 방법이다. 호흡저해도는 아래의 식 (2)와 같이 나타낼 수 있다(Cokgor et al., 2007; Dalzell et al., 2002; El-Bestawy et al., 2013; Hartmann et al., 2013).
2.1.3. 질산화저해도(nitrification inhibition)
질산화 미생물은 수중에 존재하는 암모니아성 질소(ammonia)를 아질산성 질소(nitrite) 및 질산성 질소(nitrate)로 전환시키는 질산화 과정에 관여하게 되는데, 질산화 미생물이 독성물질에 의해 저해를 받게 되면 질산화율이 감소하게 된다. 즉, 질산화저해도(nitrification inhibition)는 수중에 존재하는 독성물질의 영향으로 미생물에 의한 질산화 반응이 저해되는 정도를 말하며, 다음 식 (3)과 같이 나타낼 수 있다(Dalzell et al., 2002).
2.2. 활성슬러지에 대한 Cu, Al, Zn의 독성실험
2.2.1. 활성슬러지 및 시료
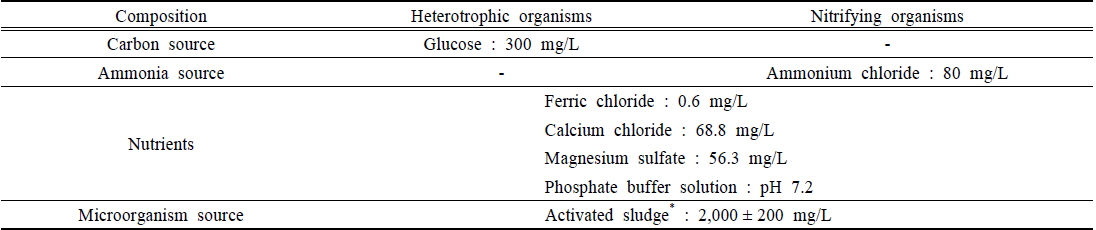
독성실험에 사용된 활성슬러지는 용인시 소재의 영덕하수처리시설 포기조에서 채수하였으며, 미생물의 활성을 유지하기 위해 준비과정 동안 지속적인 포기상태를 유지하였다. 또한 거름체(50 mesh)를 사용하여 활성슬러지와 섞여있는 협잡물을 제거하였다. 독성실험은 준비한 활성슬러지와 함께 유기물 공급을 위해 glucose(Wako, Japan)를 사용하였고, 질산화에 필요한 ammonia는 ammonium chloride (Wako, Japan)를 사용하였다. 이 외에 ferric chloride 등의 영양염류와 pH완충제를 첨가하였으며, 시료의 조성은 Table 1에 정리하였다.
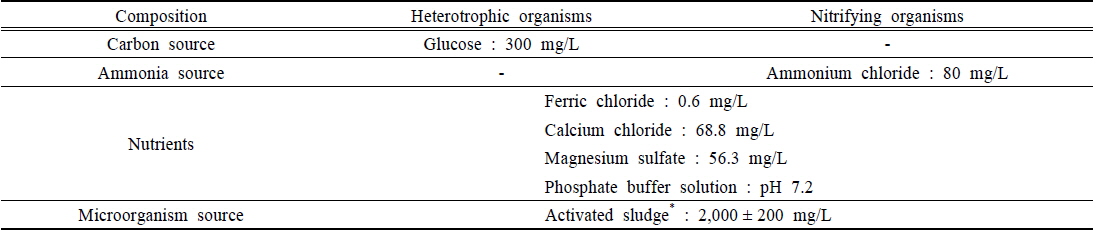
The composition of the synthetic wastewater on heterotrophic and nitrifying organisms for the toxicity test
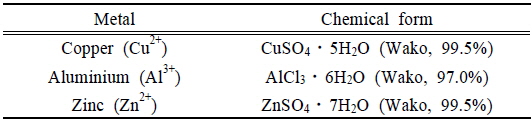
독성영향을 조사하고자 산업계에 많이 발생되어 공공하수처리시설로 유입되는 Cu, Al, Zn을 대상물질로 선정하였으며(Kim et al., 2012), 대상물질로 사용된 시약의 조성은 Table 2와 같다.
[Table 2.] The metal materials used in the experiment
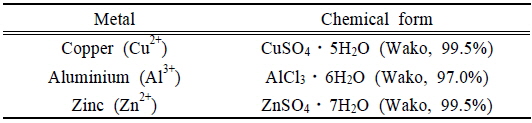
The metal materials used in the experiment
2.2.2. 급성독성 실험
종속영양미생물 및 질산화미생물에 대한 산소소모율을 측정하였으며, 대조시료를 이용하여 상대적인 저해도를 구하여 대상물질의 급성독성을 평가하였다. 실험에서는 Cu, Al, Zn 각각의 단일물질에 의한 급성독성(이하 단일독성)과 혼합물질에 의한 급성독성(이하 혼합독성)을 조사하였으며, 단일독성은 Cu, Al, Zn의 농도를 0~25 mg/L까지 5 mg/L씩 증가시켜 실험을 진행하였다. 산소소모율 측정은 300 mL 용량의 BOD 용기에 준비한 활성슬러지와 시료를 주입하고, 단계적으로 대상물질의 농도를 변화시켜 실험을 진행하였다. 실험은 초기 DO 농도가 6 mg/L 이상으로 충분히 포기된 상태에서 시작하여, 최종 DO 농도가 2 mg/L 이하로 감소될 때까지 매 15초 간격으로 DO 농도의 변화를 조사하였다. DO 측정에는 DO meter(YSI 5100 (membrane electrode type), USA)를 사용하였다. 단일독성 실험에서 미생물에게 10%의 저해도를 나타내는 독성물질의 농도(IC10)를 도출하였고, 이를 바탕으로 혼합독성을 평가하였다.
2.3. Cu, Al, Zn이 활성슬러지에 미치는 저해영향 실험
Cu, Al, Zn이 수질오염물질의 처리효율 저하 및 질산화반응 저해 등 활성슬러지에 미치는 영향을 조사하기 위하여 회분식 실험을 수행하였다. 반응기 용량은 2 L이며, 실험은 6시간 동안 진행되었다. pH 조정이 필요한 경우에는 1N 중탄산나트륨(NaHCO3)을 사용하여 7.0±0.3로 조절하였으며, DO가 부족하지 않도록 충분한 교반과 포기를 공급하였다. 실험에 사용된 시료 및 대상물질의 조성은 2.2.2의 혼합독성 실험과 동일하였다. 대상물질의 농도변화에 따른 유기물 및 암모니아 제거효율을 조사하여 활성슬러지에 미치는 저해영향을 평가하였으며, 유기물 및 대상물질의 농도 변화를 조사하기 위해 2시간 간격으로 50mL의 시료를 분취하였다. 각 항목별로 Total Organic Carbon (TOC) 항목은 TOC analyzer (Torch, Teledyne Tekmar, USA)를, 금속류 항목은 ICP/MS (ELAN DRC Plus, PerkinElmer, USA)로 분석하였으며, NH4+-N 및 NO3--N 항목의 분석에는 수질자동분석기(AQ2+, Seal Analytical, USA)를 이용하였다.
3.1.1. 단일독성 평가
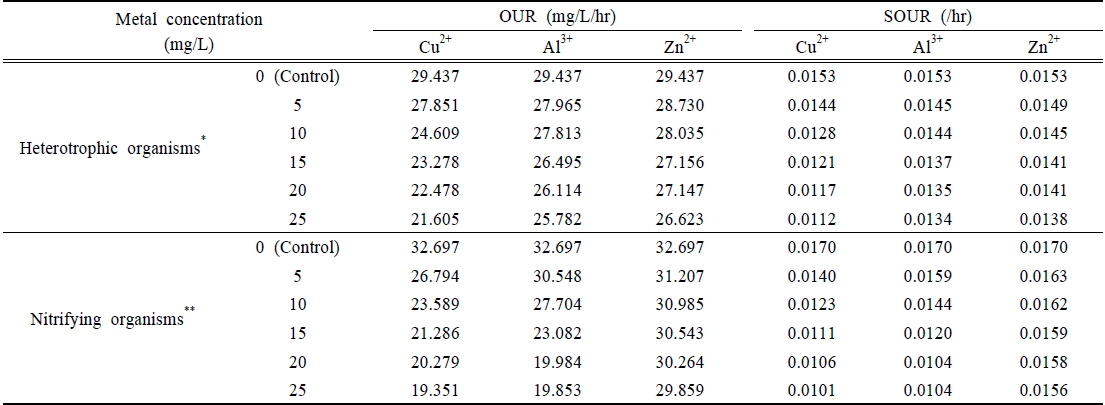
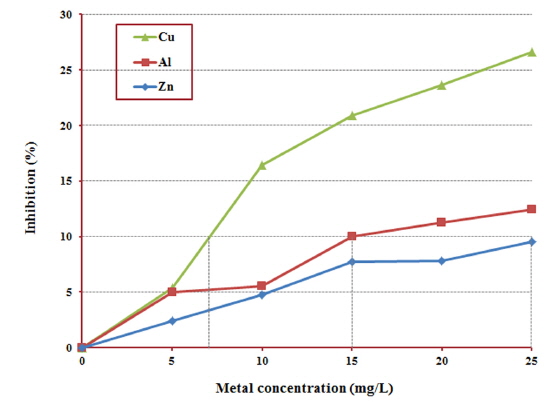
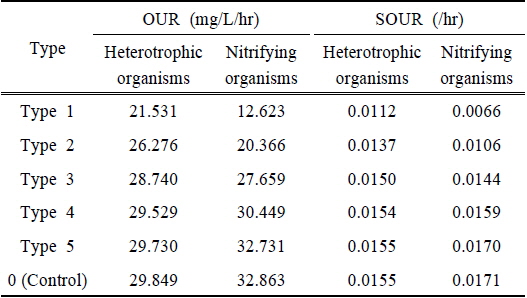
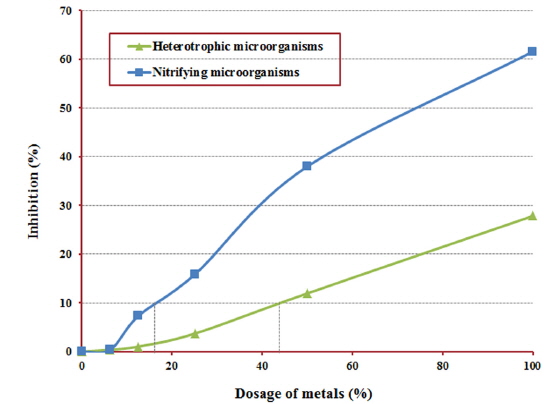
단일독성을 평가하고자 대상물질의 농도변화에 따른 산소소모율을 측정하였으며, 그 결과를 Table 3에 정리하였다. 종속영양 미생물 및 질산화 미생물 모두에서 대상물질의 농도가 증가함에 따라 산소소모율이 감소되는 것으로 조사되었다. 또한 산소소모율 결과로부터 대상물질의 농도변화에 의한 저해영향을 평가하기 위해 대조시료를 이용하여 상대적인 저해도를 구하였다. Fig. 1은 유기물의 산화에 기여하는 종속영양 미생물에 미치는 저해영향을 정리한 결과이다. 대상물질별로 살펴보면 Cu2+는 5 mg/L에서 5.4%의 저해도를 나타냈으나, 25 mg/L에서는 저해도가 26.6%로 크게 상승하는 것으로 나타났다. 반면 같은 농도에서 Al3+은 5.0%에서 12.4%, Zn2+은 2.4%에서 9.6%로 저해도가 상승하여 Cu2+에 비해 상대적으로 저해영향이 적은 것으로 평가되었다.
[Table 3.] The result of OUR and SOUR in the single dose toxicity test
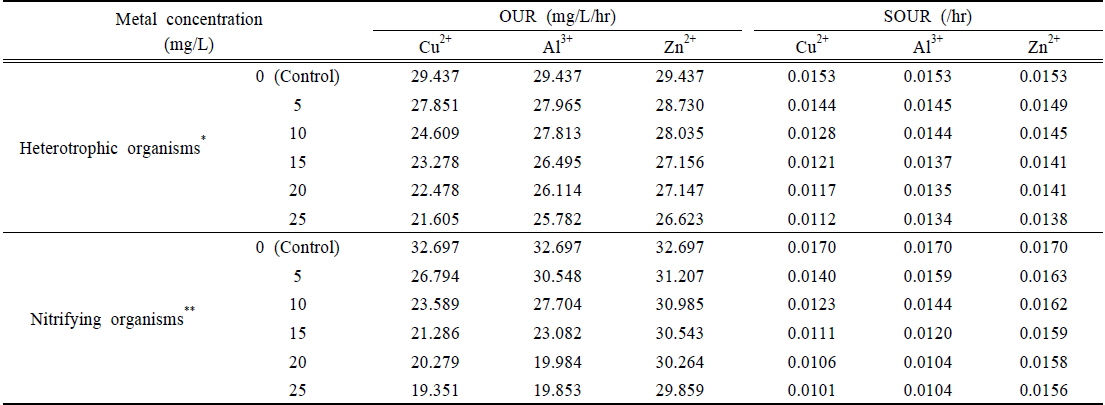
The result of OUR and SOUR in the single dose toxicity test
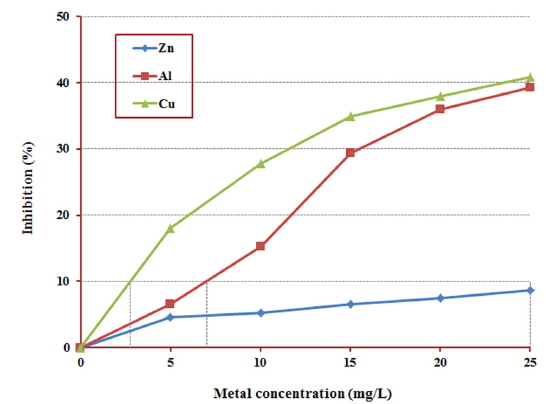
Fig. 2는 질산화 미생물에 미치는 저해영향을 나타낸 것으로, Cu2+는 5 mg/L에서 18.1% 저해도를 나타냈으며 25 mg/L에서는 저해도가 40.8%로 상승되었다. 같은 농도에서 Al3+의 저해도는 6.6%에서 39.3%로 크게 상승하였으며, 반면 Zn2+은 4.6%에서 8.7%로 큰 변화가 없는 것으로 나타났다.
Fig. 1 및 Fig. 2의 결과에서 미생물에게 10% 저해가 나타나는 각 대상물질의 IC10은 종속영양미생물에서는 Cu2+, Al3+ 각각 7, 15 mg/L, 질산화미생물에서는 3, 7 mg/L로 평가되었다. Zn2+은 종속영양미생물 및 질산화미생물 모두 전 농도구간에서 10% 미만의 저해영향을 보였으므로, 가장 높은 저해도를 나타낸 25 mg/L를 IC10으로 설정하였다. Zn2+은 종속영양미생물 및 질산화미생물 모두에서 유사한 저해영향을 나타낸 반면, Cu2+와 Al3+은 상대적으로 질산화미생물에게 저해영향이 더 큰 것으로 평가되었다. 또한 Cu2+는 낮은 농도에서도 상대적으로 높은 저해도를 나타냈으며, Al3+은 질산화 미생물에게 더 큰 영향을 미치는 것으로 평가되었다.
선행 연구에서 Lin et al. (2003)은 Cu는 1.0 mg/L의 낮은 농도에서도 독성물질로 작용한다고 보고하였다. 또한 Ong et al. (2010)은 oxygen uptake rate (OUR)을 이용하여 활성슬러지 미생물에 대한 독성을 조사한 결과에서 Cu > Cd > Ni = Cr > Zn 순으로 독성이 감소하는 것으로 나타났으며, Madoni et al. (1999)은 질산화 공정에서 수집된 활성슬러지를 대상으로 OUR을 이용하여 중금속의 독성을 평가한 결과에서 Cd > Cu > Zn 순으로 독성이 감소한다고 보고하였다. 이들의 연구에서 독성물질로 사용된 대상 금속의 종류와 독성을 나타내는 농도범위 등은 서로 상이함을 보였으나, 공통적으로 Cu2+가 활성슬러지에 미치는 영향은 Zn2+의 독성영향보다 크다는 점을 시사하고 있으며, 이는 본 실험의 결과와도 일치하는 부분이라 할 수 있다.
질산화 반응과 관련한 중금속의 저해영향에 대해서는 상반된 견해들이 보고되고 있다. Tsai et al. (2006)은 중금속이 유기물질의 제거효율에는 영향을 미치지 않으나, 암모니아 산화에 관련하는 질산화 미생물에게는 저해영향을 유발시키는 것으로 보고하였다. 반면 Madoni et al. (1999)은 Cd2+, Cu2+, Pb2+은 종속영양 미생물 보다 질산화 미생물에게 낮은 민감성을 보이나, Cr6+, Zn2+은 ammonium uptake rate (AUR) 및 OUR 실험에서 유사한 저해영향을 보인다고 하였다. 본 연구 결과에서는 Cu2+, Al3+은 질산화 미생물에게 높은 민감성을 보인 반면 Zn2+은 유사한 저해영향을 보여 선행 연구결과와는 다른 양상을 보였다.
3.1.2. 혼합독성 평가
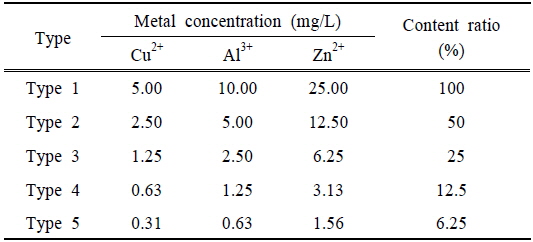
혼합독성에서는 각 대상물질이 혼합되었을 때 나타나는 저해영향을 평가하였다. 단일독성 결과에서 질산화미생물의 저해영향이 더 크게 나타났으며, 이를 기준으로 각 대상물질이 질산화미생물에 대하여 10% 이상의 저해영향을 나타낸 가장 낮은 농도를 혼합물질의 농도로 선정하였다. 혼합물질의 조성은 Cu2+, Al3+, Zn2+이 각각 5, 10, 25 mg/L가 되도록 조제하였으며, 이를 Table 4에서와 같이 단계별로 희석하여 혼합독성 실험에 사용하였다. 단일독성 실험과 동일하게 혼합물질을 이용하여 종속영양미생물 및 질산화미생물에 의한 산소소모율의 변화를 조사하였다. Table 5의 결과에서 혼합물질의 농도가 증가되면서 산소소모율이 감소되는 경향을 보였으며, 상대적으로 질산화미생물 대한 산소소모율이 큰 폭으로 감소되었다. Fig. 3은 혼합물질에 의한 종속영양미생물 및 질산화미생물의 상대저해도를 나타낸 결과로, 혼합물질의 농도가 증가함에 따라 저해도가 지속적으로 상승하였다. Type 1에서 종속영양미생물의 저해도는 27.9%, 질산화미생물의 저해도는 61.6%로 나타나, 질산화미생물에 대한 저해영향이 더 큰 것으로 평가되었다.
[Table 4.] The concentration of the mixed metals used in the mixture toxicity test
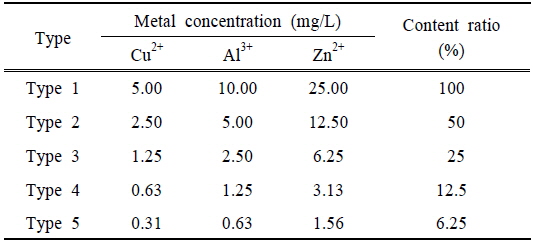
The concentration of the mixed metals used in the mixture toxicity test
[Table 5.] The result of OUR and SOUR in the mixture toxicity test
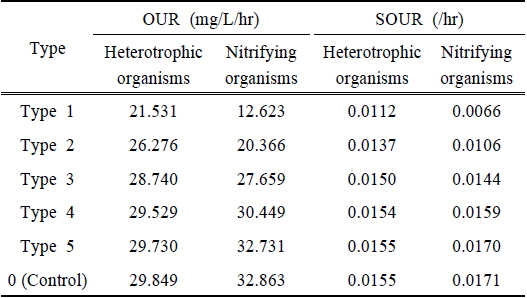
The result of OUR and SOUR in the mixture toxicity test
Cimino and Caristi (1990)는 호기성 소화공정에서 Cu와 Zn이 혼합될 때 독성영향이 크게 상승한다고 보고하였으나, 본 연구에서는 각 물질들이 독성영향에 미치는 상관관계에 대해서는 명확하게 규명하지는 못하였다. 다만 Fig. 3의 결과에서 Cu2+, Al3+, Zn2+ 혼합물질의 IC10은 종속영양미생물에서는 혼합물질 농도의 44%에 해당하는 2.2, 4.4, 11.0 mg/L, 질산화미생물에서는 혼합물질 농도의 17%에 해당하는 0.9, 1.7, 4.3 mg/L로 확인되어, 대상물질이 혼합될 경우의 저해영향은 단일물질의 독성에 비해 약 3배 이상 더 민감하게 나타나는 것으로 평가되었다.
3.2. Cu2+, Al3+, Zn2+이 활성슬러지에 미치는 저해영향
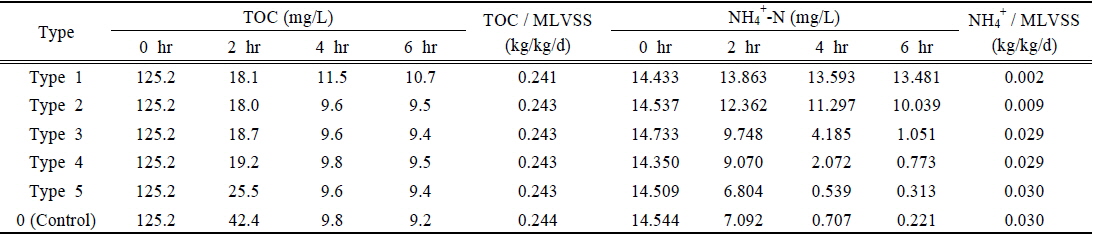
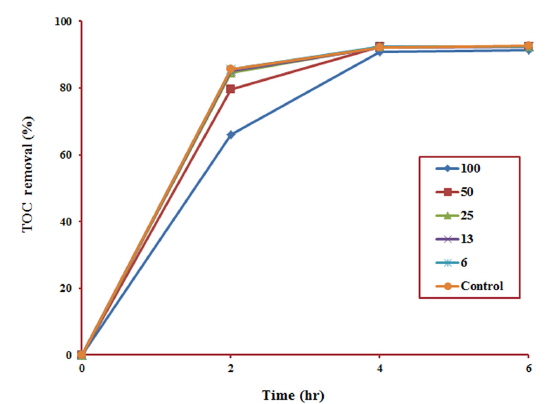
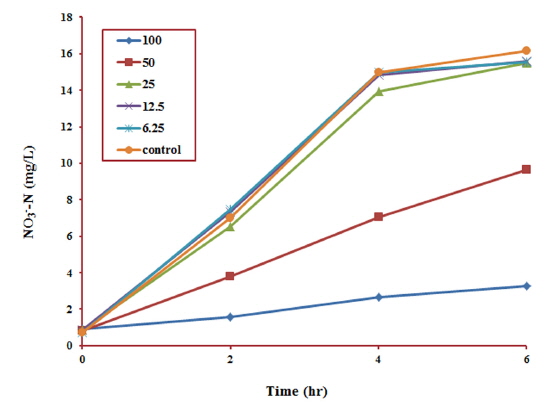
Cu2+, Al3+, Zn2+의 혼합물질이 생물학적 처리과정에 미치는 저해영향을 평가하고자 회분식 실험을 수행하였다. 혼합물질의 농도에 따른 유기물 및 암모니아 제거효율을 조사하여 활성슬러지에 미치는 저해영향을 평가하였으며, 그 결과를 Table 6에 정리하였다. Fig. 4는 혼합물질의 농도 및 반응시간에 따른 유기물의 제거효율을 정리한 결과이다. 2시간 이내의 반응초기에는 혼합물질의 농도가 증가함에 따라 유기물의 제거효율이 감소하는 경향을 보였다. 그러나 반응시간이 지속되어 4시간 이후로는 유기물의 제거효율 측면에서 별다른 차이를 나타내지 않았으며, 단위기질당 유기물제거능(TOC/MLVSS)도 모든 농도 조건에서 0.24 kg/kg/day로 매우 유사한 것으로 조사되었다. 이러한 결과는 반응초기 혼합물질의 유입에 의해 독성영향이 발현되어 미생물의 활성이 저해된 것으로 볼 수 있는데, 반응이 계속 지속되면서 활성슬러지는 외부의 저해요인에 점점 순응하게 되어, 혼합물질에 대한 저해영향이 감소된 것으로 판단할 수 있다. 한편 Chua et al. (1999)은 활성슬러지 공정에서 미생물과의 흡착능력과 흡착속도 모두 금속이 유기물보다 더 유리하다고 보고하였는데, 미생물과 금속의 흡착능력에서 그 원인을 찾을 수도 있다. 결국 반응에 주입된 혼합물질은 미생물에게 저해를 유발하는 독성물질의 역할보다는 유기물과 미생물의 결합을 방해하는 경쟁자의 역할을 한다고 볼 수 있으며, 이는 반응초기 유기물의 제거효율을 감소시키는 하나의 원인이라고 유추할 수 있다.
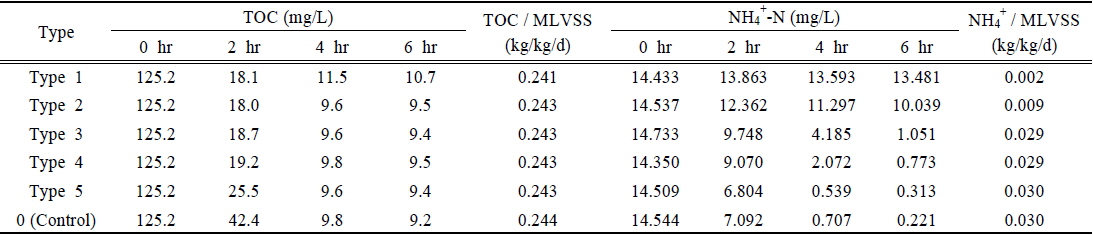
Concentrations of TOC and NH4+-N according to the reaction time and the removal of TOC and NH4+-N in the simple batch test
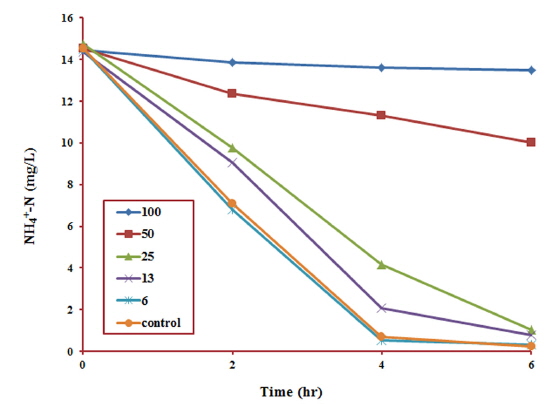
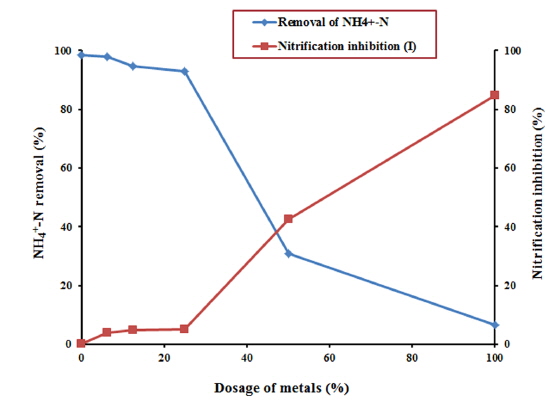
반면 Fig. 5의 결과를 살펴보면 혼합물질의 농도가 감소됨에 따라 NH4+-N 소모량이 급격히 증가하였는데, 암모니아 제거능(NH4+-N/MLVSS)은 혼합물질의 농도가 증가함에 따라 0.030에서 0.002 kg/kg/day로 크게 감소되는 것으로 조사되었다. 마찬가지로 Fig. 6에서도 혼합물질의 농도가 감소할수록 NO3--N 농도가 급격히 증가하는 것으로 확인되었으며, 유기물의 제거와는 달리 반응시간이 경과하여도 이러한 저해영향은 지속되었다. 이는 혼합물질이 질산화미생물에게 독성영향을 유발시켜 NH4+-N의 질산화 과정에서 부정적인 요인으로 작용하는 결과라고 볼 수 있다. Fig. 7은 혼합물질의 농도변화에 따른 NH4+-N 제거율과 질산화 저해도의 관계를 나타낸 것으로, NH4+-N 제거율이 감소함에 따라 질산화 저해도가 급격히 상승하는 것을 알 수 있다. 그러나 Type 3를 기점으로 NH4+-N 제거능 및 제거율에서 유사한 결과를 보여, 질산화 과정에서의 저해영향이 현저히 감소되는 것으로 조사되었다.
회분식 실험결과에서 유기물의 제거효율은 시간이 경과하면서 유사한 결과를 나타냈으나, 일정 농도 이상의 혼합물질은 질산화 과정에서 저해영향을 급격히 증가시키는 역할을 하는 것으로 조사되었다. 따라서 생물학적 처리공정에서 질산화 반응의 저해영향을 최소화시키기 위해서는 대상물질이 유입을 고려해야 할 것으로 사료되며, 실험결과 Cu2+, Al3+, Zn2+의 농도를 1.3 mg/L, 2.5 mg/L, 6.3 mg/L 이하로 유지하는 것이 바람직할 것으로 판단된다.
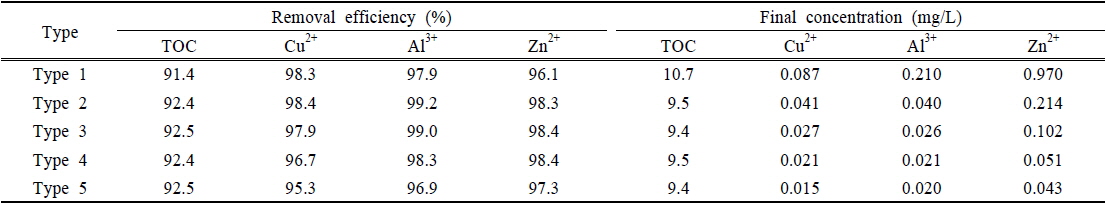
Table 7은 회분식 실험에 의한 유기물 및 혼합물질의 농도변화와 제거율을 정리한 결과이다. 실험에 주입된 혼합물질은 활성슬러지에 의해서 95% 이상 제거되었으며, 혼합물질의 주입농도에 따라 제거효율은 큰 차이를 보이지 않는 것으로 조사되었다. 또한 혼합물질은 대부분 반응초기에 빠르게 제거되는 것으로 확인되었는데, 이는 혼합물질이 활성슬러지와 흡착 등의 결합에 의해 제거되었을 가능성이 큰 것으로 판단되는 부분이다. Dhokpande and Kaware (2013)는 생물학적 처리과정에서 수 ppm 수준의 중금속은 활성슬러지에 의해 제거가 가능한 것으로 보고하였는데, 본 연구에서도 유사한 결과를 얻을 수 있었다.
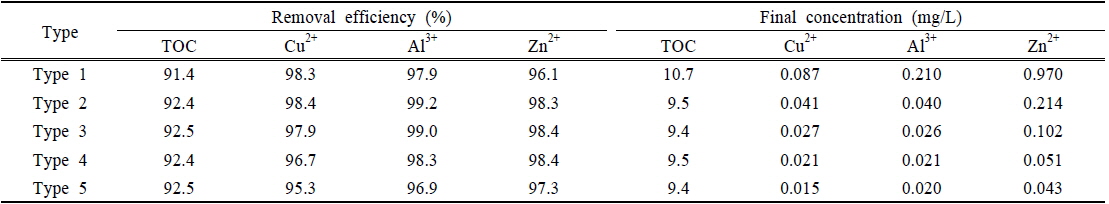
The removal efficiency of TOC and toxic materials by activated sludge in the simple batch test
만일 대상물질이 생물학적 처리과정을 거쳐 수계로 배출될 경우에는 처리 후 대상물질의 농도가 중요한 관심대상이 될 수 있다. 국내의 경우 청정지역에서 배출허용기준은 Cu, Zn은 1 mg/L 이하로 설정하고 있으며, Al은 배출허용기준을 적용시키지 않고 있다. 수생태계 보호를 위해서는 배출허용기준 보다 더 높은 처리수준을 요구하게 되나, 아직 국내에는 Cu, Al, Zn에 대한 수생태 보호기준이 없는 실정이다. 참고로 미국의 수생태 보호기준(criteria maximum concentration)에는 Cu, Al, Zn 각각 0.028, 0.750, 0.120 mg/L로 설정하고 있다. 회분식 실험결과에서 Cu, Al, Zn이 1.3, 2.5, 6.3 mg/L 이하로 유입될 경우 대상물질의 최종 농도는 각각 0.027, 0.026, 0.102 mg/L 수준으로 조사되어, 활성슬러지를 이용한 생물학적 처리공정만으로도 배출허용기준 및 미국의 수생태 보호기준 모두를 충족시키는 것으로 사료된다. 다만, 원수의 성상에 따라 다양한 변수를 가지게 되며, 고농도의 금속물질이 지속적으로 유입되어 활성슬러지에 축적되면 또 다른 장애를 유발할 수도 있다. 따라서 생물학적 처리공정의 원활한 운영관리를 위해서는 실제 공정에 적용하기에 앞서 충분한 모니터링이 요구되며, 그에 따른 추가적인 연구가 필요할 것으로 판단된다.
본 연구에서는 금속물질이 활성슬러지에 미치는 독성영향을 평가하여 생물학적 처리공정의 안정적인 운전을 위한 적정허용농도를 도출하고자 하였다.
Cu2+, Al3+, Zn2+을 대상으로 활성슬러지 미생물에 대한 단일독성 및 혼합독성을 평가한 결과 종속영양 미생물 보다 질산화 미생물에 대한 저해작용이 더 크게 나타났다.
질산화 미생물을 이용한 단일독성 실험에서 대상물질의 IC10은 Cu2+, Al3+, Zn2+ 각각 3 mg/L, 7 mg/L, 25 mg/L이었으며, 대상물질을 모두 포함한 혼합독성의 IC10은 Cu2+ 0.9 mg/L, Al3+ 1.7 mg/L, Zn2+ 4.3 mg/L로 조사되었다. 종속영양 미생물에 대한 단일독성의 IC10은 Cu2+, Al3+, Zn2+ 각각 7 mg/L, 15 mg/L, 25 mg/L, 혼합독성에서의 IC10은 Cu2+ 2.2 mg/L, Al3+ 4.4 mg/L, Zn2+ 11.0 mg/L으로 나타나 혼합독성이 단일독성 보다 약 3배 민감한 것으로 평가되었다
활성슬러지를 이용한 회분식 실험에서 Cu2+, Al3+, Zn2+은 질산화 미생물에 민감하게 작용하였으며, 생물학적 처리공정의 안정적인 운영을 위한 Cu2+, Al3+, Zn2+의 허용농도는 1.3 mg/L, 2.5 mg/L, 6.3 mg/L 이하인 것으로 평가되었다.