능성어(
우리나라에서의 능성어 양식은 약 20년 전부터 실시되어 2010년 269톤을 생산하였으나 2011년 150톤, 2013년 56톤으로 생산량이 줄어드는 추세를 보이고 있다(Statistics Korea, 2014). 하지만 최근에 들어 중국 등 수산물 소비국들에 대한 수출전략 중요 품종으로 능성어가 선정됨에 따라 집중적인 양식 기술 개발이 추진되고 있다.
국내에서 능성어 양식은 남해안 일대에서 자연산 어류를 채집하여 가두리에 입식하여 사육하는 방법과 인공종묘생산을 통한 양식방법으로 이루어지고 있다. 하지만 종묘 생산장에서는 수컷 친어 확보의 어려움과 사육초기에 원인이 불명확한 대량 폐사로 인해 안정된 종묘 생산에 어려움을 겪고 있다. 더욱이 능성어 사육과정에서 발생하는 바이러스성 질병인 바이러스성신경괴사증(viral nervous necrosis, VNN)으로 인한 대량 폐사로 인해 양식산업화에 걸림돌이 되고 있다(Kim et al., 2012; Sohn et al., 1991; 1998).
VNN은 전 세계적으로 양식산 해산어에 심각한 피해를 유발하는 질병으로 알려져 있다(Munday et al., 2002). 본 질병은 1980년대 말 일본에서 양식되는 줄전갱이(
VNN의 원인 병원체인 신경괴사증바이러스(nervous necrosis virus, NNV)는 크기가 약 30 nm 정도로 외막이 없는 정이십면체의 RNA 바이러스로서 노다바이러스과 베타노다바이러스속에 속한다(Schneemann et al., 2005). NNV는 5개의 유전자형인 striped jack NNV (SJNNV) type, tiger puffer NNV (TPNNV) type, barfin flounder NNV (BFNNV) type, redspotted grouper NNV (RGNNV) type 및 turbot NNV (TNV) type으로 구분되며(Johansen et al., 2004; Nishizawa et al., 1997), 국내 양식산 능성어 및 연안에서 서식하는 자연산 어류에서 검출되는 NNV는 모두 RGNNV type에 속한다고 보고되어 있다(Gomez et al., 2008; Kim et al., 2012).
우리나라에서 능성어의 VNN은 1990-1991년 남해안 해상가두리 양식장에서 발생된 이래로(Sohn et al., 1991; 1998), 2006-2008년도에는 거문도 및 여수에서 해상가두리에 사육중인 능성어에서 9.2-89.1%의 대량 폐사가 발생하였다(Kim et al., 2012). 능성어 양식장에서의 VNN은 사육수온이 24-26℃ 범위인 8월부터 발생하기 시작하여 수온이 20-25℃ 범위인 9-10월까지 지속되며, 성어보다는 치어에서 폐사율이 높게 나타난다(성어의 폐사율: 9.2%, 치어의 폐사율: 31-89.1%) (Kim et al., 2012). 폐사되는 패턴으로는 급성으로 인한 대량 폐사와 소량으로 지속적으로 폐사되는 경우가 있다(Kim et al., 2012). 본 질병은 종묘 생산장의 경우 친어로부터 수정란을 거쳐 자어에 바이러스가 감염되는 수직감염에 의해 발생되며, 종묘 생산장과 양성장에서는 유입수, 동일 수조에 수용한 자어 등에 의한 수평감염으로 발생하게 된다(Egusa et al., 2006; OIE, 2009).
능성어의 대량생산을 위해서는 건강한 종묘의 안정적인 생산법과 이들 종묘를 질병에 의한 대량 폐사 없이 건강하게 성장시킬 수 있는 양성법의 개발이 필수적이다. 이를 달성하기 위해서는 친어의 확보, 우량 수정란 생산, 적절한 영양의 공급, 사육 시스템의 개발 등이 이루어져야 하며, 이에 추가하여 각 성장 단계별 VNN 관리가 필수적으로 요구된다. 본 연구에서는 능성어 종묘 생산장과 양성장에서의 VNN을 예방하는 방법에 대해서 소개하고자 한다.
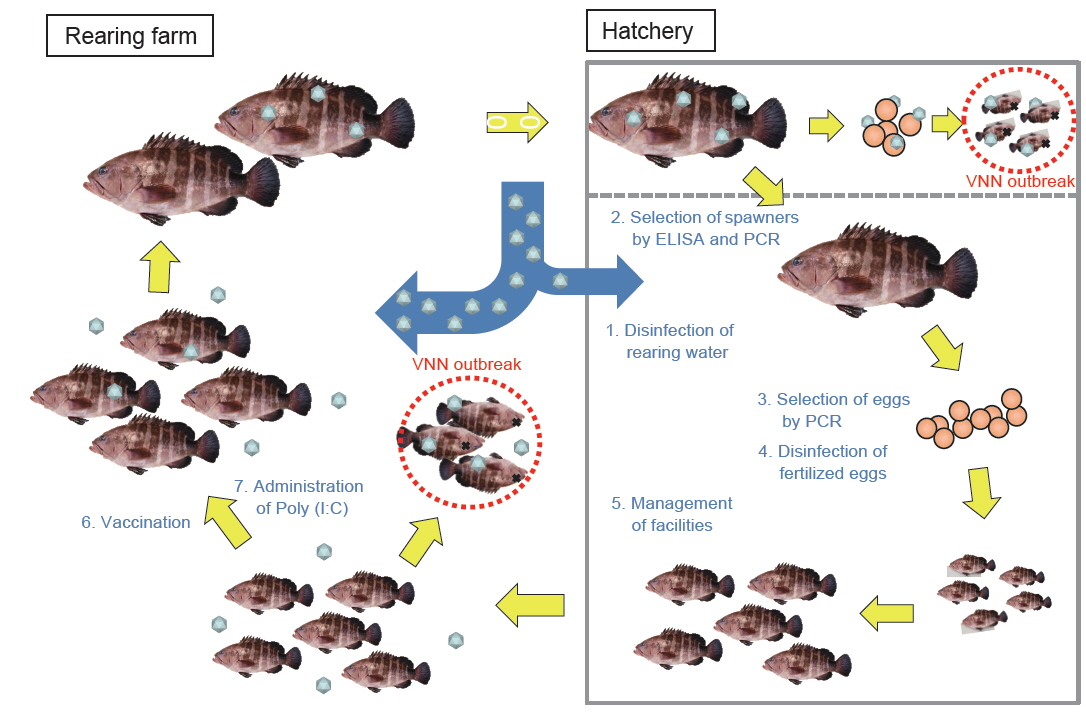
종묘 생산장에서는 NNV-보균 친어로부터 수정란을 거쳐 자어에 감염되는 수직감염뿐만 아니라 환경수로부터 유입되는 NNV, 또는 NNV에 오염된 사육 기구 등을 통한 수평감염이 발생할 수 있다. 따라서 종묘 생산장에서 NNV의 유입을 차단하기 위해서는 사육시설의 관리, NNV 감염 이력이 없는 친어 선별, NNV 무감염 난과 정자 선별, 수정란의 소독 및 사육수의 소독을 통한 능성어 사육이 이루어져야 한다(Fig. 1). 간단히 설명하면 친어로부터 혈액 및 생식소를 채취하여 NNV의 감염 유무를 확인한 후 무감염 친어를 선별하여 살균된 해수를 사용하여 관리한다. 친어로부터 채란을 통해 채취한 난과 정액에 대해 NNV 검사를 실시한 후, 음성 시료를 사용하여 수정시키고, 이들 수정란을 소독하여 종묘생산을 실시한다. 종묘생산 과정 중에 사용되는 사육수, 사육 수조, 기구 등은 살균해서 사용한다. 이와 같은 일련의 바이러스 관리 방법은 종묘 생산장에서 VNN을 예방하는데 효과적임이 확인된 바 있다(Mori et al., 1998; Mushiake et al., 1994; Tsuchihashi et al., 2002; Watanabe et al., 1998; 2000; Yoshimizu, 2009).
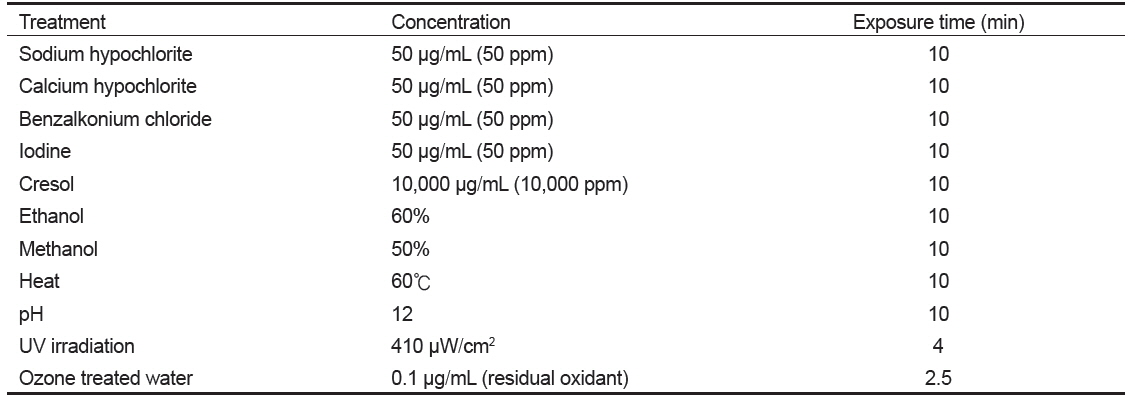
오염된 사육시설을 통해 NNV의 수평감염이 발생할 수 있으므로, 이를 예방하기 위해서는 작업자의 손 및 장화를 비롯하여 각종 사육 기구류 및 수조에 대한 소독이 필요하다. 소독에는 양식장 환경을 고려하여 소독제를 선정한 후 사용 가능하다. NNV는 50 µg/mL (50 ppm) 농도의 차아염소산나트륨(sodium hypochlorite), 차아염소산칼슘(calcium hypochlorite), 염화벤잘코니움(benzalkonium chloride) 및 요오드(iodine), 10,000 µg/mL (10,000 ppm)의 크레졸(cresol), 60% 에탄올(ethanol), 50% 메탄올(methanol), 60℃, pH 12에서 10분간 처리하면 불활화 된다(Table 1)(Arimoto et al., 1996). 또한 410 µW/cm2의 UV에 244초간, 0.1 µg/mL의 잔류옥시던트(residual oxidant)가 포함된 오존 처리수(ozone treated water)에 2.5분간 처리하면 불활화 된다(Arimoto et al., 1996). 하지만 1,600 µg/mL (1,600 ppm) 농도의 포르말린(formalin)에 10분간 처리하여도 불활화 되지 않는다(Arimoto et al., 1996).
[Table 1.] Inactiviation condition of nervous necrosis virus (Arimoto et al., 1996)
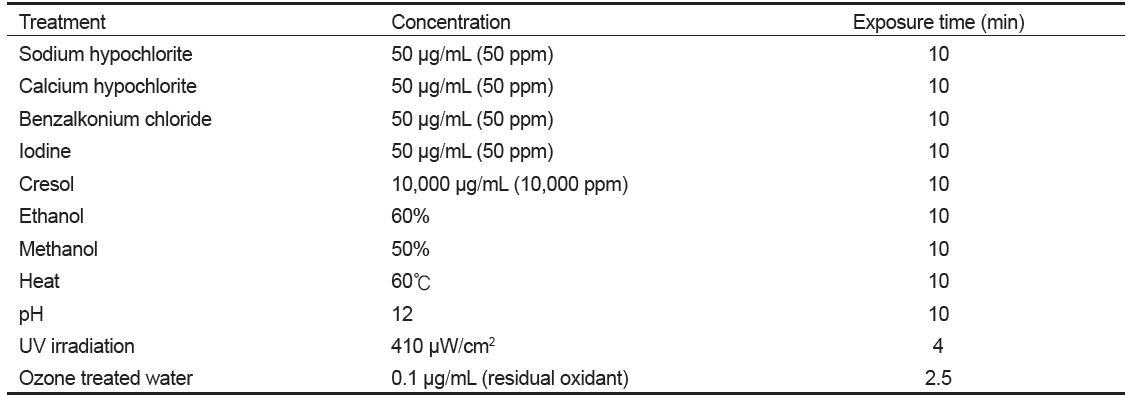
Inactiviation condition of nervous necrosis virus (Arimoto et al., 1996)
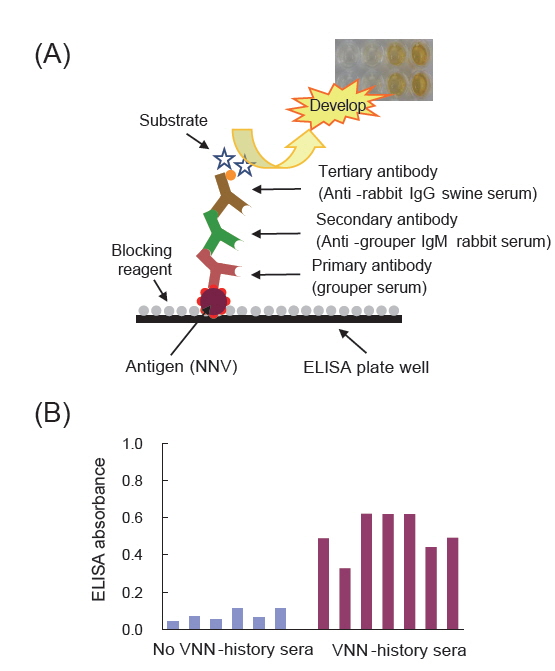
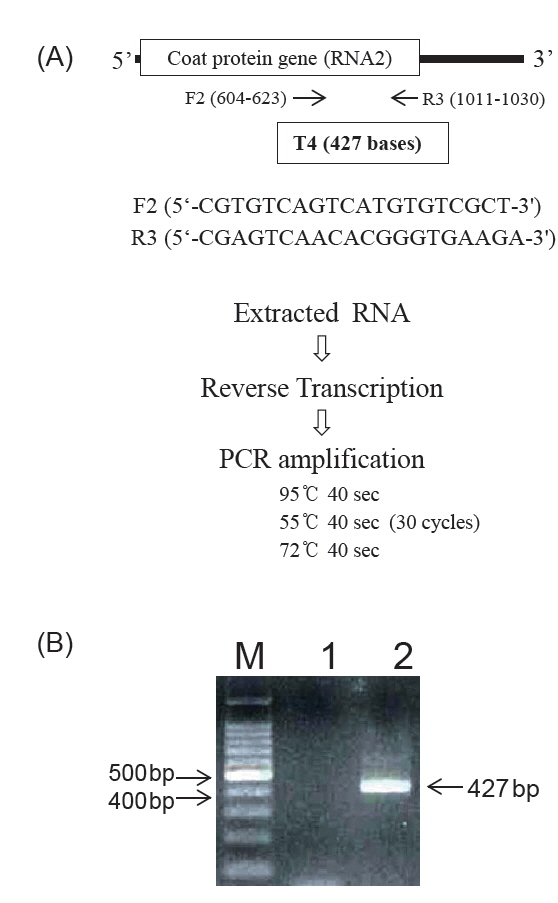
NNV-보균 친어를 통해 수정란을 거쳐 자어에 바이러스가 감염될 수 있음으로 NNV 감염 이력이 없는 친어 선별은 수직감염을 예방하는데 도움을 준다. 친어를 선별하는 방법에는 항체검출 ELISA (enzyme-linked immunosorbent assay)와 PCR (polymerase chain reaction)을 사용한다(Mushiake et al., 1994; Nishizawa et al., 1994; Watanabe et al., 2000; Yoshimizu, 2009). 항체검출 ELISA법은 어체 내의 혈중에 존재하는 NNV에 대한 특이항체 유무를 조사하는 방법으로서, NNV 항원(재조합 NNV의 외막 단백질, 정제된 NNV 또는 바이러스 배양액)에 능성어 혈청(1차 항체), 능성어 IgM에 대한 토끼 항체(2차 항체), 토끼 IgG에 대한 항체(3차 항체)을 반응시켜 혈중의 NNV 특이항체를 검출한다(Fig. 2)(Choi et al., 2014; Kim et al., 2007; 2009; Watanabe et al., 2000). PCR법은 어체 내에 존재하는 NNV 유래의 특정 유전자를 검출하는 방법으로서 빠른 시간 내에 검사가 가능하고 검출 감도가 높아 어류병원 바이러스를 검출하는데 널리 사용되고 있다(OIE, 2009). RT-PCR (reverse transcription-PCR)은 친어의 생식소(난 또는 정액도 사용 가능함)와 혈액을 사용하여 RNA를 분리한 후 NNV의 외막 단백질 유전자를 타깃으로 한 primer를 사용하여 실시한다(Fig. 3) (Egusa et al., 2006; Mushiake et al., 1994; Nishizawa et al., 1994; Tsuchihashi et al., 2002). 검출감도를 높이기 위해서는 nested-PCR도 가능하다(Dalla Valle et al., 2000).
친어로부터 난과 정액을 취해 위에서 언급한 방법과 동일하게 RT-PCR을 실시하여 NNV 유전자의 유무를 검사하며, 만일 양성개체가 있으면 난과 정액을 폐기하는 것이 수직감염을 예방하는데 도움이 된다. PCR 결과에서 NNV 음성인 난과 정액을 사용하여 수정시키는 과정에서 NNV에 오염된 수정란이 발견될 경우, 오염된 수정란은 소독을 통해 바이러스의 불활화가 가능하다. 수정란의 소독은 오존 처리수(잔류 옥시던트 농도: 0.5 mg/L)로 1분간 처리하거나(Tsuchihashi et al., 2002), 전기분해수(free chlorine 농도: 0.3 mg/L)로 3분간 처리한다(Table 2)(Watanabe et al., 2013).
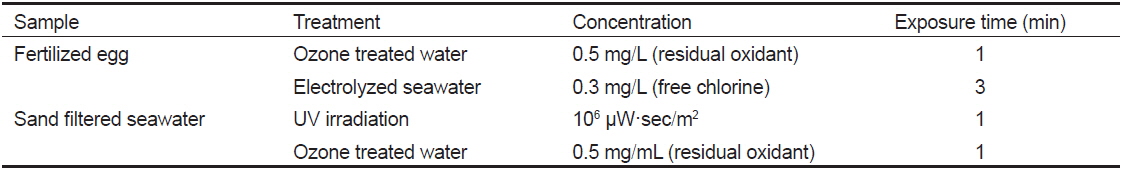
Disinfection of fertilized egg and water supplies (Tsuchihashi et al., 2002; Yoshimizu, 2009; Watanabe et al., 2013)
연안의 환경수 또는 지하 해수를 펌핑하여 모래 여과 후 양식장에 사용하는 사육수에는 NNV가 오염되어 있을 수 있으므로 사육기간 중에 이들 사육수를 경유한 수평감염이 발생할 수 있다. 따라서 사육수를 충분히 살균하여 사용함으로써 NNV의 수평감염을 예방할 수 있다. 모래 여과를 통해 양식장으로 유입되는 물은 일반적으로 자외선 또는 오존을 통해 소독한 후 친어 수조, 수정 및 부화 수조, 먹이 생물(로티퍼, 알테미아) 배양 수조 및 자·치어 사육 수조에 공급하여 사용한다. NNV를 불활화 시키기 위해서는 UV의 경우 106µW·sec/m2로 1분간 이상 조사하여 소독하여야 하며, 오존 처리수의 경우 0.5 mg/mL의 잔류 옥시던트 농도에서 1분 이상 노출시켜야 한다(Table 2)(Yoshimizu, 2009). 해수 중에 잔류 옥시던트가 남아 있을 경우 이들 사육수가 직접적으로 어류에 독성(96시간 노출된 어류의 반수치사농도: 무지개송어 9.3 ppb, 넙치 22.3 ppb)을 나타내므로(Kim et al., 1999; Wedemeyer et al., 1979) 사용하기 전에 활성탄으로 처리하여 잔류농도를 완전히 제거한 후 사용하여야 한다. 많은 양의 해수를 사용할 경우에는 사육수를 전기분해 처리하여 소독한 후 일정 시간 동안 충분히 폭기시켜 수중에 남아있는 차아염소산을 기화시킨 후 사육수로 사용한다(Kasai et al., 2000).
종묘 생산장에서 생산된 NNV 무감염 능성어를 양성장으로 이동하는 경우, 연안수 중에 상존하는 NNV가 가두리 또는 연안수를 이용하는 육상 수조식 사육장으로 유입되어 수평감염이 발생할 수 있다. 특히, 국내 능성어 양식장에서는 매년 여름철 8-9월에 VNN이 발생하고 있으므로 고수온기인 하절기에 각별한 관리가 요구된다. 사육수의 살균은 NNV의 수평감염을 예방하는데 유용하기는 하지만 현실적으로 많은 양의 물을 소독하는 것은 양식장의 경영 관계상 매우 적용하기가 힘든 방법이다. 이러한 양식 환경에서는 백신 및 Poly(I:C) (polyriboinosinic : polyribocytidylic acid)를 투여하여 NNV의 수평감염을 예방할 수 있다(Fig. 1). 간단히 설명하면 양성중인 능성어에 NNV 백신을 투여하여 NNV에 저항성을 가진 어류를 사육하는 방법, 현장에서 VNN이 발생될 경우 능성어에 Poly(I:C)를 투여하여 어체 내의 상태를 항바이러스 상태로 만들어 NNV의 체내 증식을 억제시킴으로서 VNN에 의한 피해를 최소화시키는 방법이다. 이들 두 가지 방법들은 능성어의 VNN 예방에 유효한 것으로 확인된 바 있다(Kim et al., 2012; Nishizawa et al., 2012; Oh et al., 2012; 2013a; 2013b; Tanaka et al., 2001; Yamashita et al., 2009).
일반적으로 어류질병을 예방하기 위해 주로 불활화백신이 현장에서 사용되고 있으나 어류바이러스의 경우 효능이 기대 수준에 못 미치어 국내에서는 그다지 상용화되지 못하고 있다. 능성어류의 NNV 예방법으로는 불활화백신법, 재조합백신법 및 생백신법이 보고되어 있다(Nishizawa et al., 2012; Oh et al., 2013a; Tanaka et al., 2001; Yamashita et al., 2009). NNV 불활화백신의 경우, VNN에 대한 예방 효능[RPS (relative percentage survival): <40.8%]을 얻기 위해서는 107TCID50/fish 이상의 항원을 어체 내에 투여해야 한다(Yamashita et al., 2009). 하지만, 높은 감염가의 바이러스 항원을 처리하기 위해 필요한 고가의 백신제작 경비에 비하여 그 효율은 상대적으로 낮은 이유에서 보다 경제성이 높고 효과가 탁월한 백신의 개발 필요성이 대두되어 최근 수년간 생백신의 개발 연구가 진행되고 있다. 능성어에서 최근 개발된 NNV 생백신법으로는 Poly(I:C)처리 면역법 및 사육수온을 이용한 생백신면역법이 있다(Kim et al., 2012; Nishizawa et al., 2009; 2012; Oh et al., 2012; 2013a;2013b).
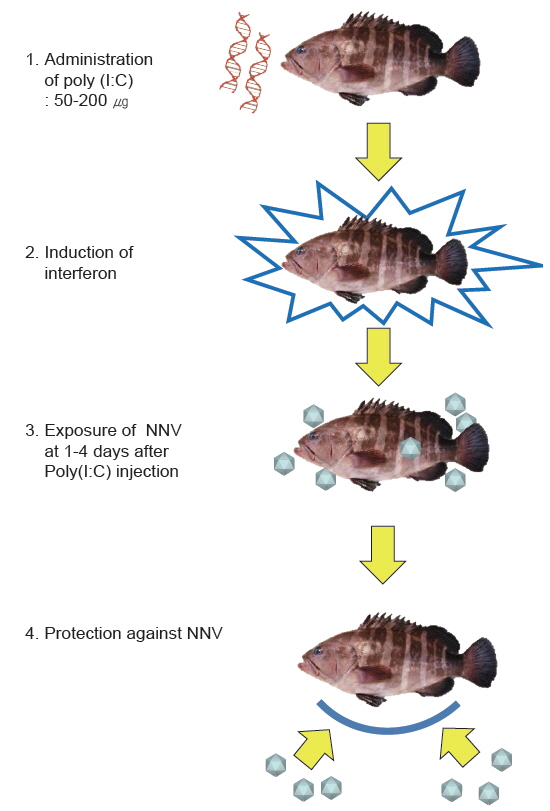
Poly(I:C)는 합성 double-stranded RNA 물질로서, 세포 내에 들어가게 되면 숙주는 바이러스가 침입한 것으로 오인하여 인터페론 생성을 유도하며 일시적이고 비특이적인 항바이러스 상태를 형성하게 된다. 이렇게 항바이러스 상태인 어류 체내에 바이러스가 침투하게 되면 이미 생성된 인터페론에 의해 바이러스의 증식이 억제되게 된다(Jensen and Robertsen, 2002; Kim et al., 2014; Plant et al., 2005). 또한 바이러스의 공격을 이겨낸 생존어는 그 바이러스에 대한 특이보호면역반응(specific protective immune response)을 획득하게 된다(Nishizawa et al., 2009). Poly(I:C) 면역법은 위의 원리를 이용하여 Poly(I:C)를 능성어에 투여하여 어체 내를 항바이러스 상태로 만든 후 NNV에 노출시키는 방법이다(Fig. 4)(Nishizawa et al., 2009). 본 방법을 능성어에 적용할 경우, NNV에 노출되어도 97.5% 이상의 생존율을 나타내었다(Kim et al., 2012; Nishizawa et al., 2009; Oh et al., 2012).
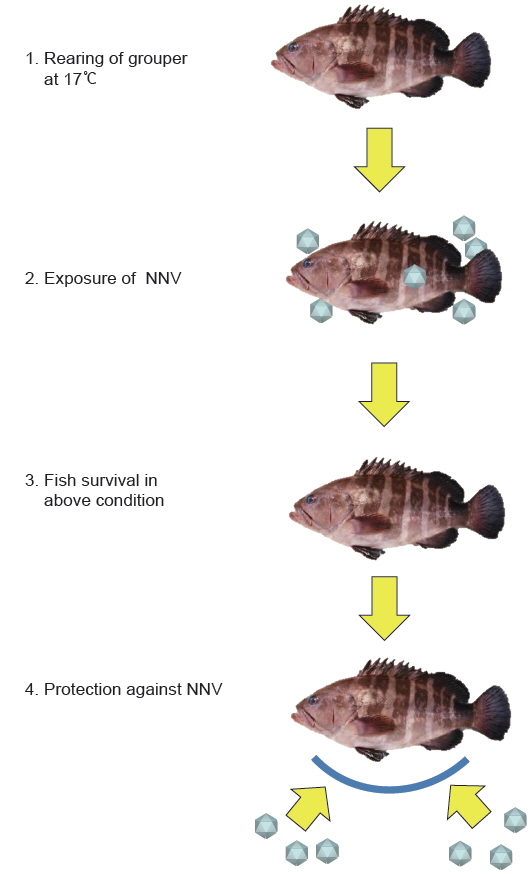
사육수온을 이용한 생백신면역법은 VNN 발병 온도 범위 밖에서 사육중인 능성어에 바이러스를 노출시켜 바이러스의 증식을 억제시키면서도 생존어의 경우 바이러스의 감염 자극에 반응하여 강력한 방어면역을 획득하는 방법이다(Fig. 5)(Nishizawa et al., 2012; Oh et al., 2013a). 본 방법을 능성어에 적용할 경우(백신 처리 시의 사육수온: 약 17℃), 백신 투여 후 생존한 개체는 NNV에 노출되어도 95.7% 이상의 생존율을 나타내었다(Nishizawa et al., 2012; Oh et al., 2013a). 본 방법은 바이러스를 어체 내에 주사하지 않고 침지 감염시켜도 가능하기 때문에 종묘 생산장에서도 사용할 수 있는 장점이 있다. 그러나 현재까지 생백신은 상품으로 제작되어 있지 않으며, 현장에서의 위험성이 남아 있어 사용하는 데는 한계가 있다. 따라서 양식 현장에서 생백신을 사용하기 위해서는 면역어에 대한 영향(성장, 생리 등), 환경수 중의 바이러스 오염 유발 가능성, 면역어의 재발 위험 가능성, 면역어의 보균자(carrier)로서의 가능성 등에 대한 철저한 검증을 통한 안전성을 밝히는 추가적인 연구가 필요하며, 이를 통하여 다양한 감염성 질병 예방에 획기적인 역할을 할 것으로 생각한다.
위에서 언급한 바와 같이, Poly(I:C)를 능성어에 투여하게 되면 숙주는 바이러스가 침입한 것으로 오인하여 인터페론 생성을 유도하며 일시적이고 비특이적인 항바이러스 상태를 형성하게 된다. 위의 원리를 이용하여 양식 현장에서 VNN이 발생할 경우, Poly(I:C) 투여를 통해 질병을 제어할 수 있다(Kim et al., 2012; Oh et al., 2012). 양식장에서 VNN이 발생하게 되면 발병 초기의 병어로부터 나온 바이러스가 건강한 개체에게 전파되어 수평감염을 일으켜 대량 폐사로 이어진다. 따라서 질병 발생시에 Poly(I:C)를 투여하게 되면 어체 내를 항바이러스 상태로 만들 수 있어 바이러스가 유입되어도 생존하게 된다. 능성어 양식장에서 VNN에 의해 28.8%가 폐사된 시점에서 Poly(I:C)를 투여한 결과(투여 농도: 50 µg/fish), Poly(I:C)를 투여하지 않은 그룹의 누적 폐사율은 90.2%를 보였으나 Poly(I:C)를 투여한 그룹에서는 단지 6.3%만 폐사되었다(Oh et al., 2012). Poly(I:C)의 현장 적용은 VNN에 의한 피해를 최소화 시킬 수 있을 것으로 사료되나 Poly(I:C)는 단가가 비싸다는 단점이 있어(1마리 투여 비용: 약 500원) 경제성을 고려하여 사용되어야 할 것이다.