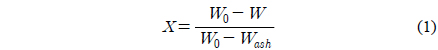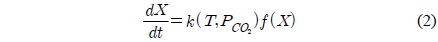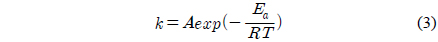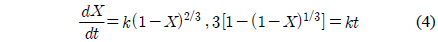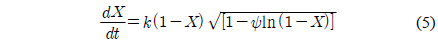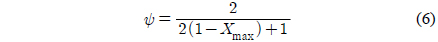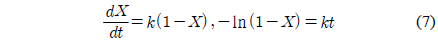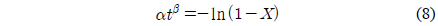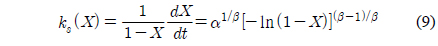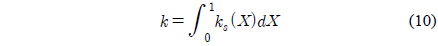In this study, we have investigated the kinetics on the char-CO2 catalytic gasification reaction. Thermogravimetric analysis (TGA) experiments were carried out for char-CO2 catalytic gasification of an Indonesian Kideco sub-bituminous. Na2CO3 and K2CO3 were selected as catalysts which were physically mixed with coal. The char-CO2 catalytic gasification reaction showed a rapid increase of carbon conversion rate at 850 ℃, 60 vol% CO2, and 7 wt% Na2CO3. At the isothermal conditions ranging from 750 ℃ to 900 ℃, the carbon conversion rates increased as the temperature increased. Four kinetic models for gas-solid reaction including the shrinking core model (SCM), random pore model (RPM), volumetric reaction model (VRM), and modified volumetric reaction model (MVRM) were applied to the experimental data against the measured kinetic data. The gasification kinetics were suitably described by the MVRM for the Kideco sub-bituminous. The activation energies for each char mixed with Na2CO3 and K2CO3 were found 55-71 kJ/mol and 69-87 kJ/mol.
기후변화협약과 환경규제 등에 대응할 수 있고, 석유나 천연가스의 고갈에 대비하여 에너지의 안정적인 확보 차원에서 석탄가스화 복합 발전(integrated coal gasification combined cycle, IGCC)에 대한 관심이 증대되고 있다. IGCC에 사용되는 다양한 종류의 석탄 중에 갈탄(lignite)과 아역청탄(sub-bituminous)이 저등급 석탄에 속하며, 세계 석탄 매장량의 약 40%를 차지하고, 저렴한 가격으로 미래 에너지 공급원으로 중요한 역할을 할 것으로 기대된다. 그러나 높은 수분 함량과 자연발화 가능성으로 인해 적극적인 활용이 부족한 실정이다[1,2].
이러한 저등급 석탄의 문제점을 극복하는 방안으로 촉매 석탄가스화 공정이 있으며, 이를 통해 저등급 석탄의 효율을 고등급 석탄을 대체할 수 있을 정도로 높일 수 있다[2,3]. 촉매 석탄가스화 공정에 사용되는 촉매는 석탄가스화 반응에 필요한 활성화 에너지를 낮추어 줌으로써 조업온도를 하강시키고 반응의 선택성을 높여서 특정한 가스화 생성물을 목적으로 조업할 경우에 사용된다. 가스화 반응에 주로 사용되는 물질은 석탄 내에 존재하는 고유금속성분과 인위적으로 첨가된 전이금속 산화물 또는 알칼리금속 탄화물 등이 알려져 있으며, 반응 속도의 상승효과 및 촉매 반응기구에 관한 연구가 부분적으로 진행되어 왔다[4-6].
가스화 반응에서 일어나는 반응들은 가스상 반응과 고체와의 다상 반응으로 나눌 수 있으며 촤(char, C) 가스화 반응은 다양한 모델을 사용하여 많은 연구가 진행되고 있으며, 국내에서도 관련 연구가 꾸준히 진행되어 왔다[7].
Kim et al.[8]은 미분탄용 역청탄의 촤와 이산화탄소 가스화 반응을 SCM (shrinking core model)과 VRM (volume reaction model)으로 해석하였다. Park et al.[9]과 Hwang et al.[10]은 이산화탄소 분위기하에서 다양한 온도(750-900 ℃)의 석탄 촉매 가스화 반응을 열중량 분석기를 사용해 연구했다. 이 연구에서는 SCM, VRM 및 MVRM (modified volume reaction model)이 사용되었다. Seo et al.[11] 등은 갈탄에 세 가지 종류의 폐촉매와 탄산칼륨을 이용하여 이산화탄소 가스화 반응속도상수 및 활성화 에너지를 조사하였으며, 반응모델로 SCM, VRM, MVRM을 적용하였다.
또한, 석탄의 고청정 또는 고효율 활용과 동시에 온실가스를 줄이기 위한 이산화탄소 포집 및 저장의 역할이 강조되면서 이산화탄소 활용에 관한 연구가 활발히 진행되고 있다. 그 중 회수한 이산화탄소를 석탄의 기류 수송이나 가스화기에 일부 순환시켜 가스화반응을 시키는 방안이 실험실 규모의 연구로 활발히 진행되고 있다[12-14].
본 연구에서는 저온 석탄가스화 반응 속도를 향상시키기 위하여 촉매를 첨가하였고, 열중량분석기(thermo gravimetric analyzer, TGA)를 이용하여 이산화탄소 분위기하에서 인도네시아 저등급 석탄인 키데코(Kideco)탄의 촉매 석탄가스화 반응 특성을 연구하였다. 4가지 온도 (750 ℃, 800 ℃, 850 ℃, 900 ℃)에 따라 촉매별 가스화반응 거동에 기-고체 반응모델인 SCM, RPM (random pore model), VRM 및 MVRM을 적용하여 모델의 적합성 정도를 검토하고, 활성화에너지값을 도출하였다.
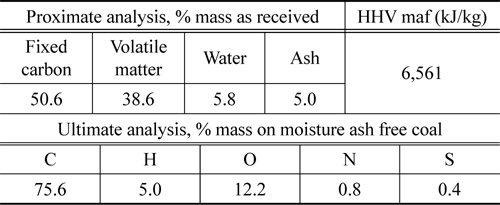
본 실험에서는 인도네시아산인 키데코탄을 사용하였으며, 미국 재료시험협회(american society for testing and materials, ASTM)에 따른 석탄의 공업 분석(ASTM D388-84)과 원소 분석(ASTM D3176) 결과를 Table 1에 나타내었다.
[Table 1.] Proximate analysis and ultimate analysis of Kideco coal
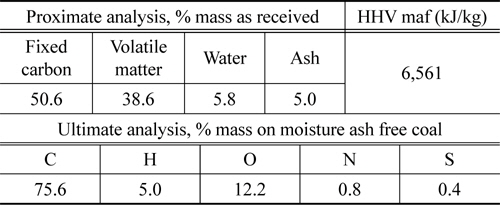
Proximate analysis and ultimate analysis of Kideco coal
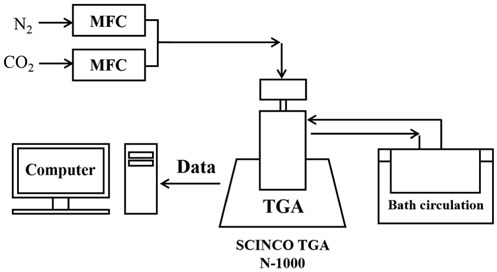
Scinco사의 열중량분석기 TGA-N1000에 공급되는 가스의 유량은 질량유량계(mass flow controller, MFC)를 이용하여 전체 유량이 50 ml/min 으로 일정하게 주입하였다. 열중량분석기에 주입되는 질소와 이산화탄소의 순도는 99.999%와 99.9%이며, Figure 1에 실험장치의 개략도 나타내었다.
키데코탄을 체(sieve)를 이용하여 75 µm 이하의 입자크기로 분류하였고, 분류된 석탄의 수분을 제거하기 위해 110 ℃ 진공오븐(OV-11)에서 24시간 건조하였다. 촉매를 첨가하기 위해 75 µm 이하의 입자크기로 분류하였고, 분류된 촉매는 건조된 석탄에 7 wt% 첨가하여 시료를 제조하였다.
건조된 석탄과 촉매의 물리적 혼합으로 제조된 시료 20 mg을 열중량분석기를 이용하여 열분해 과정과 촤-이산화탄소 가스화 반응 두 단계로 실시하였다. 석탄의 열분해는 최종온도, 승온속도 및 열분해 시간이 촤 가스화 반응에 큰 영향을 주므로 동일한 조건에서 촤를 만들었다[12,15,16]. 본 실험에서는 열중량분석기에 질소를 50 ml/min으로 충분히 흘려주어 질소 분위기로 만든 후, 상온에서 최종온도(750 ℃, 800 ℃, 850 ℃, 900 ℃)까지 30 ℃/min으로 승온시키고, 각각의 최종온도에서 무게 변화가 크게 일어나지 않는 완전한 촤 상태라고 판단되는 반응시작 60분 후에 이산화탄소를 공급하여 촤-이산화탄소 반응을 진행하였다.
최종 온도 800 ℃의 경우, Figure 2와 같이 질소분위기에서 진행되는 열분해과정은 시료에 잔류하는 수분과 휘발분이 제거되는 반응을 통해 무게감소가 일어난다. 촤-이산화탄소 촉매가스화반응은 800 ℃를 유지하는 동안 촤 상태 즉, 무게 변화가 크게 일어나지 않는 60분에 이산화탄소를 주입하였으며, 이후에는 촤-이산화탄소 가스화반응으로 무게감소가 일어난다. 이러한 실험방법은 네 가지 최종온도에 적용하였으며, 1초 간격으로 무게 변화를 확인하였다.
탄소전환율 X는 다음과 같이 정의할 수 있다.
여기서
탄소전환율의 시간의 변화율, 즉 반응성 또는 반응속도에 대한 식은 다음과 같다
k는 가스화 반응속도상수(gasification reaction rate constant)로써 온도(T)의 영향과 반응가스의 부분 압력(PCO2)의 영향을 포함한다.
여기서 A는 빈도인자(1/min),
석탄가스화는 석탄의 열분해 과정을 통해 수분과 휘발분이 제거된 촤가 수증기, 수소 및 이산화탄소와 같은 산화성 기체와 반응하여 일산화탄소와 수소가 주성분인 합성가스를 만들어내는 과정이다. 석탄가스화는 전체적으로 기상과 고상간의 반응이므로 반응의 전환정도를 정확하게 예측하기란 매우 어렵다. 따라서 많은 연구자에 의해 여러 가지 다양한 기-고체 반응모델이 제시 되었다[17].
본 연구에서는 가장 많이 사용되고 있는 SCM, RPM, VRM 및 MVRM을 반응성 평가 모델로 선정하였다.
Wen[18]에 의한 SCM은 반응 초기에 반응가스가 촤의 표면에서 반응을 시작하고 점차 반응가스가 안으로 들어가면서 입자 내부로 접근하여 반응한다고 가정한다. 이때 반응식은 아래와 같다.
RPM은 Bhatia and Perlmutter[19]에 의해 제안되었으며, 반응이 일어나는 동안 변화하는 기공의 표면을 고려해 준 모델이다. 이 때 반응식은 아래와 같다.
여기서
여기서 Xmax는 탄소전환율의 시간에 따른 변화가 가장 클 때, 즉 반응속도가 가장 빠를 때의 탄소전환율값에 해당한다.
Ishida and Wen[20]에 의한 VRM은 이종간(heterogeneous) 반응인 촤-가스 반응을 동종간(homogeneous) 반응으로 단순화한 모델로 반응가스는 촤의 내부와 외부의 모든 가능한 곳에서 균질하게 반응한다고 가정한다. 이 때 반응식은 아래와 같다.
MVRM은 Kasoaka et al.[21]에 의해 제안되었다. VRM식을 기본으로 하되, 촤의 가스화 반응속도를 분석하고, 정량적으로 반응성을 계산하기 위해 다음과 같은 식을 사용하였다.
여기서 상수값 α와 β는 최소자승법을 이용하여 전환율 실험 데이터로부터 구할 수 있다. 가스화 반응속도는 전환율에 따라 변하며 다음과 같이 유도된다.
k는 가스화반응소도 ks(X)를 전환율 구간에서 적분하여 구할 수 있다.
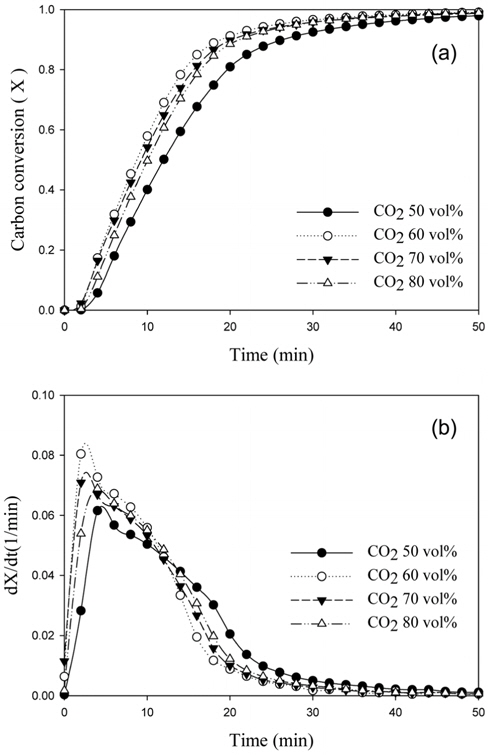
이산화탄소 농도가 촤-이산화탄소 촉매가스화 반응에서 탄소전환율에 미치는 영향을 알아보기 위하여 이산화탄소 50-80 vol%에서 실험을 진행하였다. 반응온도는 850 ℃로 유지하고, 촉매의 함량은 탄산나트륨 7 wt%로 결정하였으며[22], Figure 3에 이산화탄소 농도별 실험결과를 나타내었다. 이산화탄소 농도가 50 vol%에서 60 vol%으로 증가할수록, 탄소전환율이 빠른 것을 확인할 수 있었다. 하지만 이산화탄소 농도가 70 vol%에서 80 vol%으로 증가할 때 탄소전환율은 그 차이를 보이지 않았다. 반응속도에서도 이와 같은 경향성을 보여주었으며, 특히 이산화탄소 60 vol%는 모든 전환율에 대해 가장 빠른 전환율속도를 보였다.
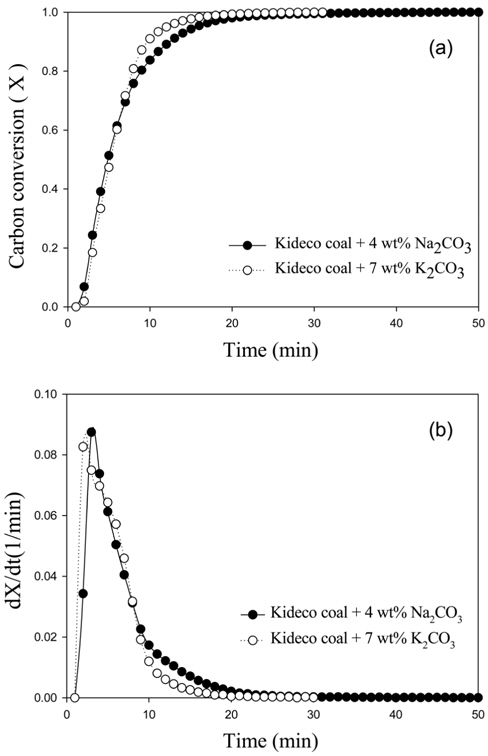
또한 실제 산업에서 촉매 석탄가스화는 wt%로 계산하여 촉매를 첨가한다. 따라서 시료 내에서 석탄(C)의 원자당 촉매(K, Na)비율, 즉 원자비가 달라지기 때문에 이를 자세히 알아볼 필요가 있다. 이에 본 연구는 7 wt%의 탄산칼륨과 동일한 원자비를 가진 4 wt%의 탄산나트륨을 첨가하여 촤-이산화탄소 가스화 반응을 비교하여 Figure 4에 나타내었다.
그 결과, 반응 시작 20분일 때 탄소전환율을 비교해보면, 4 wt%의 탄산나트륨은 탄소전환율 98% (X=0.98), 7 wt%의 탄산칼륨은 탄소전환율 99% (X=0.99)에 도달하여 비슷한 탄소전환율을 보였다. 최고 반응속도를 비교하면, 4 wt%의 탄산나트륨은 0.087 /min, 7 wt%의 탄산칼륨은 0.082 /min으로 근소한 차이이지만 거의 비슷하다고 볼 수 있다. 또한, 탄산나트륨의 가격(300-400 $/ton)이 탄산칼륨(1,300-1,500 $/ton)에 비해 매우 저렴하므로 7 wt%의 탄산나트륨이 가격적인 면에서도 경제적이다.
촉매의 활성도는 여러 연구결과에서 서로 상이하게 나타나며 이는 사용한 석탄의 등급, 석탄내의 미네랄 성분 및 반응조건 등이 서로 다르기 때문이다. 따라서 어떤 조업조건에서 우수한 특성을 보였던 알칼리 염류가 다른 조업 시에도 반드시 같은 경향을 보이는 것은 아니므로 촉매의 선정 시에는 이러한 점을 고려해야 한다[23].
위와 같은 실험결과 및 문헌조사를 통하여 본 연구는 촉매 함량 7 wt% 및 이산화탄소 60 vol%으로 촤-이산화탄소 촉매 가스화반응 조건을 결정하였다.
Irfan et al.[24]은 이산화탄소 분위기에서 가스화 온도가 반응속도를 제어하는데 있어서 가장 절대적인 영향요소임을 언급하였다. Liu et al.[25]은 1기압, 이산화탄소 분위기 및 1,000-1,300 ℃의 온도 범위에서 3종류의 촤를 활용하여 온도의 영향을 알아보았다. 그 결과, 시료별로 같은 반응시간 내에서 온도가 증가함에 따라 탄소전환율이 증가하였음을 확인하였다. Everson et al.[26]은 이산화탄소 분위기에서 TGA를 활용하여 실험을 진행하여 이산화탄소의 농도를 변화시키며 반응속도에 대한 온도의 영향을 알아보았고, 온도가 낮을수록 반응의 완료시간이 더 길어졌음을 확인하였다. Ye et al.[27]은 1.6-2.4 mm의 입자크기를 가진 석탄을 이용하여 이산화탄소 분위기에서 가스화를 진행한 결과, 명확하게 가스화의 반응속도는 반응온도가 증가함에 따라 증가한다고 하였다.
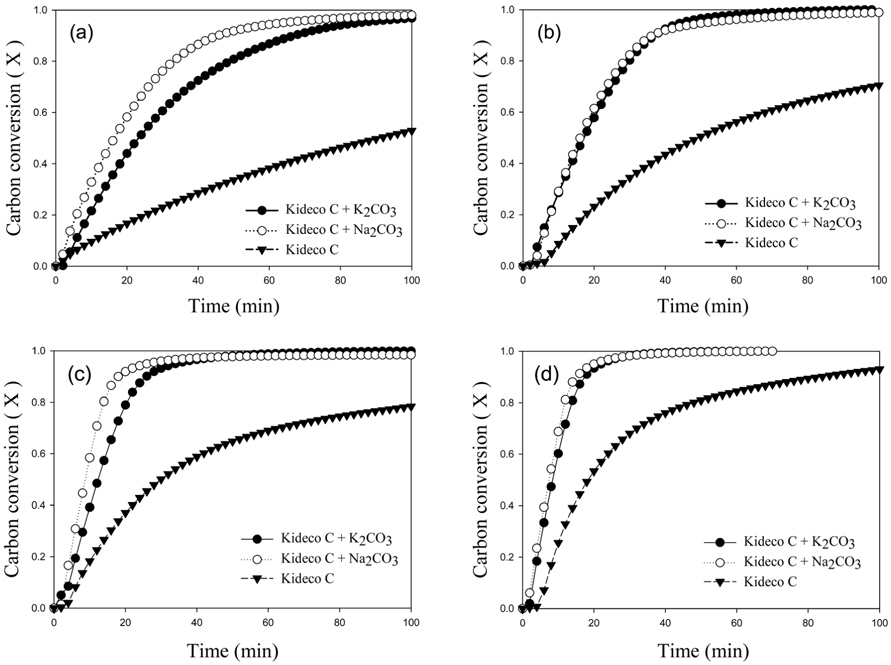
이를 바탕으로 본 연구에서는 탄산칼륨 및 탄산나트륨 두 가지 촉매를 첨가하여 촤-이산화탄소 촉매 석탄가스화 실험을 진행하였다. Figure 5는 이산화탄소 농도가 60 vol%일 때 반응온도 750-900 ℃에서 키데코탄에 7 wt%의 촉매를 첨가하지 않은 것과 탄산칼륨 및 탄산나트륨을 각각 첨가한 석탄의 촤-이산화탄소 가스화 반응의 탄소전환율을 나타낸 것이다. 실험결과를 통해 탄소전환율 100%에 도달하는 시간이 짧을수록, 우수한 촉매 활성을 가진다고 판단하였다. Figure 5에서 같은 시간을 기준으로 비교하였을 때, 촉매의 유무와 상관없이 온도가 증가함에 따라 높은 탄소전환율에 도달하는 시간이 빨라졌음을 확인할 수 있었다. 또한 탄산나트륨을 첨가한 시료가 탄산칼륨을 첨가한 시료보다 모든 온도에서 탄소전환율 100%에 도달하는 시간이 더 빠름을 확인할 수 있었다.
탄산나트륨과 탄산칼륨과 같은 알칼리금속염들의 촉매활성은 탄소질의 물리화학적 성질(표면적, 기공구조, 회분조성 등), 촉매의 첨가방법, 음이온의 종류 및 시료의 전처리방법 등이 촉매활성도에 영향을 미칠 수 있다. 그러나 대부분의 경우 주기율표의 순서(Cs > Rb > K > Na > Li)에 따라 촉매활성도는 증가하며 활성화에너지는 감소한다[28]. 알칼리전구체(탄산칼륨)를 이용한 가스화 반응 메커니즘에 대해서는 다양한 가설들이 제시되는데, 이 중 oxygen transfer mechanism이 가장 널리 알려져 있다. 탄산칼륨은 석탄의 탄소와 반응하여 표면에서 얇은 film형태의 산화물을 형성하고 다시 기상의 수분이나 이산화탄소와 산화·환원반응을 통해 가스화반응을 진행시킨다. 금속전구체를 사용하는 이유는 산화물을 직접 사용하는 것보다 석탄표면 위에 film형의 산화물을 형성하기가 유리하고 반응성을 높일 수 있기 때문이다[29,30].
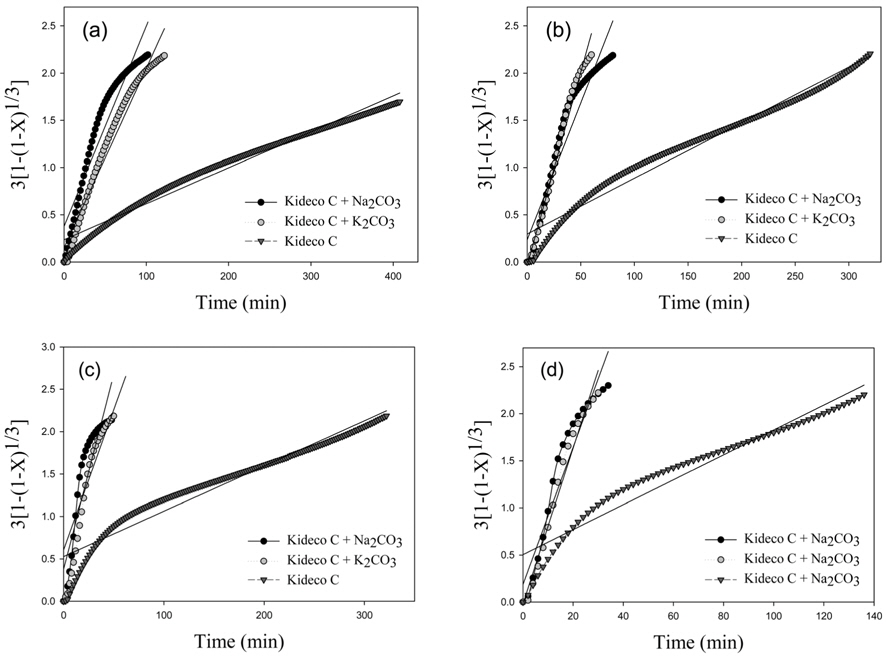
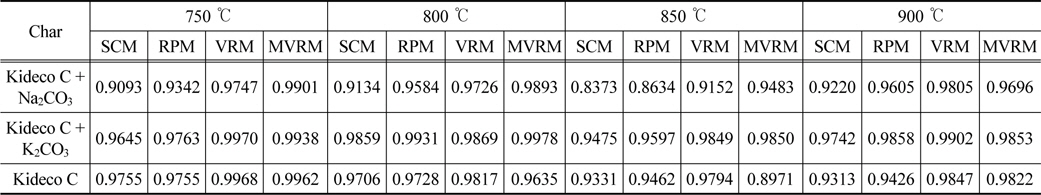
Figure 5에서 탄소전환율 100%에 가까울수록 반응속도가 매우 느리고 가스화되는 촤가 매우 적기 때문에 실험 오차를 발생시킬 수 있다. 이러한 오차의 영향을 줄이기 위해 탄소전환율 99%까지 전환율데이터를 각각의 온도에 따라 네 가지 반응모델에 적용하였다. 대표적으로 MVRM에 적용한 결과를 Figure 6에 나타내었으며, 각 모델별 상관계수(correlation coefficient, R2)값을 Table 2에 정리하였다. 상관계수값을 통하여 데이터가 모델에 얼마나 적합한지를 판단할 수 있으며, 그 절대값이 1에 가까울수록 높은 상관관계를 가지므로, 반응모델이 실험결과를 잘 예측한다고 판단할 수 있다.
[Table 2.] Correlation coefficient (R2) of SCM, RPM, VRM, and MVRM on Kideco char-CO2 gasification
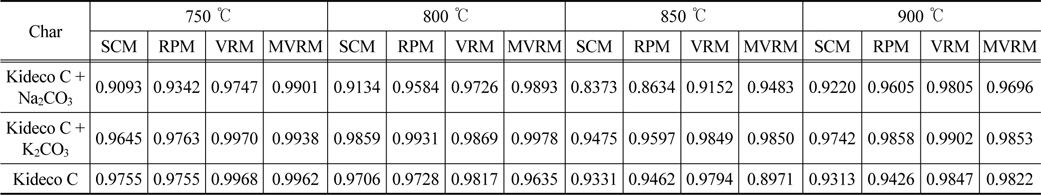
Correlation coefficient (R2) of SCM, RPM, VRM, and MVRM on Kideco char-CO2 gasification
Table 2를 통해 각각의 모델로부터 얻은 R2 값의 평균을 비교해보면, MVRM > VRM > RPM > SCM 순서로 R2 값이 1에 가장 근접하였다. MVRM의 경우 키데코탄의 모든 온도에서 가장 높은 R2 값을 보이고, 선형에 가까우므로 다른 모델보다 실제 전환율 데이터를 가장 잘 묘사하고 있다. 그러므로 키데코탄의 반응 거동을 잘 묘사하는 반응모델은 MVRM이다. 이는 식 (8)에서 두 개의 상수를 포함하고 있기 때문으로 판단된다.
Song et al.[31]은 석탄 가스화 반응인 경우에 MVRM이 전환율 거동을 비교적 잘 묘사한다고 제시하기도 하였다. SouzaSantos et al.[32]과 Ye et al.[27]은 입자크기가 크면 반응이 촤 표면에서부터 내부로 순차적으로 진행되고 ash의 저항을 받기 때문에 SCM이 적합하며, 입자크기가 작고 입자에 균열이 있을 경우 VRM이 더 적합하다고 하였다. Duman et al.[33]은 RPM의 경우, 가스화 반응이 진행되는 동안 기공의 성장(pore growth)과 겹침(pore coalescence)을 고려한 모델이므로, 이론과 실험을 동시에 만족하는 결과를 보여준다고 하였다. 하지만 높은 탄소전환율 범위에서 반응속도가 최대값을 갖거나 탄소전환율이 증가함에 따라 반응성이 증가하는 경우 바이오매스 촤를 묘사하는데 있어서 만족스럽지 못한 결과를 보여주기도 한다.
그러나 각각 다른 종류의 시료, 실험조건 및 입자크기에서 실험하였으며, 서로의 실험 조건을 비교하지 않고 단순히 반응 모델을 비교하였으므로 연구결과에 따라 다소 차이가 있다[31].
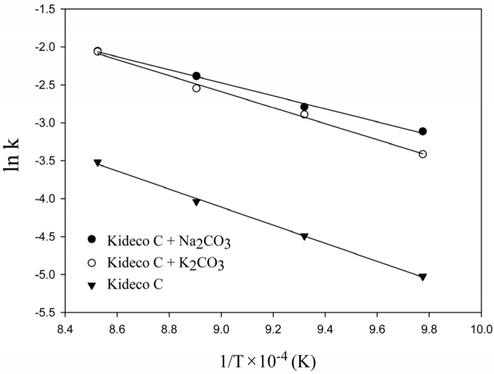
탄소전환율 50% (X=0.5)일 때, 반응속도는 평균 반응속도와 차이가 크지 않으므로 탄소전환율 50%에서 활성화에너지를 구하였다[34]. Figure 7은 대표적으로 MVRM에 적용한 촤-이산화탄소 촉매가스화반응의 반응온도에 따른 속도상수를 750-900 ℃에서 Arrhenius plot하여 나타내었다. 각각의 모델별 반응속도 상수는 자연로그를 취하여 얻을 수 있으며, SCM은 식 (4), RPM은 식 (5), VRM은 식 (7) 그리고 MVRM은 식(9)로부터 lnk
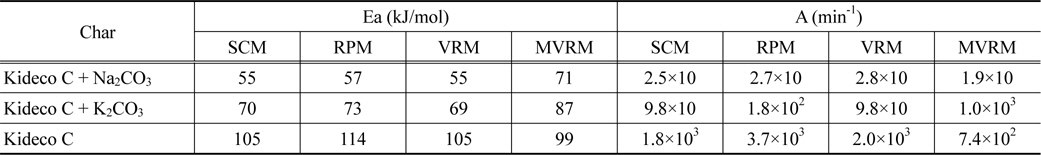
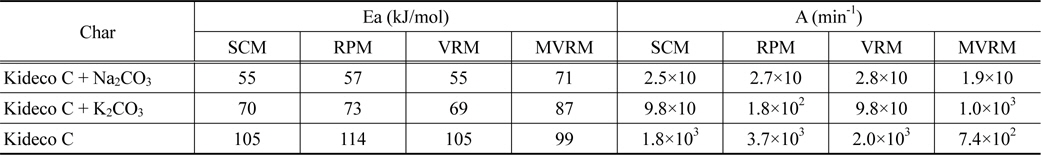
Kinetic parameters for each catalyst of the Kideco char-CO2 gasification by SCM, RPM, VRM, and MVRM
Table 3에서 탄산나트륨과 탄산칼륨을 첨가한 시료의 활성화에너지는 각각 55-71 kJ/mol, 69-87 kJ/mol로 촉매를 첨가하지 않은 시료의 활성화에너지(99-114 kJ/mol)보다 약 1.4-2배 우수한 촉매 활성을 보여주었다. 그리고 반응모델별 활성화 에너지의 값은 서로 다른 값을 보여준다. 특히 RPM의 활성화에너지값이 가장 낮은 것을 확인할 수 있는데, 이는 앞서 언급한 식 (5)에 의하여 반응속도가 가장 빠를 때의 탄소전환율의 값으로 반응속도상수를 구하였기 때문이다.
촉매 석탄가스화에서 촉매 활성은 촉매와 석탄 자체의 물리적인 특성 및 회분에 존재하는 조성과의 반응에 영향을 받는다. 또한 주기율표의 순서에 따라 1족 알칼리 금속 계열이 가장 큰 활성을 나타내며, 2족인 알칼리 토금속 그리고 전이금속 계열순서로 촉매의 활성도는 감소한다. 이런 촉매의 활성은 가스화 반응에서 촉매 염의 용융으로 탄소입자들의 응결을 증가시켜 나타나는 것으로 알려졌으며, 이에 의해서 활성화에너지가 감소할 수 있다[35]. Li et al.[35]은 탄산나트륨과 탄산칼륨의 첨가량에 따른 활성화에너지가 52-122 kJ/mol 범위에 있다고 보고하였고, Ahn et al.[36]은 인도네시아 아역청탄을 SCM으로 구한 활성화에너지가 1,100-1,400 ℃에서 71.5 kJ/mol, 900-1,000 ℃에서 144 kJ/mol라고 보고하였다[8]. 이와 같은 문헌상의 활성화에너지값들과 비교할 때 본 연구에서 사용된 촤들의 활성화에너지값은 적절한 범위에 포함된다.
가스화 반응의 반응특성을 분석하기 위해 열중량분석기를 이용하여 시간에 따른 무게 변화로 반응성을 비교하였다. 이를 위해 국내에서 가장 많이 수입되고 있는 저등급 석탄인 키데코탄으로 이산화탄소, 촉매의 종류 및 반응 온도가 촉매 석탄가스화에 미치는 영향에 대해 알아보았다. 또한 기-고체 반응을 분석하기 위해 석탄가스화 반응에서 가장 많이 사용되고 있는 반응 모델을 선정하여 가스화 반응거동 특성에 적합한 반응 모델을 선정하였고, 반응모델별 활성화에너지를 도출하여 다음과 같은 결론을 얻을 수 있었다.
1) 이산화탄소 농도가 촤-이산화탄소 촉매가스화반응에 미치는 영향을 확인하기 위하여 850 ℃에서 가스화 시킨 결과 이산화탄소 60 vol%일 때 가장 빠른 전환율속도를 보였다.
2) 석탄과 촉매의 원자비를 알아보기 위해서 7 wt%의 탄산칼륨과 동일한 원자비를 가진 4 wt%의 탄산나트륨을 촤-이산화탄소 촉매 가스화 반응시킨 결과, 두 시료가 비슷한 반응속도를 보였으며, 톤당 가격을 비교하면 탄산나트륨이 경제적인 면에서 유리하다.
3) 반응온도는 가스화에서 가장 큰 영향을 미치는 인자로, 촉매의 유무와 상관없이 750-900 ℃에서 온도가 증가할수록 반응속도가 증가하였으며, 탄산나트륨을 첨가한 시료가 탄산칼륨을 첨가한 시료보다 모든 온도에서 탄소전환율 100%에 도달하는 시간이 더 빠름을 확인할 수 있었다.
4) 네 가지 반응모델 적용 시 모든 촤들은 MVRM의 상관계수가 높은 값을 가졌으며, MVRM > VRM > RPM > SCM 순으로 가스화반응 거동에 적합한 모델임을 확인하였다.
5) 촤-이산화탄소 촉매가스화 반응에 대한 활성화에너지는 촉매의 종류와 적용 모델에 영향을 받았으며, 문헌의 결과와 유사함을 확인하였다.
따라서 촤-이산화탄소 촉매가스화반응에서 촉매의 종류와 이산화탄소 농도 및 반응온도에 따라 반응속도와 촉매의 활성에 큰 영향을 주므로 촉매가스화반응에서 매우 중요한 인자라는 것을 확인할 수 있었다.