This study investigated the inhibitory effect of high hydrostatic pressure (HHP) treatments on histamine production in mackerel
고등어(
한편, 고등어는 가을에서 겨울 사이에 대량 어획되는데, 어획후 선도가 급속히 저하되므로 일부만이 선어로 이용되고, 주로 염장등의 방법을 통해 이용되고 있다(Lee et al., 1998). 그러나 이러한 염장법의 경우 고등어의 선도 유지를 위해 첨가한 소금이 지질의 산패를 촉진(Ryu et al., 2002)할 뿐만 아니라 식염 중의 질산염 및 아질산염이 반응을 이루어 발암성 물질이 생성될 가능성이 있는 것으로 보고되었다(Sung et al., 1997). 또한 한번 생성된 histamine은 열에 안정하여 가열처리에 의해 없어지지 않기 때문에 histamine의 생성을 근본적으로 억제할 수 있는 새로운 고등어의 가공 처리법이 필요한 실정이다.
따라서 이와 같은 고등어 이용 시 발생하는 문제점 개선 및 이용 증대를 위하여 저장성 및 안정성을 높이는 연구로 고등어의 포장방법을 달리하거나(Yang and Lee, 2000), 방사선 조사(Cho et al., 1985; Kim and Ha, 1989), 자외선 조사(Song et al., 2005), 저온 삼투압 탈수법(Lee et al., 1993) 등의 비가열 처리방법이 진행되고 있으며, histamine 생성 억제에 대한 연구로 histamine 분해균에 대한 연구(Mah and Hwang, 2009; Leuschner et al., 1998; Dapkevicius et al., 2000)와, histamine 생성 균에 대한 항신료의 항균작용(Mah et al., 2009; Wendakoon and Sakaguchi, 1993) 및 histamine decarboxylase 저해 효과 (Shakila et al., 1996; Wendakoon and Sakaguchi, 1995)에 대한 연구가 진행되고 있다.
한편 초정수압 처리는 비가열처리 기술로, 식품에 적용 시 영양소의 파괴를 최소화하면서 미생물 살균 효과를 나타내는 신기술로서 안전하고 고품질의 식품을 얻을 수 있는 기술이며 현재 그 응용 사례가 증가하고 있는 실정이다(Park et al., 2010; Han and Jeong, 2005; Patterson, 2005). 작용 원리로는 초정수압의 압력이 병원성 및 부패 미생물의 비공유 결합과 소수성 결합에 영향을 주어 세포막을 붕괴시키고 단백질 변성을 초래하여 미생물 사멸을 유발하는 것으로 알려져 있다(Bover-Cid et al., 2011). 그러나 이러한 초정수압 처리의 경우 현재 조미 오징어의 저장성 증대(Gou et al., 2011) 및 생굴의 미생물 생육억제(Park et al., 2006)에 대한 연구는 진행되었으나, 고등어의 histamine 생성 억제에 대한 연구는 진행된 바 없다.
따라서 본 연구에서는 고등어 선도 저하의 방지 및 내부 histamine 생성을 억제하는 방법으로 고등어 필렛에 대한 초정수압 처리의 효과를 조사하여 새로운 고등어 가공법에 대한 기초자료를 제공하고자 한다.
본 실험에 사용된 고등어(
생고등어의 머리와 내장을 제거하여 제조된 고등어 필렛을 각각 진공 포장하여 초정수압기(215L-600 ULTRA, AVURE Technologied Inc. WA, USA)의 processing chamber에 넣어 수온 약 18-24℃에서 200, 300 및 400 MPa로 3분간 초정수압 처리한 후, 4℃에서 5일 간격으로 25일 동안 저장하면서 실험을 진행하였다.
일반 세균수 측정은 고등어 필렛의 머리, 등, 배, 꼬리 부위로부터 고등어 육을 무균적으로 2 g 취한 후, 식품공전상(Korean Food and Drug Administration, 2013)의 일반세균수 시험법에 따라 멸균 PBS (Phosphate buffered saline, pH 7.4)를 10 배 (w/v) 가하여 1000 rpm에서 1분간 균질화(Ace Homogenizer, AM-7, Nihonseiki, Japan) 한 다음 10배 단계 희석법으로 희석하였다. 일반 세균수는 시료 희석액을 PCA (Plate count agar, BD DifcoTM, USA)에 도말하여 37℃에서 24-48시간 배양한후, 생성된 집락을 계수하였으며 2회 반복하였다.
어육 내 histamine 생성량 측정은 Kanki et al. (2007)의 방법에 따라 분쇄한 고등어 육 1 g에 0.1 M EDTA (pH 8.0)를 24 mL 첨가하여 1분간 교반하고 100℃의 물에 20분간 정치시킨후, 얼음물에 10분간 냉각시켰다. 이를 여과지로 여과한 다음, 여과액을 Histamine assay kit를 사용하여 UV/visible spectrophotometer로 470 nm에서 흡광도를 측정하여 histamine 함량을 정량 하였으며 3회 반복하였다.
>
pH 및 volatile basic nitrogen (VBN) 함량 측정
pH는 세절한 고등어 5 g에 10배의 증류수를 가하여 균질기 (Ace Homogenizer, AM-7, Nihonseiki, Japan)로 10,000 rpm에서 2분간 균질화 한 후, 실온에서 pH meter (HM-30V, TOA, Kobe, Japan)를 이용하여 측정하였으며 2회 반복하였다. VBN 측정은 식품공전상(Korean Food and Drug Administration, 2013)의 Conway법을 이용하였다. 세절한 고등어 10 g에 5배의 증류수를 가하여 10분간 교반, 5분간 정치를 두 번 반복하여 30분간 침출하였다. 이를 여과한 후, 5% H2SO4로 pH 4.0으로 보정하고 100 mL로 정용하였다. Conway unit 내실에 처리한 시료 및 0.01 N H2SO4를, 외실에는 K2CO3 포화용액을 각각 1 mL씩 첨가하고 혼합하여 25℃에서 1시간 반응시킨 후, 0.01 N NaOH로 적정하였다. 지시약으로 brunswik 시약을 이용하였으며 3회 반복하여 측정하였다.
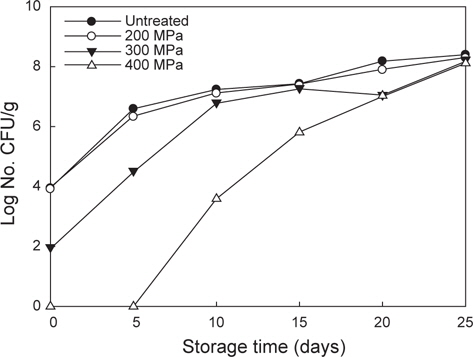
고등어 필렛을 제조하여 진공포장한 후 200, 300 및 400 MPa로 초정수압 처리하여 생균수의 변화와 생육 억제 효과에 대해 살펴본 결과(Fig. 1), 처리 직후에 무처리와 200 MPa 처리구에서는 각각 8.83 및 8.26×103 CFU/g의 균수를 보였으나 300 MPa 처리구에서는 9.48×101 CFU/g, 400 MPa 처리구에서는 균이 전혀 나타나지 않음을 확인하여 초정수압 처리 압력이 증가함에 따라 균의 생육 억제 효과를 확인하였다. 또한 저장일차가 증가하면서 무처리와 200 MPa 처리구는 지속적인 균의 증가를 보였으나, 저장 5일차 300 MPa 처리구의 경우 3.35×104 CFU/g, 400 MPa 처리구의 경우 균이 나타나지 않아 무처리구 및 200 MPa 처리구의 3.94, 2.14×106 CFU/g에 비해 균의 성장이 현저히 억제된 것을 확인하였다. 10일차 이후에는 무처리, 200 및 300 MPa에서 106 CFU/g 이상으로 생균수가 증가함을 확인하였으나, 400 MPa의 경우 10일차에 3.89×103 CFU/g, 15일차에 6.37×105 CFU/g으로 나타나 저장기간 중에도 초정수압 처리에 의해 무처리구보다 2-3 log cycle 정도 균의 생육이 억제됨을 확인하였다. 이 결과는 저장 초기의 경우, 300 MPa 처리 시 균수가 감소하였고, 400 MPa 처리 시 균이 나타나지 않아 초정수압 처리로 인해 미생물의 세포막 구조의 손상을 일으켜 정상적인 생육이 어렵게 되어 미생물 수가 감소된다는 Bull et al. (2005), Stephens (2005)의 보고와 일치하였다. 또한 이 결과는 Gou et al. (2011)의 조미 오징어에 400 MPa의 초정수압을 처리 후 저장기간 동안 미생물의 수가 대조군에 비교하여 저장 초기 2.77 log cycle의 감소를 보인 결과와 유사하며, 또한 Park et al. (2006)은 생굴에 350 MPa 초정수압 처리 후 저장 7일차에 약 103 CFU/g로 저장기간 동안 균수의 증가가 억제됨을 확인한 바 있다.
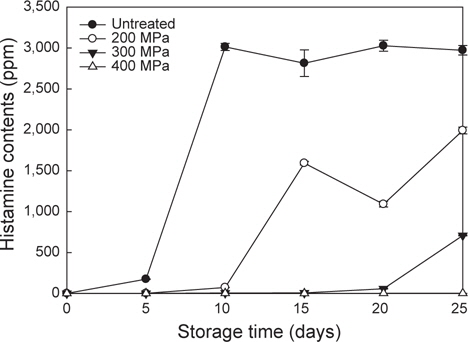
초정수압 처리에 의한 고등어육 중의 histamine 생성 억제 효과를 알아보기 위하여 고등어 필렛을 진공 포장 후 200, 300 및 400 MPa로 초정수압 처리하여 histamine 생성 억제 효과에 대해 실험한 결과(Fig. 2), 저장 5일차에 무처리구의 경우 175.64 ppm으로 나타났으나, 초정수압 처리구의 경우 4 ppm 이하로 거의 나타나지 않았다. 무처리구는 저장 10일차에 histamine 함량이 급격히 증가하여 3013.33 ppm의 함량을 보였으나, 초정수압 처리구의 경우 200 MPa에서 73.21, 300 MPa에서 6.15, 400 MPa에서 2.18 ppm으로 압력이 높아짐에 따라 histamine 생성이 억제됨을 확인하였다. 15일차의 경우 무처리구가 2814.36 ppm으로 높게 유지되었고, 200 MPa 처리구의 경우 1592.82 ppm으로 증가하였으나, 300 및 400 MPa의 경우 저장 20일차까지 histamine이 거의 생성되지 않았다. 그 후 저장 25일차에 300 MPa의 경우 750 ppm으로 나타났으며 400 MPa의 경우 거의 나타나지 않았다. 생균수 결과에서 300 및 400 MPa의 경우 생균수가 저장기간이 증가함에 따라 증가하는 경향을 보였으나, histamine은 생성되지 않았다. 이는 미생물이 생산한 histidine decarboxylase 효소의 단백질 구조가 초정수압 처리에 의해 가수분해 되어 효소 활성 부위가 영향을 받아 기질과의 결합이 불가능해져 활성을 잃었기 때문으로 사료된다(San Martin et al., 2002). 따라서 초정수압 처리가 histamine 생성 미생물의 생육을 억제할 뿐만 아니라 histidine decarboxylase의 활성을 억제함으로써 고등어 내의 histamine의 생성을 억제하는 것으로 사료된다(Kim, 2012).
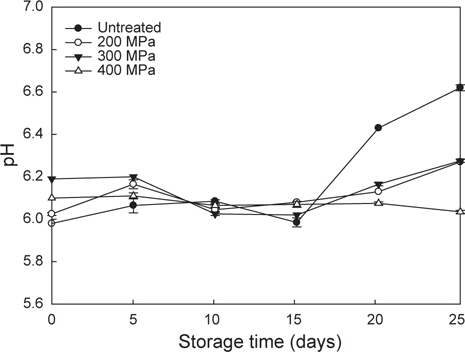
초정수압 처리에 의한 고등어육 중의 pH 변화를 알아본 결과(Fig. 3), 저장 초기 무처리의 경우 5.98, 초정수압 처리구는 6.03-6.19로 나타나 처리에 의해 pH가 약간 증가함을 보였다. 초정수압 처리구의 pH가 무처리구에 비해 약간 높게 측정된 것은 초정수압 처리에 의해 단백질 구조가 변화됨에 기인한 것으로 사료되며, 이는 대구 근육에 초정수압 처리한 경우 일부 단백질의 변성에 의해 pH가 약간 증가하였다는 Angsupanich and Ledward (1998)의 보고와 동일하였다. 또한 Hong et al. (2008)은 돈육에 초고압 열처리한 경우 초고압 처리에 의해 수분이 단백질 구조 사이로 침투함에 따라 단백질 풀림 현상이 일어나면서 단백질이 변성되어 돈육의 pH가 약간 증가한다고 보고하였다. 저장 15일차까지 무처리구와 처리구 모두 큰 변화를 보이지 않았으나, 저장 20일차에 무처리구의 경우 pH가 6.43으로 증가하였으나, 초정수압 200 및 300 MPa 처리구는 6.27-6.28으로 약간 증가함을 보였으며, 400 MPa의 경우 그대로 유지되는 것을 확인하였다. 이는 생굴에 초고압 처리 후 저장기간 동안 pH 변화를 측정한 연구에서 대조구에 비해 저장 중 pH 변화가 거의 없었던 결과와 유사하였다(Park et al., 2006). pH는 어육의 선도 저하에 따라 어육 중의 효소나 미생물에 의해 생성되는 암모니아, TMA (Trimethylamine), DMA (Dimethylamine)과 같은 염기성 물질의 축적에 의해 점차 상승하는 것으로 알려져 있다(Nam et al., 2011). 초고압 처리에 의한 미생물 생육과 histamine 생성이 억제된 결과(Fig.1, 2)를 미루어 볼 때, 초고압 처리에 의해 미생물 및 효소 활성이 감소함에 따라 암모니아, TMA, DMA 등의 축적이 적어 pH가 유지된 것으로 사료된다.
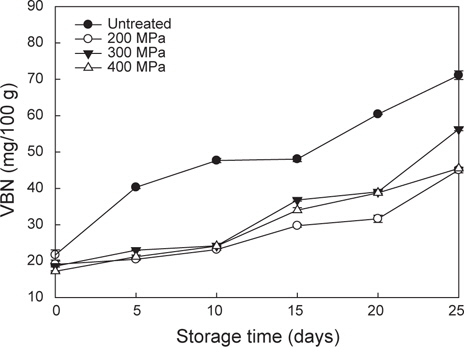
초정수압 처리에 의한 고등어육 중의 VBN 함량 변화를 알아 본 결과(Fig. 4), 저장 초기에 무처리는 21 mg/100 g의 함량을 보였고, 초정수압 처리구는 200, 300 및 400 MPa에서 각각 19, 18, 17 mg/100 g의 VBN 함량을 나타내어 처리압력이 높아짐에 따라 VBN 함량이 감소한 것을 확인하였다. 저장 5 일차에서 무처리의 경우 VBN 함량이 40 mg/100 g 으로 급격한 증가를 보였으나, 초정수압 처리구는 20-23 mg/100 g으로 낮은 VBN 함량을 보였다. 이후 저장기간이 증가함에 따라 무처리구는 지속적으로 VBN 함량이 증가하여 저장 20일차에 60 mg/100 g의 함량을 보였으나, 초정수압 처리구는 31-38 mg/100 g으로 낮은 함량을 보였다. 수산물의 선도 지표가 되는 VBN 함량은 일반적으로 5-10 mg/100 g을 극히 신선한 어육, 15-25 mg/100 g이 보통 선도의 어육, 30-40 mg/100 g이 부패 초기 어육, 50 mg/100 g이 부패가 심한 어육으로 판정하는데(Song et al., 2005), 무처리구의 경우 저장 5일차 이후 40 mg/100 g을 초과하여 초기 부패 단계로 나타났으나, 초정수압 처리구의 경우 저장 10일차 까지 VBN 함량이 처리 직후와 큰 차이가 없는 것을 확인하였다. 또한 무처리구의 경우 저장 20일차에 심한 부패가 진행되었으나, 초정수압 처리구는 부패 초기 단계인 것으로 사료되어진다. 이러한 결과는 Kang et al. (2011)의 고추장굴비에 초고압 처리한 후 저장기간동안 VBN 함량의 변화를 측정한 결과 대조구에 비해 낮은 VBN 함량을 보인 결과와 유사하다. VBN은 주로 세균의 증식에 의해 단백질이 분해되면서 증가하게 되는 것으로 알려져 있다(Song et al., 2005). Kurk et al. (2011)은 닭가슴살 필렛에 초고압 처리한 실험에서 처리 압력이 높아질수록 균이 감소하거나 사멸하였으며, VBN도 감소함을 보여 미생물 수의 감소에 인해 단백질 분해가 감소하였기 때문이라고 보고하였다. 따라서 본 연구에서의 VBN 함량 감소는 초정수압 처리에 의해 미생물의 살균효과와 단백질의 구조변화에 기인한 것으로 사료된다. 결론적으로 고등어에 초정수압 기술의 적용은 저장 중 고등어의 품질 저하로 인해 발생 되는 다량의 히스타민 생성을 억제 시켜 고등어 섭취로 인한 histamine 유래 식중독에 대한 안전성을 확보할 수 있는 방안이 될 것이며, 품질 특성에 대한 연구가 추가로 진행된다면 고등어의 미생물학적 안전성과 저장성 향상을 위한 새로운 가공방법으로 응용가능할 것으로 사료된다.