To investigate the characteristics of hybrid eggs and larva produced by olive flounder
잡종은 무척추동물, 어류, 조류 및 포유류의 많은 종에서 발생하며(Rhymer and Simberloff, 1996), 특히 대부분의 경골어류가 체외수정을 하고 유사한 번식습성을 가지기 때문에 다른 척추동물과 비교해서 잡종의 발생률이 높다(Leary et al., 1995). 이러한 어류의 특성 때문에, 잡종 연구에서 어류는 중요한 실험 재료로써 사용되어져 왔다(Verspoor and Hammer, 1991).
어류에서 잡종은 지리적으로 분리 분포하고 있는 두 집단간의 분류학적 위치를 검토하고(Kim and Kim, 1993), 외래종(introduced species)의 유입에 의한 토착종(native species)의 유전적 오염정도를 파악하기 위해서 연구되어져 왔다(Rubidge et al., 2001). 인위적으로 어류 잡종을 생산하는데 있어서 초기발생 및 성숙 가능 여부 등의 많은 변수가 존재하고 있지만(Varadi et al., 1995), 최근에는 양식업이 발전하면서 두 종의 장점을 가진 새로운 양식대상종을 개발하기 위한 연구가 진행되고 있다(Kim et al., 1995; Chevassus, 1998; Nam et al., 2008). 이러한 연구가 진행되고 있는 것은 잡종 1세대에서 발현되는 어떤 형질이 친어로 사용되는 두 종의 형질보다 더 우수하게 되는 잡종강세(heterosis)로 설명될 수 있다(Glamuzina et al., 2001). 하지만 잡종강세는 모든 형질에서 나타나는 현상이 아니기 때문에 우수한 형질을 가진 잡종을 생산하기 위해 다양한 어종간의 잡종연구가 계속해서 이루어지고 있다.
넙치(
따라서 본 연구에서는 넙치, 강도다리 및 두 종간 잡종 수정란의 수온별 발생속도 및 생물학적 영도를 조사하고, 넙치 및 잡종 부화자어의 성장도를 조사하여 생물학적 기초자료를 제공하고자 한다.
실험에 사용된 강도다리 정액은 강도다리의 방정과 넙치의 산란시기가 다른 것을 고려하여, 2012년 2월 약 1달동안 부산광역시 기장군 국립수산과학원 양식관리과에서 사육중인 강도다리의 정액을 채취하여 Lim et al. (2007)의 결과에 따라 희석액을 제조하였으며, 동해방지제인 10% DMSO (dimethyl sulfoxide)를 사용하여 -196℃ 액체질소에 냉동보존하였다.
2012년 2월 28일에 냉동보존한 강도다리 정액을 전라남도 여수시에 위치한 종묘배양장의 강도다리 암컷중에서 성숙한 어미를 선발하여 복부압박법으로 얻은 알과 건식법으로 인공 수정시켜 강도다리 수정란을 생산하였다.
2012년 3월 30일에 냉동보존한 강도다리 정액을 경상남도 거제시의 국립수산과학원 육종연구센터에서 사육중인 넙치 암컷에서 동일한 방법으로 얻은 알과 건식법으로 수정시켜 잡종(넙치♀ × 강도다리♂)을 생산하였고, 동일하게 사육중인 넙치 암컷과 수컷에서 알과 정액을 채취하여 넙치 수정란을 생산하였다. 생산된 수정란은 국립수산과학원 양식관리과로 수송 후에 수온별 난발생속도를 관찰하였다.
넙치, 강도다리 및 잡종 수정란의 수온별 난발생속도를 조사하기 위하여, 아크릴 재질의 사각수조(53×33×18 cm)에 자동온도조절기와 수중 히터를 이용하여 5, 10, 15, 20, 25 및 30℃를 실험구로 설정하고 수온을 유지하였다. 각 수정란은 마이크로 필터(∅ 50 μm)와 자외선살균기로 여과ㆍ살균한 34 psu해수를 담은 1 L 비이커에 수용하여 수온이 유지되고 있는 사각수조에 두고 3반복으로 실험을 진행하였다. 수정란의 발생단계는 광학현미경(Axioskop 2 plus; Carl Zeiss, Jena, Germany)를 이용하여 30분마다 관찰하였다. 수온별 난발생속도 차이를 조사하기 위해 강도다리는 포배기, 낭배기, 쿠퍼씨포(Kuffer's vesicle) 출현기, 꼬리 지느러미 형성기를 기준으로 하였고, 넙치와 잡종는 포배기, 낭배기, 쿠퍼씨포 출현기, 부화 직후 자어기를 기준으로 하였다(Fig. 1). 발생단계는 각 단계에 도달한 수정란의 비율이 50%가 될 때를 그 발생단계의 소요시간으로 산정하였다. 또한 강도다리, 넙치 및 잡종 수정란의 부화율을 조사하기 위해 15℃에서 각 수정란의 부화율을 3반복으로 조사하였다.
부화한 넙치 및 잡종 자어를 1.2톤 FRP수조에서 초기 먹이 생물인 rotifer와 Artemia 부화유생을 공급하면서 종묘생산을 하였다. 부화 후 24일까지는 rotifer만 공급하면서 지수식으로 수온 15℃, 자연광주기를 유지하였으며, 그 이후로 Artemia와 rotifer를 혼합 급이 하면서 유량을 조금씩 늘려 유수식으로 전환하였다. 유수식으로 전환 후에는 배합사료를 공급하면서 자연수온으로 사육을 하였으며, 4월부터 8월까지 사육 중 2주 간격으로 전장(total length)을 측정하였다. 넙치 및 잡종의 성장도 평균±표준오차로 나타냈으며, 유의차는 SPSS 통계프로그램(Ver. 18.0)을 사용하여 Independent t-Test로 유의차를 분석하였다.
강도다리 수정란에서 낭배기까지의 소요시간은 5℃에서 34시간, 10℃에서 24시간, 15℃에서 14시간 30분, 20℃에서 9시간이 소요되었다. 쿠퍼씨포 형성기까지 소요시간은 5℃에서 58시간, 10℃에서 34시간, 15℃에서 20시간이 소요되었다. 25℃와 30℃에서는 낭배기까지 발생도중 모두 폐사하였으며, 20℃는 쿠퍼씨포 형성기까지 발생도중 폐사하였다.
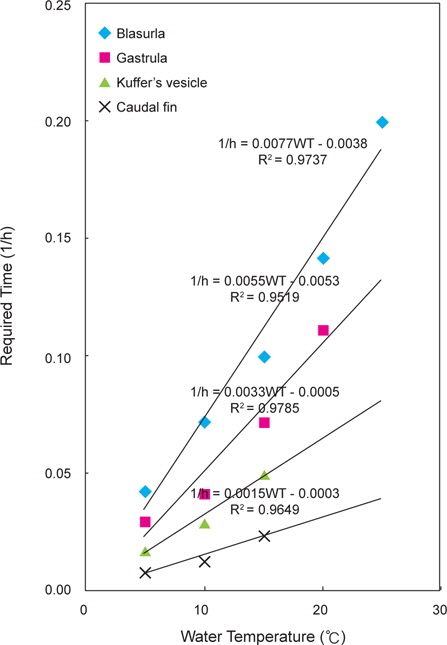
본 연구에서 강도다리 수정란의 발생 수온(WT)과 발생단계별 소요시간(h)의 관계식은 다음과 같다(Fig. 2).
포배기 : 1/h=0.0077WT-0.0038 (R2=0.9737)낭배기 : 1/h=0.0055WT-0.0053 (R2=0.9519)쿠퍼씨포 형성기 : 1/h=0.0033WT-0.0005 (R2=0.9785)꼬리지느러미 형성기 : 1/h=0.0015WT-0.0003 (R2=0.9649)
이들 관계식을 기초로 강도다리 수정란의 초기발생에 있어서 난발생이 진행되지 않는 생물학적 영도(biological minimum temperature)를 산정한 결과 0.5℃로 나타났다.
넙치 수정란에서 낭배기까지의 소요시간은 5℃에서 39시간, 10℃에서 19시간 30분, 15℃에서 14시간 30분, 20℃에서 10시간, 25℃에서 7시간, 30℃에서 5시간이 소요되었다. 쿠퍼씨포 형성기까지는 5℃에서 69시간 30분, 10℃에서 37시간 30분, 15℃에서 25시간 30분, 20℃에서 15시간 30분이 소요되었다. 25℃와 30℃는 낭배기까지 발생하였으나 모두 폐사하였으며, 부화에 도달한 실험수온은 10, 15 및 20℃였다.
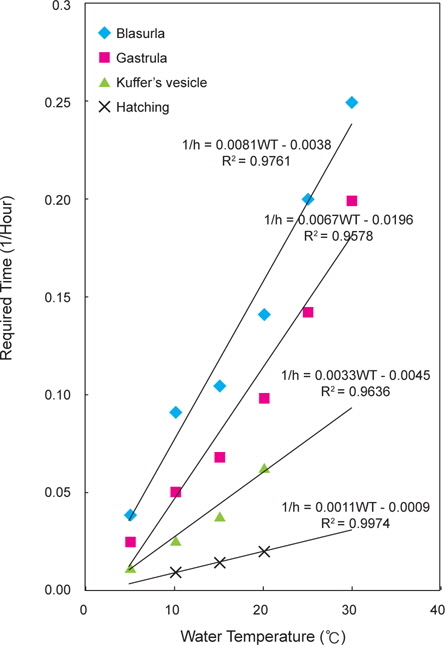
넙치 수정란의 발생에서 수온과 발달단계별 소요시간의 관계 식은 다음과 같다(Fig. 3).
포배기 : 1/h=0.0081WT-0.0038 (R2=0.9761)낭배기 : 1/h=0.0067WT-0.0196 (R2=0.9578)쿠퍼씨포 형성기 : 1/h=0.0033WT-0.0045 (R2=0.9636)부화 : 1/h=0.0011WT-0.0009 (R2=0.9974)
이들 관계식을 기초로 넙치 수정란의 생물학적 영도를 산정한 결과 1.8℃로 나타났다
잡종 수정란에서 낭배기까지의 소요시간은 5℃에서 35시간, 10℃에서 19시간 30분, 15℃에서 14시간 30분, 20℃에서 10시간, 25℃에서 7시간, 30℃에서 5시간이 소요되었다. 쿠퍼씨포 형성기까지는 5℃에서 69시간 30분, 10℃에서 33시간 30분, 15℃에서 23시간 30분, 20℃에서 15시간 30분이 소요되었다. 넙치 수정란에서의 결과와 같이 25℃와 30℃는 낭배기까지 발생 후 모두 폐사하였고, 부화까지 도달한 실험구는 10, 15, 20℃였다.
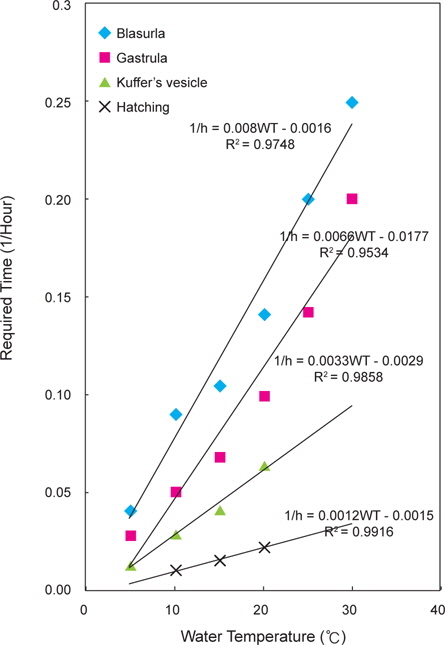
잡종 수정란의 발생에서 수온과 발달단계별 소요시간의 관계 식은 다음과 같다(Fig. 4).
포배기 : 1/h=0.008WT-0.0016 (R2=0.9761)낭배기 : 1/h=0.0066WT-0.0177 (R2=0.9578)쿠퍼씨포 형성기 : 1/h=0.0033WT-0.0029 (R2=0.9636)부화 : 1/h=0.0012WT-0.0009 (R2=0.9974)
이들 관계식을 기초로 잡종 수정란의 생물학적 영도를 산정한 결과 1.3℃로 나타났다.
넙치, 강도다리 및 잡종 수정란의 난발생이 진행되는 수온별 소요시간은 모든 실험구에서 수온이 높아질수록 짧아지는 경향을 보였다.
부화율은 강도다리가 63.5%, 넙치가 75.8%로 나타났으며, 잡종은 20.0%로 나타났다.
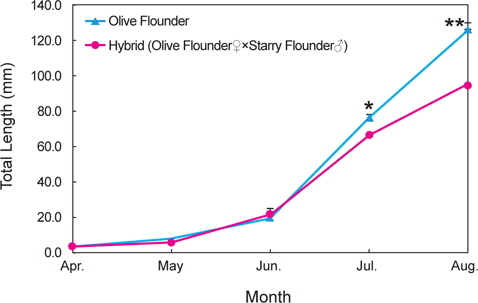
넙치 및 잡종 자어의 성장은 Fig. 5와 같다. 넙치 자어는 4월에 3.7±0.1 mm에서 6월 19.8±1.9 mm, 8월 126.6±3.5 mm까지 성장하였다. 잡종 자어는 4월에 4.0±0.1 mm에서 6월 21.1±1.6 mm, 8월에 95.2±2.4 mm로 성장하였다. 6월까지는 넙치 및 잡종 자어의 성장에서 유의한 차이가 없었지만, 7월과 8월에는 넙치가 잡종보다 더 빨리 성장하는 것을 관찰할 수 있었다.
수온은 어류에서 수정란의 발생과 자·치어에서의 성장 및 생존에 가장 중요한 요인 중 하나이다(Kamler, 2002). 일반적으로 수정란의 발생과 자·치어의 성장은 낮은 수온에서는 지연되고 높은 수온에서는 더 빨라지는 경향을 가지며, 각 어종에 따른 특유의 생활사와 생태적인 특징에 따라서 정상적인 발생을 위한 적정 수온 범위를 가지게 된다(Rana, 1990). 본 연구에서도 잡종 수정란의 부화까지 소요시간은 10℃에서 91.5시간, 15℃에서 62.5시간, 20℃에서 43.5시간이 소요되어 수온이 상승할수록 부화시간도 단축되는 경향을 보였으며, 넙치 및 강도다리 수정란의 수온별 발생속도에서도 같은 경향을 보였다. 이 결과는 고등어(
어류 양식에서 수온에 대한 이해는 성장과 생존에 관련된 적정수온을 통해 양식 시스템을 개선시키는데 매우 중요하며, 더 나아가 수정란의 수온별 발생속도는 그 종이 서식하는 자연환경을 유추할 수도 있다(Hyojin et al., 2012). 또한 부화 최적 수온은 대체로 자연산란 시기의 수온과 일치한다고 알려져 있다(Jun et al., 2002).
본 연구에서 생물학적 영도는 강도다리가 0.5℃, 잡종이 1.3℃, 넙치가 1.8℃로 나타났다. 이 결과는 가자미목에 속하는 돌가자미(
최근 바리과(Family Serranidae)에서 생산성이 뛰어난 잡종을 생산하기 위한 연구가 활발히 진행되고 있으며, 동남아시아를 중심으로 산업적으로도 이용되고 있다. 이들 바리과에서 이러한 연구들이 활발히 이루어지고 성공적인 잡종이 생산되는 것은 각 종들의 유전적인 관계가 매우 밀접하기 때문이다(Kiriyakit et al., 2011). 가자미목에 속하는 넙치와 범가자미(
잡종 형질에서 일부는 친어로 사용된 두 종 중에서 한쪽을 따르지만 대부분의 형질은 친어로 사용된 두 종의 중간을 나타내는 것으로 보고된바 있다(Kim et al., 1995). 본 실험에서 생물학적영도는 잡종이 넙치와 강도다리의 중간으로 친어로 사용된 두 종의 중간 형질을 나타내었다. 하지만 넙치와 강도다리 잡종의 형태학적인 특징에서는 수컷으로 사용된 강도다리에 조금 더 가깝다는 보고가 있었으며(Nam et al., 2008), 본 연구에서 5개월간 성장을 지켜본 결과에서도 잡종의 체형 및 지느러미 모양 등이 넙치보다 강도다리와 유사하게 나타났다. 또한 자연수온에서의 넙치 및 잡종의 성장이 4~6월까지는 유의차를 보이지 않았으며, 강도다리의 경우도 Byun et al. (2007)의 결과에서 평균수온이 14℃일 때 부화 후 52일째의 성장이 13.5±1.7 mm로 넙치 및 잡종 자어의 성장과 차이를 보이지 않았다. 하지만 수온이 상승하기 시작하는 7월과 8월에 넙치의 성장이 더 빨라지는 것을 관찰할 수 있었다. 이 결과는 잡종의 수온에 대한 내성이 강도다리와 마찬가지로 고수온기에 사료섭식율이 낮아지고 성장이 느려지는 냉수성 어종의 특징임을 나타내었다.
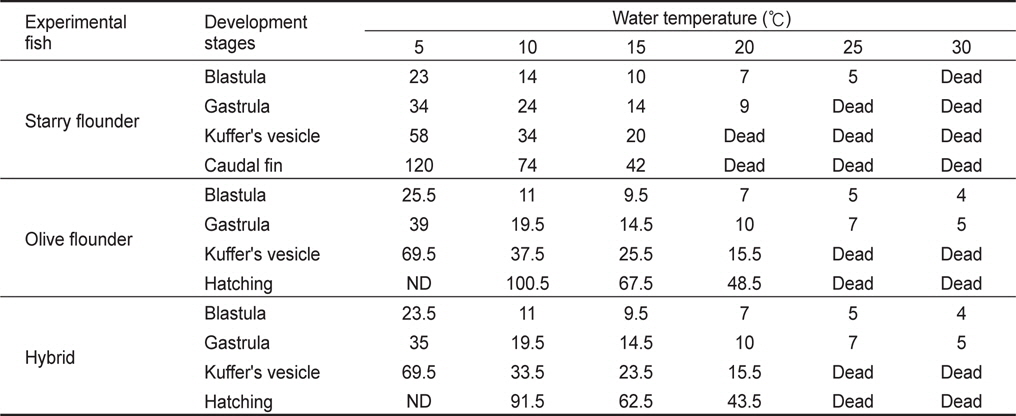
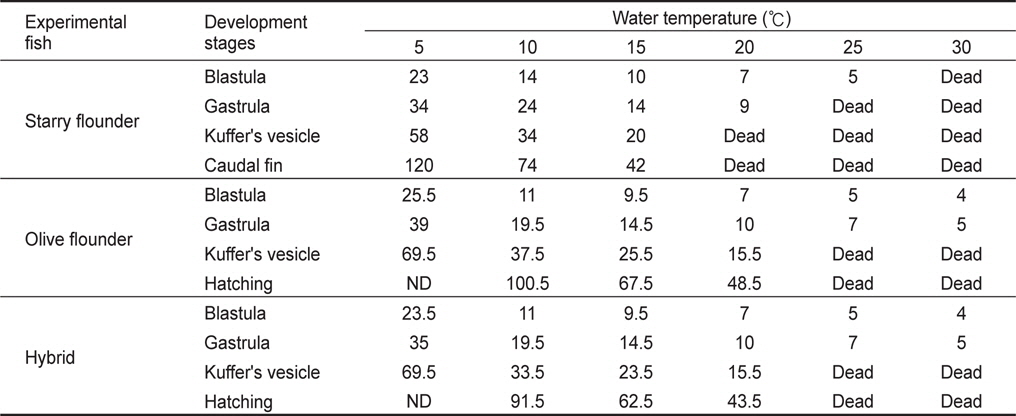
Elapsed time (hour) after fertilization of olive flounder Paralichthys olivaceus, starry flounder Platichthys stellatus and hybrid between olive flounder female and starry flounder male to distinctive development stages at different water temperature
잡종 초기생활사에 대한 이해는 종묘생산 기술 향상과 양식을 위한 새로운 종의 선정으로 이어질 수 있다(Kiriyakit et al., 2011). 본 연구에서 잡종의 종묘생산시 넙치 및 강도다리의 종묘생산 방법과 동일하게 rotifer, Artemia와 같은 먹이생물과 배합사료를 공급하여 성장하는 것을 관찰할 수 있었다. 이것은 넙치와 강도다리 잡종의 부화 및 변태 등의 초기생활사가 친어로 사용된 두 종과 유사하다고 판단할 수 있다.
본 연구는 넙치와 강도다리 잡종의 수온별 난발생속도, 생물학적 영도 및 성장도를 나타내었다. 잡종의 형질은 생물학적 영도에서는 친어로 사용된 두 종의 중간 정도를 보였으며, 성장도는 수컷으로 사용된 강도다리와 유사한 특징을 보였다. 잡종의 생리학적인 특징은 친어로 사용된 어류의 종류나 암·수차이에 의해서도 달라진다. 본 연구는 넙치 암컷과 강도다리 수컷 사이의 잡종을 생산하는데 있어서 기초자료로 활용될 것으로 기대되며, 잡종 특징을 파악하기 위해서 더 많은 연구가 진행될 필요성이 있다.