Brown patch caused by
2010년과 2011년에 경상북도 청도군 소재 골프장 그린에서 봄철인 5월중순과 가을철인 9월 하순에 전형적인 갈색잎마름병이 그린의 creeping bentgrass 종과 그린 주변에 식재 된 Kentucky bluegrass 혼합 품종에서 발생하였다(Fig.1 A). 5월 하순에 Kentucky bluegrass품종에서 발생한 병의 초기 증상은 잎의 선단부가 갈색으로 변색하여 갈색의 타원형 patch를 형성하고, 시간이 지나면서 갈색 잎 부분은 황색이 퇴화되어 잎의 끝이 마르며 patch의 가장자리로부터 밀짚 색으로 나타나고, 심한 부분은 고사하는 증상을 보였다(Fig. 1 B). 10월 상순에 Kentucky bluegrass품종에서 발병한 갈색잎마름병의 병징은 봄철과 다른 증상을 보였다(Fig. 1 C, D). 원형과 타원형의 갈색의 patch가 링의 형태로 나타나고, patch 가장자리는 회갈색과 검은 황갈색의 증상이 나타났다. Patch의 크기는 다양하였다. 이 병 잔디 주변이나 고사한 잔디에 균핵은 발견되지 않았다.
본 연구에 사용된 병원균은 2010년과 2011년에 경상북도 청도군 소재 골프장 그린에서 봄철과 가을철에 전형적인 갈색잎마름병 증상을 보이는 creeping bentgrass “Penn cross” 품종과 Kentucky bluegrass의 잎과 줄기에서 채집하였다. 채집한 이병 잎과 줄기에서 병환부와 건전부 경계의 조직을 잘라 1% sodium hypochlorit에서 1분간 표면살균 후, 70% ethanol에서 다시 30초간 살균하였다. 표면 살균한 병든 조직은 멸균수로 세척하여, 멸균된 거름종이(Whatman No. 1)에 올려놓아 수분을 제거하고, water agar (WA)에 미리 준비한 항생제 용액 (살균증류수: 100 ml; pimaricin: 100 mg; ampicillin: 1000 mg)을 1%을 첨가하여 만든 배지에 치상하고, 25℃ 항온기에서 3일간 배양하였다. 치상한 조직에서 자라나온 균사 선단의 균사를 떼어서 PDA (Potato Dextrose Agar) 배지에 옮겨 25℃ 항온기에서 배양한 15개 균주 중 생리적 반응이 동일한 균주 B-7을 대표 균주로 보관하면서 본 실험을 수행하였다. 공시 균주의 보관은 25℃ 항온기에서 계대 배양을 하면서 시험하거나, 3일간 배양한 균총의 선단부에서 직경 5 mm의 균사 조각을 떼어내어 cap tube(직경: 1 cm; 높이: 10 cm)에 5조각씩 넣고, 보관용액 5 ml(살균수: 5 ml; streptomycin (3,000 μg): 0.5 ml)를 넣어 25℃ 항온기에 보관하며 실험에 사용하였다.
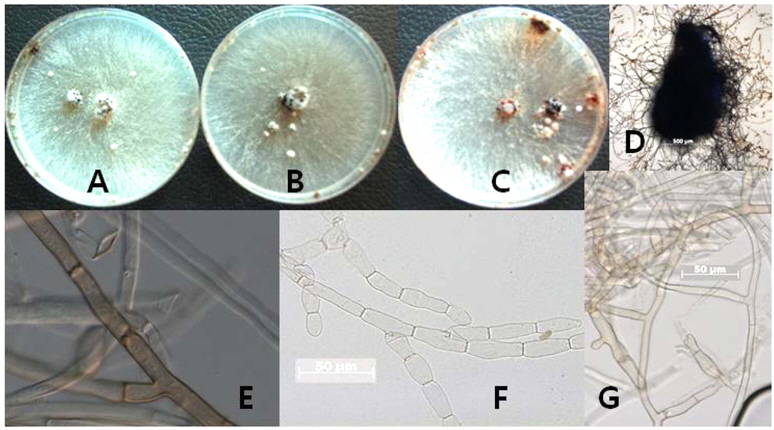
PDA배지에서 배양한 결과 생육초기에는 균사 색깔은 흰색을 띠며 왕성하게 생장을 하고(Fig. 2 A, B) 배양시간이 지남에 따라서 균사는 갈색으로 변하고, 균사 위에 검은 균핵을 형성한다(Fig. 2 C, D). 광학현미경하에서 관찰한 균사는 clamp 연결을 가지고 있으며, 균사의 모양은 어린 균사와 성숙한 균사의 모양이 다른 것을 관찰할 수 있었다(Fig. 2 E, F, G). 어린 균사는 분지각이 90도 보다 작으며, 성숙한 균사는 분지각이 직각으로 꺾이고, 격막이 있으며, 뿌리 모양으로 자라는 것을 볼 수 있다.
병원균의 균사의 형태적인 특징조사를 위하여 PDA배지에 접종 후 25℃항온기에서 5일간 자란 균사조각을 떼어내어 광학현미경하에서 격막 등을 관찰하였고, 생리적인 특성은 생육 온도와 배지종류에 대한 반응을 조사하였다. 생육온도는 PDA배지 중앙에 3일간 배양한 가장자리 균총의 직경 5 mm의 균사 조각을 떼어내어 접종한 후 20℃,23℃, 25℃, 28℃, 및 30℃에서 3일간 배양한 후 균총 직경을 조사하였다. 배지의 종류에 대한 균사생장 반응을 조사하기 위하여 생육온도와 같은 방법으로 균주를 PDA배지에 접종한 후 25℃에서 72시간 배양 후 균사 생장량을 측정하였다.
균사의 생육에 대한 두 종간에서 최적 생육온도에 뚜렷 한 차이를 보였다(Fig. 3). 공시 균주인 B-7은 대조 균주인
분자생물학적 동정을 위하여 25℃ 항온기에서 3일간 배양한 후 DNA를 추출하여 ITS 영역의 DNA의 증폭을 위하여 universal primer인 ITS5(5'-GGA AGT AAA AGTCGT AAC AAG G-3)와 ITS4(5'-TCC TCC GCT TATTGA TAT GC G-3')를 사용하였다(White et al., 1990). DNA증폭을 위한 25 μl의 반응액(template로 사용할 병원 균의 DNA 5 μl; 10배의 Taq buffer 2.5 μl; dNTP 2.5 μl; ITS50.5 μl; ITS4 0.5 μl; Taq polymerase, 0.125 μl; 살균증류수 13.875 μl)을 만들어 반응시켰다. 반응조건은 94℃에 서 4분 동안 pre-denaturation을 실시하였고, 95℃에서 30 초간 denaturation, 50℃에서 30초간 annealing, 72℃에서 1분 동안 extension하는 것을 30회 수행한 후, 72℃에서 7분간 최종 반응시켰다. PCR산물은 2% agarose gel을 만들어 50V에서 120분 동안 전기영동하였다. 리보소옴 ITS 지역의 DNA 염기서열을 분석을 위하여 ITS1 (5'-TTC GTA GGT GAA CCT GCG G-3')과 ITS4 (5'-AAC ATG CGT GAG ATT GTA AGT-3') primers 사용하여 분석하였으며 (White et al., 1990), DNA 염기서열은 솔젠트(주)에서 실시하였다. ITS 염기서열은 Thompson et al. (1994) 방법을 따랐으며, phylogenetic tree는 MEGA version 4를 사용하여 Rhizoctonia alpina (CBS 309.35) 염기서열과 GenBank 의 염기서열을 참고로하여 작성하였다(Tamura et al., 2007). 거리는 Tamura-Nei parameter model을 이용하여 산출하였고, phylogenetic tree는 Neighbor-Joining (NJ) 분석을 통하여 구축하였다.
공시 균주인 B-7을 DNA 리보소옴 ITS 지역과 RAPD 분석을 한 결과
Hong et al. (1998)은
병원성을 검정하기 위하여 발병이 잘되는 creeping bentgrass품종인 “Penn Cross” 와 Kentucky bluegrass 혼용 품종(Midnight 33%, Moonlight 33%, Prosperity 33%)을 재배하는 경남 합천의 (주)한울스포츠잔디 농장에서 뗏장을 구입하였다. 잔디는 관행 관리에 의해 1년 이상 자란 잔디를 뗏장으로 떼어내어 그린용 홀 컷터로 잔디를 잘라내어 화분에 옮긴 후, 온실에서 20일간 관리한 잔디에 병원균을 접종하였다. 접종원은 Chang (2011)의 방법에 따라 수행되었다. PDA 배지에서 자란 활력이 양호한 균총의 가장자리 균사를 지름 5 mm의 크기로 자른 균총 1조각을 PDB (Potato Dextrose Broth) 배지에 접종한 뒤 25 ± 1℃ 암 상태에서 5일간 배양하였다. 배양된 균사는 수확하여 멸균된 거름종이에 올려놓아 수분을 제거하고, 무게를 단 후 다시 멸균수를 넣어 30초간 균일하게 균사를 마쇄하였다. 접종원은 균사 생체 중 0.1 g ml-1가 함유된 1 ml를 포트당 접종을 하고, 바닥에 1 cm 높이로 물을 채운 플라스틱에 포트를 넣고, 밀봉한 후 48시간 동안 25 ± 1℃ 암 상태의 생장상(growth chamber)에서 배양한 후 온실로 옮겨 발병 정도를 조사하였다.
인공 접종한 병원균은 Kentucky bluegrass와 creeping bentgrass의 “Penn Cross” 품종에서 감염 초기증상을 잎의 선단부가 갈변하고, 이병 부위가 수침상으로 변하면서 점차 갈색이 퇴화하고, 시간이 경과됨에 따라 patch 형태를 유지하면서 잎과 줄기는 고사하여 최종 회갈색이 되었다 (Fig. 5). 인공 접종하여 발병된 병반부에서 다시 병원균을 재분리하여 PDA배지에서 배양한 후, 균핵 형성의 특성과 광학현미경에서 균사의 격막과 균사모양을 관찰한 결과 접종한 균과 일치하여 동일한 균으로 확인되었다.
따라서 본 병은 한지형 잔디인 Kentucky bluegrass 품종에서