This study investigated the physiological effects of a diet containing calcium oxide (CaO) on the olive flounder,
칼슘은 척추동물 내에서 뼈 및 치아의 형성, 신경전달 활성근육의 수축 및 이완, 혈액 응고, 체액의 산, 알칼리성 평형, 호르몬과 여러 효소들의 활성, 세포분열 등에 중요한 역할을 하는 물질로 알려져 있다(Paterson, 1978; NRC, 1993).
어류는 지속적인 성장을 위해 살아가는 동안 계속해서 체내에 칼슘을 축적하고, 수중에 녹아있는 칼슘을 아가미를 통하여 흡수한다. 아가미는 어류와 물 사이의 접촉점이 되는 가장 중요한 부위이며(Parry, 1966), 수중 칼슘을 흡수하는데 있어 가장 중요한 기관이다(Herrmann-Erlee and Flik, 1989; Flik et al., 1993). 어류는 아가미를 통해 수중에 존재하는 칼슘을 직접적으로 흡수하며, 그 중 일부는 장을 통하여 흡수된다. 칼슘 배설은 주로 소변을 통해 이루어진다(Flik et al., 1993). 해산어류는 상당한 양의 칼슘(약 10 mmol 1-1)이 용해되어 있는 해수를 마시기 때문에 고농도의 뇨를 배출하여 수분이 유출되는 것을 방지하고 동시에 현저한 칼슘을 축적하므로, 장 상피세포의 칼슘 투과유량이 담수어류에 비해 낮은 편이다(Flik et al., 1996). 반면 담수어류는 주변 이온농도 보다 체내 삼투압이 높아 몸 안으 로 물이 계속 유입되기 때문에 이것에 대응하기 위해 묽은 뇨를 생산하며, 칼슘 손실은 칼슘의 재흡수 활동을 통해 최소화시킨다(Hickman, 1968; Schmidet-nielsen et al., 1975; Renfro et al., 1982).
어류는 번식시기에 달하면 평소보다 더 많은 칼슘을 필요로 하며, 무지개송어(
어류는 일반적으로 사육수로부터의 칼슘 흡수에 의존하는 것으로 알려져 있으나, 사료를 통해 칼슘을 추가적으로 공급했을때 아메리칸 시클리드(
어체 내의 칼슘흡수율과 체내활성을 살펴보기 위한 실험은 2012년 6월부터 7월까지 약 1개월간 진도의 양식장에서 사육중인 넙치(
칼슘섭이군과 대조군의 사육수조는 각각 3개의 수조로 구분하여 사육하였으며, 칼슘섭이군에는 사료에 1,500 mg/ton의 농도가 되도록 CaO를 첨가하여 실험을 실시하였다.
CaO의 제작은 패각류를 고온(1,500-5,000℃)에서 극도로 높은 전압으로 고온소성 통전하는 방법으로 제작된 제주에코바이오텍의 제품을 사용하였으며, 사료에 첨가된 CaO의 농도는 미성숙시기의 넙치를 이용한 예비 실험을 통하여 CaO를 공급시 넙치의 혈중 칼슘 농도가 50% 전후 상승하는 농도를 기준으로 설정하였다. 실험어는 성숙기의 평균 전장 34.1±1.3 cm 및 평균 체중 410.5±50 g의 넙치 성어와 평균 전장 18.83±0.29 cm 및 평균 체중 70±10 g의 넙치 치어를 각각 사용하였다.
한편, 넙치의 면역력에 미치는 CaO의 영향을 조사하기 위해 제주도내의 양식넙치 치어를 대상으로 사료 내 CaO가 2,000 mg/ton 이 되도록 첨가하여 1개월간 사육한 후 병원균의 공격실험을 3반복 실시하였다. 사육기간 동안의 수온은 24.68±1.3℃였고, 실험어의 평균 전장은 19.6±1.7 cm 및 평균 체중 69±17g이었으며 각 수조당 20마리씩 수용하여 대조군, PBS (phosphate buffered saline) 투여군,
혈액분석을 실시하기 위하여 실험넙치를 0.01%의 2-Phenoxy-Ethanol로 마취한 뒤, 항응고제 처리를 하지 않은 3 mL 주사기를 사용하여 미부 정맥에서 혈액을 채혈하였다. 채취된 혈액은 상온에서 2시간 보관 후에, 원심분리기를 이용하여 12,000 rpm에서 10분간 혈청을 분리하였다. 이후 분리된 혈청을 사용하여 aspartate amino transferase (AST), alanine amino transferase (ALT) 및 혈액 내 칼슘 양을 측정하였다. 칼슘분석은 자동 분석기용 Ca2+ 측정용 시약(아산제약)을 사용하였으며, AST 와 ALT는 stanbio laboratory 에서 제조된 키트를 사용하였다. 모든 혈액성상분석은 혈액 자동 분석기(CH 100 PLUS)로 측정하였다.
넙치에서 분리한 혈청, 아가미 점액 및 체표 점액을 각각 15μL씩 96 well plate에 분주한 후 150 μL
간의 단백질 함량은 Lowry et al. (1951)의 방법에 따라 bovine serum albumin (BSA)을 사용하여 750 nm에서 흡광도를 측정하였다.
혈중 단백질 함량은 stanbio laboratory에서 제조된 키트를 사용하여 혈액 자동 분석기(CH 100 PLUS)로 측정하였다.
CaO 급이 후의 성숙시기와 성장시기 넙치의 비늘의 외형 상태를 파악하기 위하여 Zu (2004)의 실험 방법을 이용하여 채취 및 염색을 실시하였다. 채취는 핀셋으로 비늘이 상하지 않게 비늘 안쪽을 잡아 채취하였으며, 비늘 염색은 조직 염색 시에 사용되는 eosin에 약 5초간 담가두어 색을 침적시키고, 95% ethanol에서 잔여물을 제거한 뒤 슬라이드에 염색된 비늘을 올려놓고, 광학현미경을 사용하여 관찰하였다.
간의 외형 평가는 Tanaka et al. (2013)의 연구에서 사용된 간의 출혈 정도를 육안으로 판단하는 실험방법에 따라 대조군과 칼슘섭이군 넙치의 간 외관 컨디션을 비교하기 위하여 해부를 통해 육안으로 간의 상태를 확인하였다.
조직 관찰은 어체로부터 간을 절개하여, bouin’s solution에 24시간 고정한 후 수세와 탈수과정을 거쳐 파라핀에 포매 후, 박절기로 5 μm 절편을 제작하여 hematoxylin-Eosin (H&E) 염색하였다.
CaO 공급이 넙치의 면역력에 미치는 영향을 조사하기 위하여 병원균을 이용한 공격실험을 실시하였다. 실험은 일반사료만 급이한 대조군과 CaO 2,000 mg/ton의 농도로 첨가한 사료를 한달 간 급이한 칼슘섭이군 넙치를 사용하였으며, 각 그룹당 20마리로 나누어 3반복 실험을 실시하였다.
공격실험은 PBS (phosphate buffered saline)와 병원균
SPSS (Ver.21) 통계분석 프로그램을 활용하여 t-test로 분석하였으며, P<0.05에서 유의성을 판단하였다.
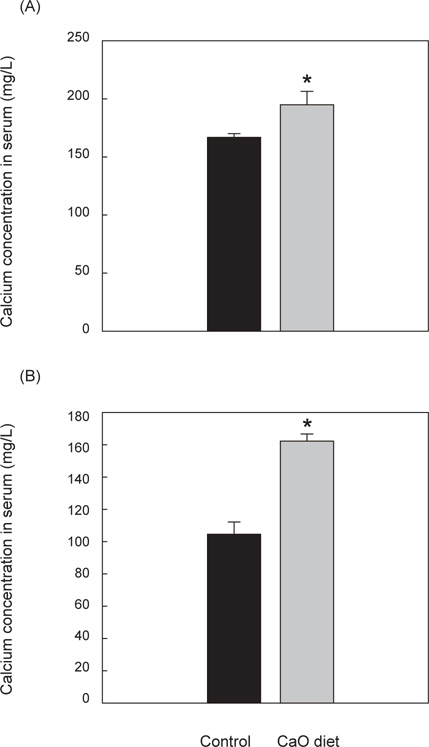
성숙기와 미성숙기 넙치의 혈액 내 칼슘 분석 결과, 성숙기 대조군의 혈중 칼슘량은 165.9±5 mg/L, 성숙기 칼슘섭이군의 혈중칼슘량은 195.27±9 mg/L 으로 대조군에 비하여 칼슘섭이군의 혈중 칼슘량이 유의적으로 높게 나타났다(P<0.05) (Fig. 1A). 미성숙기 대조군의 혈중 칼슘량은 105±7 mg/L이며 미성숙기 칼슘섭이군의 혈중 칼슘량은 162.73±4 mg/L으로 칼슘섭이군의 혈중칼슘량이 유의적으로 높았다(P<0.05)(Fig. 1B).
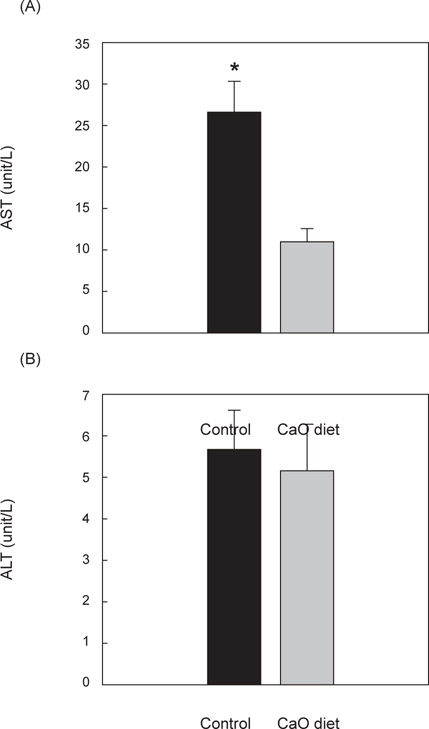
ALT/AST 측정은 성숙기 성어만을 대상으로 측정하였다. AST 측정결과 대조군 26.38±4 U/L, 칼슘섭이군 10.88±2 U/L으로 대조군보다 칼슘섭이군에서 유의적으로 낮게 나타났으며(P<0.05), ALT 측정결과 역시 대조군 5.63±1 U/L, 칼슘섭이군 5.13±1 U/L로 대조군보다 칼슘섭이군에서 더 낮게 나타났으나 유의적인 차이는 나타나지 않았다(Fig. 2).
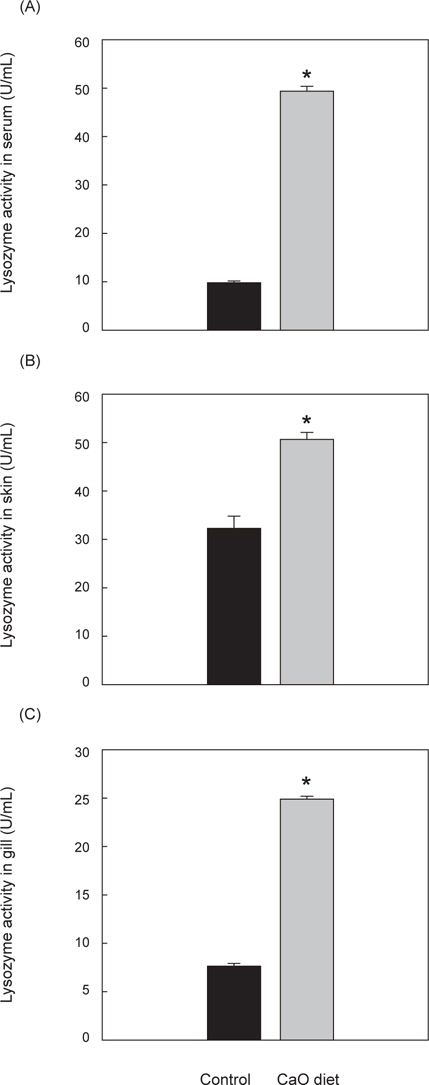
비특이적 면역활성 중 하나인 lysozyme 활성 측정 결과 혈청에서의 lysozyme 활성은 대조군 10±0.1 U/mL, 칼슘섭이군 50±0.5 U/mL로 칼슘섭이군이 유의적으로 더 높은 활성을 나타냈으며(P<0.05), 체표점액 lysozyme 활성 역시 대조군 32.5±2.5 U/mL, 칼슘섭이군 83±2.5 U/mL로 유의적으로 더 높게 나타났다(P<0.05). 또한 아가미 점액에서의 lysozyme 활성이 대조군 7.5±0.3 U/mL, 칼슘섭이군 25±0.2 U/mL 로 칼슘섭이군이 유의적으로 높은 활성을 가졌다(P<0.05)(Fig. 3).
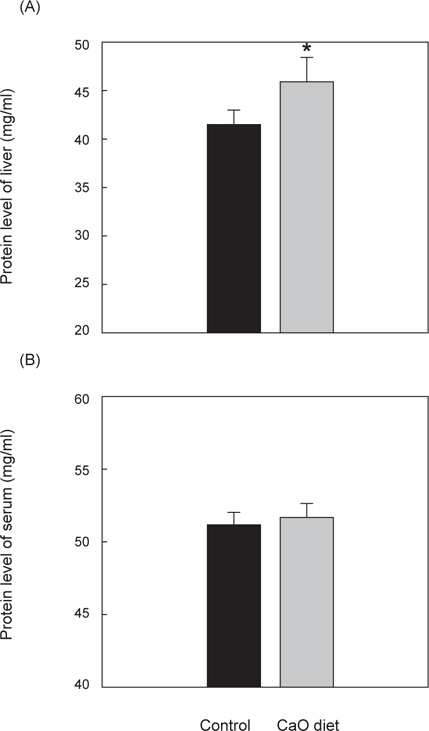
간 내의 단백질 대조군의 단백질 함량은 41.6±1 mg/mL, 칼슘섭이군의 단백질 함량은 45.9±3 mg/mL이었으며 칼슘섭이구의 간 단백질 함량이 유의적으로 높은 것을 확인할 수 있었다(P<0.05).
혈액 내의 대조군의 단백질 함량은 51.3±1 mg/mL, 칼슘섭이군의 단백질 함량은 51.8±1 mg/mL로 대조군과 칼슘섭이군에서의 유의적인 차이는 발견할 수 없었다(Fig. 4).
미성숙기의 대조군과 칼슘섭이군 넙치의 비늘을 채취하여 염색한 결과 대조군의 비늘 끝은 요철모양으로 비늘 사이의 틈이 갈라져 있는 형태였으나(Fig. 5A), 칼슘섭이군의 비늘은 갈라짐 없는 일정한 형태를 나타내었다(Fig. 5C). 이후 성숙기의 대조군과 칼슘섭이군 넙치의 비늘 염색 결과 또한 대조군의 비늘끝이 심하게 불균형 한 것에 비해(Fig. 5B) 칼슘섭이군의 비늘 끝은 일정한 형태를 나타내었다(Fig. 5D).
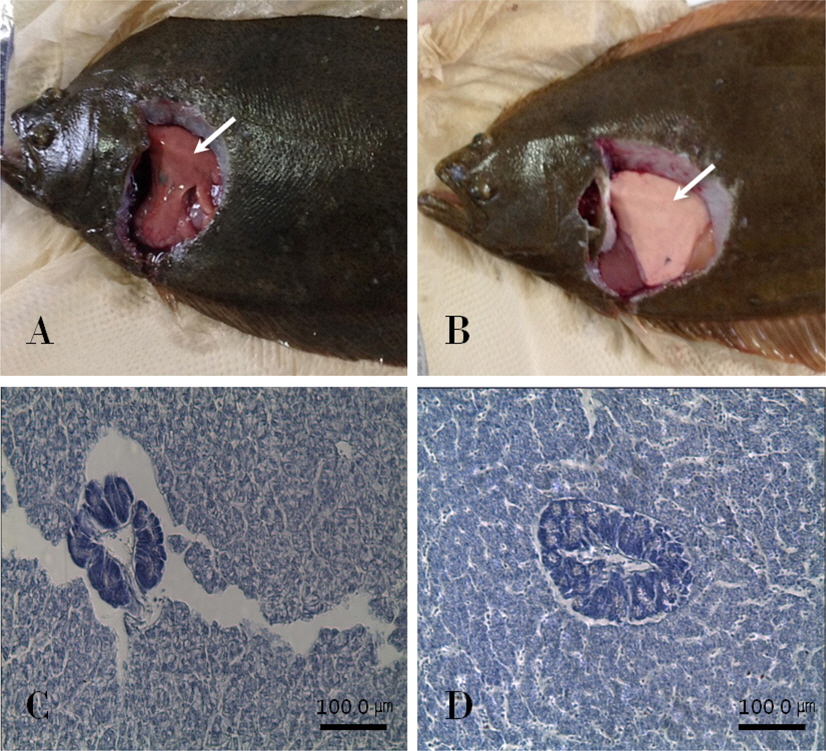
대조군과 칼슘섭이군 넙치의 간을 해부하여 육안으로 확인해 본 결과 대조군(Fig. 6A)의 간은 출혈이 일어나서 붉게 된 반면에 칼슘섭이군에서는 출혈이 관찰되지 않았다(Fig. 6B).
또한 조직학적 방법으로 간 조직을 확인해본 결과 칼슘섭이군의 간세포간의 조밀도가 대조군에 비해 조밀한 것을 확인할 수 있었다(Fig. 6C, 6D).
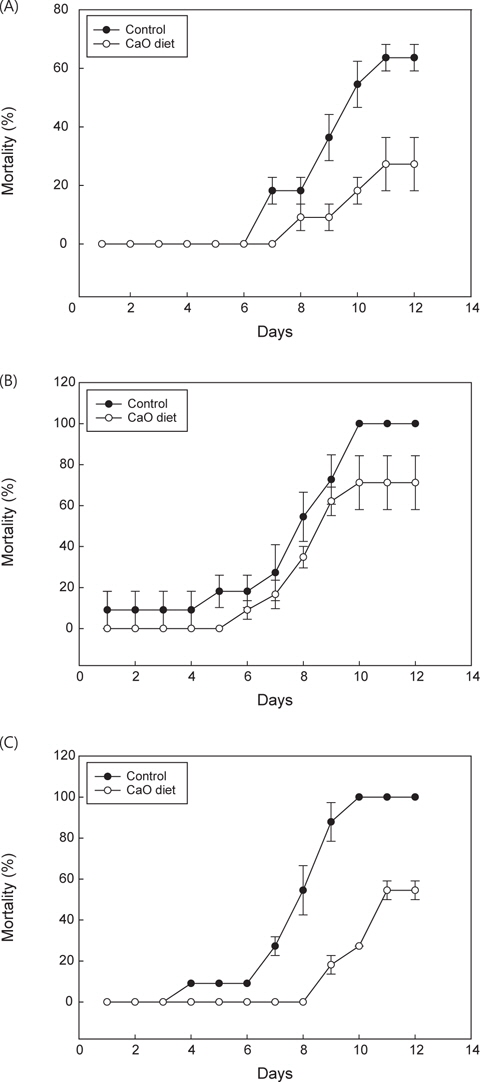
PBS군의 환경변화 및 절식에 따른 폐사율을 관찰한 결과 칼슘섭이군이 대조군에 비해 폐사율이 적은것으로 나타났다(Fig. 7A).
칼슘은 어류의 면역력과 성장에 중요한 역할을 하는 물질로서 사람과 어류뿐만 아니라 식물 등 다방면에서 중요성이 대두되고 있다. 어류양식에서도 칼슘을 이용한 실험은 연구되고 있으나 산화칼슘인 oxide calcium (CaO)을 이용한 연구는 거의 진행되지 않았다.
어류의 혈액은 생리상태의 변화를 파악할 수 있는 요인이며, 성숙 시기에는 혈중 칼슘 요구량이 급격히 증가하는 것으로 알려져 있다(Yeo and Mugiya, 1998; Chen et al., 2004). 본 연구에서 CaO 공급이 넙치의 혈액 내 칼슘 흡수량에 미치는 영향을 확인하기 위하여 미성숙기와 성숙기 넙치의 혈중 칼슘 농도를 측정한 결과 대조군에 비하여 칼슘섭이군의 혈중 칼슘량이 유의적으로 높았음을 확인할 수 있었으며(P<0.05), 앞에서 언급 되었던 Hossain and Furuichi (2009)의 연구결과와 유사한 결과를 나타내고 있다. 이것은 넙치와 같이 해수 내에서 칼슘을 충분히 흡수하지 못하는 어종의 경우 사료 내 칼슘첨가가 어류 체내의 칼슘을 보충해 줄 수 있다는 것을 시사한다. 또한 이전의 넙치 사료 내 칼슘 첨가 시에 사용되는 tricalcium phosphate(TCP)는 흡수율이 높지 않은 것으로 나타났으나(Hossain and Furuichi, 2000), CaO의 경우 대조군에 비하여 칼슘섭이군의 체내 칼슘농도가 증가된 것으로 보아 CaO가 이온화된 형태로 존재하여 어류의 장내 칼슘흡수에 용이하게 작용한 것으로 여겨진다.
AST와 ALT는 간을 비롯한 체내의 장기에 존재하는 아미노산 합성 효소로서, 간과 특정 장기가 손상을 입을 시에 수치가 상승하는 것으로 알려져 있으며, 간 기능 검사시에 주로 사용되고 있다. 어체의 생리상태가 좋지 않을수록 간의 장애(Gordon, 1968)가 일어나고 활성이 높아져 혈중 농도가 증가하는 것이 보고 되었다(Casilas and Ames, 1985; Rao et al., 1990). 본 연구에서의 대조군과 칼슘섭이군의 AST 측정 결과 대조군보다 칼슘섭이군에서 유의적으로 낮게 나타났으며(P<0.05), ALT는 두 실험구간 유의적인 차이는 없었지만 칼슘섭이군이 낮아지는 결과를 나타내어 칼슘 섭이가 AST, ALT를 감소시켜 간 기능 개선에 효과가 있는 것으로 여겨진다.
비특이적 면역활성 중 하나인 lysozyme은 자연계에 넓게 분포하는 효소로서, peptidoglycan이 주성분인 세균의 세포벽 성분을 분해하는 작용을 가지고 있으며, 이외에도 보체의 옵소닌화, 항바이러스, 항암작용 등에도 관여를 하는 것으로 보고 되었다(Jolles and Jolles, 1984). Lysozyme은 어류의 점액, 림프조직, 혈장 및 기타 체액에 존재하는데(Hikima, 2001), 어류의 피부 표면과 아가미에 주로 존재하는 점액 lysozyme은 세균 침입에 대한 초기방어역할을 수행한다고 알려져 있으며, 성별, 수온, pH, 독성물질 노출, 감염 및 스트레스 정도에 따라 lysozyme 활성이 다양하게 나타난다(Saurabh and Sahoo, 2008).
동물에서 lysozyme은 c-type (chicken or conventional type), g-type (goose-type) 그리고 i-type (invertebrate type)으로 세종류의 lysozyme이 존재하며, 그 중 어류에는 c-type과 g-type의 lysozyme이 존재한다(Hikima, 2000). 이 c-type과 g-type lysozyme은 그람 양성균 및 음성균에 항균효과가 있는 것으로 알려졌으며(Itami et al., 1992; Yousif et al., 1994; Hikima et al., 2001; Minagawa et al., 2001; Zheng et al., 2007), 특히 c-type lysozyme은 calcium-binding lysozyme으로 불리며 칼슘과 결합하는 특징이 있다(Saurabh and Sahoo, 2008). 따라서 칼슘이 선천면역인 lysozyme 활성에 있어 중요한 역할을 하는 것으로 판단되어 본 실험에서 lysozyme 활성 측정을 통한 면역력을 평가하였다. 넙치의 혈청, 아가미 점액, 체표 점액의 lysozyme 측정 결과 모두 대조군에 비해 칼슘섭이군의 lysozyme 활성이 유의하게 증가했음을 확인할 수 있었다. 이는 CaO가 lysozyme을 비롯한 면역 기능 활성을 증가시켰기 때문으로 여겨지며 따라서 CaO의 급이가 넙치의 체내면역을 증가시키는 효과가 있는 것으로 판단된다.
간 외형 평가는 일반적으로 포유동물과 사람의 컨디션을 확인 하기 위하여 이루어지며, 대상이 간 주변에 외상을 당하거나 질병성 또는 스트레스성 징후를 보였을 때 간 출혈이 일어나는 것으로 알려져 있다(Tanaka et al., 2013). 본 실험의 결과, 칼슘섭이군의 간 출혈이 대조구에 비해 거의 일어나지 않았으며, 간 조직 또한 조밀한 형태를 가지는 것으로 확인되었다. 어류가 CaO를 충분히 흡수 하였을 경우 외부스트레스에 대한 저항성을 강화시켜 스트레스성 간 출혈을 저하시켰기 때문으로 사료되며, 간 조밀도가 대조군에 비해 높게 나온 것은 면역력이 증가함에 따라 외부자극에 대한 저항성이 강해졌기 때문으로 판단된다. 간이 손상을 입을 시에 수치가 상승하는 것으로 알려진 AST와 ALT 결과 또한 본 실험에서 대조군에 비해 칼슘섭이군에서 활성이 낮게 나타나 CaO가 외부스트레스 저항성을 높여주는 것으로 판단된다.
또한 CaO의 첨가에 따른 넙치의 면역활성기능을 조사하기 위하여 어류 병원성 세균인
경골어류의 칼슘은 약 95%가 뼈와 비늘에 포함되어 있으며(Flik et al., 1986), 이 부위들은 성 성숙기와 초기성장시기와 같이 칼슘 수요가 높아지는 기간에 대체적으로 칼슘을 공급해주는 저장소의 역할로 작용한다. 특히 어류의 산란기에는 칼슘수요가 급격히 증가되기 때문에 외부 또는 뼈와 비늘에서 부족한 칼슘을 보충하게 되는데 금붕어, 송사리(Mugiya and Watabe, 1977) 및 무지개 송어(Carragher and Sumpter, 1991; Persson et al., 1994; 1995; 1997)의 연구에 따르면 이와 같은 시기의 초기 칼슘 동원은 주로 뼈보다 비늘에서 이루어지는 것으로 다수 보고 되어있다. 이처럼 산란기와 초기성장기에 많은 양의 칼슘이 비늘에서 동원되게 되므로 이 시기에는 어류에서 비늘에서의 칼슘 재흡수가 높아져 비늘의 연륜이 옅어지고 두께도 얇아지는 현상을 보여 체표에서의 면역력이 약화될 가능성이 높아진다.
Mugiya and Watabe (1977)는 칼슘 요구량이 높아지는 시기에 넙치의 비늘에서 칼슘 방출이 이루어져 체내로 칼슘이 동원되는 것으로 보고하고 있으며, 본 실험 결과에서도 양식넙치의 사육 중 비늘로부터 칼슘의 재흡수가 이루어지는 것으로 나타났다. 이에 본 실험에서와 같이 CaO의 섭취를 인위적으로 유도할 경우 장관으로부터 충분한 칼슘이 넙치의 체내로 흡수 되어 비늘에서의 칼슘 재흡수가 이루어지지 않고 비늘의 모습이 일정한 형태를 유지하는 것으로 판단된다.
상기의 결과를 미루어보아 산란기나 초기성장기 같이 많은 양의 칼슘을 필요로 하는 시기에 CaO 형태의 칼슘을 사료나 사육수의 형태로 공급 및 적용한다면 어류가 필요로 하는 정도의 칼슘을 충분히 보충할 수 있고 이로 인해 면역력을 적절하게 유지 또는 상승시켜줌으로써 외부 스트레스나 병원균 저항성을 높여줄 수 있을 것으로 사료된다.