This study determined the level of fermented soybean meal (FSM) that could be substituted for fish meal in the diet for parrot fish
오늘날 양어사료는 어류 생산 경비의 50-70%를 차지하고 있기 때문에 양식산업의 생산성 및 경제성 향상에 중요한 열쇠가 되고 있다(Bai, 1996). 양어사료의 단백질원으로는 어분, 혈분, 우모분, 육분, 육골분, 피혁분 등의 동물성 단백질원과 대두박, 콘글루텐, 면실박, 채종박 등의 식물성 단백질원이 이용된다(NRC, 1993). 지금까지 해산어용 배합사료의 단백질원으로는 어분을 주로 사용하고 있으며, 양식의 발달과 함께 그 수요도 증가하고 있으나, 어분 생산량은 점차 감소함에 따라, 가격이 급격히 상승하고 물량도 부족한 추세이다(McCoy, 1990; Rodriguez-Serna et al., 1996). 이러한 문제를 해결하기 위하여 어분 대체품의 개발이나 어분 대체원으로서 동물성 및 식물성 단백질원들의 효과에 대한 연구가 어종별로 활발히 수행되고 있다(Shimeno et al., 1993; Lee et al., 1996; Bai et al., 1997; Choi et al., 2004; Lim et al., 2004; Yoo et al., 2006). 어종에 따라 차이는 있지만, 양어사료에 사용되는 어분의 30-50%를 식물성 단백질로 대체가 가능하다고 알려져 있다(Francis et al., 2001). 그리고 많은 연구자들에 의해 어분의 대체 단백질원으로써 대두박이 가장 적합한 단백질원으로 보고되고 있다(Olli and Krogdahl, 1995; Boonyaratpalin et al., 1998; Arndt et al., 1999; Choi et al., 2004; Lim et al., 2004). 대두박은 높은 단백질가, 일정한 구성성분, 낮은 가격과 공급의 안정성에서는 적정한 단백질원이다. 하지만 어분에 비해 필수아미노산인 methionine 함량이 낮고, 소화가 잘되지 않는 탄수화물이 약 30%를 차지하고 있으며, phytic acid가 많이 포함되어 있어 필수미네랄 이용성의 저하 및 단백질 흡수 저하와 같은 비영양적 작용을 하는 것으로 보고되고 있다(Olli et al., 1994; Storebakken et al., 2000). 또한 대두박은 필수지방산인 omega-3 계열의 고도불포화지방산(highly unsaturated fatty acid, n-3 HUFA)을 전혀 함유하고 있지 않기 때문에 추가로 공급이 되어져야만 하는 문제점을 가지고 있다. 사료 중의 지질은 필수지방산의 공급원으로뿐만 아니라 에너지원으로서도 중요한 영양소이다. 일반적으로 해산어류의 필수지방산은 n-3 HUFA이고, 어류의 정상적인 성장을 위해서는 그 어종이 요구하는 종류와 양이 사료에 첨가되어야 한다(Castell et al., 1972; Watanabe et al., 1974; Kanazawa et al., 1982; Takeuchi et al., 1983; Lee et al., 1993a, b, c, d). n-3 HUFA가 다량 함유된 어분, 어유, 간유 등은 저장중이나 사료 제조 후 산화되기 쉬우므로 어류의 건강에 나쁜 영향을 줄 수도 있다. 또한 어유나 간유는 다른 동물성 및 식물성 지질보다 가격이 비싸므로 n-3 HUFA를 함유하는 대체유를 개발하는 것 또한 시급한 문제로 대두되고 있다.
이러한 점을 착안하여 이번 연구에서는 육상양식장 고형오물을 해삼사료자원화를 위한 발효과정중의 해양미생물을 이용하여 탈지대두박을 발효시켜 양어사료의 어분대체원으로서 사용하였을때 발효대두박의 단백질, 아미노산 그리고 지방산 조성을 살펴보고, 또한 기초사육실험을 통해 대체 가능성을 알아보고자 하였다.
발효 균주 및 재료
사료제조용 원료인 탈지대두박에 당밀(brix 45%) 5%를 첨가하여 DHA를 다량 함유하는
발효대두박 일반 성분 분석
실험에 사용된 발효대두박 일반성분 분석에서 수분은 상압가열 건조법, 조단백질은 Kjeldahl법(AOAC, 1995), 조지방은 choloroform과 methanol을 2:1 비율로 혼합한 용액을 용매로 한 Bligh and Dyer 추출법(1959), 조섬유는 Automatic analyzer(Fibertec, Tecator)를 이용하였고, 조회분은 직접 회화법으로 분석하였으며(AOAC, 1995), 가용성 무질소물은 100에서 위 성분의 합계를 뺀 값으로 계산하였다(AOAC, 1995).
발효대두박 아미노산 분석
총 아미노산의 분석을 위한 시료는 고형물의 경우 시료 2.0 g에 6 N HCl 5 mL를 넣고, 액상의 경우는 시료 5 mL에 HCl 5 mL 넣어, 밀봉한 다음 heating block (HF-21, Yamato Scientific Co., Ltd. Japan)에서 가수분해 (110℃, 24시간) 한 후, glass filter로 여과, 감압 농축 및 sodium citrate buffer (pH 2.2)로 정용하여 제조하였다. 아미노산의 분석은 전처리 시료의 일정량을 아미노산 자동분석계(Pharmacia Bioteck Biochrom 30, England)로 실시하였다.
발효대두박 지방산 분석
총 지질 추출은 Bligh and Dyer (1959) 방법에 준하였다. 즉, 시료를 비커에 취하여 homogenizer (Nihonseiki Kaisha Ltd. Japan)에 15,000 rpm으로 5분간 잘게 부순 다음, chloroform과 methanol을 2:1로 혼합한 용액을 이용하여 총 지질을 추출하였다. 추출된 시료를 일정량 취하고, 0.5 N NaOH-methanol 용액을 이용하여 검화하였으며 BF3-methanol을 사용하여 methyl화 하였다. 그런 다음, Iso-octane을 이용하여 추출된 시료를 지방산 methyl ester 시료로 사용하였다. 지방산 분석에 사용하는 Cas Chromatography는 OmegawaxTM-320 (bonded polyglycol phase) capillary column (30 m×0.32 mm×0.25 μm, I.D., SUPELCO, Supelco Park, PA, USA)를 장착한 Glarus 600 (Perkin Elmer, USA)를 이용하였다.
실험 사료
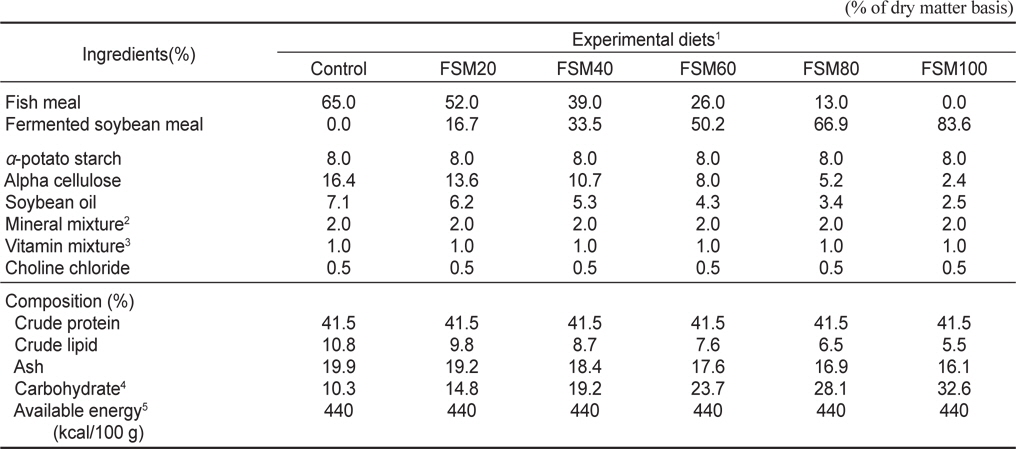
실험 사료의 조성표는 Table 1에 나타낸 바와 같이 단백질원으로 어분(fish meal)만을 사용한 구를 대조구로 하고, 대체 단백질원으로 발효대두박을 이용하여 어분의 20, 40, 60, 80 그리고 100%를 대체하는 사료를 제작하여 실험을 하였다. 모든 실험구의 사료는 단백질 함량 41.5%로 제조하였으며, 지질원으로는 Soybean oil을 사용하여 가용에너지가 440 kcal/100 g이 되도록 조절하였다. 이 때 가용에너지는 사료의 단백질, 지질 및 가용성 무질소물을 각각 4.5, 9.0 및 3.0 kcal/g으로 계산하였다(Lee and Lee, 1996).
[Table 1.] Ingredients composition of the experimental diets
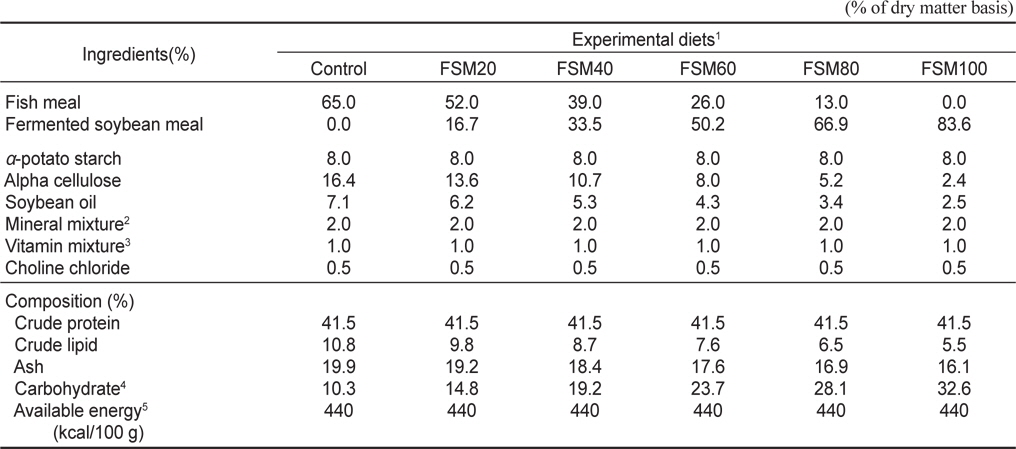
Ingredients composition of the experimental diets
실험어 및 사육관리
실험어는 국립경상대학교 해양과학대학 해양생물 사료공학 연구실에서 사육중인 돌돔을 사용하였다. 실험 시작 전 1주일 동안 실험수조에서 예비 사육을 실시한 후, 실험 시작 시 평균 체중 4.0 g 되는 돌돔 치어를 80 L 수조에 각각 3반복으로 25마리씩 수용하여 8주간 사육실험을 하였다. 사료 공급은 1일 3회 공급하였다. 성장은 2주마다 측정하였으며 측정하기 전 24시간 동안 절식시킨 후, Aquis-10 (100 ppm)으로 마취시켜 전어체 무게를 측정하여 증중율(Weight gain, %), 사료효율(Feed efficiency, %), 일일사료급이율(Daily feed intake, %), 성장률(Specific growth rate, %/day), 그리고 생존율(Survival rate, %)을 조사하였다.
사육장치
실험에 사용한 사육 장치는 유수식을 겸한 순환여과식 사육장치로서 순환수의 첨가에 의해서 배설물이 즉시 사육 수조 밖으로 배출될 수 있도록 사이펀 장치를 부착하였으며, 사육수조의 크기는 60×45×30 cm 의 사각아크릴 수조에 수량은 80 L, 주수량의 보충에 의한 순환률은 20 회전/일 시켰다. 이 때 주수량은 3.0 L/min 였다. 사육 기간 중 전 사육수조에는 에어스톤을 설치하여 용존산소량은 5 mL/L를 유지하였으며, 사육수온은 24.3±0.8℃였으며, 염분농도는 33±0.5 psu 를 유지하였다.
모든 자료는 분산분석(one-way ANOVA)을 실시하여 Duncan's multiple range test (Duncan, 1955)로 평균 간의 유의성(
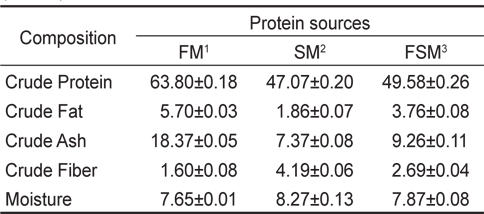
해양미생물을 이용하여 발효과정을 거친 발효대두박의 일반 성분 분석 결과는 Table 2에서 나타낸 바와 같이 조단백질은 47.07%에서 49.58%로, 조지방은 1.86%에서 3.76%로 증가되었으며, 조회분은 7.37%에서 9.26%로 증가되었다. 조섬유의 경우는 발효과정을 통해 4.19%에서 2.69%로 낮아졌다. 대두박은 다른 식물성 박류에 비하여 단백질과 에너지 수준은 높고, 조섬유와 조회분 함량은 낮아서 특히, 단위동물 사료원료로서 적합하다. 대두단백질은 식물성 단백질 공급원 가운데 아미노산 조성이 가장 우수한 것 중 하나에 속한다. 일반적으로 대두유 가공시 부산물인 탈지대두박은 원료 대두에서 지방을 제거하고, 단백질 약 50%, 탄수화물 25-30%로 대부분의 영양소가 소실되지 않아, 식품 및 영양학적 관점에서 중요한 소재로서 사용되어지고 있다.
[Table 2.] Chemical composition of the dietary protein sources (unit: %)
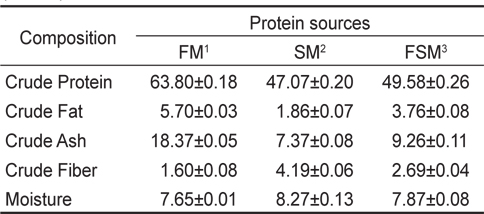
Chemical composition of the dietary protein sources (unit: %)
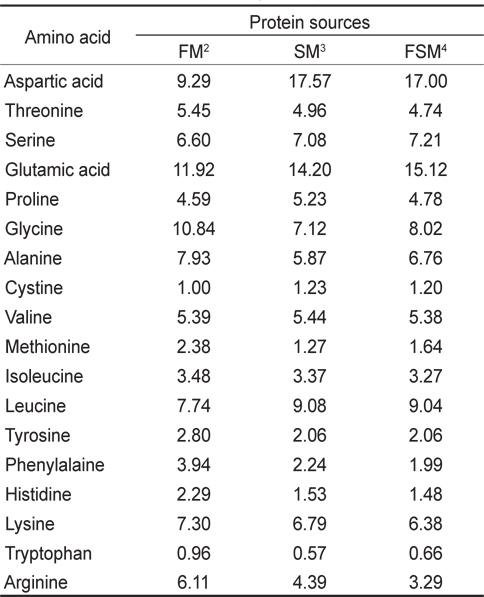
탈지대두박과 발효대두박의 아미노산 분석결과는 Table 3에 나타낸와 같이 발효과정을 통해 발효된 대두박의 lysine함량은 6.79%에서 6.38%로 낮아졌으며, methionine 함량은 1.27%에서 1.64%로 높아지는 것으로 나타났다. Tryptophan은 0.57%에서 0.66%로 높아지는 것으로 나타났으며, threonine은 4.96%에서 4.74%로 낮아지는 것으로 나타났다. Isoleucin 함량은 3.37%에서 3.27%로 나타났으며, valine은 5.44%에서 5.38%로 나타났다. 대두박은 다른 박류에 비하여 아미노산 함량이 높고, 아미노산 조성이 우수한 편이지만 비율면에서 필수아미노산 중 lysine 함량이 높은 반면, methionine과 cystine 함량이 낮은 편이다. 그러나 발효과정을 통해 필수아미노산인 methionine과 tryptophan등이 높아짐으로서 발효대두박의 단백질 가치가 대두박에 비해 높다는 것을 의미한다.
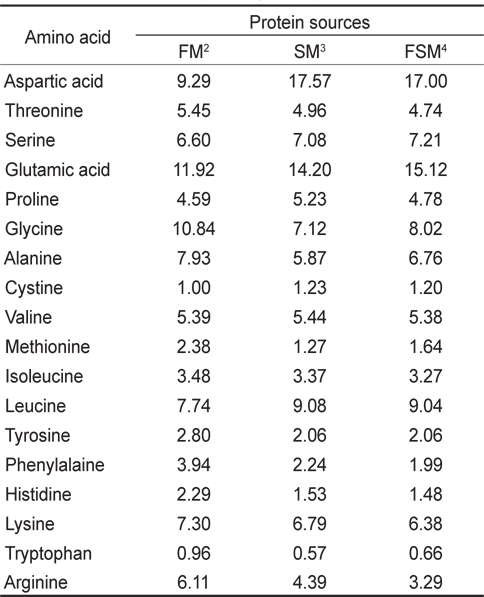
Total amino acid (TAA) composition (% in protein) of the dietary protein sources (% of dry matter)1
단백질은 양어사료 배합에 있어 사료가격뿐 아니라 어류의 성장에 가장 큰 영향을 미치는 영양소이다. 그러나 단백질 그 자체로서의 중요성보다는 필수아미노산의 공급측면이 더 중요한 것이기 때문에 단백질원의 선택시 필수아미노산의 균형이 잘 이루어져 있는가를 고려하여야 한다. 지난 40여 년간의 연구에도 불구하고 필수아미노산의 양적 요구량이 성장실험을 통하여 완전히 밝혀진 어종은 단지 9종에 불과하다. 그러나 이들 요구량 조차도 성장이 빠른 초기단계에 국한되어 있으며, 사료섭취량이 증가하는 육성 및 성어단계의 요구량은 여전히 경험적인 추정에 의거하여 사료배합에 임하고 있는 실정이다. 아미노산 요구량 설정시 많은 시간과 경비가 소요되기 때문에 상대적으로 간편한 체조직내 아미노산의 증가량에 의한 방법이나 이상적인 단백질 균형법에 의거하여 요구량을 설정하고 있지만, 이렇게 설정된 요구량을 관행의 사료배합에 응용하는데는 신중을 기할 필요가 있다. 양질의 어분 생산량은 수요에 미치지 못하고 있기 때문에, 어분 대체원을 이용한 사료 배합시 설정된 아미노산 요구량 수치의 이용에는 더욱 주의를 기울여야 할 것이다. 특히, 설정된 라이신 요구량과 체조직 Asimilation/Energy 비율을 고려한 요구량의 추정은 사료 내 아미노산 불균형의 문제를 야기할 수도 있기 때문에 신중을 기해야 할 것이다.
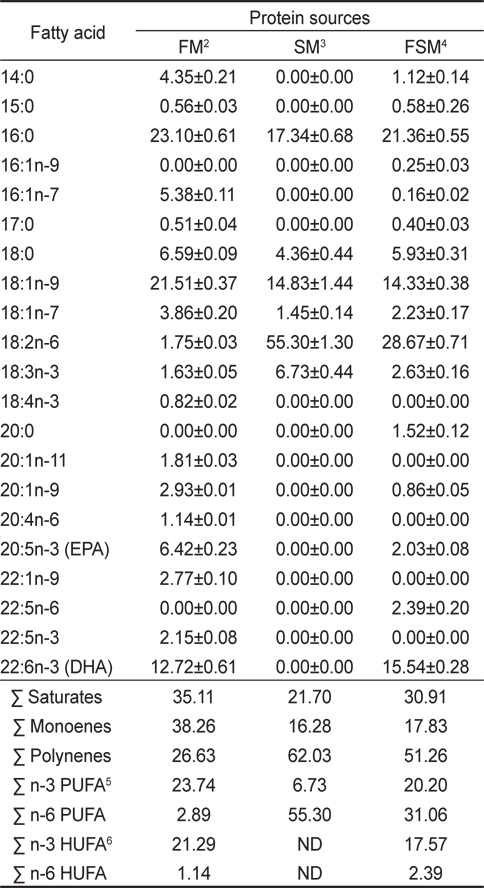
탈지대두박과 발효대두박의 지방산조성은 Table 4에서 나타낸바와 같이 탈지대두박은 특징적으로 많이 함유하고 있는 18:2n-6 지방산이 55.30%였고, 20:5n-3 (EPA)와 22:6n-3(DHA)가 전혀 없었지만, 발효과정을 통해 18:2n-6는 28.67%로 감소하였고, EPA와 DHA는 각각 2.03%와 15.54%로 증가되었다. n-3 PUFA는 6.73%에서 20.20%로 증가되었으며, n-6 PUFA는 55.30%에서 31.06%로 감소되었다. 또한 발효대두박을 어분과 비교하였을때 n-3 HUFA의 경우 비슷한 함량을 나타내었으며, 해산어류의 필수지방산인 DHA는 어분보다 더 높은 함량을 나타내었다. 육상 동물의 정상적인 성장을 위해 필수적으로 요구되는 지방산은 리놀레산(linoleic acid: 18:2n-6)인 반면 어류는 리놀레산(18:2n-6), 리놀렌산(18:3n-3), 아리키돈산(20:4n-6), EPA (20:5n-3) 및 DHA (22:6n-3)와 같은 다양한 종류의 필수지방산을 필요로 한다. 어분의 경우 EPA 6.42%와 DHA 12.72%을 포함하고 있지만, 대두박의 경우 전혀 포함하고 있지 않아 단순 대두박을 대체할 경우 필수지방산으로 인한 성장 저해요인이 될 수도 있다.
[Table 4.] Total Fatty acid composition of the dietary protein sources (% of total fatty acids)1
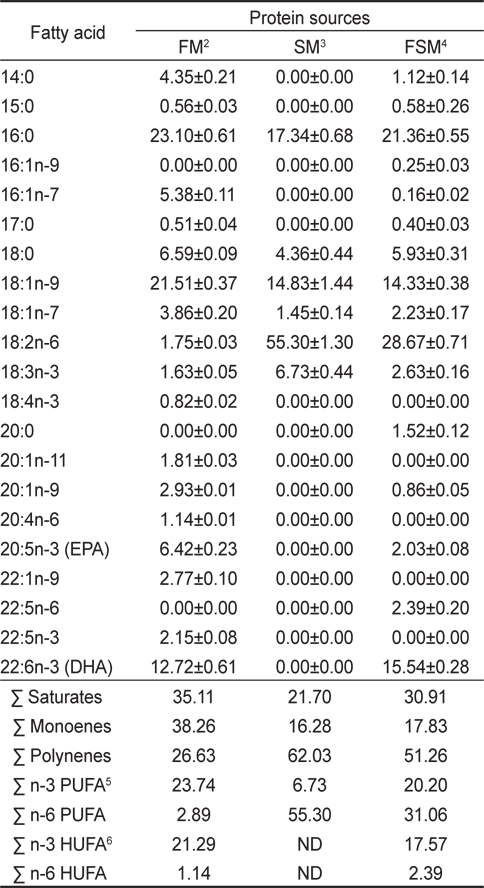
Total Fatty acid composition of the dietary protein sources (% of total fatty acids)1
어류에 있어 필수지방산은 성장과 생존현상 유지뿐 아니라 번식생리에도 상당한 영향을 미친다는 것은 널리 알려진 사실이다. 타 동물과 마찬가지로 어류 또한 그들의 체내 세포의 기능유지를 위해 필연적으로 어떤 지방산을 요구하게 되는데, 이러한 지방산은 체내에서 자체적으로 합성될 수 없어 사료로서 공급해 주지 않으면 정상적인 성장과 생존을 이룰 수 없게 된다. 육상가축에 있어 필수지방산은 n-3계열의 리놀렌산(18:3n-3)과 n-6계열의 리놀레산(18:2n-6) 및 아라키도닉산(20:4n-6)이나, 18:3n-3와 20:4n-6 두 지방산은 18:2n-6 지방산으로부터 육상가축의 체내 전변이 이루어질 수 있다는 것이 밝혀진 이래, 리놀레산(18:2n-6)만이 필수지방산으로 분류되고 있다. 그러나 먹이연쇄에서 유래한 진화과정의 결과로 어류는 그들 환경 내 염분의 유무에 따라 필수지방산의 질적 요구량이 달라진다. 또한 어류의 필수지방산은 어종에 따라 특이성을 나타내는데, n-3계열의 지방산 또는 n-6계열의 지방산만을 요구하는 어종이 있는 반면 이들 두 계열의 지방산을 동시에 요구하는 어종도 존재한다.
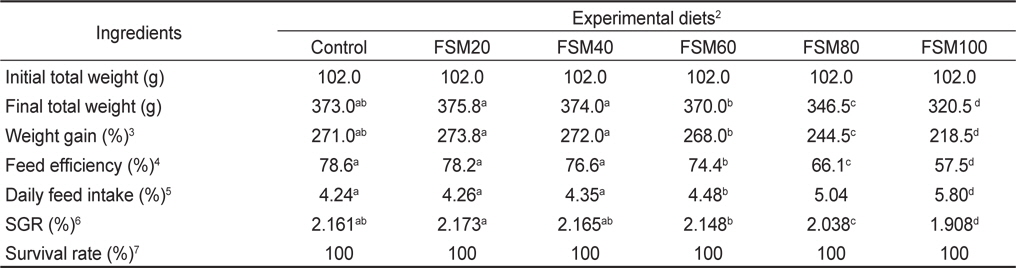
발효대두박 대체 비율에 따른 실험 결과는 Table 5에 나타낸 바와 같이 증체율은 FSM20구와 FSM40구에서 각각 273.8%와 272.0%로 대조구의 271.0%와 유의적인 차이는 없었으며(
[Table 5.] The results of parrot fish (Oplegnathus fasciatus) fed experimental diets for 8 weeks1
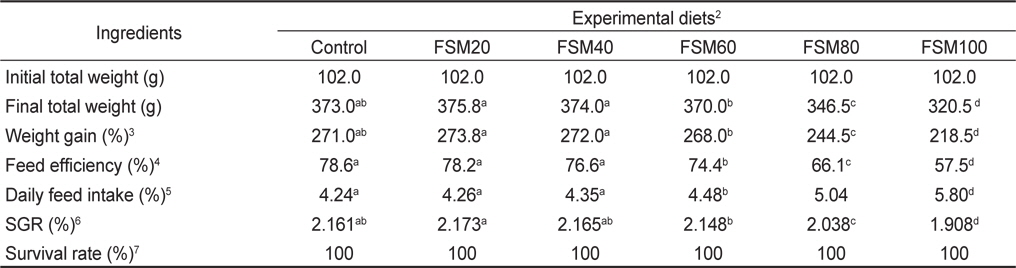
The results of parrot fish (Oplegnathus fasciatus) fed experimental diets for 8 weeks1