Phlorotannins, the major constituent in brown algae, possess various biological activities; however, there is little information their toxicological effects. To assess the safety of phlorotannins, we investigated the acute oral toxicity of a high-purity phlorotannin preparation (PRT; total phlorotannin content 90%) in beagle dogs. Six beagle dogs (3 males, 3 females) were assigned randomly to three experimental groups. PRT was administered at oral doses of 250, 500, and 750 mg/kg by capsule. Vomiting by male and female beagles was observed with 500 and 750 mg/kg on the first day. In addition, one beagle given 750 mg/kg had soft stool and diarrhea on days 3 and 13. No deaths or abnormal clinical signs were observed during the experiment. All groups showed similar body weight gain and food consumption. Our acute toxicity study showed that PRT did not cause any toxicological effects in beagle dogs.
갈조류는 오랫동안 아시아 지역 국가들에서 인간의 식량원으로 이용되어 왔으며, 기능성 식품 및 의약품의 원료로 사용되고있다(Smit, 2004; Le et al., 2009; Hwang et al., 2010). 갈조류에는 페놀(phenol)류, 카로티노이드(carotenoid)계 색소, 테르펜(terpene)류 및 다당류(polysaccharide) 등의 다양한 성분을 함유하고 있으며 특히, phlorotannin이라 지칭되는 페놀성 화합물은 갈조류의 대표적인 주요 생리활성 성분이다(Shibata et al., 2004; Wang et al., 2009).
Phlorotannin은 phloroglucinol을 기본 단위로 하는 중합체로 매우 광범위하며, 갈산(gallic acid)이나 플라본(flavone)을 포함하고 있는 육상 폴리페놀과는 구조적으로 다르다(Shibata et al., 2002; Shibata et al., 2004). 현재까지 다양한 갈조류에서 약 150가지의 phlorotannin 성분들이 분리되었는데(Isaza Martınez & Torres Castaneda, 2013) 일반적으로 dieckol, eckol, bieckol, eckstolonol 및 triphlorethol A 등의 성분들이 있으며, 이들 중 dieckol이 가장 큰 비중을 차지하고 있다(Cho et al., 2012a). 대체적으로 갈조류 중
최근에, 감태 생리활성의 주요 구성성분인 phlorotannin에 관한 연구보고에 따르면 항산화(Zou et al., 2008), 항염증(Kim et al., 2009), 항균(Nagayama et al., 2002), 항알레르기(Shim et al., 2009), 신경세포 보호작용(Yoon et al., 2008) 및 기억력 증진(Myung et al., 2005) 등의 다양한 효능이 보고되고 있으며, Cho et al. (2012a, 2012b)은 감태의 phlorotannin이 GABAA receptor agonist로 작용하여 수면증진 효과를 나타낸다는 연구를 보고하였다. 또한, Kim et al. (2014)은 합성흡착제를 이용한 고함량 phlorotannin 정제방법에 대한 연구를 보고하였으며, Cho et al. (2014)은 감태로부터 추출 및 정제한 고함량 phlorotannin 정제물이 기존 phlorotannin 보다 증가된 수면증진 효과를 나타낸다는 연구를 보고하였다.
반면에, 현재까지 phlorotannin의 생리활성에 대한 연구는 활발히 진행되고 있지만, 안전성에 대한 연구는 매우 미비한 실정이다. Phlorotannin을 식품원료나 의약품의 원료로 사용하기 위해서는 안전성에 대한 연구가 활발히 이뤄져야 하지만 아직까지 감태의 phlorotannin에 대한 안전성을 연구한 사례는 극히 드물며, 보고된 연구들은 설치류를 대상으로 자체적으로 연구하였거나 함량이 낮은 phlrotannin을 대상으로 안전성을 연구 하였다(Hwang et al., 2008).
따라서 본 연구에서는 갈조류인 감태로부터 추출 및 정제된 고함량 phlorotannin 정제물(high-purity phlorotannin preparation; PRT)을 기능성 식품원료로 사용하기 위한 안전성 평가를 위해서 비설치류를 이용한 일반 독성시험에 실험동물로 널리 사용되고 있는 비글견(beagle dog)을 대상으로 단회 경구투여 독성시험을 실시하였다.
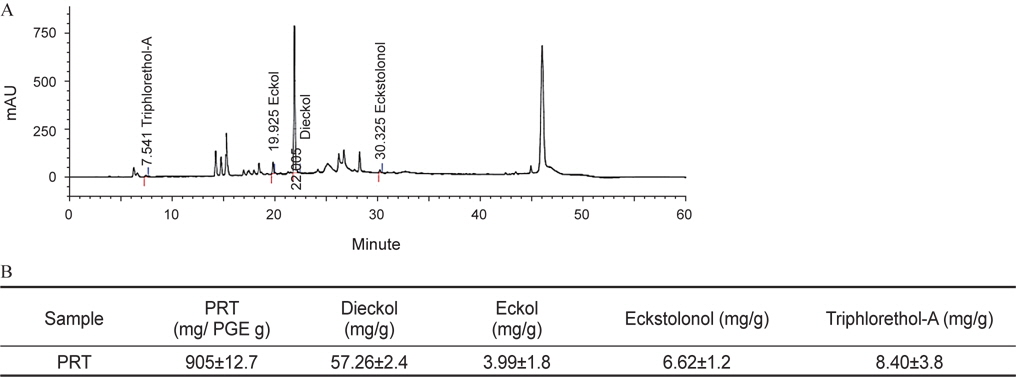
PRT (lot no. SD-GT-E-004)는 갈조류인 감태를 추출 및 정제한 것으로 ㈜에스앤디(Chenogwon-gun, Korea)에서 받아 실온에서 차광 및 방습하여 실험에 사용하였다. PRT의 총 phlorotannin 함량은 90% (905 mg phloroglucinol equivalents/g,w/w)이고 대표적인 지표성분은 dieckol (57.26 mg/g)이며, 그 외 활성성분으로는 eckol (3.99 mg/g), eckstolonol (6.62 mg/g), triphlorethol-A (8.40 mg/g) 등이 함유되어 있다(Fig. 1).
식품의약품안전처 고시 제 2013-40호 “비임상시험관리기준” 및 OECD Principles of Good Laboratory Practice (1997) ENV/MV/CHEM/(98)17에 따라 수행되었다. 식품의약품안전처 및 OECD에서는 비설치류를 이용한 반복투여 독성시험의 경우, 비글견의 수를 각각 암수 3마리 및 4마리씩 설정하라고 명시되어 있지만, 비설치류를 이용한 단회투여 독성시험의 경우에는 동물 수나 시험 방법에 대해 정확한 지침이 따로 없는 상황이다. 따라서 보통 국내에서 비글견을 이용한 단회투여 독성 시험을 수행할 때에는 한 용량으로 암수 2마리씩 진행하는 방법과 두 용량으로 암수 1마리씩 진행하는 DE (dose escalation)법을 사용하는데 본 연구에서는 DE법을 이용하여 독성시험을 수행하였다.
실험동물은 예방접종과 기생충을 구제하여 검역절차를 받은 생후 5개월 된 비글견 6마리(male 3마리; female 3마리)를 중앙 실험동물㈜ (Seoul, Korea)에서 구입하여 약 2주간 순화시킨 후 그 기간 중 일반증상을 관찰하여 체중감소가 없는 건강한 비글견 4마리(male 2마리; female 2마리)를 선발하여 실험에 사용하였다. 실험기간 중 사육환경조건은 온도 23±3℃, 상대습도 55±15%, 환기횟수 10-20회/h, 조명시간 12 h (lights on at 8:00) 및 조도 150-300 Lux의 조건하에 이루어졌으며, ㈜켐온 비임상연구소 제1동물사육구역 3호실에서 수행되었다. 시험자들은 모두 고압증기멸균(121℃, 20 min)된 멸균작업복과 보호장구를 착용하였다.
비글견은 스테인레스제망 사육상자(W 895×L 795×H 765 mm)에 넣어 순화기간 및 투여 관찰기간 동안 1마리씩 사육하였으며, 사육상자에는 시험번호 및 동물번호를 기입한 개체식별카드를 부착하여 식별하였다. 사료는 ㈜카길 에그리 퓨리나(Sungnam, Korea)에서 생산하는 실험동물용 개사료를 공급받아 1일 300 g씩 제한급여하였으며, 물은 지하수를 자외선 살균기 및 미세여과장치로 소독한 후 물병을 이용하여 자유섭취 하도록 하였다.
투여용량의 설정을 위한 예비실험으로 대조군 및 PRT를 500, 1,000 및 2,000 mg/kg의 농도로 비글견 암수 각 1마리에 투여한 결과, 사망동물과 체중변화의 이상은 관찰되지 않았다. 하지만, 1,000 mg/kg 투여군 수컷과, 2,000 mg/kg 투여군 암수 모두에서 시험물질 성상의 구토가 관찰되었다. 상기의 결과를 반영하여 1차 투여의 투여량을 250 및 500 mg/kg으로 설정하여 실험을 진행하였으며, 1차 투여 후 500 mg/kg 투여군 암수에서 시험물질 성상의 구토가 관찰되었다. 따라서 개체 차이에 의한 구토 여부를 판단하기 위하여 2차 투여의 투여량을 500 및 750 mg/kg으로 설정하였다. 대조군은 예비실험에서 구토, 일반증상 및 체중변화의 이상이 발견되지 않아 본 실험에서 제외되었다.
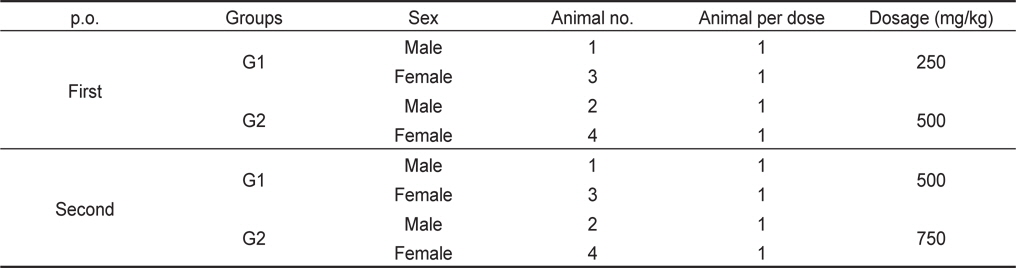
군분리는 비글견 6마리(male 3마리; female 3마리)의 순화기간 중 일반증상을 관찰하여 건강한 것으로 판정한 동물의 체중을 측정하여 순위화 하고, 평균에 가까운 동물 암수 2마리를 선택하여 Table 1과 같이 무작위 분배하였다.
[Table 1.] Experimental groups for acute oral administration of beagle dogs
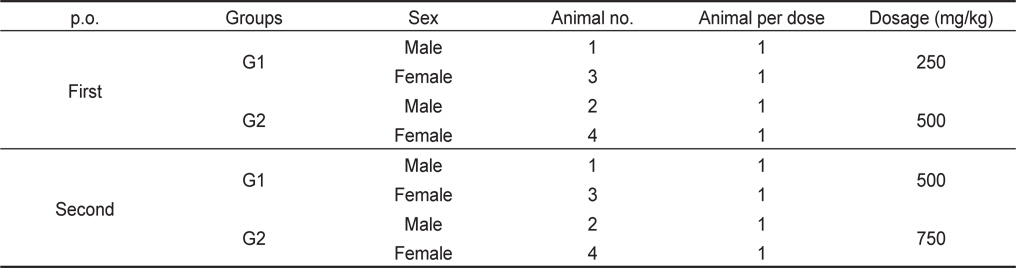
Experimental groups for acute oral administration of beagle dogs
PRT는 진한갈색분말로 중량 그대로를 동물 체중에 맞게 칭량한 후 경구투여용 젤라틴 캡슐(11 size, Torpac Inc., Japan)에 충진하여 조제하였다. 선발된 비글견은 투여 전 하룻밤 절식시킨후 시험물질을 충진시킨 캡슐을 오전 11시 이전에 1일, 7일 간격으로 총 2회 단회 투여하였다. 투여 당일 사료는 시험물질 투여 4시간 후에 급여하였다.
1) 일반증상 및 사망동물의 관찰
실험기간 동안 모든 동물에 대하여 매일 1회 이상 증상관찰을 실시하였다. 단, 투여 당일에는 투여 후 1시간까지 지속적으로, 투여 후 6시간까지 매 시간마다 관찰하였다. 각 투여 일을 1일로 설정하여 1차 투여 후의 증상은 7일까지, 2차 투여 후의 증상은 15일까지 관찰하였다. 일반 임상증상 항목으로서 soft stool, vomiting, diarrhea의 정도를 기록하였으며 사망 유무를 관찰하였다.
2) 체중 및 사료섭취량
모든 동물에 대하여 1차 투여 시에는 1, 4 및 7일째의 체중을 측정하였고, 2차 투여 시에는 1, 4, 7 및 15일째의 체중을 측정하였다. 사료 섭취량은 300 g 제한 급여를 하면서 매일 측정하였다.
3) 부검
2차 투여 일을 기준으로 15일간 관찰기간이 종료된 후에 모든 생존동물에 대해 pentobarbital (45 mg/kg, Hanlim Pharm. Co. Ltd., Seoul, Korea)을 정맥내 투여하여 마취시킨 후 액와동맥(Axillary vein & artery)을 절단하는 방법으로 방혈하여 안락사시킨 후 육안적으로 모든 장기를 검사하였다. 모든 시험군의 동물에서 육안적 이상장기가 관찰되지 않아 고정 및 조직병리학적 검사는 실시하지 않았다.
그룹 당 실험동물이 암수 각각 1마리씩이기 때문에 얻어진 결과에 대한 통계처리는 실시하지 않았다.
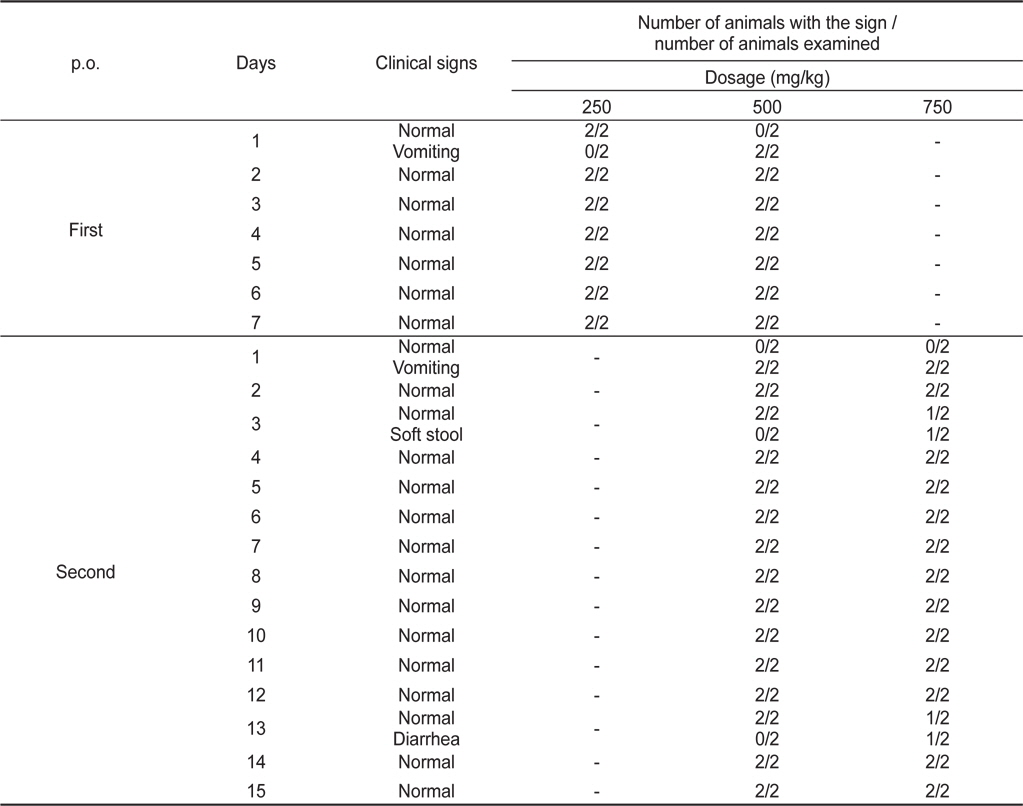
PRT를 암수 비글견 각각 1마리씩 250 및 500 mg/kg의 농도로 1차 단회 경구투여한 결과, 250 mg/kg 투여군에서는 별다른 이상증상을 나타내지 않았지만, 500 mg/kg 투여군에서 시험물질 성상의 일시적인 구토(vomiting)가 수컷에서 투여 약 2시간 후, 암컷에서 투여 약 3시간 후에 관찰되었다(Table 2). 이후, 7일동안 별다른 이상증상을 나타내지 않았고 사망동물 또한 관찰되지 않았다(Table 3).
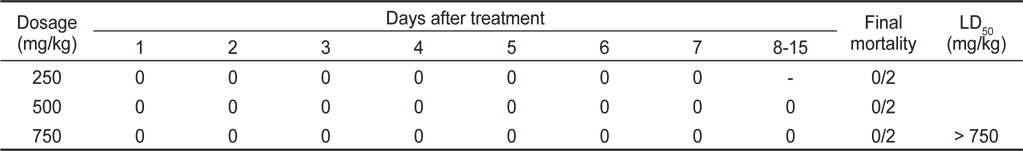
1차 투여한 비글견 4마리를 대상으로 투여농도를 높여 500 및 750 mg/kg의 농도로 2차 단회 경구투여하여 15일간 독성징후와 동물의 사망발현에 대해 관찰한 결과, 투여 약 2시간 후에 500 및 750 mg/kg 투여군 암수 모두에서 시험물질 성상의 일시적인 구토가 관찰되었다(Table 2). 또한, 투여 후 3일째 750 mg/kg 투여군 암컷에서 연변(soft stool)이 관찰되었고, 13일째 750 mg/kg 투여군 수컷에서 설사(diarrhea)가 관찰되었으나, 이는 비글견을 이용한 실험에서 자연스럽게 관찰될 수 있는 정도였다. 실험이 종료되는 15일까지 사망동물은 발견되지 않았으며 별다른 이상 징후를 나타내지 않은 것으로 보아 비글견에 있어서의 PRT의 LD50 value는 750 mg/kg을 상회하는 것으로 판단되었다(Table 3).
[Table 2.] Effect of the acute oral administration of PRT on the clinical signs of beagle dogs
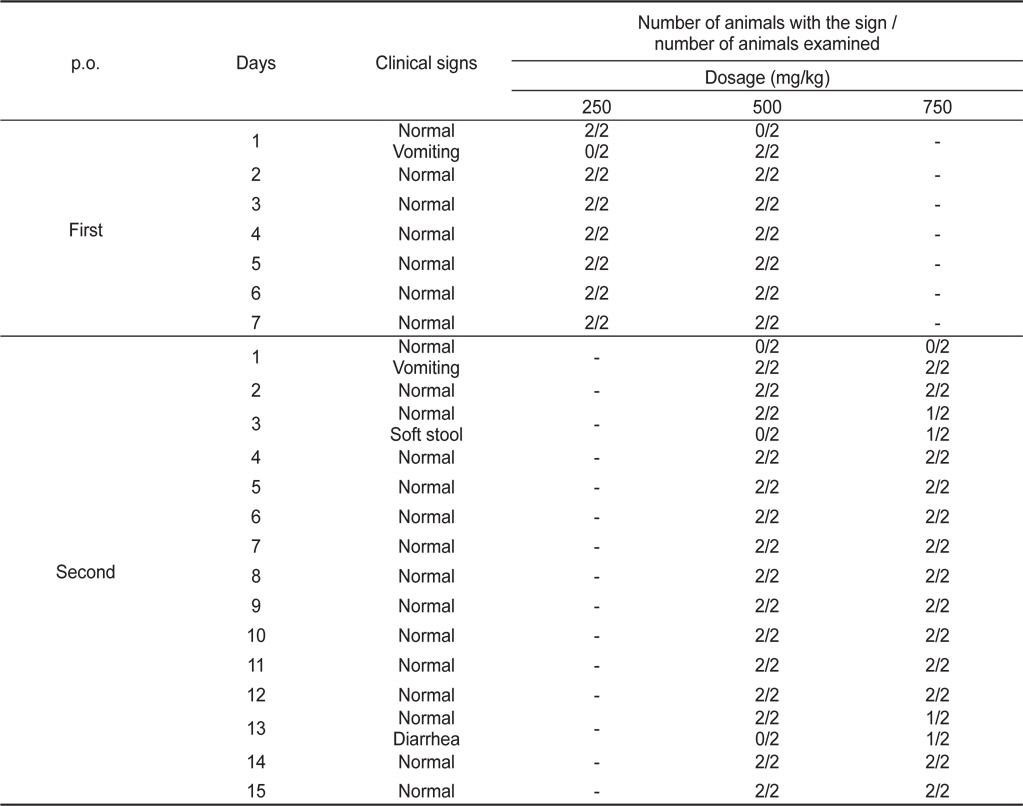
Effect of the acute oral administration of PRT on the clinical signs of beagle dogs
[Table 3.] Effect of the acute oral administration of PRT on the mortality of beagle dogs
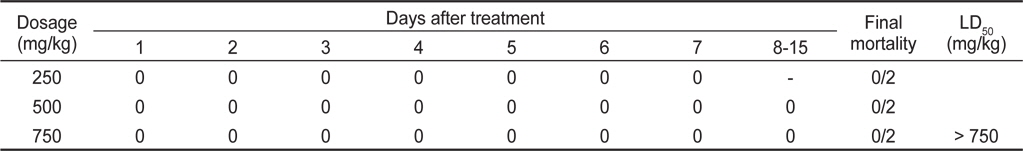
Effect of the acute oral administration of PRT on the mortality of beagle dogs
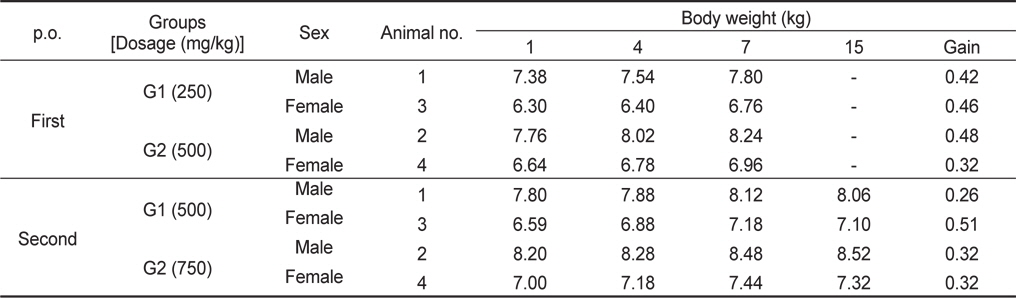
250 및 500 mg/kg 농도의 1차 PRT 투여군과 500 및 750 mg/kg 농도의 2차 PRT 투여군 모두 시험기간 7일 및 15일동안 별다른 체중 급감 이상 징후는 관찰되지 않았으며 정상적인 성장이 관찰되었다(Table 4).
[Table 4.] Effect of the acute oral administration of PRT on the body weight of beagle dogs
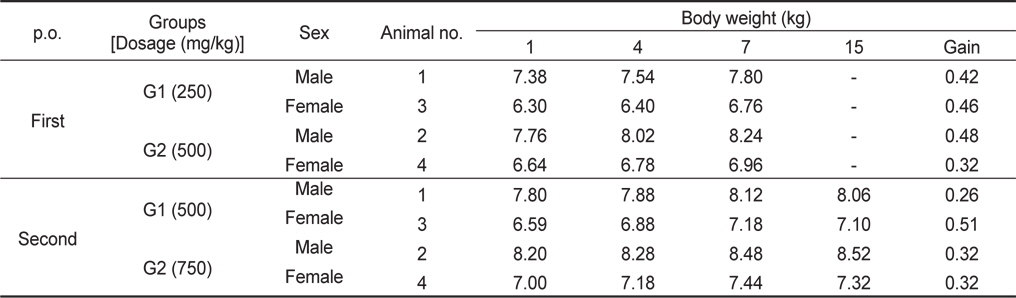
Effect of the acute oral administration of PRT on the body weight of beagle dogs
PRT를 비글견에 단회 경구투여하여 15일간 관찰한 후 부검한 결과, 투여군의 모든 개체 장기에서 유의성 있는 변화나 시험물질의 투여로 인한 비특이적인 소견은 관찰되지 않았으며(Table 5), 본 실험에 사용된 PRT에 대한 어떠한 이상도 발견할 수 없었다.
[Table 5.] Effect of the acute oral administration of PRT on the autopsy findings of beagle dogs

Effect of the acute oral administration of PRT on the autopsy findings of beagle dogs
최근 세계적으로 천연물에 대한 관심이 급증하면서 천연물 소재를 이용한 식품이나 의약품 개발에 관한 연구가 활발하게 이루어지고 있다(Kim et al., 2009). 의약품 또는 기능성식품을 개발하기 위해서는 임상시험 이전단계에서 실험동물을 이용하여 안전성을 평가하여야 하는데 식품의약품안전처의 “의약품 등 의 독성시험기준” 에서 제시하는 시험방법에 따라 적절하게 실시되어야 한다. 특히, 식품의약품안전처 건강기능식품 개별인정원료로 승인 받기 위해서는 필요에 따라 독성시험결과가 함께 첨부되어야 하며, 기본적으로 단회투여 독성시험(설치류, 비설치류), 13주 반복투여 독성시험(설치류) 및 유전독성시험(복귀 돌연변이시험, 염색체이상시험, 소핵시험)을 우수실험실운영기준(Good Laboratory Practice, GLP)에 따라 지정된 기관에서 OECD 독성시험 지침(Toxicity Test Guideline)에 의거하여 시험해야 한다(Park et al., 2010; Park and Cho, 2011; Kang et al., 2013).
독성시험 중 단회투여 독성시험은 시험물질을 실험동물에 단회투여 하였을 때 단기간 내에 나타나는 독성을 질적 및 양적으로 검사하는 시험을 말하며, 두 종 이상의 동물을 사용하도록 요구하고 있고, 그 중 한 종은 설치류, 또 다른 한 종은 토끼 이외의 비설치류를 제시하고 있는데 일반적으로 설치류에는 랫드가, 비설치류에서는 개를 현재 가장 많이 사용하고 있다. 특히, 비글견은 독성시험에 적당한 시험동물로서 일반독성시험에 널리 사용되고 있으며 풍부한 시험기초자료가 축적되어 있어 시험결과의 해석 및 평가에 유용하게 이용되고 있다(Song et al., 2005). 또한, 설치류를 이용한 단회투여 독성시험에서는 치사량을 확인하기 위해 용량을 고함량으로 설정하여 사망률과 LD50을 측정하는 반면, 비설치류를 이용한 단회투여 독성시험의 경우에는 개나 원숭이에게 치사량까지 투여할 수 없으므로 단회투여 독성시험 이후에 시행될 반복투여 독성시험의 용량설정을 위한 시험으로 진행되며, 설치류에서 나타나지 않는 특이적 독성이 비설치류를 통하여 발현될 가능성이 있기 때문에 설치류와 함께 수행되는 것이 일반적이다.
이렇듯 의약품이나 건강기능식품의 개발을 위해서는 안전성 및 유효성을 확보하기 위한 독성학적 연구가 꼭 수행되어야 하지만, 지난 20년동안 감태의 생리활성 성분인 phlorotannin은 다양한 연구로 많은 생리활성이 규명된(Kang et al., 2010) 반면, 독성과 관련된 연구는 극히 한정적이며, 현재까지 GLP기관에서 OECD 독성시험 지침에 따라 시행된 독성학적 연구는 전무한 상황이다. 따라서 본 연구에서는 phlorotannin의 안전 성 평가의 일환으로 PRT를 비글견에 DE (dose escalation)법을 이용하여 단회 경구투여 하였을 때 나타나는 급성독성의 유무와 섭취량의 한계를 조사하기 위하여 식품의약품안전처의 독성시험가이드라인에 따라 GLP기관으로부터 독성시험을 수행하였다.
시험물질 PRT를 250 및 500 mg/kg의 농도와 500 및 750 mg/kg의 농도로 각각 1마리의 암수 비글견에 1차 및 2차 투여한 후 각각 7일 및 15일간 일반증상, 사망률, 체중측정 및 부검소견을 관찰하였다. 독성시험 중 시험물질 PRT 500 및 750 mg/kg 투여군 암수에서 관찰된 시험물질성상의 일시적인 구토는 시험 물질에 의한 변화로, 일반적으로 개는 인두나 위의 자극으로 쉽게 구토를 일으키며, 특히 비글견의 구토는 구토중추의 발달로 인하여 독성작용 없이 경미한 위장관의 자극에 의해서 유발되기도 한다(Ahn et al., 2001; Henrik et al., 2003). 또한, 본 실험에서는 전신적인 이상증상, 체중변화 및 부검소견에서의 이상이 동반되지 않았기에 전신적인 독성작용에 의한 것이 아닌 시험물질 고유의 맛, 냄새 등의 물리적인 특성에 의한 변화로 사료된다.
이상의 결과로 보아 PRT의 비글견에 DE (dose escalation)법을 이용한 단회 경구투여 독성시험에서는 500 및 750 mg/kg 이상으로 과량 적용된 시험물질의 물리적인 자극에 의해 감수성이 큰 개체에서 구토증세가 일부 관찰되었으나, 모든 투여군에서 사망 예는 전혀 관찰되지 않았으며 일반적인 임상증상에서도 아무런 이상이 발견되지 않았다. 또한 동물의 사후 부검 결과에서도 각 장기의 독성학적인 변화는 관찰되지 않았다. 따라서 PRT의 비글견에서 최소 치사량은 750 mg/kg을 상회할 것으로 판단되며, 이는 임상적용용량인 500 mg/day 보다 90 배 높은 용량(성인 60 kg 기준)으로 본 연구를 통하여 PRT는 별다른 독성이 없는 안전한 물질인 것으로 판명되었다.