The study investigated the chemical composition, pH, and texture of salted jellyfish processed in Indonesia, Thailand, and China as a pilot study for processing the jellyfish
최근 해수온도 상승 등의 해양환경 변화는 우리나라를 비롯한 전세계의 해파리 대량 출현의 주 원인이 되고 있다(Dong et al., 2010; Richardson et al., 2009; Uye, 2008). 우리나라 연근해에 대량 발생하는 해파리는 보름달물해파리, 노무라입깃해 파리이며, 특히 여름철에 집중 발생된다. 이들 해파리는 원자력발전소 가동을 멈추게 하거나 어구와 어획물에 손상을 주는 등 직∙간접적인 피해를 주고 있으며, 그 피해액은 연간 68.2-204.6백만 달러에 달한다(Kim et al., 2012). 대량 발생하는 해파리를 활용하고자 해파리로부터 항균 peptide (Moon et al., 2011; Ovchinnikova et al., 2006), green fluorescent protein (Smith et al., 2002), 항고혈압(Lim et al., 2013), 콜라겐(Nagai et al., 2000)등의 기능성 소재가 연구되었으며, 화장품 의약품, 식품으로 활용하는 연구가 진행되고 있으나(Yang 2002; Hsieh et al., 2000), 식품을 제외하고는 산업적인 이용에 한계가 있다.
태국, 인도네시아, 필리핀, 중국 등지의 중앙태평양에서 어획되는 약 8종의 해파리가 식용 가능하며(Huang, 1988), 이들 중
염장해파리 가공기술은 태국과 중국 등에서 확립되어, 제품이 생산되고 있으며, 전 세계에 수출하고 있다. 우리나라에 유통되는 염장해파리는 전량 수입되고 있으며, 2013년 수입량은 3,823천톤이며, 주요 수입국은 태국과 중국으로 수입량은 각각1,610톤(42.1%)과 870톤(22.8%)을 차지한다. 그 밖에 인도네시아, 말레이시아, 베트남에서 수입되고 있다. 염장해파리 수입단가는 2003년 kg당 1.2달러에서 지속적으로 상승하여 2013년에는 kg당 평균 2.8달러에 도달하였다(KCS, 2014). 따라서 본 연구에서는 국내에 유통되는 수입산 염장해파리 가공제품에 대한 이화학적 성분을 분석하여 품질지표를 마련하여 우리 나라 연근해에 대량 출현하는 노무라입깃해파리의 가공방법을 확립하고자 한다.
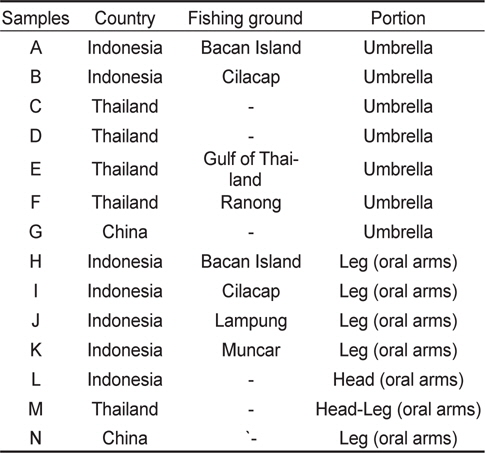
염장해파리는 기장군 정관면 소재 B사, 경기도 소재 C사, 부산시 사하구 소재 H사 등 수입업체를 통하여 국가별 해파리를 수집하였으며, 인도네시아 Bacan 지역에서 제조된 염장해파리 우산과 입다리를 포함하여 총 14개 시료를 시료로 사용하였다 (Table 1). 그러나 실험재료의 해파리 원료 종에 대한 정보와 일부 재료는 제조지역을 확인할 수 없었다.
[Table 1.] The profile of salted jellyfish processed in Indonesia, Thailand and China
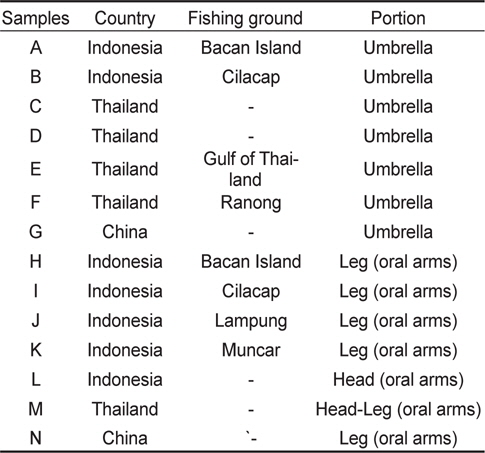
The profile of salted jellyfish processed in Indonesia, Thailand and China
일반성분의 분석은 AOAC법에 준하여 실시하였으며, 수분함량은 상압가열건조법, 조단백질 함량은 Kjeldahl 분석법, 회분 함량은 550℃에서 직접 회화법으로 측정하였으며, 조지방함량은 Soxhlet추출법으로 분석하였다(AOAC, 1995).
pH 측정은 시료 5 g을 취하여 증류수 45 mL를 가해 균질화시킨 후 pH meter (pH-200L, iSTEK, USA)로 측정하였다.
염분 함량은 시료 5 g을 증류수 20 mL와 혼합하여 균질화 한 후, 여과하여 100 mL로 정용하여 Morh법으로 측정하였다 (Hooi et al., 2004).
수분활성도는 시료 2 g을 수분활성도 측정장치(AQS-31-TC, NAGY Instruments, Germany)를 이용하여 실내온도 25℃에서 측정하였다.
색차는 우산 부위를 가공한 7종 해파리 시료를 간이형 직시색차계(Color reader CR-10, Konica Milolta Sensing, Inc., Japan) 를 이용하여 명도(L, Lightness), 적색도(a, redness) 및 황색도(b, yellowness)를 측정하였다.
조직감 측정은 물성측정기(Compac-100 II, Sun scientific, Japan)를 사용하여 탄력성, 응집성, 씹음성, 깨짐성, 경도, 강도를 측정하였다. 우산 부위를 가공한 7종 해파리 시료의 중앙부위를 40×20×2 mm로 절단하여 NO. 34 (치형A) adaptor를 이용하여 측정하였다. 이때 측정조건은 최대하중 10 kg, 진입깊이 2 mm, 속도 60 mm/min 이었으며, 실험 결과값은10회 이상 측정하여 그 평균값을 사용하였다.
총아미노산 분석은 우산 부위를 가공한 7종 해파리 시료 2 g을 6 N HCl로써 110℃의 heating block에서 24시간 가수분해 하였다. 시료용액을 감압건고시킨 후, pH 2.2의 구연산 완충액으로 50 mL로 정용하여 0.20 μm membrane filter로 여과하여 아미노산 분석기(Sykam 4300, Sykam, Germany)을 이용하여 분석하였다.
일반세균수는 Standard Methods for the Examination of Water and Wastewater (APHA, 1970)의 방법에 따라 Standard plate count agar (SPC, Difco)를 사용하여 35±0.5°C 에서 24-48시간 배양한 후, Colony Forming Unit (CFU)로 나타내었다.
통계 처리는 SAS 프로그램을 이용한 분산분석표를 작성하였으며, Duncan의 다중범위검정(Duncan's multiple range test)으로
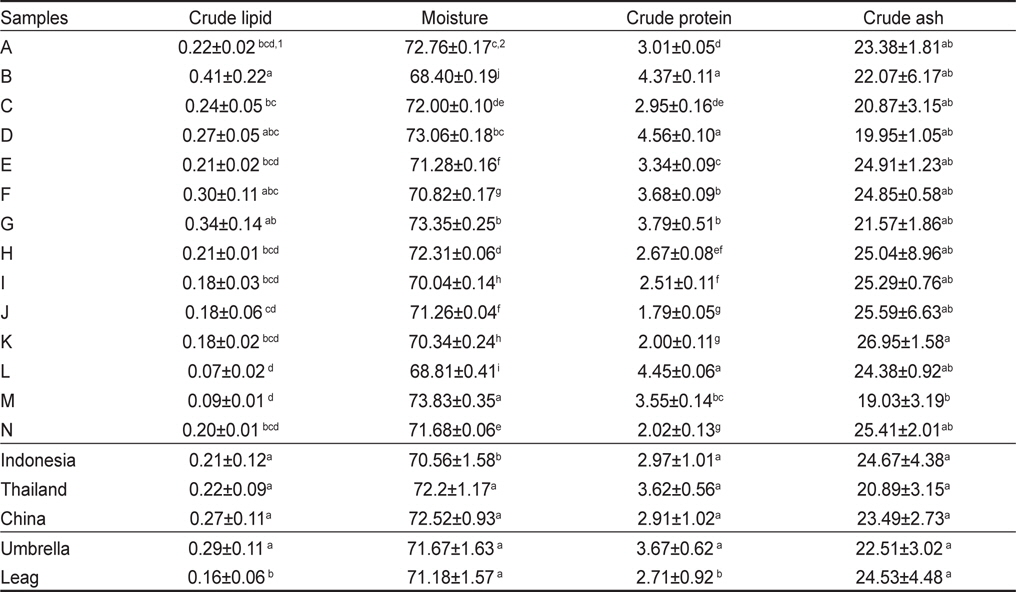
해파리 시료 14종의 일반성분을 분석한 결과, 수분함량은 68.4-78.3 g/100 g, 조지방 함량은 0.07-0.41 g/100 g, 조단백질 함량은 1.79-4.37 g/100 g이었다(Table 2). 해파리 생물의 수분함량은 96.1 g/100 g, 조회분 함량은 1.25 g/100 g, 조단백질 함량은 2.92 g/100 g, 조지방 함량은 0.01 g/100 g 이하이며, 삼투압 조절을 위하여 2-3% 염분을 함유하고 있다(Heieh et al., 2001; Wootton et al., 1982). 부위별 일반성분 함량을 살펴보면, 우산과 입다리의 수분함량은 각각 71.43±1.63 g/100 g, 71.18±1.57 g/100 g이었으며, 회분 함량은 각각 22.51±3.02, 24.53±4.48 g/100 g으로, 부위별 수분과 회분 함량은 유의적인 차이는 없었다(
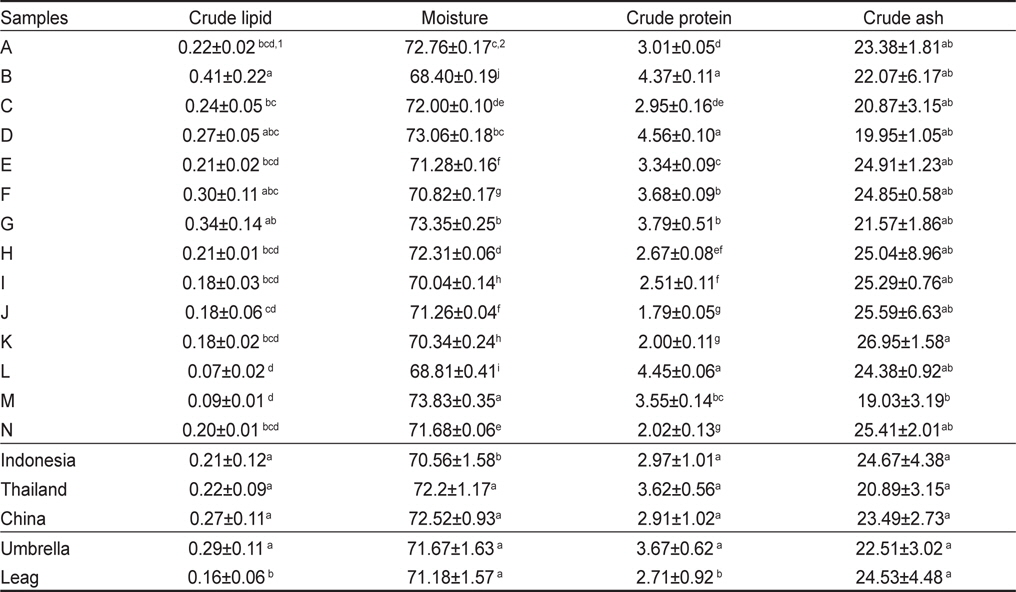
The proximate composition of salted jellyfish processed in Indonesia, Thailand and China (g/100 g)
태국과 말레이시아에서는 해파리 조직감을 증가시키고, 염장액에서 탈수효율을 높이기 위하여 소량의 소다를 사용하지만 중국에서는 다양한 어종이 어획되거나 다양한 형태로 제조하기 때문에 소다를 사용하지 않다고 보고하고 있으나(Hsieh et al., 2001), 국가별에 따른 수분함량의 차이는 식품첨가물에 의한 영향보다는 유통과정 중 탈수 정도에 따라 나타나는 것으로 사료된다. 따라서 염장해파리 제조시 염장은 어류 등을 염장하여 저장성을 증가시킨 제품과는 달리 60-70% 수분을 가지도록 하는 것이 중요하다.
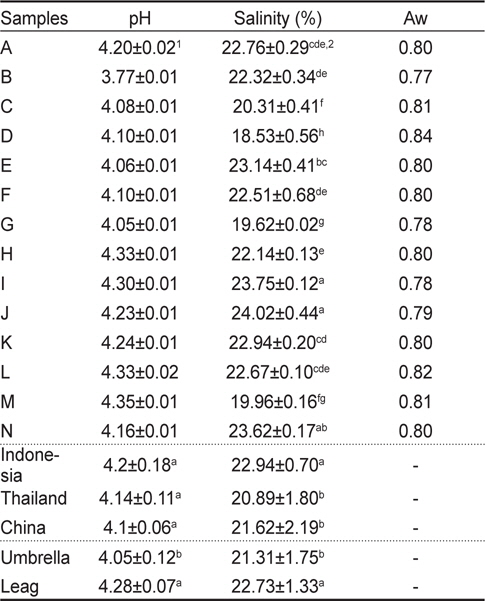
해파리 시료 14종의 pH, 염분 함량, 수분활성도를 측정하였다(Table 3). 염장해파리의 평균 pH는 3.77-4.35이며, 생물 해파리(pH 6.67)와 비교할 때 매우 낮은 값이었다. 염장해파리의 pH가 생물해파리에 비해 pH가 낮은 이유는 가공시 첨가되는 명반의 pH (2.69-2.94)에 영향을 받기 때문이다.
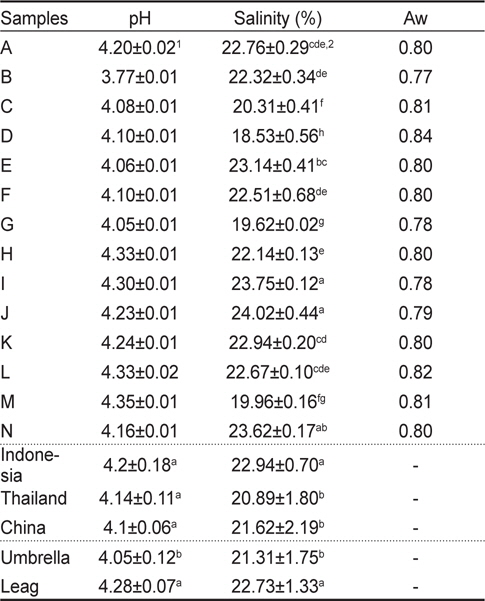
The pH, salinity and water activity of salted jellyfish processed in Indonesia, Thailand and China
해파리 부위별 pH차이는 우산이 4.28, 입다리는 pH 4.05로, 입다리의 pH가 우산보다 낮았다. 원산지에 따른 염장해파리의 pH는 인도네시아(4.20), 태국(4.14), 중국(4.10) 순이었으나, 원산지간의 유의적인 차이는 없었다(
해파리 시료의 평균 염분 함량은 18.5-23.6%이었으며, 부위별에 따른 평균 염분 함량은 우산과 입다리가 각각 21.31, 22.73% 이었으며, 부위별에 따른 유의적인 차이는 없었다(
염장해파리 14종의 수분함량은 Table 2와 같이 68.4-78.3 g/100 g으로 다소 높은데 반하여, 수분활성도는 0.77-0.80으로 매우 낮았다(Table 3). 일반적인 염장해파리 제조를 위하여 소요되는 기간은20-40일이며, 최종 제품의 수분함량은 60-70%, 식염 함량은 16-25%이라고 보고되고 있다(Hsieh et al., 2001).가공된 해파리의 수율은 해파리 원료 종과 가공법에 따라 다소 차이가 있으나 대략 7-10%정도이다(Huang, 1988; Subasinghe, 1992). 일반적인 수산건제품은 수분함량의 감소로 인하여 최종제품의 수분활성도는 0.75-0.80의 범위이며, 반건조 식품은 약 0.60-0.90 정도의 범위를 갖는다고 보고되었다(Jin et al., 2008; Shim et al., 2011). 낮은 pH, 수분활성 도, 높은 염분 함량에 의하여 염장해파리 14종에서는 일반세균이 검출되지 않았으며(결과 미제시), 세균 등의 미생물로부터 비교적 안전하여 저장성이 향상된다. 일반적으로 염장해파리는 1년까지 의 유통기한을 가지며, 서늘한 곳에 보관시에는 2년까지도 유통이 가능하다. 그러나 상온에서 장기간 저장 시 염장해파리 특유의 조직감이 상실되거나 부패할 수 있다.
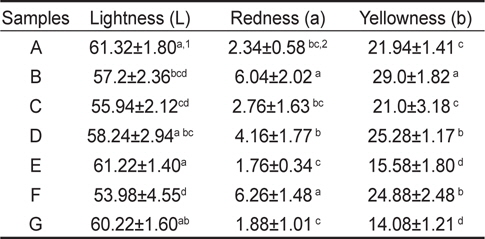
해파리 시료 중 우산 부위를 가공한 7종의 시료에 대한 색차를 분석한 결과, 평균 명도가 53.98-61.32, 평균 적색도 1.76-6.26, 평균 황색도 14.08-29.00이었다(Table 4). 적색도는 태국산 F시료, 황색도는 인도네시아 B시료가 가장 높았으며, 태국산 E시료와 중국산 G시료가 황색도가 가장 낮았다.
[Table 4.] The color difference of salted jellyfish processed in Indonesia, Thailand and China
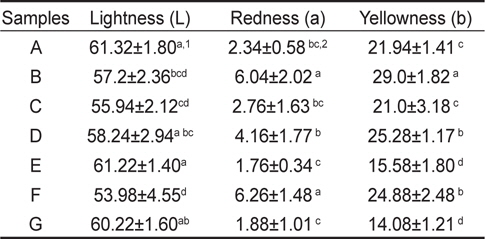
The color difference of salted jellyfish processed in Indonesia, Thailand and China
원산지에 따른 해파리 시료의 명도는 인도네시아산 57.20- 61.32, 태국산 53.95-61.22, 중국산 60.02이었으며, 황색도는 인도네시아산 21.88-29.00, 태국산 15.58-25.28, 중국산 24.89이었다. 그리고 적색도는 인도네시아산 2.34-6.04, 태국산 1.76-6.26, 중국산 1.88이었다.
우리나라로 수입되는 해파리 종은 근구해파리과(Rhizostomatidae)에 속하는
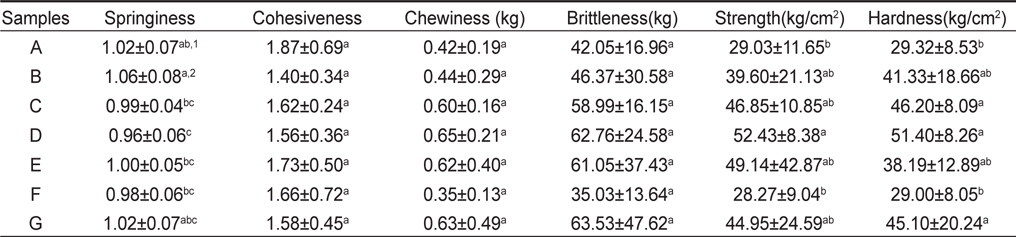
또한 염장해파리 품질 및 가격 결정에 영향을 주는 것은 조직감이다. 염장해파리의 특유의 조직감은 제품이 탄력을 가지면서 씹힘성이 좋고, 씹히는 소리가 나면서 꼬들꼬들한 상태를 말한다. 우산 부위를 가공한 해파리 시료 7종의 조직감은 응집성, 씹힘성, 깨짐성, 탄력성, 경도, 강도 등을 측정하여 평가하였다 (Table 5). 응집성, 씹힘성, 깨짐성은 시료간의 유의적인 차이는 없었다(
[Table 5.] The texture profiles of salted jellyfish processed in Indonesia, Thailand and China
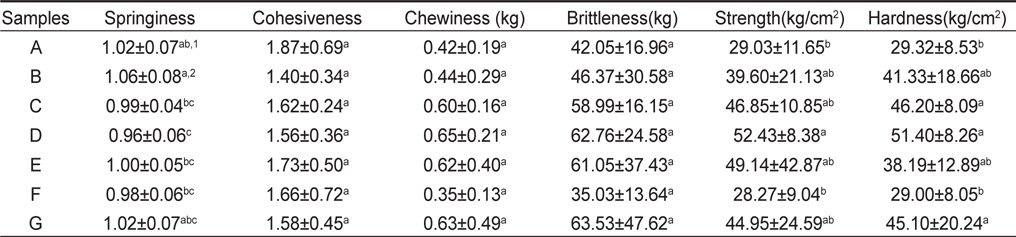
The texture profiles of salted jellyfish processed in Indonesia, Thailand and China
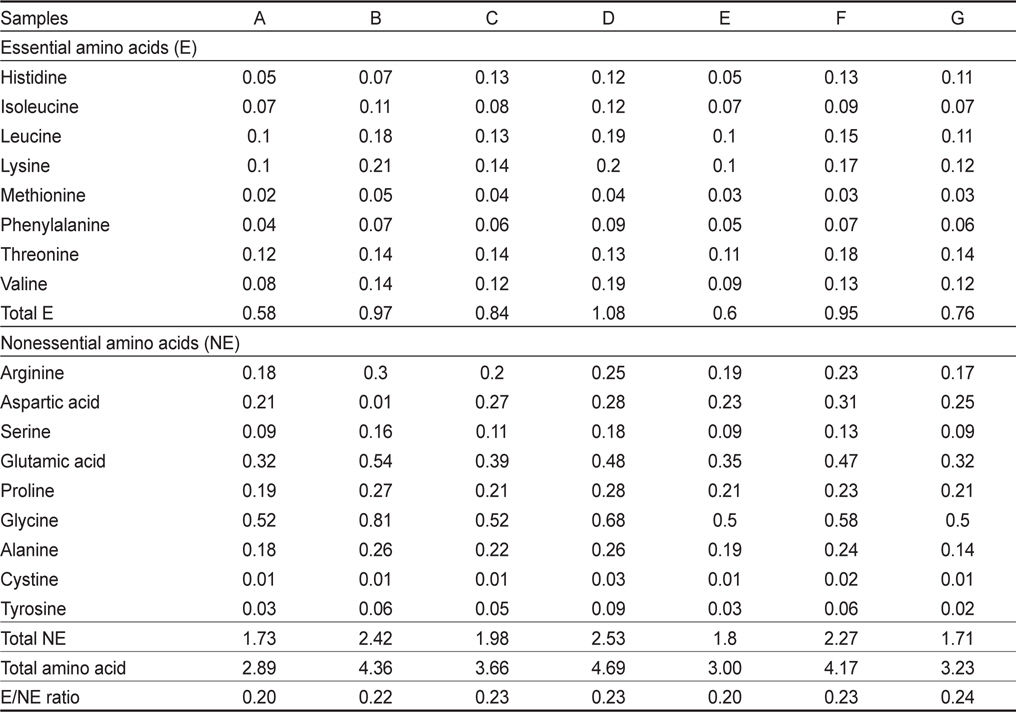
해파리 시료 중 우산부위를 가공한 7종 시료의 총아미노산 함량은 2.30-4.69 g/100 g이었다(Table 6). 이들 아미노산 중 glycine 함량이 0.50-0.81 g/100 g이었으며, 총아미노산 함량의 17.3-28.03%로 가장 많은 함량을 차지하였다. 그 다음으로 glutamic acid, aspartic acid 함량이 높았다. 필수아미노산 함량은 0.58-1.08 g/100 g이며, 전체 함량에 20.07-37.37%로 매우 낮았다. 일반적으로 어류의 필수아미노산 함량은 40% 이상이며, 대부분의 수산물의 필수아미노산과 비필수아미노산 일반적인 비율인 0.74에 비하여, 염장해파리는 0.20-0.24로 매우 낮았다(Shim et al., 2011; Iwasaki et al., 1985). Kimura et al. (1983)은 해파리의 아미노산 중 glycine 함량이 전체 함량의1/3을 차지하고 있으며, hydroxyproline과 hydoroxylysine 비율이 높아, 해파리의 구성 단백질이 콜라겐이라고 보고하였다.
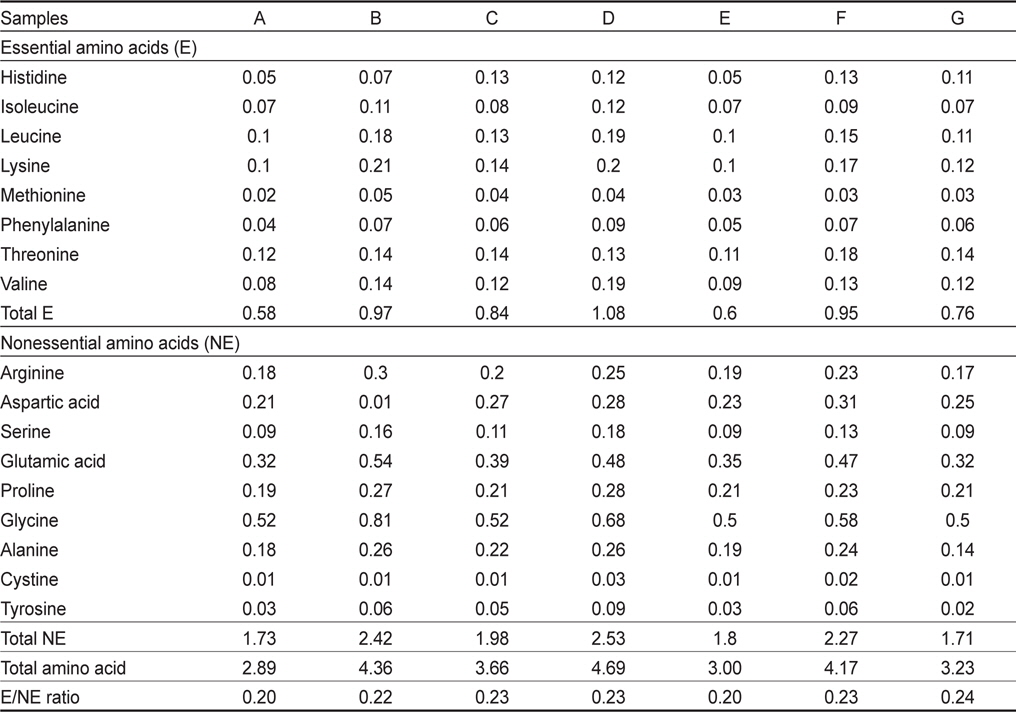
Total amino acid content of salted jellyfish processed in Indonesia, Thailand and China (g/100 g)
따라서 우리나라에 수입되는 염장해파리의 수분함량은 68- 78 g/100 g이며, pH는 4.2이하, 염분 함량은 18.5% 이상 이었다. 제품의 품질에 가장 큰 영향을 미치는 조직감은 강도에서 큰 차이를 나타내어 28.27-52.43 kg/cm2이었다. 색택은 원료 종에 따른 차이가 매우 크기 때문에 품질지표로 이용하는 것은 한계가 있다. 이러한 이화학적 성분 특성은 수산업 등에 직접적인 피해를 주고 있는 노무라입깃해파리의 염장해파리 가공시에 품질지표로 활용하여 국산 염장해파리 가공산업화가 가능할 것으로 사료된다.
또한 염장해파리 14종의 시료의 칼로리를 계산하면, 평균 12.98-29.75 cal/100 g이다(결과 미제시). 지방 함량이 매우 적으며, 수분과 단백질, 그리고 회분으로 구성되어 있으며, 탄수화물은 당당백질로 단백질과 결합되어 소량 존재한다(Kimura et al., 1983). 염장해파리에 많이 함유되어 있는 회분은 식염에 의한 것이며, 염장해파리를 섭취할 때 물에 일정시간 침지시켜 식염을 제거한 후에 조리하여 섭취한다. 따라서 염장해파리는 지방 및 콜레스테롤이 함유되어 있지 않은 자연 다이어트 식품으로 각광받을 수 있기 때문에 국내 해파리 가공산업화의 경쟁력도 갖출 수 있을 것으로 사료된다.