Catalytic gasification of raw coals at mild condition is not realized yet mainly due to deactivation of catalysts via their irreversible interaction with mineral matters in coal. In this work, the gasification behavior of ash-free coal (AFC) was compared with that of the parent raw coal. In order to modify the gasification conditions, the raw coal gasified with fixed variables (water supply, space velocity, temperature, catalysts) in a fixed bed reactor. When catalysts are added by physical mixing method with coal, K2CO3 was the most effective additives for steam gasification of coal. However, the activity of ash-free coal (AFC) was much less reactive than raw coal due to high temperature extraction in a 1-methylnaphthalene under 30bar at 370℃ for 1 h, almost removed oxygen functional groups, and increased carbonization. The addition of K2CO3 in AFC achieved higher conversion rate at low temperature (700℃). At that time, the molar ratio of gases (H2/CO and CO2/CO) was increased because of water-gas shift reaction (WGSR) by addition of catalysts. This shows that catalytic steam gasification of AFCs is achievable for economic improvement of gasification process at mild temperature.
세계적으로 전기 생산의 평균 40% 이상은 석탄연소에 의해 이루어진다. 국내 상황도 유사하여 약 35% 이상의 전력공급은 석탄 화력 발전에 의해 이루어진다. 현재 우리나라는 석탄 수요의 대부분을 수입에 의존하여 세계 3위의 석탄 수입국이 되었다[1]. 이처럼 석탄사용량이 큰 비중을 차지할 수 있는 것은 대체할 수 있는 신재생 에너지의 원가가 석탄원가에 미치지 못하며, 석탄의 매장량은 가채년수에 비해 17배가량 되어 추후 가채년수는 200년 이상이 될 것으로 판단하고 있기 때문이다. 또한 분포지역이 비교적 고르며 가격이 저렴하다는 것이다. 이로 인하여 향후 30년 이상은 화석연료 의존성이 지속될 것으로 예상하고 있다[1,2]. 하지만 CO2를 포함하여 기타 공해 물질들을 배출하여 지구온난화를 부추기는 요인 중 하나로 작용하고 있다. 이를 위해 오랜 기간 이산화탄소 포집 저장기술(carbon capture and storage, CCS)로 CO2를 줄이려고 하는 노력이 전세계적으로 이루어 지고 있지만, 현재 기술적 미숙과 경제성이 부합하지 않아 당장의 해결책으로는 한계가 있다. 이러한 당면 과제를 현실적으로 대응하기 위해서는 석탄의 최소 사용량으로 발전효율을 증가시키는 기술 및 공해 유발 물질 발생 최소화를 위한 기술개발이 필요하다.
석탄의 에너지 전환 중 대표적인 기술은 석탄가스화 복합발전(integrated gasification combined cycle, IGCC)이 있다[3]. 가스화 복합발전기술은 석탄화력발전에 비해 높은 발전 효율을 가지며, 직접 연소 발전에 비해서는 황산화물 90% 이상, 질소산화물 75% 이상, 이산화탄소 25%까지 저감할 수 있는 환경친화적 기술이기 때문에 세계 각국에서 개발에 힘쓰고 있다[4]. 또한 석탄 가스화를 통한 합성가스(H2 + CO)의 생산은 대표적인 수소 생산 기술의 하나로 세계적으로 약 30%의 수소 생산을 담당하고 있다[4,5]. 일반적으로 석탄 가스화는 고온(> 1,000 ℃), 고압(> 30 bar) 조건에서 상업적으로 이루어지므로 경제적 부담이 크며 위험하다[6-9]. 온순 조건에서 반응을 실현하기 위해 많은 과학자들에 의해 촉매의 도입이 검토되었다[10-12]. 하지만 촉매 물질들은 가스화 조건에서 석탄 내 회분과 반응하여 활성을 잃게 되어 재활용이 불가능하므로 경제성이 떨어진다[13-16]. 이 같은 문제를 해결하기 위해 석탄의 회분을 제거한 탄이 여러 방법으로 개발되고 있으며, 무회분탄의 촉매가스화는 촉매를 재활용할 수 있는 경제성을 갖게 된다[17,18].
따라서 본 실험에서는 열추출법을 통해 저등급 탄인 삼화탄을 무회분탄으로 제조하여 촉매 유무와 온도에 따른 가스화 반응성을 원탄과 비교하여 평가하였다. 우선 원탄을 대상으로 수증기 공급량을 최적화하고 석탄에 대해 가장 활성이 좋은 촉매를 선정하였다. 원탄과 무회분탄에 촉매를 혼합하여 온도별로 가스화 하여 비교하였다. 이후 저온에서의 무회분탄과 원탄의 촉매 수증기 가스화 반응성을 비교하여 무회분탄의 저온 촉매가스화 공정 가능성을 논의하였다.
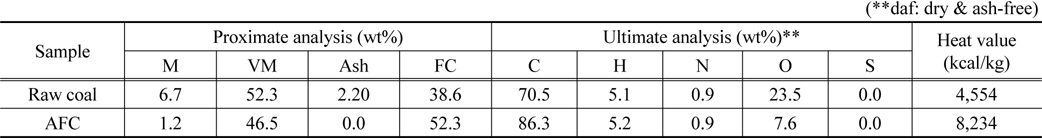
무회분탄의 제조는 0.5 L의 고온고압 회분식 반응기에서 이루어졌다[19]. 실험 장치는 크게 추출, 여과, 건조 부분으로 구성되어 있다. 일정량의 석탄과 용매(1-methylnaphthalene, 1-MN)를 혼합하여 슬러리를 제조한 뒤, 반응기에 넣은 후 질소가스를 이용하여 내부 공기를 제거하였다[20]. 350 ℃로 승온 후 1시간 동안 교반하여 석탄에 포함된 유기성분들을 1-MN 용매에 용해시킨다. 이때 용매에 용해된 용액(Solvent extract)을 하부에 위치한 금속 필터로 불용분인 잔탄 성분을 분리하여 석탄 용액만을 얻는다. 얻어진 용액을 진공오븐(300 ℃)에서 12시간가량 건조하면 용액 중의 용매가 휘발되어 무회분탄(ash-free coal, AFC)이 얻어진다. 삼화 원탄과 무회분탄의 공업분석, 원소분석, 및 발열량 분석 결과를 Table 1에 나타냈다.
[Table 1.] Proximate/ultimate analysis and calorific value of coals
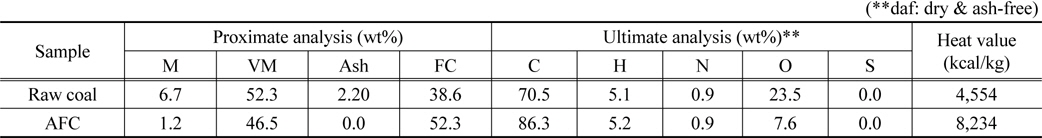
Proximate/ultimate analysis and calorific value of coals
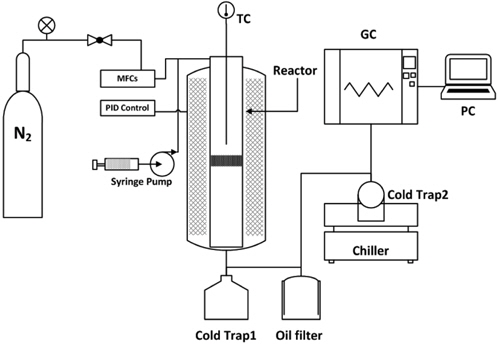
실험에서 직접 제작한 고정층 반응기를 사용하였으며 그 공정도를 Figure 1에 나타내었다[20]. 가스화 반응장치는 스팀공급을 위한 실린지 펌프(syringe pump), carrier 가스의 정량적 공급을 위한 질량유량계(mass flow controller, MFC), 튜브형 furnace 및 석영 반응기, 미반응 수증기 및 생성된 타르 제거를 위한 cold trap 및 oil trap, 그리고 정량적 생성 가스 분석을 위한 가스 크로마토그래피(GC, agilent 6890)로 구성하였다. 공급된 물은 150 ℃로 가열된 튜브에서 기화되어 반응기로 공급되었다. 100 cc/min (SV 15000 h−1) N2를 운반 기체로 사용하였다.
반응기는 내경 10.2 mm 두께 1.3 mm, 높이 450 mm의 크기로, 중간에 frit을 만들어 고체 석탄의 반응 시 가스 생성물만이 통과하도록 하였다. 두 개의 cold trap은 모두 2 ℃에서 수증기와 타르를 액화하여 GC로의 유입을 방지하였다. 생산된 가스는 front 컬럼(Porapak N)에서 비교가스 N2을 사용하여 H2와 CH4를 정량하였고, back 컬럼(Porapak Q와 Molsieve)에서는 비교가스 He을 이용하여 CO와 CO2를 정량하였다. GC 오븐 온도 35 ℃에서 12분의 간격으로 측정하였으며, 측정은 반응기 온도 170 ℃에서 수증기 주입과 동시에 30 ℃/min으로 승온하며 시작하였다. 촉매의 종류로는 Dolomite {CaMg(CO3)2}, Olivine {(Mg, Fe)2SiO4}, K2CO3, NiOX, CaO/MgO = 1:1 (wt% ratio) Fe2O3을 대상으로 실험하였다. 석탄과 함께 200 mesh이하로 분쇄하여 가스화 반응에 도입하였다.
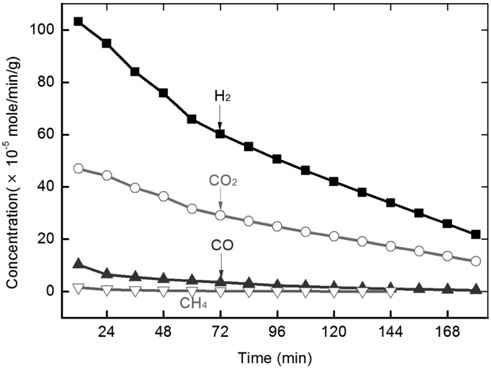
삼화 원탄의 수증기 가스화를 700 ℃에서 30 vol% 수증기를 공급하며 15,000 h−1의 공간속도에서 실시한 결과, 예상대로 H2, CO, CO2를 주로 생산하였으며, 반응 초기 소량의 CH4도 검출되었다(Figure 2). 반응 시작 직후 약 1 × 10−3 mole/min/g의 H2를 생산하다 시간 경과에 따라 점차 줄어들어 180분 경과 후에는 약 2 × 10−4 mole/min/g이 발생되었다. CO2의 경우 H2 보다 적은 양이 생산되어 180분 동안 1.2 × 10−4−4.8 × 10−4 mole/min/g을 나타냈다. 한편 CO는 더욱 적어 1 × 10−4 mole/min/g 이하가 생산되었다. 본 실험에서 관찰한 수증기 가스화는 반응 조건(온도, 압력, 공간속도) 및 석탄 종류에 의해 영향을 받으나 일반적으로 Figure 2와 유사한 경향을 보였다.
즉 일정 시간 동안 생성된 가스의 양을 전체 생성 가스의 양으로 나누어 준 값을 전환율로 정의하였다. Figure 2와 같은 형식의 그래프에 나타난 면적을 계산하여 생성가스 양을 얻었다. CH4의 생산양은 전체의 1% 미만이므로 제외하였으며, 이후 석탄의 반응성은 시간 경과에 따른 전환율의 변화를 통하여 나타냈다.
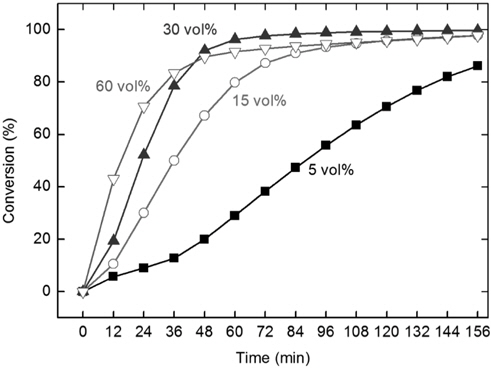
삼화 원탄을 대상으로 수증기 공급량이 가스화 반응성에 미치는 영향을 700 ℃와 15,000 h−1 조건에서 알아보았다(Figure 3). 기존에 알려진 가장 활성이 뛰어난 K2CO3 (10 wt%)를 첨가하여 가스화 반응 자체가 율속 단계가 되는 것을 방지하였다[10,12,13,21]. 수증기의 양을 5 vol%에서 30 vol%로 증가시킴에 따라 시간에 따른 전환율은 빠르게 증가하였다. 5 vol% 공급시 48분 이내에는 약 20% 이하의 낮은 반응성을 보였으며, 이후 기울기가 증가하여 156분에는 약 90%의 반응이 진행되었다.15 vol%에서는 5 vol% 대비 크게 증가된 전환율을 보였으나 30 vol% 대비 낮아져 96분 이후에 90% 이상의 전환율이 얻어졌다. 30과 60 vol%의 경우 모두 48분 이내에 ~90% 이상의 반응이 진행되었으며, 서로 큰 차이는 보이지 않았다. 이에 추후 실험에서는 30 vol% 수증기를 공급하며 진행하였다.
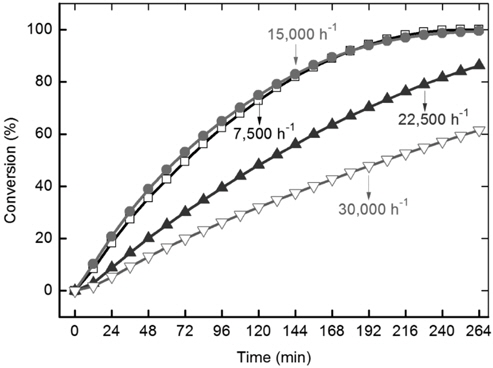
반응물인 수증기(30 vol% in N2)의 공급 속도를 변화시켜 700 ℃에서 가스화 반응을 실시한 결과를 Figure 4에 나타냈다. 15,000−30,000 h−1 범위에서 공간속도의 증가는 전환율을 감소시켰다. 하지만 7,500−15,000 h−1 범위에서는 영향을 받지 않았으며 공간속도와 무관한 전환율을 보였다. 이에 본 실험에서는 15,000 h−1을 기준 조건으로 정하여 이하 실험을 진행하였다.
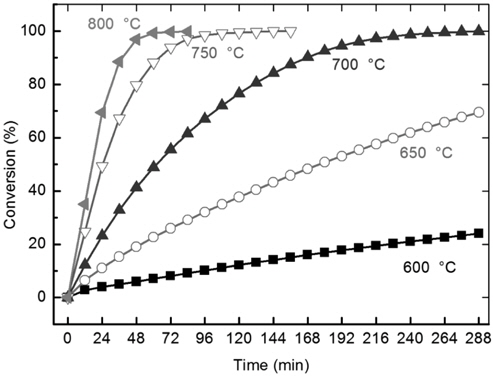
삼화 원탄의 온도 변화에 따른 가스화 반응성을 600-800℃에서 비교하였다. Figure 5에 보이듯이 전환율은 온도에 크게 의존하여 600 ℃에서는 288분 경과 후에도 25% 이하가 전환되었고, 650 ℃에서는 72분 경과 시 ~25% 전환율을 보이다 288분 이후에는 ~70% 반응이 이루어졌다. 700 ℃로의 승온에 의해 반응은 급격히 활발해지며 72분 경과 시 ~57%, 168분 이후 90% 이상의 전환이 관찰되었다. 또한 750 ℃에서는 72분에 그리고 800 ℃에서는 36분에 ~90%의 전환율을 보였다. 650 ℃ 이하 저온 반응에서는 시간 경과에 따른 전환율의 변화가 선형의 관계를 보였으나, 700 ℃ 이상에서는 시간 경과에 따라 변화하는 경향을 나타냈다.
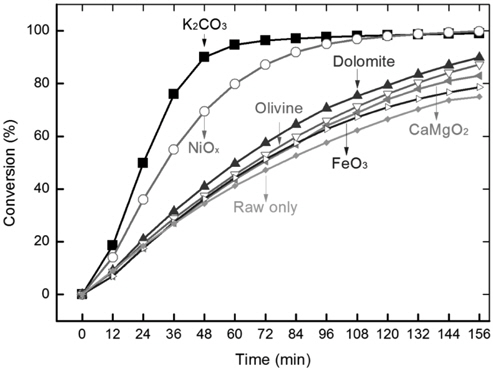
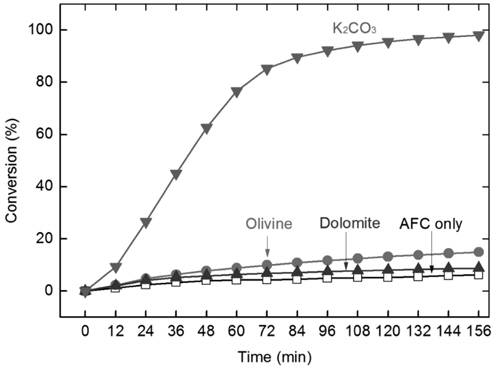
삼화 원탄에 dolomite, olivine, K2CO3, NiOx, CaO/MgO (CaMgO2) = 1:1 (weight ratio), Fe2O3를 각각 10 wt% 첨가한 뒤, 막자 사발을 이용하여 고체 상 혼합을 실시하였다. 이후 각각의 시료를 가스화한 후 촉매가 첨가되지 않은 원탄(Raw)과 전환율을 비교하였다(Figure 6). 검토된 6개 촉매 중 K2CO3가 가장 빠른 전환율을 보여 반응이 약 72분 후에 완료되었다. 다음으로 높은 활성을 보인 것은 NiOX로 약 120분 후에 반응이 완결되었다. 하지만 다른 4개의 촉매를 포함하는 시료들은 고체상 혼합에 의해서는 활성을 보이지 못했으며, 이때 촉매를 포함하지 않는 원탄과 유사하거나 약간 빠른 전환 속도를 보였다.
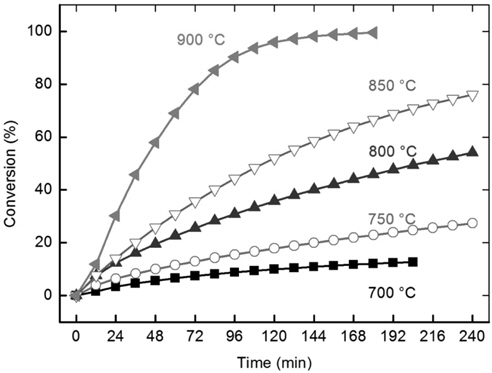
1-Methylnaphthalene을 이용한 열추출법에 의해 제조된 삼화 무회분탄의 수증기 가스화 반응성을 700-900 ℃에서 알아 보았다(Figure 7). 예상대로 온도 증가에 따라 전환율은 증가하였다. 하지만 상대적으로 원탄에 비해 낮은 반응성을 보여 700 ℃에서는 200분 경과 후에도 약 10% 수준의 전환율을 보였다. 점진적인 전환 속도 증가가 관찰되어서 200분 후에 750 ℃에서 약 25%, 800 ℃에서는 50%, 그리고 850 ℃에서는 70%의 전환율을 나타내었다. 하지만 무회분탄의 전환 속도는 850 ℃에서도 원탄의 700 ℃ 속도보다 느리게 나타났다(Figure 5). 무회분탄의 900 ℃ 반응에서 급격한 반응 증가가 나타나 96분에 약 90%의 전환율을 보였다.
촉매의 도입이 무회분탄의 반응성에 미치는 영향을 알아보기 위해, 촉매(K2CO3, dolomite, olivine)를 석탄 양 대비 10 wt% 로 고체 상 혼합으로 첨가하여 700 ℃에서 실험하였다(Figure 8). 원탄과 유사하게 K2CO3에 의해 전환 속도의 급격한 증가가 나타났다. 즉 반응 시작 후 24분 경과 시 이미 20% 이상의 전환율을 보였고, 84분 후에는 90% 이상의 전환율을 보였다. 반면 dolomite와 olivine은 촉매를 첨가하지 않았을 때와 큰 차이가 없었으며, 156분 경과 후에도 모두 20% 이하의 전환율을 보였다.
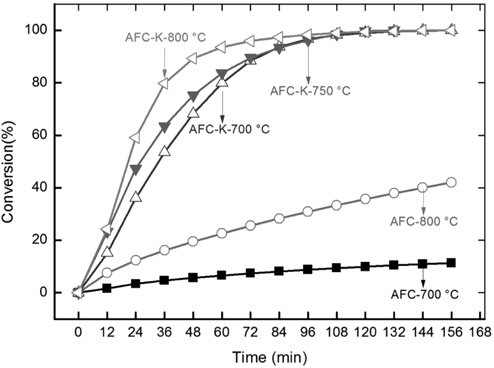
무회분탄의 촉매 가스화 시 온도의 영향을 관찰하였다. 가장 뛰어난 활성을 보인 K2CO3 10 wt%를 첨가한 무회분탄을 대상으로 700-800 ℃에서 실시하였으며 그 결과를 Figure 9에 나타냈다. 온도에 따라 초기 반응 속도에 차이를 보였다. 800 ℃에서는 48분만에 90% 이상의 전환율을 보였으며 700-750 ℃에서는 72분 경과 후 90%의 전환이 이루어졌다. 반면 Figure 9에 보이듯이 촉매가 없는 경우 800 ℃에서도 약 25% 만이 전환되어 촉매가 첨가된 경우와 큰 차이를 보였다. 반응성이 큰 저등급석탄인 삼화 원탄은 72분 경과 후 700 ℃에서 약 55% 보였다(Figure 5). 이후 72분에 약 90% 전환율을 보이고 96분에 반응이 완결된 무회분탄의 700 ℃에서의 촉매 가스화보다 느리게 전환되었다.
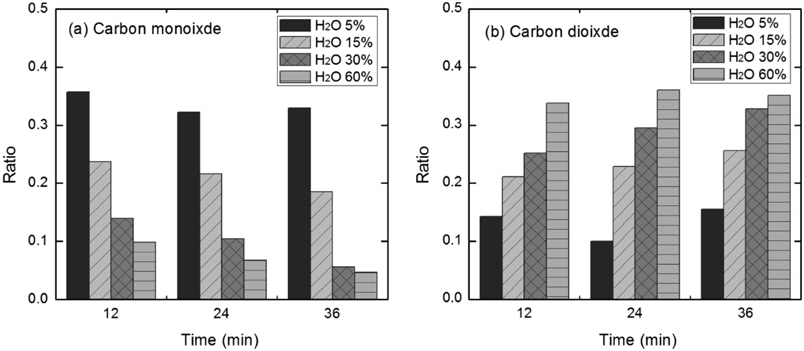
삼화 원탄의 가스화에서 반응물인 수증기 공급량을 다르게 하면 30 vol% 미만에서는 수증기 양에 비례하여 전환속도가 증가하다가 30-60 vol%에서는 포화되는 거동을 보였다(Figure 3). 이때 처음 36분 동안 CO와 CO2 생산 비율을 살펴보면 아래의 Figure 10과 같다. 36분 이후에는 30 vol% 이상의 경우 대부분의 시료가 소모되어 나타내지 않았다. 수증기 양의 증가에 따라 CO 비율은 평균 0.34에서 0.07로 감소한 반면 CO2 비율은 평균 0.12에서 0.35로 증가하였다. 수증기 공급량의 증가에 따른 CO 생성 비율의 변화는 30 vol% 이하에서는 매우 분명하게 나타났으나 30 vol%와 60 vol% 사이에는 비교적 적은 차이를 보였다. 그래프로 보여주지 않았으나 H2 생성비율은 5 vol%에서 30 vol%로 변화하면 평균 0.53에서 0.61로 점차 증가하였고, 60 vol%에서는 30 vol%와 유사한 값을 나타냈다. 이러한 생성 가스 조성의 수증기 공급량에 따른 변화는 수성가스전환[water-gas shift, CO + H2O ↔ CO2 + H2 (1)] 반응의 영향으로 생각된다. 수증기 함량 증가에 따라 WGS 반응물인 CO는 반응에 참여하여 소모되고 생성물인 CO2은 점차 증가했다. 추후 생성물의 조성은 반응물로서 수증기 함량의 조절을 통해 이루어 질 수 있음을 확인하였다.
공간속도가 15,000-30,000 h−1인 영역에서 수증기 가스의 공간속도를 줄였을 때 전환 속도는 증가하였다(Figure 4). 이는 반응물인 수증기와 석탄의 접촉시간 증가에 기인하며, 현재 시스템에서 가스화의 율속 단계는 확산(diffusion) 등의 외부 요인이 아닌 화학 반응 자체임을 확인할 수 있었다.
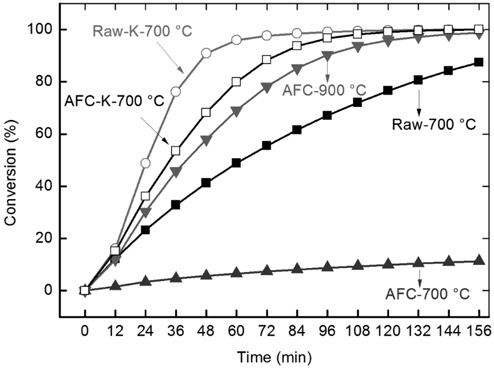
삼화 원탄과 무회분탄의 가스화 및 K2CO3에 의한 촉매 가스화 반응성을 비교하여 Figure 11에 나타냈다. 원탄의 700 ℃반응은 156분 경과 후 80% 이상의 전환율을 보인 반면 무회분탄은 약 10%를 보여 두 시료간의 반응성 차이를 뚜렷이 보여준다. 무회분탄은 900 ℃로의 승온에 의해서야 원탄의 700 ℃ 반응보다 높은 전환율을 나타냈다(Figure 7). K2CO3 도입에 의해 무회분탄의 700 ℃ 가스화 반응성은 크게 증가하여 원탄과의 차이를 줄였으며, 무회분탄의 900 ℃ 보다 높은 값을 보였다. 삼화 원탄과 같은 저등급석탄의 가스화 반응성은 산소 기능기의 양 증가에 의해 증가한다[22]. Table 1에 제시된 원소분석 결과는 원탄의 산소 함량은 23.5 wt%이고 무회분탄은 7.6 wt%임을 보여준다. 이러한 차이는 반응성이 높은 산소 기능기가 무회분탄 제조 시 300 ℃ 건조 공정 중 열분해에 의해 소모되었기 때문으로 생각되며, 이에 의해 반응성의 차이를 설명할 수 있다[23-25]. 또한 무회분탄의 화학적 조성은 추출조건에 의해 영향을 받는다고 알려져 있으며, 본 실험에서는 370 ℃라는 높은 온도에서 비극성 용매(1-methylnaphthalene)로 추출되어 비교적 높은 방향성(aromaticity) 및 낮은 H/C, O/C를 갖는 원탄 대비 반응성이 감소된 무회분탄이 얻어진 듯하다[26]. 이렇게 고등급석탄의 특징을 갖는 무회분탄은 구조가 상대적으로 더 조밀하여 반응물 및 생성물의 이동에 불리한 구조를 갖고, 이에 의한 반응 속도의 감소도 나타난 듯하다[27-29].
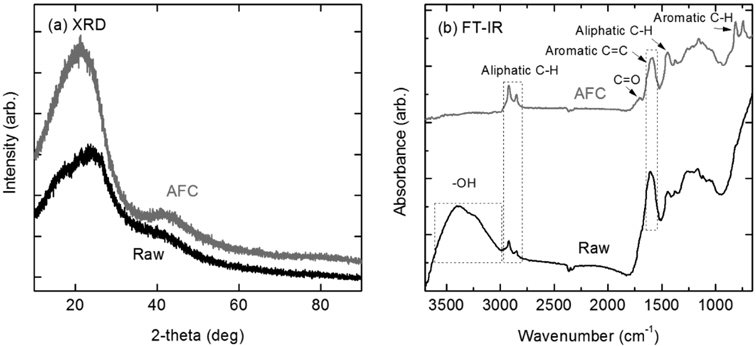
삼화 원탄과 무회분탄의 X-선 회절분석기(XRD) 및 분광광도계(fourier transform infrared spectroscopy, FT-IR) 결과를 Figure 12에 함께 나타냈다. 석탄에 포함된 대부분의 성분들은 무정형의 탄소 물질이므로, Figure 12(a)에는 XRD에서 얻어지는 일반적인 뾰족한 peak 대신 넓고 둥그스름한 패턴이 얻어졌다[30]. 여기서 2θ 값 26°과 43°에 나타난 peak는 많이 탄화된 흑연(graphite)에 기인하며, 무회분탄에서 원탄보다 peak 강도가 커졌다. 이는 무회분탄이 좀 더 탄화된 반응성 낮은 탄소 성분들로 구성되어 있음을 나타내며, Table 1의 분석 결과와 일치했다. 두 시료의 FT-IR 스펙트럼을 Figure 12(b)에 나타냈다. 카보닐(carbonyl)은 ~1,720 cm−1에서 두 시료 모두에서 관찰되었으나 하이드록실(hydroxyl)은 원탄에서만 ~3,500cm−1에서 관찰되었다. 지방족 C-H (~2,940 cm−1, ~1350 cm−1)와 방향족 C=C (~1610 cm−1)에 의한 흡수는 두 석탄에서 공히 나타났으나, 방향족 C-H (750-870 cm−1)에 의한 흡수는 무회분탄에서만 뚜렷이 나타났다[31]. 이것은 무회분탄의 높은 방향성(aromaticity)에 기인하였으며, 결국 낮은 가스화 반응성의 원인이 된 것으로 판단된다.
고체상 혼합에 의해 도입된 다양한 촉매들 중에서 K2CO3만이 높은 활성을 보였다(Figure 6, 8). 기 보고된 결과에 따르면 칼륨은 석탄 가스화 반응에서 가장 높은 활성을 보이며, 가스화 진행에 따라 이동성을 나타냄이 알려져 있다[32]. 본 실험을 통해 칼륨 촉매가 무회분탄의 가스화 속도를 고체 상혼합에 의해서도 크게 증가시킬 수 있으며(Figure 9), 회분에 의한 비활성화 염려 없이 촉매 재활용도 가능함을 확인하였다.
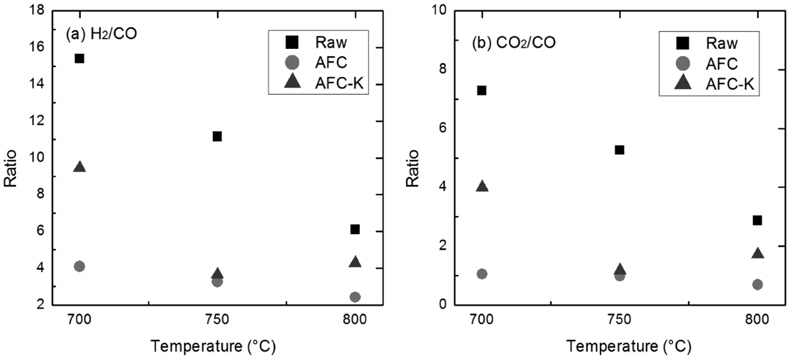
Figure 13에 보이듯이 가스화 생성물의 비율(H2/CO, CO2/CO)은 온도, 석탄의 종류 및 K2CO3 촉매 유무에 따라 달라졌다. 삼화 원탄에서 두 비율은 온도 증가에 따라 모두 감소하였다. 즉 H2/CO는 ~15 (700 ℃)에서 ~6 (800 ℃)으로, CO2/CO는 ~7 (700 ℃)에서 ~3 (800 ℃)으로 변하였으며, 이는 기존에 얻어진 경향 및 열역학적 계산과 비교적 일치하였다[27,33]. 삼화 무회분탄은 온도에 거의 영향 받지 않았으며, H2/CO는 4 이하의 값을, 그리고 CO2/CO는 2 이하의 값을 나타냈다. 이러한 거동은 주로 고등급석탄에서 관찰되며, 본 실험에서 제조된 무회분탄이 고등급석탄의 성질을 갖고 있음을 다시 확인할 수 있었다[34]. 무회분탄의 가스화 반응이 K2CO3에 의해 활성화된 경우 H2/CO 및 CO2/CO가 증가하였으며 또한 온도 의존성도 관찰되었다. 이러한 촉매의 영향은 기존의 관찰과 일치하였다[27]. 일반적으로 석탄의 가스화 반응은 탄소의 수증기 개질 반응(C + H2O ↔ CO + H2 (2)), 수성가스전환 반응 (1), 및 역 Boudouard 반응(CO2 + C ↔ 2CO (3))이 동시에 일어나며 H2, CO, CO2를 생산한다[35]. 온도 증가에 따라 (2)와 (3)의 정반응과 (1)의 역반응이 열역학적으로 우세하게 되어 H2/CO와 CO2/CO 비율을 감소시킨다. 무회분탄의 반응에 도입된 촉매는 수성가스전환 반응도 활성화하여 CO2 생성을 증가시키고, 동시에 CO를 줄임으로 Figure 13에 보이듯이 H2/CO와 CO2/CO 비율을 증가시킨 것으로 판단된다[36].
저등급석탄에 해당하는 삼화 원탄과 이 원탄에서 열적 용매추출법을 통해 회분이 제거된 무회분탄의 수증기 가스화 반응성을 평가하였다. 수증기 함량에 따라 삼화 원탄 가스화 생성물의 조성을 조절할 수 있으며, 율속 단계는 확산(diffusion)등의 외부 요인이 아닌 화학 반응 자체임을 확인하였다. 원탄은 700 ℃에서 무회분탄 대비 훨씬 높은 전환율을 보였는데, 이는 원탄의 높은 산소 함량과 낮은 탄화도에 기인함을 원소분석 및 XRD 결과에서 확인하였다. 고체상에서도 유동성을 갖는 K2CO3는 석탄의 종류에 상관없이 높은 활성을 보였다. 특히 무회분탄의 반응성은 K2CO3에 의해 급격히 증가하였는데, 이를 통해 회분에 의한 비활성화 없이 무회분탄의 저온 촉매 가스화 반응이 실현 가능함을 확인하였다.