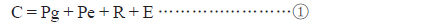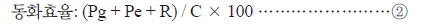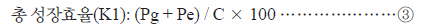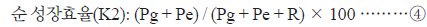Spiny lebbeid shrimp
동물의 에너지수지에 관한 연구는 에너지 흐름을 이해하고 동물생태계의 기능을 파악하는데 있어 유용한 수단이 된다. 생태계는 복잡한 먹이사슬 또는 먹이그물과 같은 영양적 구조로 집단 간의 에너지흐름의 양에 밀접하게 관련되어 있으며, 이러한 복잡한 먹이망 속에서 그 물질의 전환에 따른 에너지 흐름을 파악하기 위해서 에너지수지를 분석하는 것이 매우 중요하다 (Klekowski and Duncan, 1975). 어느 한 생물의 개체에 유입되는 모든 에너지는 열로써 상실하거나, 다른 영양 단계로 전이된다. 생물학적 물질계는 물질전환에 따른 에너지 흐름에 의해서 체계화되어 있다. 그리고 먹이사슬로 또는 먹이그물과 같은 영양적 구조는 집단의 에너지 흐름의 양에 밀접하게 관련된다. 그러므로 에너지 흐름의 파악은 자연집단의 에너지수지를 분석하는 것이 필요하지만, 우선 개체의 생활사에 따른 에너지수지를 정확하게 분석하는 것이 매우 중요하다(Park, 1989).
갑각류의 에너지수지에 관해서는 자연과 실험실 내 집단을 대상으로 많은 연구가 진행되어 있으며(Clutter and Theilacker, 1971; Levine and Sulkin, 1979; Emmerson, 1984; Harms, 1987; Kim and Chin, 1991), 성장, 산소소비, 질소배설 및 섭취에 대한 에너지 함량을 파악하여 에너지수지 방식을 통해서 그 영양적 체계를 구성해 볼 수 있다(Park, 1989). 동물의 에너지수지에 관한 연구는 다른 영양 단계 간의 에너지 전이유형을 이해하는 총체적 지표가 되며, 그 동물의 생산성과 생태적 효율을 예측하는 자료로서 유용하다(Vernberg and Vernverg, 1981).
가시배새우,
따라서 본 연구는 가시배새우 유생을 대상으로 성장, 탈피, 호흡, 섭취 및 에너지 함량을 측정하여 유생 발달 동안 에너지수 지를 분석하고 섭취와 성장에 따른 유생의 에너지 흐름의 경향을 파악함으로써 개체 및 개체군에 대한 생리적 기초 자료를 얻는데 그 목적이 있다.
실험에 사용한 가시배새우 유생은 평균 체장 117.22 mm, 중량 38.65 g의 모하로부터 얻었다. 내장을 제거한 민들조개,
초기 유생의 개체별 성장을 측정하기 위하여 수온 8±0.3℃, 250 mL 용기(사육수, 200 mL)에 수용한 후 부화 직후 유생을 1마리씩 수용하여
유생의 산소소비량은 250 mL 산소병에 가시배새우 부화 직후 유생을 5마리씩 수용한 후, 실험 전후 각 용존산소를 DO meter (YSI 556MPS, USA)로 측정하였고, 실험 전후의 용존산소차로써 정량하였다. 각 실험은 5회 반복한 평균치로 개체당 단위시간당 산소소비량을 μLO2/ind/day로 표시하였다. 산소소비량은 대사열 생산에 의해 소비된 에너지로 전환시키기 위하여 Gnaiger (1983)가 이용한 산소분자의 에너지 전화계수를 이용하였다(1 mgO2 = 3.38 cal). 대사에 쓰인 에너지는 4.71×10-3 cal/ μLO2의 변환계수를 사용하여 계산하였다. 개체의 산소소비량은 환경수의 산소 분압에 영향을 받기 때문에(Ikeda, 1974), 산소소비 측정이 끝날 때의 실험용기 내 용존산소량이 실험 시작시 산소량의 60% 이하로 떨어지지 않게 조절하였다.
유생의 섭취량 측정 시에는 250 mL의 용기에 가시배새우 유생을 1마리씩 수용한 후 일정량의 계수된
각 유생단계 및 전체 유생발생에 대한 에너지 수지는 Standard IBP 방정식(Klekowski and Duncan, 1975)으로 나타내었다.
①식에 C는 섭취에너지, Pg는 유생단계별 체성장에 쓰인 에너지, Pe는 탈피에 쓰인 에너지, R은 호흡에 쓰인 대사에너지, E는 대사산물인 뇨 배설에너지 그리고 대사되지 않고 배출되는분 배출에너지, 섭취에너지(C)와 동화에너지(A = Pg + Pe + R)간의 차로서 나타내었다(Dawirs, 1983).
수산동물의 동화효율 측정은 먹이섭취량과 분배출량을 측정하여 먹이섭취량에 대한 동화량을 백분율로 하여 동화효율을 구하였다. 가시배새우의 유생에 대한 섭취, 성장, 탈피 및 호흡을 측정한 자료를 사용하여 다음 효율들을 계산하였다.
②식은 섭취량 중 동화된 양의 백분율을 나타낸다.
③식은 섭취량 중 성장으로 전환된 양의 백분율을 나타낸다.
④식은 동화량 중 성장으로 전환된 양의 백분율을 나타낸다.
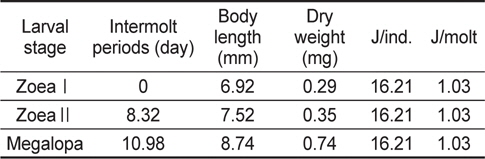
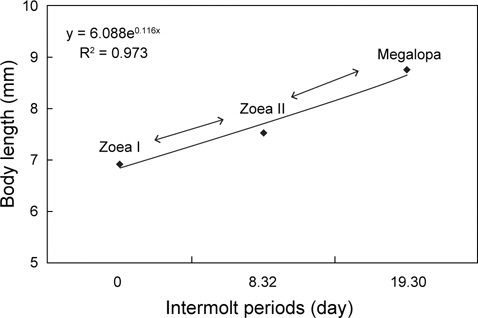
가시배새우의 부화 후 경과시간에 따른 유생(zoea I, II 및 megalopa)의 체장, 건조중량 및 유생과 탈피체의 에너지함량은 Table 1에 나타내었다. Zoea I기에서 megalopa기까지의 체장 성장은 지수적인 증가를 보였다(Fig. 1).
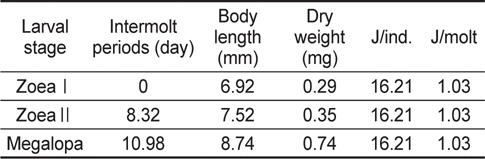
The intermolt periods, body length, body weight and energy contents of Lebbeus groenlandicus for the different larval stages
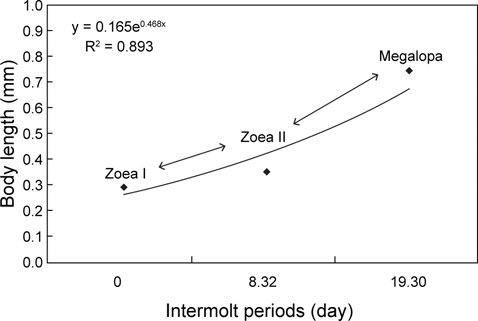
성장에 사용된 에너지 즉, 생체 에너지 함량은 J/ind.로 산출하였다. ZoeaⅠ기에서 megalopa기까지 성장하는 동안 megalopa기의 생체에너지는 16.21 J의 에너지를 체성장에 사용하였다. 성장에 수반되어 탈피체로 손실된 에너지는 탈피체 에너지함량을 J/molting body 로 계산하였는데, zoeaⅠ기부터 megalopa기까지 유생 1마리가 사용한 탈피에너지는 1.03 J이었다(Table 1). 체장성장과 건조중량은 경과 일수에 대해서 각각 y=6.088e0.116x (R2=0.973)와 y=0.165e0.468x (R2=0.893)로 나타났다(Fig. 1과 2).
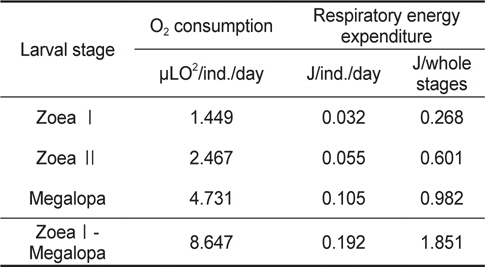
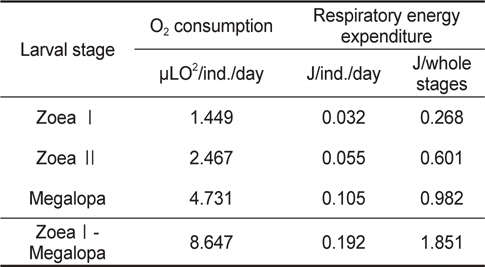
Individual oxygen consumption and respiratory energy expenditure of Lebbeus groenlandicus for the different larval stages
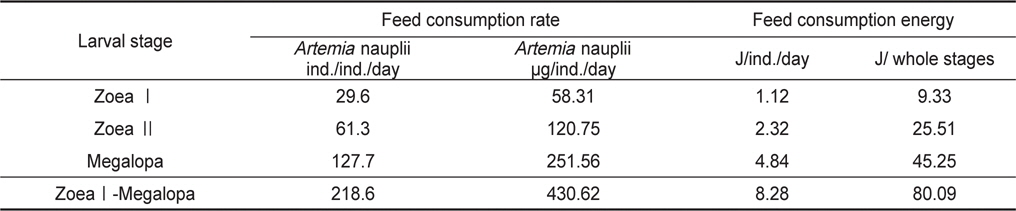
가시배새우의 zoea 유생들과 megalopa 유생들에 의해 섭취된 일간섭취량과 일간섭취에너지를 Table 3에 나타내었다. ZoeaⅠ기의 29.6
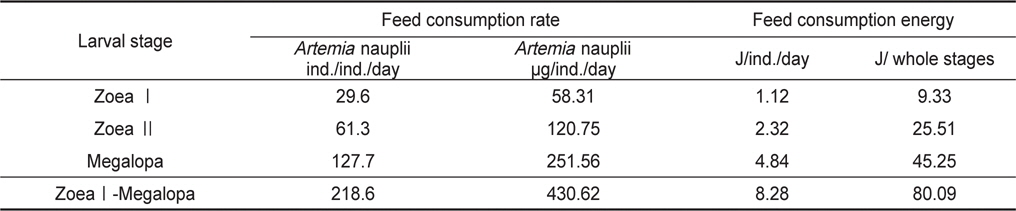
Consumption rate and consumption energy of Lebbeus groenlandicus for the different larval stages
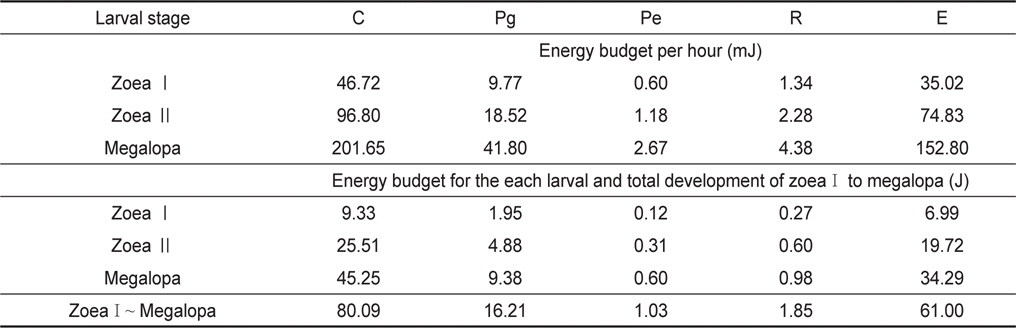
성장에 따른 전 유생기 동안의 유생의 성장 에너지함량(Pg) 및 탈피체의 에너지함량(Pe)은 Table 1에서 제시한 결과를 사용하였으며, 호흡 대사에너지(R)는 Table 2의 자료로부터 계산하였다. 그리고 섭취에너지(C)는 Table 3의 일간 섭취량과 일간 섭취에너지로부터 계산하였다. 뇨배설과 분배출에너지(E)는 섭취에너지(C)와 동화에너지(A)의 차이로서 계산하였다. 전 유생기 동안의 누적에너지수지를 Table 4에 나타내었다. 가시배 새우 유생의 섭취, 탈피체, 호흡 및 배설 에너지는 성장과 함께 증가하였다. ZoeaⅠ기에서 megalopa기까지의 총 누적 섭취에너지는 80.09 J이었으며, 이것은 성장에 16.21 J, 탈피체 손실에 1.03 J 그리고 호흡에 1.85 J의 에너지를 사용하며 뇨와 분으로 61.00 J의 에너지가 배설과 배출이 이루어지는 것으로 조사되었다.
[Table 4.] Energy budgets of Lebbeus groenlandicus for the different larval stages
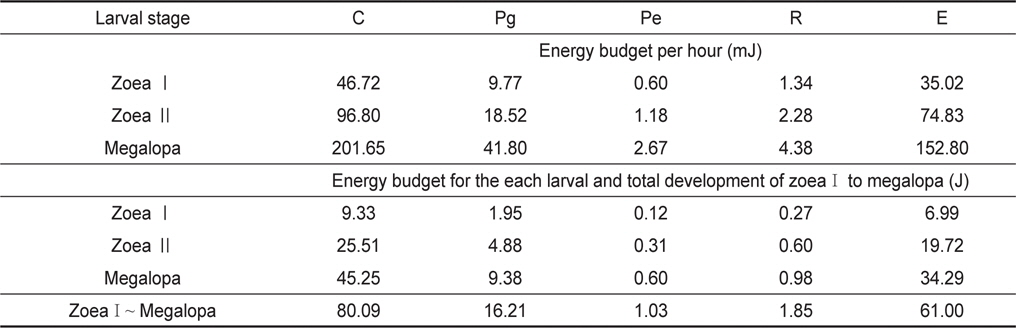
Energy budgets of Lebbeus groenlandicus for the different larval stages
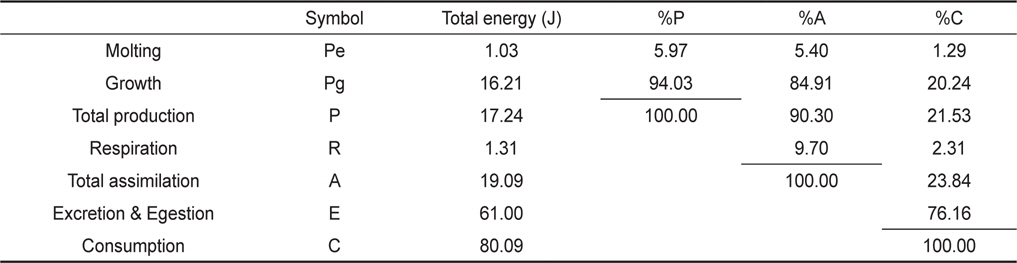
가시배새우 유생의 섭취, 성장, 탈피 및 호흡을 측정한 자료로부터 생태효율을 Table 5에 나타내었다. 유생의 동화효율은 19.09%이었으며, 총 성장효율(K1)은 21.53%, 순 성장효율(K2)은 90.30%로 나타났다. 각 에너지수지 구성요소들의 섭취에너지에 대한 백분율은 성장이 20.24%, 탈피체가 1.29%, 대사에너지가 2.31% 그리고 뇨와 분으로 76.16%를 각각 차지하였다. ZoeaⅠ기부터 megalopa기까지의 총 동화에너지는 전체 섭취 에너지의 23.84%인 19.09 J이었으며, 각 에너지수지 구성 요소들이 동화에너지에 대한 백분율은 성장이 84.91%, 탈피체가 5.40% 그리고 대사에너지가 9.70%를 각각 차지하였다. 또한 zoeaⅠ기에서 megalopa기까지의 총생산에너지는 총 동화에너지의 90.30%, 총 섭취에너지의 21.53%인 17.24 J이었으며, 이것은 성장이 94.03%, 탈피체가 5.97%를 각각 차지하였다.
[Table 5.] Accumulative energy budget of Lebbeus groenlandicus larvae
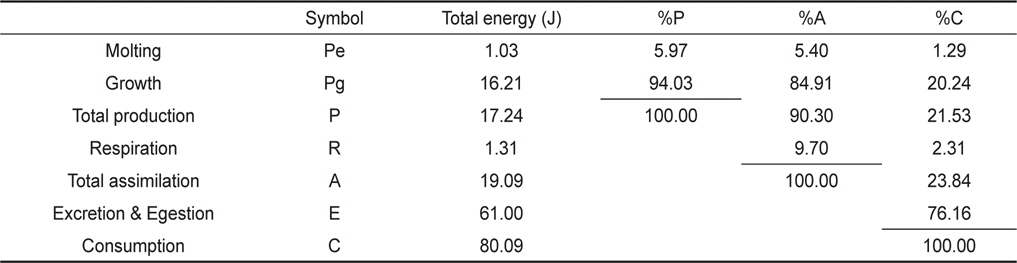
Accumulative energy budget of Lebbeus groenlandicus larvae
해산동물의 에너지 흐름을 파악하기 위해서는 사전에 그 생물의 생활사를 정확하게 조사하는 것이 필요하다. 갑각류의 성장 은 환경에 따라 다양한 반응을 보이지만(Hartnoll and Dalley, 1981), 특히 섭취, 성장 및 대사율은 생육단계별로도 많은 변동을 보이는 것으로 알려져 있다(Reeve, 1969; Hiroko et al., 1990).
십각목 갑각류 유생의 성장은 일반적으로 지수적 성장을 나타낸다(Mootz and Epifanio, 1974; Logan and Epifanio, 1978; Johns and Pechenik, 1980; Stephenson and Knight, 1980; Dawirs, 1983). 본 연구에서 실내 사육한 가시배새우의 유생성장은 지수적 성장을 보였으며, Park (1989)의 실험실 내에서 사육한 보리새우,
가시배새우 유생의 산소소비량은 체중이 유생발육이 진행될수록 증가하였다. 이는
수서무척추동물은 동화에너지의 거의 2/3를 호흡에 사용하는 것으로 알려져 있고(Clutter and Theilacker, 1971), 특히 생물에 있어서 호흡을 통한 대사에너지는 에너지수지 구성 요소 별 사용에너지의 백분율에 많은 변동을 야기 할 수 있다. Chin et al. (1992)은 호흡열 상실에 따른 에너지 계산은 동물이 서식지에서 경험하는 수온 범위 내의 여러 수온구에서 산소소비량을 측정하고, 이 결과로부터 얻어진 수온 및 체중과 상관관계를 갖는 산소소비량 회귀식을 적용하는 것이 생물의 호흡을 통한 대사에너지에 대한 이해도를 높일 수 있는 방법이라고 제안하였다.
가시배새우 유생의 섭취량은 Park (1989)이 보고한
가시배새우의 총 성장효율(K1)은 21.53%로
대사활동 과정에서 에너지의 소비는 에너지수지로 구체적으로 설명된다(Adams and Breck, 1990). 다양한 생물학적, 물리적, 화학적 조건 하에서 오는 에너지수지에 관한 생체역학 모델구축(Bartell et al., 1986)을 위한 일환에서 본 연구의 가시배새우 유생 에너지수지에 대한 구체적인 정보는 매우 유용하게 활용될 것으로 판단된다.