To determine an efficient growth system for algal cultivation and to develop adequate culture system utilizing LED light, we investigated the effects of fluorescent and light emitting diode (LED) light source on the growth of
해조류는 해양생태계 내에서 일차생산자로서 이산화탄소를 흡수하여 태양광을 에너지원으로 광합성을 수행하며, 빛에 민감하게 작용한다. 또한 유영생물 및 무척추동물의 산란처와 서식처로 중요할 뿐만 아니라, 열대 우림에 비해 대기 중 이산화탄소 흡수 능력이 2-5배 정도 높고, 연안 오염물질의 정화 기능 등 지구 환경과 해양생태계에서 매우 중요한 역할을 담당하고 있으며, Alginic acid, carrageenan, agar 등의 산업소재 및 식품첨가물로 이용되어온 천연자원임과 동시에 최근 다양한 신물질의 원천 생물로 가치가 급증하고(Gram et al., 2009), 해양바이오매스 및 신재생에너지 개발 등 바이오산업소재로서 중요성이 부각되고 있다(Han, 2008).
해양의 기초생산자인 해조류에게 빛은 광합성을 위한 원동력이다. 특히 빛의 파장이나, 조성은 세포의 색소, 화학적 조성, 이온수송 및 생장속도에 관여하는 등 해조류의 생리적인 측면을 조절하는 중요한 요인으로 알려져 있다(Wallen and Green, 1971; Vesk and Jeffrey, 1977; Rivkin, 1989; Schmid and Dring, 1993). 이와 같이 광원 및 광량은 해조류가 광합성을 함에 있어서 가장 중요한 인자로 인식되고 있다. 배양의 형태 및 목적에 따라 사용하는 광원은 차이가 있지만 일반적으로 태양광이나 형광등, 메탈등, 수은등이나 백열등과 같은 일반광을 가장 많이 사용한다. 그러나 일반광은 높은 유지비용 및 과도한 열의 발생으로 인해 최근 광원으로 연구되고 있는 발광다이오드(Light-Emitting Diode: LED)나 광섬유(Optical fibar)에 비하여 배양 효율 및 경제성이 낮은 것으로 인식되고 있다(Chen et al., 2008; Heo et al., 2002). 발광다이오드(LED)는 기술 및 연구개발을 통하여 기존 조명보다 고효율, 저전력소비, 환경친화적으로 발전되고 뛰어난 내구성 및 견고성을 갖추어 다양한 산업에 이용되고 있으며, 빛을 필요로 하는 다양한 분야에 응용이 가능하다. 뿐만 아니라 식물의 광합성 및 생장에 필요한 파장을 분리하여 단일사용 하거나 혼합 사용하는 등 임의로 조절이 가능하며, 조명시간 동안 분 단위 또는 초단위로 점등 시간의 조절이 가능하다. 또한 발광다이오드는 광량개선과 함께 기존 조명의 광원과 같은 연색지수(Color Rendering Index: CRI)와 온도(Correlated Color Temperature: CCT) 특징을 갖추고 있어, 광량 효율이 향상된 제품들이 출시되고 있다. 따라서 에너지 절감 효과 및 환경보전 측면에서 미국 유럽 등 선진국에서는 국가적 수행과제로서 발광다이오드 광원 개발 비중이 급속도로 높아지고 있다. 현재 발광다이오드를 인공 광원으로 이용한 연구는 식물재배와 미세조류 배양 및 생장에 이용되고 있으나(Barta et al., 1992; Kawai et al., 1996; Lee and Palsson, 1994; Oh et al., 2007), 해조류에 기술을 적용한 연구 사례는 없었으며 연구개념 조차 제시되지 않은 실정이다. 따라서 본 연구는 해조류의 생장에 미치는 광의 영향을 연구하기 위하여 실내배양 실험을 통해 생장 특성을 비교하였다. 여기서 도출된 결과를 분석하여 해조류 배양에 효율적인 생장 시스템을 탐색하고, 발광다이오드(LED) 광원을 활용한 효율적인 배양 시스템 개발을 위한 기초자료 확보차원에서 본 연구를 수행하였다.
연구대상 시료인 녹조 구멍갈파래(

Indoor culture condition used to influence of temperature, light source, light intensity, photoperiod and culture medium
광원에 따른 생장 변화를 알아보기 위하여 배양 후 1 주일 간격으로 엽체의 길이를 측정하였고 그 결과를 이용하여 상대생장률(RGR, Relative Growth Rate)을 아래의 식을 이용하여 계산하였다(Rueness and Tananger, 1984; Beadle, 1993). RGR = (ln Xt2 – ln Xt1) / T2 – T1 여기서
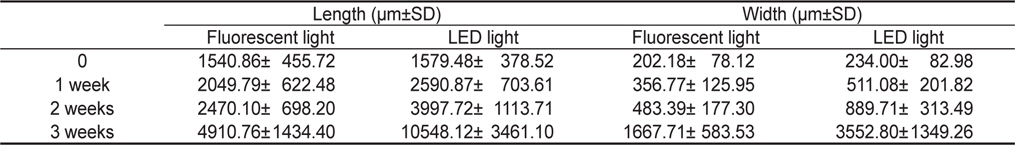
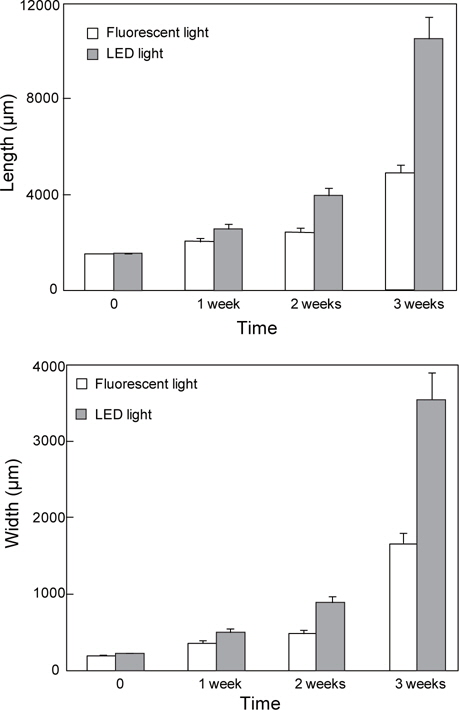
실험에 사용한 어린 엽체의 체장과 엽폭은 형광등의 경우 체장 1540.86±455.72 μm, 엽폭 202.18±78.12 μm 였고, LED조명에서는 체장 1579.48±378.52 μm, 엽폭 234.00±82.98 μm이였다. 배양 1 주 후 형광등 조건에서 엽체 체장은 2049.79±622.48 μm, 엽폭 356.77±125.95 μm로 생장하였으며, LED 조명 조건에서 체장과 엽폭은 2590.87±703.61 μm, 511.08±201.82 μm로 각각 측정되었다. 배양 2주 후 엽체의 체장과 엽폭은 일반광에서 2470.10±698.20 μm, 483.39±177.30 μm로, LED에서 3997.72±1113.71 μm, 889.71±313.49 μm를 나타냈으며, 3주 후에는 형광등 조건에서 체장 4970.76±1434.40 μm, 엽폭 1667.71±583.53 μm, LED 조명 조건에서 체장 10548.12±3461.10 μm, 엽폭 3552.80±1349.26 μm로 나타났다(Table 2, Fig. 1).
[Table 2.] Ulva pertusa. Changes on length and width under two light system
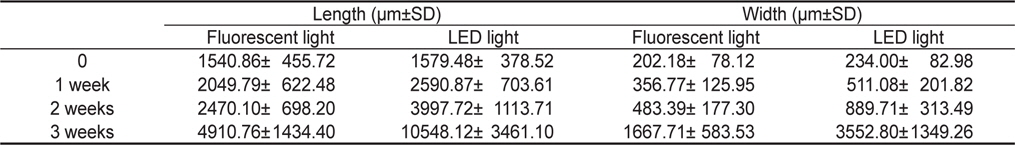
Ulva pertusa. Changes on length and width under two light system
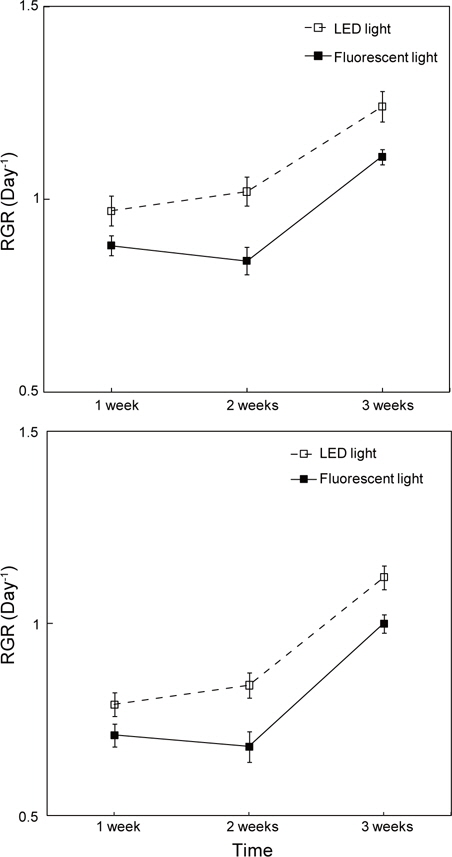
광조건에 따른 구멍갈파래의 상대생장률(RGR)을 살펴보면, LED 조명 배양 조건에서 체장 생장률은 0.99-1.26 day-1, 엽폭의 생장률은 0.8-1.13 day-1로 나타났으며, 일반광 에서의 체장과 엽폭 생장률은 0.89-1.11 day-1, 0.72-1.01 day-1로 각각 조사되었다. LED 조명하에서는 체장과 엽폭의 상대생장률이 전 배양기간에 걸쳐 증가하는 경향을 나타내고 있으나, 형광등 배양 조건에서는 배양 2주 후에 정체기를 나타내지만 이후 증가하는 양상을 보였다(Fig. 2).
해조류의 생장과 성숙은 다양한 환경조건(수온, 광, 영양염, 섭식, 경쟁)의 영향을 받는 것으로 알려져 있으나(Lüning, 1990; Pizaro and Santelices, 1993), 그 중 수온과 광이 가장 중요한 제한 요인으로 밝혀져 있다(Druehl et al., 1987; Vásquez and Vega, 2001). 광원이 해조류의 생장에 미치는 영향에 관한 이전 연구는 단일파장을 이용한 실험이 대부분이다. Mercada et al., (2002)은 홍조류
본 연구에서는 파장에 따른 구멍갈파래의 생장 실험이 수행되지 않아 어떤 파장이 생장에 중요하게 기여를 하는지 확인하지 못하였다. 그러나 온도, 광주기와 광량이 동일한 조건하에서, LED 조명을 사용한 실험구에서 배양 1 주 후 형광등 조건의 엽체에 비해 체장은 1.9배, 엽폭은 1.5배 크게 생장하는 것으로 나타났다. 또한, 2주 후의 체장과 엽폭은 각각 2.6배, 2.0배, 3주 후 체장은 1.7배, 엽폭은 1.2배 크게 생장하는 것으로 확인되어 형광등 조건에 비해서 LED 조명이 생장에 더욱 효율적이라는 연구 결과를 얻을 수 있었다. 가시광선과 자외선을 이용한 해조류 생장에 대한 연구결과에서, 구멍갈파래의 어린 발아체는 청색광에서 가장 효율적이라고 보고된 바 있다(Han et al., 2004). 본 연구에 사용된 형광등과 LED 조명은 복수파장으로서 모두 청색파장을 포함하고 있다. 따라서, 이번 연구결과에서도 청색파장이 생장률에 영향을 준 것으로 예상되며, LED 조명 내 청색파장이 구멍갈파래의 광합성 과정에 긍정적 작용을 한 것으로 판단된다.
본 연구는 녹조류 구멍갈파래를 이용하여 광원에 따른 해조류의 생장 반응을 규명하기 위한 연구로 해조류 배양과 해조류 종묘의 대량 생산시 인공광원으로 LED 조명을 적용할 수 있는가에 대한 기초 자료를 제공하기 위하여 수행하였다. 추후에 해조류를 대상으로 각각의 개별 파장에 대한 연구가 수행된다면, 새로운 광원으로 사용될 수 있는 LED가 해조류의 생장과 관련된 다양한 생리학적 기작을 명확하게 설명 할 수 있을 것으로 기대된다.