We examined the effect of starvation on the occurrence of tunic softness to determine the cause of mass mortality of cultured
우리나라의 전 연안에 분포하고 있는 멍게류는 약 20여종이 있으며(Hong, 2006), 이들 중 식용으로 활용되는 것은 멍(우렁쉥이), 돌멍게, 붉은멍게, 주름미더덕, 개멍게, 미더덕 등이며. 이중에서 산업적으로 양식이 되고 있는 것은 멍게, 주름미더덕 그리고 미더덕으로 특히 멍게가 남해안과 동해안을 중심으로 많이 양식되고 있다.
멍게생산량은 2004년 7,464톤, 2010년에 6,300톤 및 2012년 9,030톤으로 2000년 이후 해마다 7,000-8,000톤 정도를 나타내고 있으며(KOSIS, 2013), 반면 멍게 폐사 현황은 2005년 57.6%, 2006년 68.0%, 2008년 80.4% 그리고 2009년에는 67.5%으로 추정하고 있으며, 피해금액은 약 200억 원 이상으로 추정되고 있다(NEMA, 2012). 멍게의 폐사는 피낭이 연화되고 수관부의 수축반응이 감소하는 현상인 물렁증과 여름철에 주로 발생하는 쪼그랑증으로(Hur, 2009) 나타나고 있다. 이 가운데 대량 폐사의 주요인은 물렁증에 기인(Shin et al., 2011; Kim et al., 2012)하는 것으로 보고되고 있다.
멍게에 관한 연구는 국내에서는 양식기술개발에 관한 연구가 주로 보고되고 있으며, 형태변화 및 발생(Hirai, 1941, 1965), 유생의 부화율과 변태(Yoo et al., 1990), 초기성장(Jang, 1979), 성장(Yoo et al., 1988) 등 다양하게 보고되고 있다. 그러나 생태생리에 관한 연구는 중금속 축적(Kim et al., 2001), 수온, 염분과 용존산소의 영향(Shin et al., 2007; Na et al., 1991; Hong et al., 2000) 및 에너지수지(Shin et al., 2011) 등으로 주로 폐사와 관련한 내용들이다. 국외 연구는 주로 미더덕을 포함한 피낭류에 관하여 에너지수지(Jiang et al., 2008) 일주리듬(Ryland, 1990) 및 먹이 흡수효율(Armsworthy et al., 2001) 등 다양한 분야에서 연구되고 있다. 한편 대량폐사의 원인이 되고 있는 멍게류의 물렁증에 관한 연구는 일본에서 멍게
일반적으로 수온, 염분, 용존산소 등 해양 환경의 요인들은 연안에 서식하고 있는 양식 생물의 생리적 과정에 영향을 미치며(Bohle, 1972; Widdows, 1985), 고수온, 저염분 및 빈산소 등 계절적으로 발생하는 극단적인 해양 환경의 변화에 의해 연안양식 생물의 대량 폐사가 발생하기도 하고 생산량의 변동이 발생하기도 한다. 또한 수서생물의 생리적 상태는 그들의 영양조건 및 영양 섭취상태에 달려있다. 그러나 양호한 생리적 상태를 유지하고 개선하기 위한 요인으로서 영양의 중요성을 간과하기 쉽다. 최근 환경변화 및 생리적인 변화에 따른 대량폐사를 사전에 방지하기 위해 사전 예측 기법으로 생물의 건강도 평가의 중요성이 부각되고 있다. 건강도 평가방법으로 RNA와 DNA 정량 및 비율분석(Clemmesen, 1993, 1994)이 이용되고 있으며, RNA는 먹이섭취의 양과 질 및 환경에 따라 변동하며 DNA는 생체량 또는 세포수를 반영하는 지표로 먹이를 섭취못하거나 환경변화에 대하여도 비교적 일정한 값을 보이므로(Clemmesen, 1993, 1994) 먹이와 관련한 지표로 많이 이용된다
남해안에서 양식하고 있는 멍게의 물렁증 발생 및 폐사요인은 장기간 양식으로 인한 양식장 환경악화 및 연안오염, 환경 변동으로 인한 생리적인 스트레스와 밀식에 의한 조류소통 및 먹이부족 등으로 보고(Chang et al., 1982; Jung et al., 2001)되고 있다. 그러나 최근 물렁증 발생의 원인은 기생충(Shin et al., 2011) 및 세균감염(Kim et al., 2012)으로 보고되고 있어 이를 더욱 가속화 할 수 있는 환경요인을 찾을 필요가 있을 것으로 여겨진다 .
본 연구는 물렁증이 주로 발생하는 수온구에서 먹이를 절식하여 물렁증 발생 여부를 관찰하였으며, 외부형태적 변화 및 건강성 및 조직학적 반응을 조사를 통하여 절식에 따른 물렁증발생 가능성을 분석하였다.
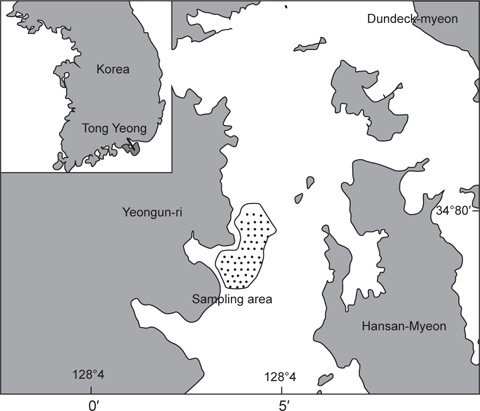
실험에 사용된 멍게는 2011년 5월부터 2012년 10월 동안 경남 통영시 영운지선 양식장(Fig. 1)에서 양성중인 멍게를 직접 채취한 후 즉시 실험실로 운반한 후, 유수식 5 m3 사육수조에 수용하여 일주일간 순치 시킨 후 실험에 사용하였다. 순치기간 중 먹이는 매일 2회씩 시판중인 복합규조류를 공급하였다. 수온은 순치기간 동안 실온을 유지하였으며, 염분 33.5±0.5 psu, 용존산소 7.7±0.5 mg/L을 유지하였다. 각 실험에 사용된 멍게는 순치중인 건강한 개체를 선별하여 사용하였으며, 평균체고 72.10±7.08 mm, 평균체폭 42.81±6.38 mm, 평균습중량 73.69±16.12 g 였다. 건강한 멍게의 판정은 자극에 대한 수관부의 반응이 1-2초 내에 나타나며, 돌기가 수직으로 뽀족하고 피낭 색이 선명한 것을 기준으로 선택하였다.
절식에 따른 멍게의 물렁증 발생을 조사하기 위해 수온 8±0.5, 12±0.5℃, 15±0.5℃ 및 실온(대조구, 15±0.5℃), 염분 33.5±0.5 및 용존산소 농도는 7.7±0.5 mg/L에서 수행하였다. 실험은 지수식 및 순환여과식으로 행하였으며, 실험수온은 냉각기와 히터를 이용하여 조절하였다. 대조구는 매일 2회씩 시판중인 복합규조류를 먹이로 제공하였다. 절식은 여과해수(ø 1 μm)에서 먹이를 공급하지 않고 35일간 사육하면서 물렁증 발생여부를 관찰하였다. 생존율은 12시간 간격으로 냄새를 맡거나 수관부의 수축반응 등을 통해 파악하였으며, 반응이 없을 시죽은 것으로 간주하였다. 물렁증 발생 여부는 냄새, 수관부의 수축반응, 피낭의 연화상태, 피낭돌기의 탄력 및 피낭색을 관찰하여 물렁증 발생 여부를 분석하였다.
멍게의 건강도를 분석하기 위하여 RNA/DNA 반응 변화 및 조직학적 분석을 수행 하였다. RNA/DNA 농도 반응은 부위 별로(간췌장, 아가미, 육질)분리하고 RNA농도, DNA농도를 분석하였다. RNA/DNA 분석은 -70℃에서 동결건조 시킨 후(18시간), 마쇄(TE-SDS용액 400 μL)하여, 원심분리(4℃, 1시간) 한 후 상등액을 이용 595 mm에서 형광광도계(Fluoroskan Ascent FL)로 DNA와 RNA양을 측정하였으며, 20 μL RNAse를 첨가하여 RNA를 분해한 후 그 차이를 DNA양으로 계산하였다.
조직학적 분석을 위하여 각 환경요인에 노출시킨 후 채취한 시료는 vernier calipers와 전자저울로 측정형질을 계측한 후 해부하여 육안과 해부현미경을 통하여 해부학적 특징을 기재하였다. 그리고 피낭, 수관부, 새낭, 육질부 및 소화선을 적출하여 조직학적 분석을 실시하였다. 광학현미경 표본제작은 시료를 Bouin 용액에 24시간 동안 고정하여 파라핀절편법으로 5 μm 두께로 연속절편 후 Mayer's hematoxylin-eosin (H-E) 염색과 Alcian blue-periodic acid and Schiff's solution (AB-PAS, pH 2.5) 반응을 실시하였다.
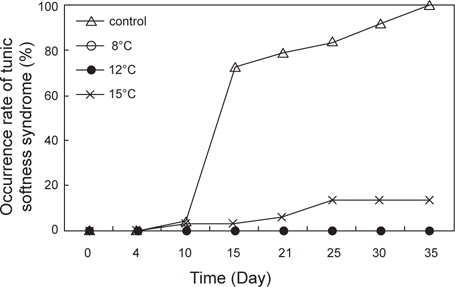
수온 8±0.5, 12±0.5℃, 15±1℃ 및 대조구(실온)에서 35일간 절식시킨 멍게의 생존율과 물렁증 발생률을 Fig. 2와 Fig. 3에 나타내었다. 수온 8 ±0.5℃와 12℃±0.5℃에서 생존율은 100%였으며, 수온 15±0.5℃에서는 노출 10일째부터 폐사가 발생하기 시작하여 노출 35일째 생존율은 50%를 나타내었다(Fig. 2). 반면 먹이를 공급한 대조구에서는 노출 15일째 생존율이 급격히 감소하기 시작하여 35일째 모두 폐사하였다 (Fig. 2). 절식에 따른 물렁증 발생률은 노출 35일째 대조구에서는 100%, 수온 15±0.5℃에서 15%를 나타내었으며, 수온 8±0.5℃와 12±0.5℃에서는 물렁증 발생이 관찰되지 않았다.
물렁증이 주로 발생하는 수온 8℃, 12℃, 15±0.5℃ 및 대조구(15±0.5℃)에서 35일간 절식시키는 동안 멍게의 형태적인 변화를 Fig. 4에 나타내었다. 먹이를 공급한 대조구에서는 멍게의 피낭 및 피낭색의 뚜렷한 형태적인 변화가 관찰되지 않았다. 그러나 절식시킨 모든 시험구에서는 피낭이 수축되어 쪼그라들어 크기가 작아졌으며, 피낭색은 진한 붉은 색으로 변하는 것이 관찰되었다. 그러나 절식에도 불구하고 실험 기간 동안 구근이 계속 자라는 것이 관찰되었다.
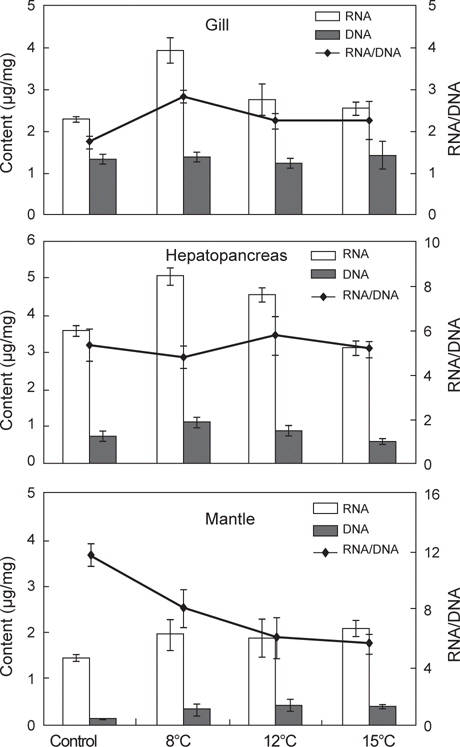
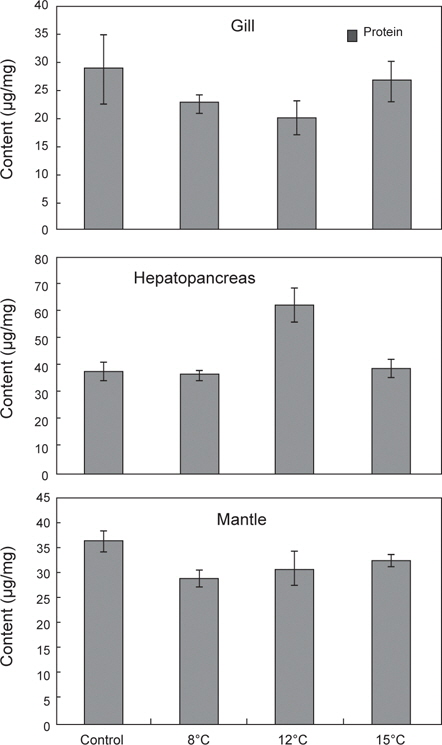
35일간 절식시킨 멍게의 각 부위별 RNA/DNA 농도 및 단백질 함량 변화를 조사하였다(Fig. 5). RNA/DNA 농도비는 아가미와 간췌장에서 수온 8±0.5℃ 높았으나 단백질 함량은 낮게 나타났다. 소화기능과 관련된 간췌장에서는 수온 12±0.5℃에서 단백질 함량이 가장 높았으나, 그 외의 수온에서는 유사한 값을 나타내었다.
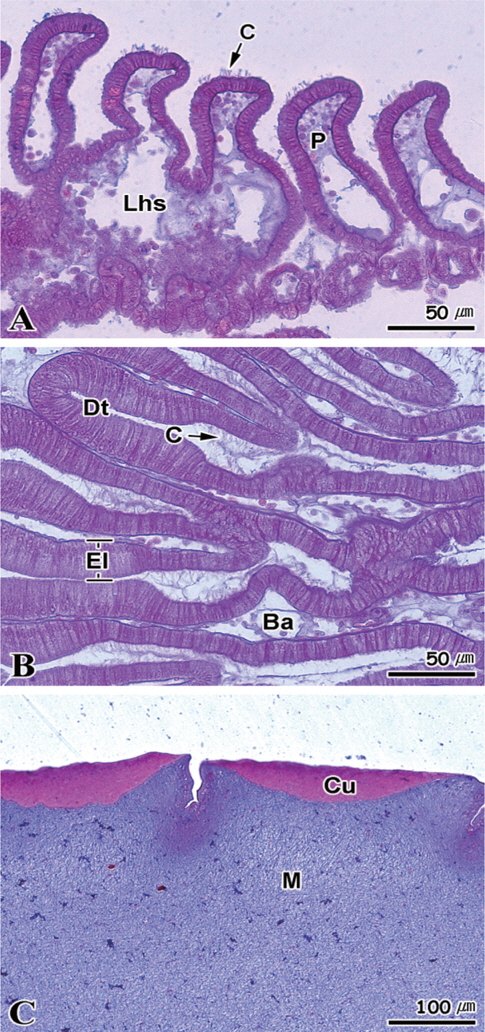
각 실험수조에서 대조구와 35일 동안 절식시킨 멍게의 새낭, 소화선과 피낭에 대한 조직학적 반응을 Fig. 7-10에 나타내었다. Fig. 7은 정상멍게의 기관별 조직학적 반응을 나타낸 것이다. 새낭은 다수의 새낭돌기(papillae)들이 일렬로 배열되어 있으며, 새낭돌기 내부는 혈구들이 존재하는 혈림프동이 관찰되었다. 새낭돌기의 정단부에는 다수의 섬모들이 존재하고 있었으며, 새낭의 상피세포층은 단층의 원주형상피세포로 구성되어 있었다(Fig. 7A). 소화선은 위와 장의 전단부 외벽 바깥에 망상구조를 형성하는 기관으로 다수의 소화선세관(digestive tubule)과 맹낭(blind ampulla)들로 이루어져 있으며 도관을 통하여 위와 연결 된다. 상피세포들은 단층의 원주형섬모세포로서 자유면에는 섬모들과 다수의 미세융모(microvilli)를 가지며, 세포질에는 글리코겐 과립들을 함유한다(Fig. 7B). 멍게 피낭은 외부로부터 큐티클(cuticle), 기질(matrix)로 구성되어 있으며, 다수의 주름들이 존재하고 있었는데 주름의 정단부에는 반원모양의 큐티클층으로 이루어져 있었다. 큐티클은 얇은 막구조로서 비세포성 층이다(Fig. 7C).
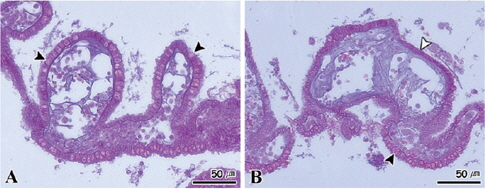
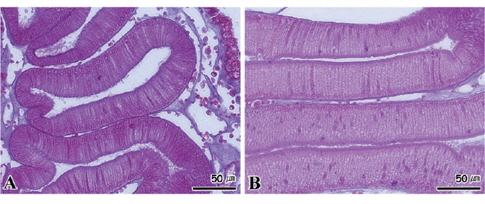
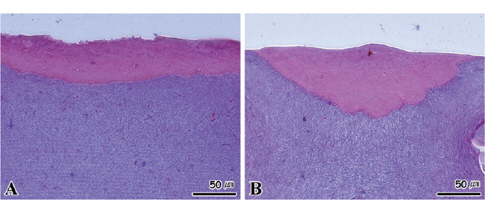
수온 8℃와 15±0.5℃에서 절식한 멍게의 새낭은 상피세포가 비대해지면서 세포의 길이가 다소 짧아지는 조직상이 관찰되었다(Fig. 8A). 15℃에서 절식한 멍게의 새낭의 경우에는 상피세포의 비대와 함께 세포의 괴사가 진행되었다(Fig. 8B). 반면 절식 기간 동안 소화선과 피낭은 모든 수온 농도구에서 특이적인 조직병리학적인 증상이 나타나지 않았다(Fig. 9, 10).
멍게 대량폐사의 주요 원인은 여름철 고수온과 먹이생물 부족(Chang et al., 1982; Hong et al., 2000), 고수온에 의한 대사장애(Na et al., 1991) 및 급격한 수온변동에 따른 생리적 스트레스(Hong et al., 2000)등의 주로 환경요인에 기인하는 것으로 보고되어 왔다. 그러나 멍게의 폐사현상은 1970년대 중 후반에는 주로 여름철에 폐사로 이는 고수온과 저비중, 빈산소(Chang et al., 1982)등에 기인한 것으로 추정하고 있다. 그러나 1990년대 후반부터 발생하고 있는 멍게의 폐사증상은 피낭이 연화되는 물렁증 현상으로서 주로 저수온기인 12월에서 이듬해 6월까지 고수온기 이전에 발생하고 있으며 최근 원인체는 편모충(Shin et al., 2011) 및 세균에서 분비되는 대사물질(Kim et al., 2012)으로 외부 감염에 의한 증상으로 보고되고 있어 양식장 환경의 중요성이 강조되고 있다. 또한 Moon at al. (2003)에 의하면 물렁증은 주로 먹이생물 발생량이 높고 생육상태가 양호한 내만 양식장에서 많이 발생하는 것으로 보아 단일의 물리환경적인 요인으로 보기 어렵다고 추정하고 있어 물렁증 발생과 먹이부족간의 관계는 매우 모호하다.
수서생물의 생리적 상태는 그들의 영양조건 및 영양 섭취상태에 달려있다. 그러나 양호한 생리적 상태를 유지하고 개선하기 위한 요인으로서 영양의 중요성을 간과하기 쉽다.
물렁증 발생률이 높은 수온 8℃, 12℃ 및 15℃에서 먹이를 공급하지 않은 그룹과 실온(15℃)에서 먹이를 공급하며 사육한 대조구에서 멍게의 물렁증 발생을 관찰한 결과, 절식에 따른 물렁증 발생률은 수온 15℃에서 노출 35일째 15%를 나타내었으며, 수온 8℃와 12℃에서는 물렁증 발생이 관찰되지 않았으며, 절식기간이 길어질수록 피낭이 수축되며 색깔이 짙어지는 것이 관찰되었다. 또한 통영 주변 멍게 양식장의 식물성플랑크톤 발생 변동 조사결과 물렁증 발생이 심한 곳에 비해 물렁증 발생이 적은 양식장에서 플랑크톤의 발생이 낮았으며, 영양염의 농도도 낮았다(Hur, 2009)는 보고에 따라 먹이 부족에 의해 체내 보유물이 에너지원으로 이용되어 성장이 저하되면서 피낭의 수축이 발생하는 것으로 보인다. 특히 멍게 물렁증 원인체가 양식장 주변해역 및 저질에서 유래하는 감염성 세균 및 기생충이므로 먹이가 풍부한 해역에서 증식할 수 있는 가능성이 크므로 빈영양염 해역에 비해 물렁증 감염률이 높아 폐사율이 증가할 수 있을 것으로 여겨진다.
최근 수서생물의 건강도 지표로서 글리코겐 함량 또는 RNA/DNA ratio 등이 유용하게 이용되고 있다. RNA/DNA ratio 는 생물의 영양과 성장을 나타내는 유용한 지표로 많이 연구 (Clemmesen, 1993, 1994)되어 오고 있다.
본 연구에서 35일간 절식시킨 멍게의 각 부위별 RNA/DNA 농도 및 단백질 함량은 아가미와 간췌장에서는 뚜렷한 반응을 나타내지 않았다. 반면 근육부분에서는 RNA/DNA 농도와 단백질 함량은 먹이를 공급한 대조구에서 높게 나타났으며, 절식한 그룹에서 낮았다. 이는 절식한 그룹에서 피낭이 수축하는 현상과 관계가 있을 것으로 여겨진다. 즉 멍게의 피낭기질은 주로 단백질성 셀룰로오즈 섬유질로 느슨하게 구성되어 있어(Hirose et al., 2009) 먹이결핍에 의해 절식기간이 길어짐에 따라 체내 보유물인 단백질이 에너지원으로 이용되고 피낭기질의 섬유질이 더욱 느슨해지면서 수축반응이 발생하는 것으로 여겨진다. 이는 본 연구에서 조직학적 반응에서 피낭의 특이한 병리조직학적 증상이 없었으며, 세포의 길이가 다소 짧아지며 상피세포가 비대해지는 것은 영양부족으로 나타나는 증상으로 물렁증 발생과는 관계가 없는 것으로 판단된다.
위의 결과를 종합하여보면, 먹이결핍은 멍게의 물렁증 유발에 직접적인 영향을 미치지 않는 것으로 여겨진다. 그러나 먹이결핍에 의한 영양부족으로 면역력 및 생리적 기능이 저하되어 물렁증 원인체에 감염되어 물렁증이 발생할 수 있을 것으로 여겨지므로 물렁증이 주로 발생하는 시기의 지속적인 모니터링과 관리가 필요할 것으로 여겨진다.