This study evaluated fermented soybean meal (FSM) as a fish meal (FM) replacement and determined the appropriate amount of FSM in juvenile olive flounder diet. Twenty-four aquaria with a flowing-water system were stocked with fish averaging 20.9 g at a density of 25 fish/tank. Five experimental diets were prepared replacing FM with 0, 10, 20, 30, or 40% FSM based on FM protein (designated FSM0, FM10, FSM20 FSM30, and FSM40, respectively). Two additional diets were prepared that replaced 30 or 40% of the FM with FSM with added amino acids (methionine and lysine) (designated FSM30+AA, and FSM40+AA, respectively). Fish (triplicates) were fed one of the eight experimental diets (50% crude protein and 16.7 kJ available energy g-1 diet) for 8 weeks. Survival did not differ among the treatments during the feeding experiment. There were no significant differences in weight gain (WG) or specific growth rate (SGR) among the fish fed diets with up to 30% of the FM replaced. However, fish fed FSM40 or FSM40+AA had a reduced WG and SGR, as compared to FSM0 (control) (
해산어는 담수어나 육상동물과 비교하여 탄수화물에 대한 생리적 이용성이 낮아 단백질을 많이 이용하며 이에 대한 의존도가 높다. 또한, 양식사료에서 단백질 원료의 비용이 차지하는 비율은 약 40-70%로 높기 때문에 단백질 사료원료의 선택은 사료단가에 큰 영향을 미친다. 단백질 사료 원료 중에서 어분은 높은 단백질 함량과 기호성으로 양식 사료에서 가장 많이 사용되어 왔다. 우리나라 주 양식어종인 넙치의 경우 배합사료내 약60% 정도의 어분이 사용되고 있다. 최근 국제 어분의 가격은 10년 전 대비 3배 가량 상승하였으며, 어분의 수급 부족 및 가격 상승으로 인해 어분에 의존한 양어용 배합사료의 생산은 지속되기 어려운 상황이다(Olsen and Hasan, 2012). 대부분의 어분을 수입에 의존하고 있는 우리나라로서는 큰 위기가 아닐 수 없으며, 어분을 대체할 수 있는 단백질 원료에 대한 연구가 시급한 상태이다. 세계적으로 이러한 문제점을 해결하기 위해 식물성 및 동물성 대체 사료원료 개발에 대한 연구를 활발히 진행해 오고 있다(Burr et al., 2012; Collins et al., 2012; Deng et al., 2006; Luzier et al., 1995).
특히, 사료원료들 중 대두박은 식물성 단백질원으로 단백질 함량이 40% 이상이고, 아미노산 조성이 비교적 양호할 뿐 아니라 가격이 싸며 공급이 안정적이어서 많은 연구가 수행되었다. 그러나, 대두박의 경우 필수아미노산 조성의 불균형 및 phytic acid 및 trypsin inhibitor 등의 항영양인자가 성장을 저하시킨다고 밝혀지면서 대두박의 생물학적 이용성을 높이기 위한 연구가 다양하게 이루어지고 있다(Watanabe et al., 1988; Dabrowski et al., 1989; Murai et al., 1989; Pongmaneerat and Watanabe, 1993). 식물성 원료내 항영양인자의 함량을 낮추기 위한 방법으로 발효를 통한 원료 이용성 향상 연구들이 수행되고 있다(Gatlin et al., 2007). Yamamoto et al. (2010)의 연구에서는 무지개 송어용 사료에서 어분을 발효대두박과 콘글루테밀로 완전대체 하였을 때 대조구와 비슷한 성장결과를 나타내었다고 보고하였다. Lactic acid 발효는 대두박내 함유되어있는 trypsin inhibitor 활성을 낮추고 sucrose와 비전분다당류인 raffinose 함량을 떨어뜨리는 것으로 보고되었다(Refstie et al., 2005). 그러나, 국내 넙치를 대상으로 한 발효 대두박 연구는 거의 없는 실정이며, 이와 관련된 연구가 시급한 실정이다.
본 연구에서는 식물성 단백질원의 생물학적 이용률을 극대화하고자 발효시킨 대두박(발효대두박)을 사용하였으며, 또한 치어기 넙치 사료내 발효대두박 함량을 달리하여 실용배합사료에 어느 정도까지 어분을 대체할 수 있는지 규명하고자 수행하였다.
넙치 실험에 사용된 실험사료의 사료원료와 일반성분 조성 및 구성 아미노산은 Table 1과 2에 나타내었다. 실험사료의 단백질원으로 갈색어분(칠레산), 발효대두박(대만) 및 오징어간분을 사용하였으며, 지질원으로 어유를 사용하였으며, 수협사료에서 자사 제품생산을 위해 사용하는 원료를 구매하여 사용하였다. 이 외에 사료 첨가제로서 대두레시틴, 비타민 및 미네랄 혼합물을 사용하였다. 모든 실험사료의 영양소 함량은 조단백질 50%, 조지질 10% 전후가 되도록 설계하였다. 본 실험의 사료원료인 발효대두박(DaBomb-P, DaBomb Protein Corp, Taiwan)은
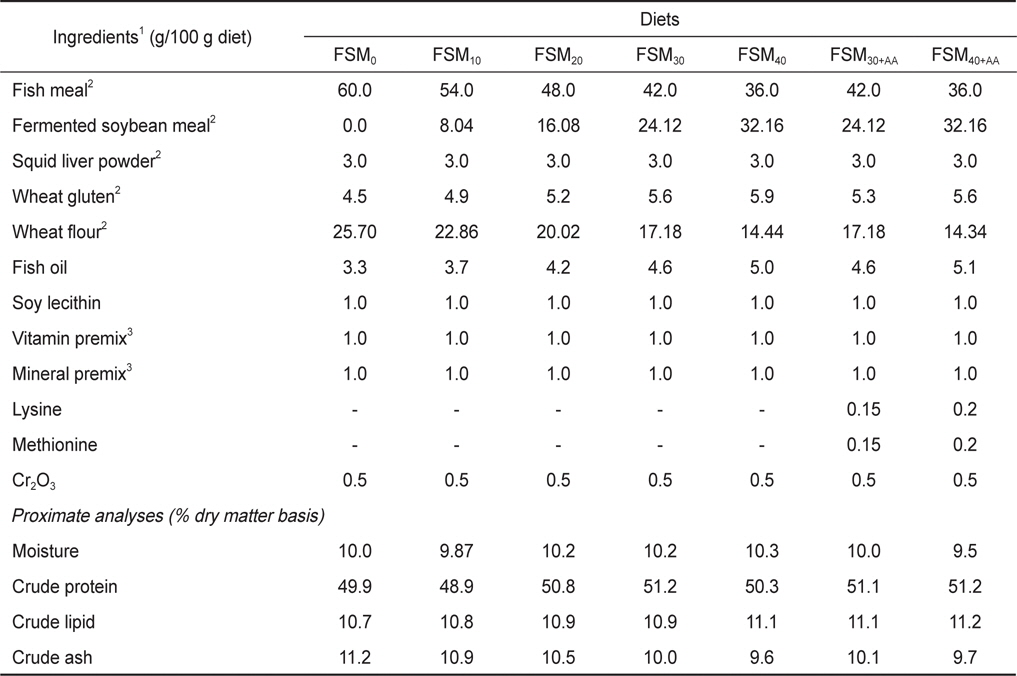
[Table 1.] Diet composition and proximate analysis of the experimental diets
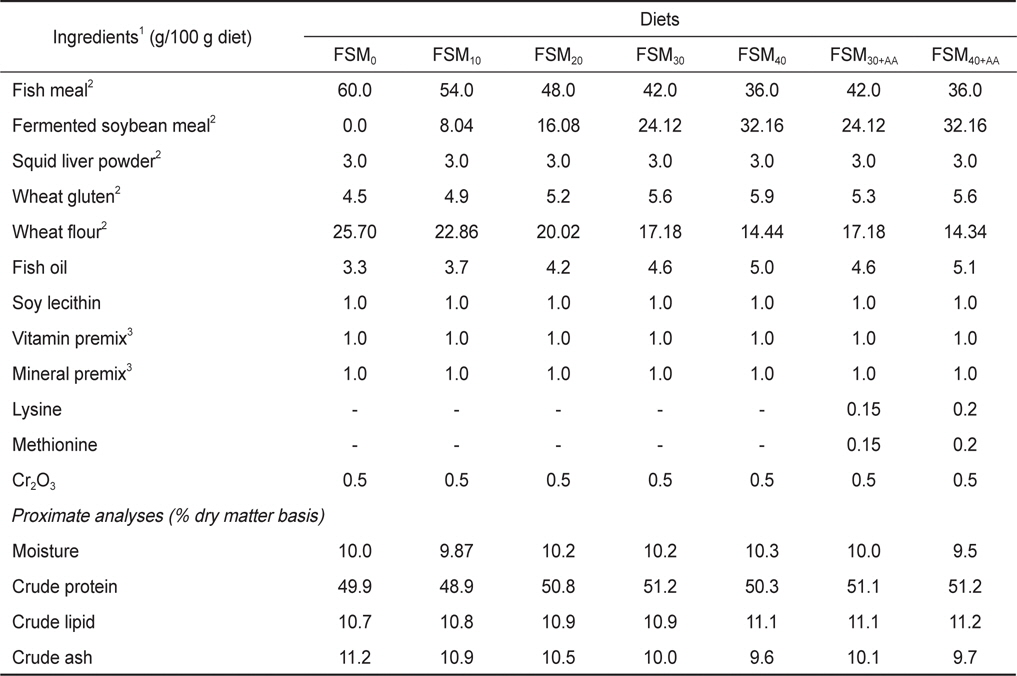
Diet composition and proximate analysis of the experimental diets
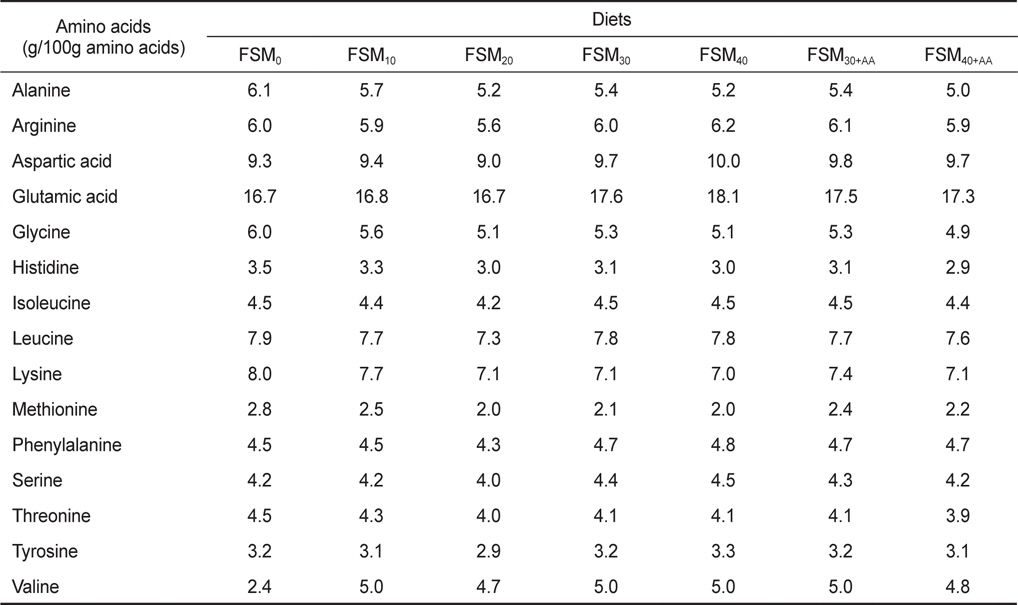
[Table 2.] Amino acids composition (g/100 g amino acids) of the experimental diets
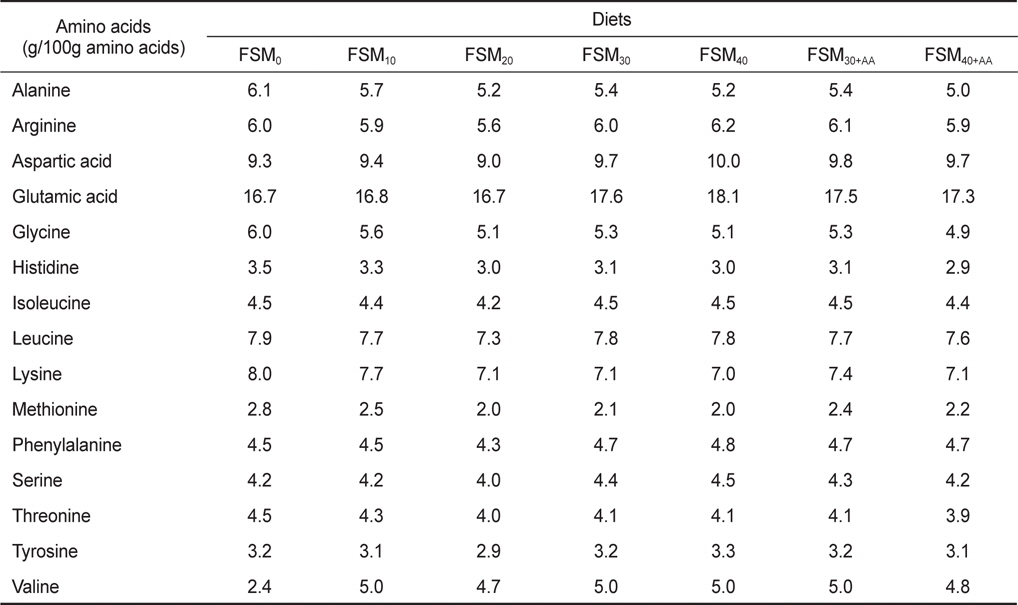
Amino acids composition (g/100 g amino acids) of the experimental diets
실험어는 평균무게 20.9±1.8 g (mean±SD)의 넙치 치어를 24개의 400 L polypropylene 원형수조에 25마리씩 실험구별로 3반복으로 무작위 배치하였다. 각 실험수조는 유수식 사육장치로 사육수가 분당 20 L 가 되도록 흘려주었으며, 수조마다 에어를 공급하였다. 사료공급은 1일 2회 만복 공급하였으며, 사육기간 중 평균수온은 22.3±1.8℃ (17.7-25.0℃)였다.
분 샘플은 실험실에서 자체 고안한 분 수집 장치를 이용하여 수집하였다. 6가지 사료의 외견상 건물 및 단백질 소화율 측정은 산화크롬(Cr2O3) 방법(Hanley, 1987)을 사용하였으며 Cho and Slinger (1979)와 Sugiura et al. (1998)의 방법에 의해서 계산하였다. 각 영양소의 소화율 측정은 간접방법으로 지표물질인 산화크롬(Cr2O3)을 이용하여 사료와 분의 단백질을 측정한 후 사료와 분내의 산화크롬 양을 측정하여 다음 식에 의하여 각 사료의 단백질소화율을 측정하였다.
건물 소화율(%) = 100 × (사료 중의 Cr2O3, % / 분 중의 Cr2O3, %)
단백질 소화율(%) = 100 × (사료 중의 Cr2O3, % / 분 중의 Cr2O3, %) × (분 중의 단백질, % / 사료 중의 단백질, %)
어체 측정은 사육실험 시작과 종료 시에 측정 전 48시간 절식시킨 후 MS-222 100 ppm 수용액으로 마취시켜 수조에 수용된 모든 실험어의 전체무게를 측정하였다. 실험종료 후 생존율, 증체율, 일간성장률, 사료효율, 일간사료섭취율 등을 조사하였다. 일반성분은 실험사료와 각 수조별로 실험어 5마리씩 무작위로 샘플하여 전어체를 분석하였으며, AOAC (1995) 방법에 따라 수분은 상압가열건조법(135℃, 2시간), 조단백질은 kjeldahl 질소정량법(N×6.25), 조회분은 직접회화법으로 분석하였다. 조지질은 조지질추출기(Velp SER148, Italy)를 사용하여 ether로 추출한 후, 측정하였다. 구성아미노산 분석은 시료 0.5 g을 정량 하여 시험관에 넣고 6 N-HCl 15 mL를 가하여 감압 밀봉한후 110℃의 dry oven에서 24시간 이상 동안 산 가수 분해시켰다. Glass filter로 분해액을 여과하고 얻은 여액을 55℃에서 감압 농축하여 염산과 물을 완전히 증발시킨 다음, 농축된 시료를 sodium citrate buffer (pH 2.20)로 25 mL 정용플라스크에 정용하여 0.45 μm membrane filter로 여과 한 시료액을 아미노산 자동 분석기(Biochrom 30, Biochrom Ltd., England)를 사용하여 다음과 같은 조건으로 분석하였다. Cation separation column (oxidised feedstuff column, 4.6 mm×200 mm)을 사용하였고 0.2 M sodium citrate buffer (pH 3.20, 4.25)와 1.2 M sodium citrate buffer (pH 6.45) 및 0.4 M sodium hydroxide solution을 이동상으로 사용하였다. 이동상의 유속은 0.42 mL/ min, ninhydrin 용액의 유속은 0.33 mL/min, column 온도는 48-95℃, 반응온도는 135℃로 조절하여 분석하였다.
결과의 통계처리는 SPSS program (Version 11.0)을 사용하여 One-way ANOVA test를 실시한 후, Duncan’s multiple range test (Duncan, 1955)로 평균간의 유의성을 검정하였다(유의수준,
치어기 넙치 사료의 조단백질 함량 및 아미노산 조성은 대조구와 비교하여 유사한 수준을 보였으며(Table 1 and 2), 이는 사료내 발효대두박으로 인한 성장이나 아미노산 중 한 가지 또는 그 이상이 결핍되었을 때 나타나는 증상은 없는 것으로 판단된다.
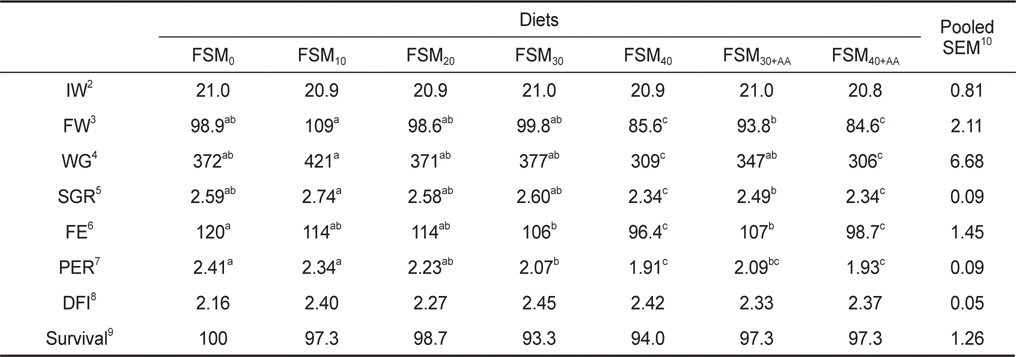
치어기 넙치를 대상으로 8주 동안 사료내 어분 대체원으로서 발효대두박의 사육효과 실험 결과는 Table 3에 나타내었다. 생존율은 93-100%로 높은 생존율을 보였으며, 모든 실험구에서 유의한 차이가 없었다(
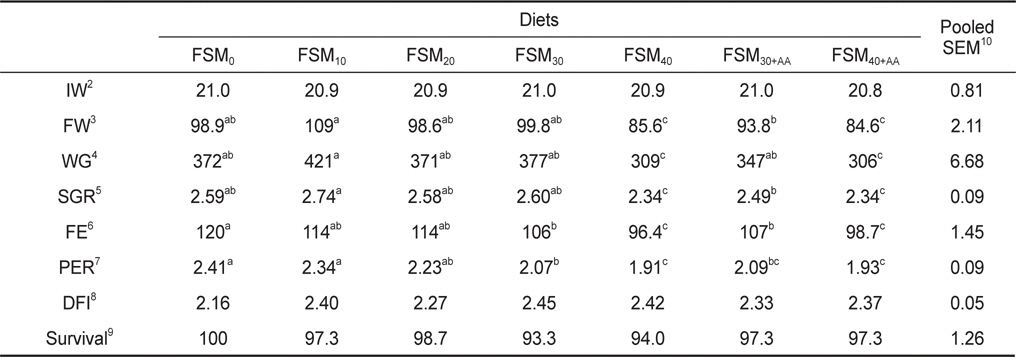
Growth performance of olive flounder Paralichthys olivaceus fed the experimental diets for 8 weeks1
일반적으로 식물성보다는 육식성 어류에서 사료내 식물성 원료의 이용성이 낮은 것으로 보고되었다(Olsen and Hasan, 2012). 이는 육식성 어류가 식물성원료에 존재하는 항영양인자에 보다 민감하게 반응하는 것을 나타내고 있으며, 영양소 흡수와 이용성을 저하시키는 것으로 보고되고 있다(Wee and Shu, 1989). 이전의 연구에서 대두박에 의한 어분 대체율은 조피볼락(Lim et al., 2004), 방어(Shimeno et al., 1993), 쥐노래미(Lee and Lee, 1998)에서 10-30% 범위였으며, 넙치 치어용 사료에서는 사료내 어분 단백질의 20%까지 탈피대두박으로 대체할수 있었다(Choi et al., 2004). 식물성 원료의 이용성을 높이기 위한 방안으로 발효를 포함한 사료가공법이 있으며 (Gatlin et al., 2007), 국내 양식용 어류를 대상으로 한 연구는 많지 않은편이다. Lim et al. (2010)의 연구에서는 30%의 어분 단백질을
대두박을 어분대체 단백질원으로 사용할 때 고려해야 할 것은 제한적인 필수아미노산 조성을 들 수 있는데(NRC, 1993), 대두박의 대체 수준이 높을수록 사료내 특정 아미노산(제한 아미노산)의 불균형으로 어류의 성장이 저하된다고 보고되고 있다(Jackson et al., 1982; Murai et al., 1989). 최근 많은 어종을 대상으로 식물성 단백질에 의한 어분대체 연구가 활발이 이루어지고 있으며, 식물성 원료의 이용성을 높이기 위한 방안으로 제한 아미노산인 methionine 및 lysine을 보충하여 대체율 향상 연구들이 수행되고 있다(Collins et al., 2012; Cheng et al., 2013; Deng et al., 2006; Murai et al., 1982; Shiau et al., 1988).치어기 넙치를 대상으로 사료 내 탈피대두박을 사용하여 어분 단백질의 20%까지 대체하고, 합성 아미노산(methionine and lysine)을 첨가할 경우 어분 단백질의 30%까지 대체할 수 있다 고 보고되었다(Choi et al., 2004). 그러나 사료내 제한 아미노산을 보충하여도 성장 개선 효과가 없다는 연구보고도 있다(Murai et al., 1982; Andrew and Page, 1974; Lim and Dominy, 1989).
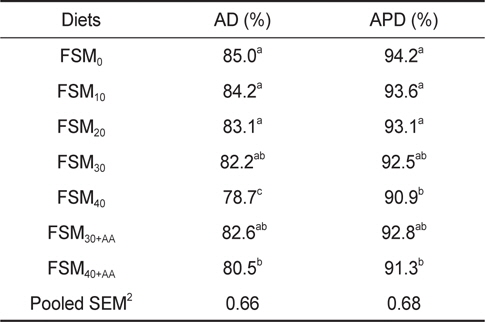
실험사료의 외견상 소화율(AD)과 외견상 단백질 소화율 (ADP)은 Table 4에 나타내었다. 외견상 소화율 및 단백질 소화율은 각각 78.7-85.0% 과 90.9-94.2% 범위였으며, FSM10, FSM20, FSM30 및 FSM30+AA 실험구는 대조구와 비교하여 유의적 차이가 없는 반면에 FSM40 및 FSM40+AA 실험구는 대조구 보다 유의적으로 낮은 소화율가를 나타내었다(
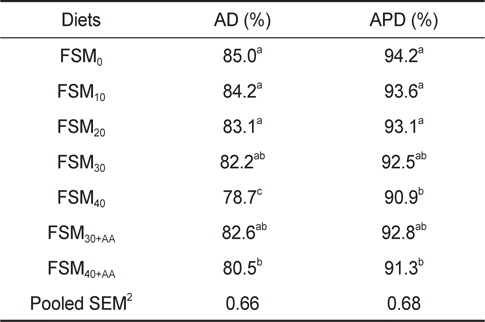
Apparent dry matter digestibility (AD) and apparent protein digestibility (APD) of olive flounder Paralichthys olivaceus fed the experimental diets for 8 weeks1
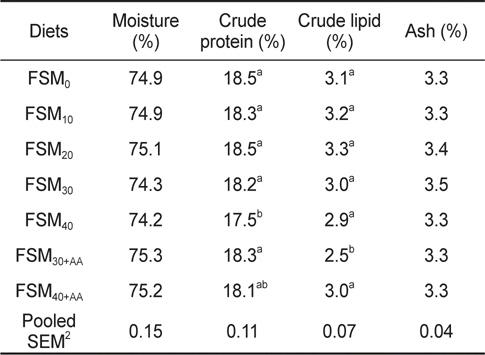
사육실험 종료 후, 실험사료를 섭취한 치어기 넙치의 전어체 일반분석 결과는 Table 5에 나타내었다. 조단백질 함량은 FSM40 실험구를 제외한 모든 실험구에서 대조구와 비교하여 유의적인 차이를 나타내지 않았다. 조지질 함량은 FSM30+AA 실험구를 제외한 모든 실험구에서 유의적인 차이를 나타내지 않았다.
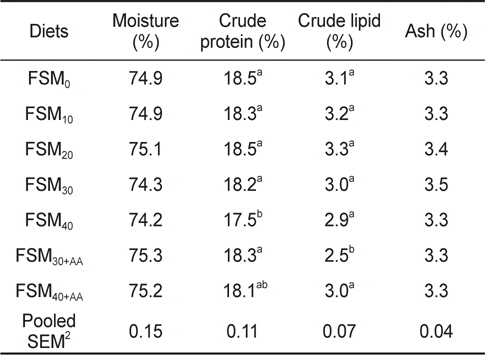
Proximate composition of whole body in flounder Paralichthys olivaceus fed the experimental diets for 8 weeks1
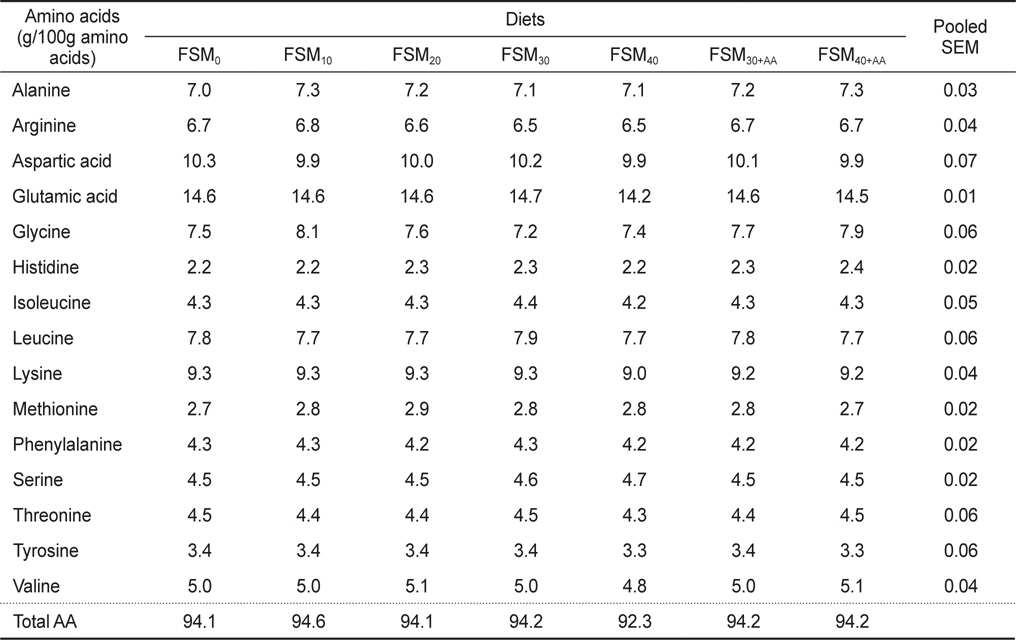
실험사료를 섭취한 치어기 넙치의 구성아미노산 분석 결과는 Table 6에 나타내었다. 본 실험에서 전어체 구성 아미노산 함량은 92.4-94.6 g/100 g amino acids로 나타났으며, 각 실험구들 사이의 구성 아미노산 사이에는 유의차가 나타나지 않았다 (
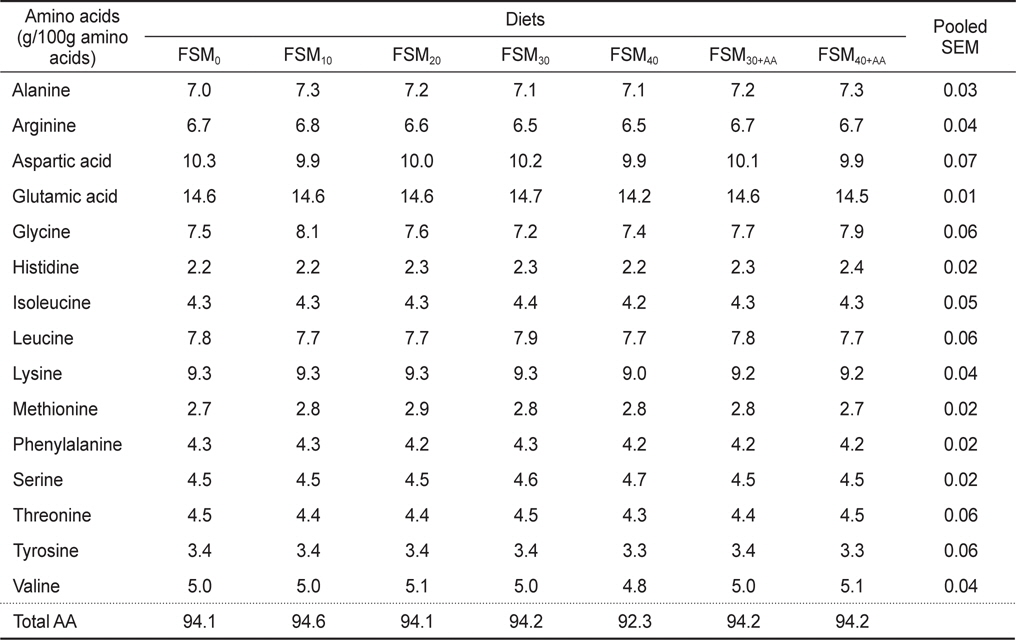
Amino acid contents of whole body in flounder Paralichthys olivaceus fed the experimental diets for 8 weeks1
따라서 본 실험의 결과를 토대로 치어기 넙치에 있어서 어분대체원으로서 발효대두박은 합성 아미노산의 보충 없이 어분단 백질의 30%까지 대체가 가능할 것으로 보이며, 앞으로 발효효소의 가공처리 조건에 따른 발효대두박의 이용성에 대한 연구가 추가적으로 진행되어야 할 것이다.