Scuticociliates are regarded as serious pathogens in marine aquaculture worldwide. In Korea, they cause mass-mortalities in fish such as the commercially important olive flounder
스쿠티카증(scuticociliatosis)은 어류, 갑각류 및 연체동물에서 발생하는 Scuticociliatida목(order)에 속하는 조직섭이성(histophagous) 섬모충에 의한 감염증을 말하며, 근래 우리나라를 비롯하여 전세계적으로 해산양식에 크게 문제가 되는 기생충성 질병이다. 원인충인 스쿠티카충은 대부분의 섬모충과는 달리 신장, 혈관 및 뇌조직까지 감염을 유발하여 높은 폐사율을 나타내며 우리나라에서는 특히 넙치양식장에 큰 경제적인 손실을 입히고 있다(Harikrishnan et al, 2010; Iglesias et al., 2002; Bae et al., 2009). 넙치
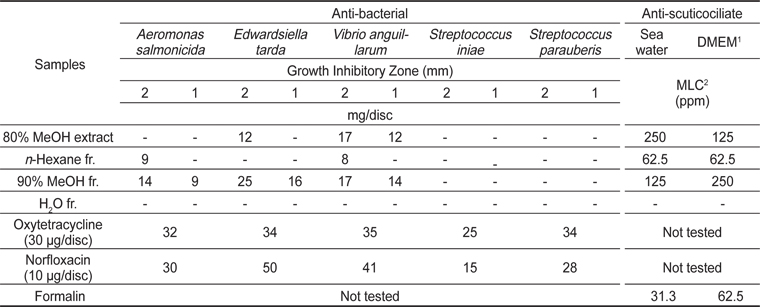
Anti-bacterial and anti-scuticociliate activities of Polysiphonia morrowii extract and its fractions
현재 스쿠티카증에 대한 대책으로는 포르말린(37% 포름알데히드 수용액)이 유일하게 스쿠티카충 구제제로 승인되어 사용되고 있으나 사용농도가 100-200 ppm으로 높아 어체에 스트레스를 줄 수 있으며 최근 미국 독성학 프로그램 보고서(2011)에 의하면 포름알데히드는 1981년 보고서에서의 “reasonably anticipated to be a human carcinogen”에서 “known to be a human carcinogen”로 그 위험성이 격상되어 식품안전상의 문제도 대두되고 있는 현실이다. 현재까지 스쿠티카충 구제물질에 관한 연구로는 항생제, 기생충 구제제를 포함한 다양한 화학요법제 그리고 resveratrol과 같은 천연유래물질 등을 이용한
따라서, 본 연구에서는 스쿠티카증의 주된 발병상황인 세균과의 혼합감염에도 효과적으로 대응할 수 있는 물질을 도출하기 위하여 항스쿠티카충 활성뿐만 아니라 항균활성도 동시에 갖는 물질을 천연물에서 도출하고자 활성검색을 실시하였다. 그 과정에서 홍조류인 모로우붉은실[
그람음성균으로
본 연구에 사용된 모로우붉은실(
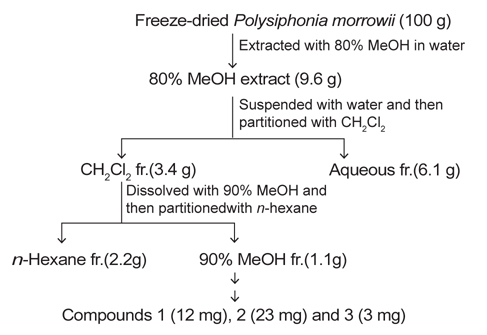
모로우붉은실의 90% 메탄올 분획물(1.1 g)을 ODS column chromatography (methanol:water=5:95~100:0)를 실시하여 9개의 소분획으로 나누었다. 그 중 소분획물 II (120 mg)를 SephadexTM LH-20 column chromatography (100% methanol) 을 실시하여 얻은 5개의 subfraction 중 2번 subfraction (70 mg)을 다시 SephadexTM LH-20 column chromatography (methanol:acetone=1:9)로 실시하여 각각 Compound 1 (12 mg)과 Compound 2 (23 mg)를 얻었다. 소분획물 VI (150 mg)를 SephadexTM LH-20 column chromatography (CH2Cl2:MeOH=1:9)을 실시하여 소분획물 VI-V를 얻었고, 이에 대한 HPLC 정제 과정을 거쳐 Compound 3 (3 mg)을 분리하였다(Fig. 1).
본 연구에 사용된 14종의 합성브로모페놀 유도체는 Tokyo Chemical Industry Co., Ltd. (Tokyo, Japan)에서 구입하여 사용하였다. Oxytetracycline, norfl oxacin, flumequine은 Sigma-Aldrich사(St. Louis, USA) 제품을 사용하였다.
시료를 75% 에탄올 수용액에 녹인 후 직경 6 mm 멸균 paper disc에 설정 농도로 흡착하여 실온에서 건조시켰다. 세균을 108 CFU/mL로 배양하고 BHI agar plate에 100 μL씩 접종한 후 건조된 disc를 올리고, 24 h동안 25℃에서 배양하여 disc를 포함한 growth inhibition zone의 직경을 측정하였다. Positive control로서는 norfloxacin (10 μg/disc)과 oxytetracycline (30 μg/disc) disc를 사용하였다(Kang et al., 2005).
화합물들은 희석용액에 대한 용해도를 높이기 위해 최소한의 dimethyl sulfoxide (DMSO)에 용해하였으며(최종 농도 0.25% 이하), BHI broth 배지에 2배 농도 구배로 희석하여 세균증식에 미치는 영향을 측정하였다. 실험에 사용된 세균은 24 h 전에 배양하여 106 CFU/mL로 조정하였으며, 시료와 동량(1:1)으로 96-well microplate에서 혼합하여 20 h 25℃ 인큐베이터에서 배양하였다. 세균의 증식을 억제하는 최소농도 [최소생장억제농도(minimal inhibitory concentration, MIC)]를 육안으로 확인하고, 이를 재확인하기 위해 Langfi eld et al. (2004)의 방법으로 20 h 동안 배양된 96-well microplate 에 0.2 mg/mL의
스쿠티카충 배양액을 500×
시료의 어류 주화세포에 대한 세포독성은 neutral red uptake assay (Kim et al., 2011)를 이용하였다. 어류 주화세포를 phenol red가 첨가되지 않은 DMEM으로 부유시킨 뒤, 96-well plate에 1×106 cell/mL로 100 μL씩 seeding하여 20℃에서 24 h 동안 배양시킨 후, 시료를 농도 별로 처리한 뒤 20℃에서 48 h 동안 반응시켰다. 0.33% neutral red solution을 각 well당 3 μL씩 분주하여 20℃에서 2 h 동안 반응시킨 뒤, 1% acetic acid in 50% 에탄올에 녹여 microplate reader (Spectra Max 340, Molecular Devices, USA)를 사용하여 흡광도(540 nm-690 nm)의 차이를 측정하였다.
>
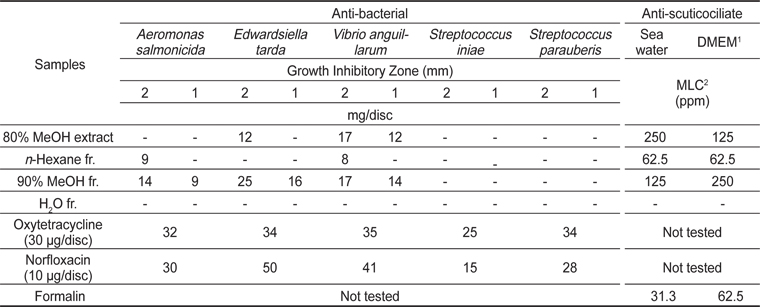
모로우붉은실 추출물과 분획물의 in vitro항균활성 및 항스쿠티카충 활성
모로우붉은실의 80% 메탄올 추출물 및 이의 분획물들의 주요 어병세균에 대한 항균활성을 Disk diffusion법을 이용하여 검색한 결과는 다음과 같다(Table 2). 80% 메탄올추출물로부터 얻은 분획물 중 90% 메탄올 분획물에서 그람음성균인
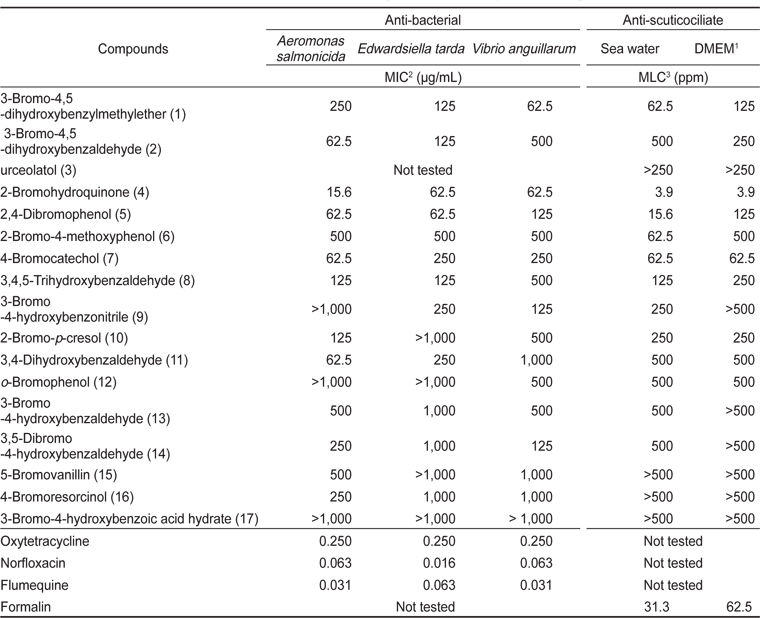
Anti-bacterial and anti-scuticociliate activities of isolated compounds 1, 2, 3 and synthetic bromophenol derivatives (4-17)
90% 메탄올 분획물로부터 활성물질의 분리 및 화학구조의 분석
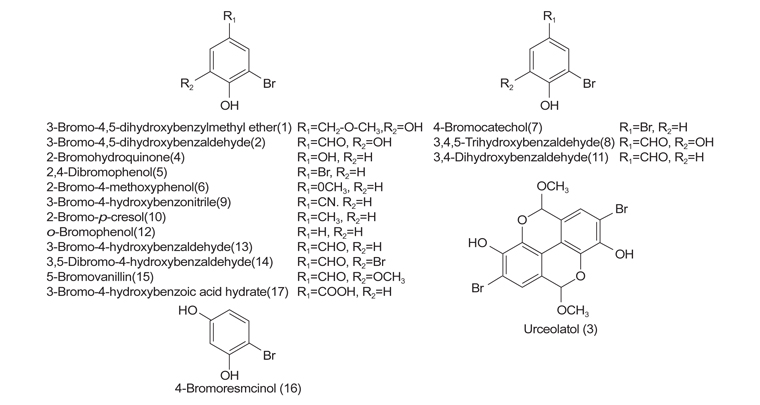
90% 메탄올 분획물에 대한 reverse-phase silica gel 컬럼크로마토그래피 및 Sephadex-LH 20 컬럼크로마토그래피 등의 일련의 분리·정제과정을 실시하여 Compound 1, 2 그리고 3를 분리하였다. 분리된 화합물의 MS, NMR 등의 다양한 분광학적 분석법을 이용하여 그 화학구조를 규명한 결과 세 화합물은 모두 브로모페놀계 화합물로Compound 1은 분자식 C8H9O3Br을 갖는 3-bromo-4,5-dihydroxybenzylmethylether (1), Compound 2는 분자식 C7H5O3Br을 갖는 3-bromo-4,5-dihydroxybenzaldehyde (2), Compound 3은 분자식 C16H12O6Br2을 갖는 Compound 1의 dimer 형태인 urceolatol (3) 로 동정되었다(Kurihara et al., 1999; Han et al., 2005; Liu et al., 2006; Kim et al., 2011) (Fig. 2).
>
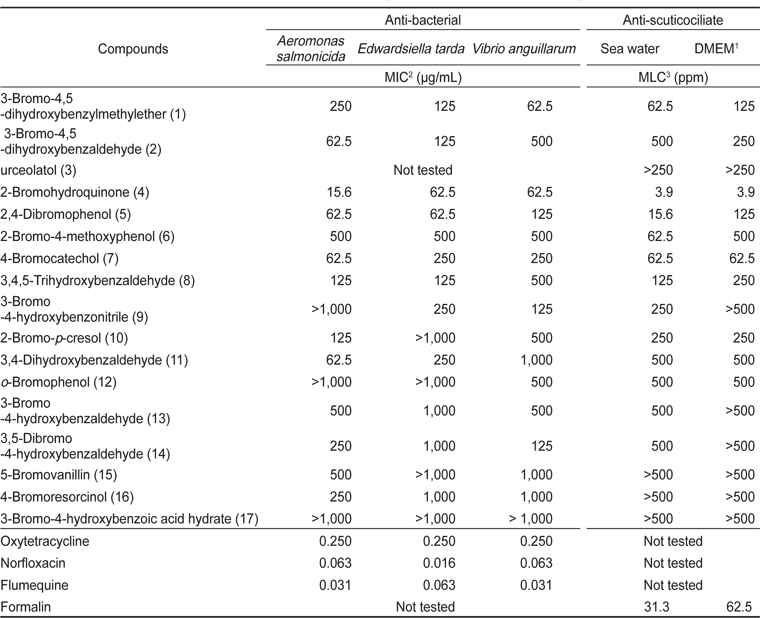
분리된 브로모페놀계 화합물 및 합성 브로모페놀 유도체들의 in vitro항균 및 항스쿠티카충 활성
90% MeOH 분획물로부터 분리된 화합물 3종에 대한
17종의 브로모페놀유도체들을 그람음성세균인
본 연구에서는 홍조류인 모로우붉은실의 80% 메탄올추출물이 스쿠티카증의 주요 원인충인
분리된 3종의 브로모페놀 유도체를 포함하여 17종의 브로모페놀 유도체의 작용기와 해수조건에서의 항스쿠티카충 활성을 비교하여 본 결과, 몇 가지 구조-활성 상관성을 발견할 수 있었다. i) 2-bromophenol (12) (MLC=500 ppm)의 구조를 기준으로 관찰하였을 때 4번 탄소(Fig. 2의 R1)의 수소원자가 hydroxyl 기로 치환되거나(2-bromohydroquinone (4), MLC=3.9 ppm), bromine으로 치환되거나(2,4-dibromophenol (5), MLC=15.6 ppm), methoxyl기로 치환되거나(2-bromo-4-methoxyphenol (6), MLC=62.5) 또는 methyl 기(2-bromo-