본 연구에서는 탄산리튬과 탄산망간을 사용하여 습식혼합방법으로 스피넬 리튬망간 산화물(LMO)을 합성하였다. 합성한 리튬망간 산화물의 물리적인 특성은 X-선 회절 분석기(X-ray diffraction, XRD)와 주사전자현미경(scanning electron microscopy, SEM) 사용하여 분석하였다. 회분식 실험을 통해 LMO의 리튬이온에 대한 흡착특성을 살펴보았다. Langmuir 흡착 등온식으로부터 구한 리튬의 최대흡착량은 27.21 mg/g였다. LMO는 뛰어난 리튬 이온체의 특성을 가지고 있었으며, Ca2+ < K+ < Na+<Mg2+ < Li+ 순서로 분배계수(Kd)가 나타나 해수로부터 리튬을 회수하는데 용이할 것으로 사료된다.
전 세계적으로 매장량이 극히 적은 희귀 금속중의 하나인 리튬은 2차 전지, 항공기용 경합금의 원료, 핵융합 발전용 연료 등 여러 분야에서 사용되면서 그 수요가 증가하고 있다. 전 세계 리튬의 육상매장량은 약 400만톤으로 알려져 있으며,해수에는 약 2,300억톤의 리튬이 존재하는 것으로 알려져 있다[1]. 그러나 앞으로 리튬의 사용량을 고려할 때 육상에 매장된 리튬의 양으로는 그 수요를 충족하는데 한계가 있다. 따라서 막대한 양의 리튬을 포함하고 있는 해수는 부족한 리튬의 수요를 공급해줄 주요 공급원이 될 것이다.
수중의 리튬을 회수하는 방안으로 미생물 농축[2], 용매추출[3], 흡착법[4], 멤브레인[5] 등을 이용하는 다양한 방법들이 연구되고 있다. Tsuruta[2]는 미생물을 이용한 생물농축 방법을 이용하여 리튬을 회수하는 연구를 행하였으며, Kim et al.[3]은 용매 추출을 이용하여 리튬을 회수하고자 하였다. 하지만 미생물을 이용한 생물농축 방법은 미생물의 배양조건을 조절하는데 많은 주의가 필요하며, 용매 추출법은 많은 양의 유기 용매가 필요로 할 뿐만 아니라 유기 용매가 손실하게 되면 환경오염, 불쾌한 악취 및 화재의 원인이 되기도 한다[6]. 이에 반해 흡착공정은 공정이 간단하며 효율적이기 때문에 다양한 흡착제를 이용한 리튬이온의 흡착연구가 진행되고 있다. Seron et al.[4]은 흡착제로 활성탄을 사용한 경우에 리튬이온 의 흡착능이 약 1 mg/g이었다고 하였으며, Navarrete et al.[7]은 제올라이트를 Na+ type으로 치환하여 사용한 경우에 리튬 이온의 흡착량이 3.2 mg/g이 되었다고 하였다. 또한 Navarrete et al.[8]은 이온교환수지 Amberlite IR 120을 흡착제로 사용 한 경우에 리튬이온의 흡착량이 약 10.5 mg/g이었다고 보고하였다.
그러나 활성탄이나 이온교환수지를 흡착제로 사용하는 경우에는 리튬이온의 흡착량이 그다지 높지 않기 때문에 최근에는 리튬이온에 대한 높은 선택성과 흡착량을 가지는 리튬망간 산화물(Lithium manganese oxide, LMO)을 이용한 리튬 이온의 흡착 연구가 주목을 받고 있다. Yoshizuka et al.[1]은 고체상의 산화망간니즈와 수산화리튬을 혼합하여 LMO을 합성하였으며 리튬이온의 흡착량은 10.4 mg/g이었다고 보고하였고, Chung et al.[9]과 Kim[10]은 고체상의 탄산망간과 탄산 리튬을 혼합기로 혼합하여 합성한 LMO의 흡착량은 25 mg/g이 되었다고 하였다. 또한 Wang et al.[11]도 고체상의 탄산망간과 수산화리튬을 혼합하여 합성한 경우의 LMO의 흡착량이 23 mg/g이었다고 보고하였다. 그러나 이들 연구자들은 고체 상 원료물질들을 볼밀이나 혼합기 등으로 건식으로 혼합하여 사용하였다. 그러나 고체상물질을 혼합하는 경우에는 균일한 혼합이 용이하지 않아 균일한 LMO를 얻기가 어렵다. 그러므로 원료물질을 볼밀이나 혼합기 등을 사용한 기계적 혼합방 식보다는 액상에 고체상의 원료물질을 분산시켜 습식 혼합을 한다면 원료물질이 균일하게 혼합되어 LMO의 형성이 용이할 것으로 기대된다.
따라서 본 연구에서는 혼합을 용이하게 하기 위하여 탄산리튬과 탄산망간을 에탄올에 분산시켜 습식혼합을 한 후 소성하여 LMO를 합성하였다. 합성한 LMO를 흡착제로 사용하여 pH 영향, 흡착등온, 흡착 속도, 열역학적 해석 및 공존이온 의 영향을 검토하였다.
LMO의 합성은 탄산리튬(Samchun, EP)과 탄산망간(Samchun, EP)을 사용하여 행하였다. 탄산리튬과 탄산망간을 각각 1.67 mol과 1.33 mol을 취한 뒤 20 mL 에탄올을 용매로 사용하여 12 h 동안 습식혼합한 후 70 ℃ 건조기에서 12 h 건조한 뒤 전기로(Thermolyne, F-62700)에서 500 ℃로 4 h 동안 소성하여 LMO을 합성하였다. 이를 0.5M HCl (Junsei, EP)을 이용하여 24 h 동안 처리한 후 증류수로 수차례 세척하고 85 ℃ 건조기(Kukje Scientific Instrument, SPC 135)에서 12 h 동안 건조한 후 이를 흡착제로 사용하였다.
산처리 전후에 대한 각 시료의 X-선 회절 분석기(X-ray diffrac-tion, XRD, Rigaku, D/MAX2100H)를 사용하여 측정하였다. 흡착제의 미세구조를 관찰하기 위하여 주사전자현미경(scanning electron microscopy, Tescan, VEGA II LSU)을 사용하여 SEM 사진을 촬영하였다.
리튬이온 흡착 실험은 회분식으로 수행하였다. 500 mL 삼각플라스크에 일정 농도의 리튬이온 용액 200 mL를 채우고 여기에 흡착제를 0.2 g을 투입하였다. 그 후 수평 진탕기(Johnsam., Js-Fs-2,500)를 사용하여 72 h 동안 교반하면서 일정 시간 간격으로 시료를 채취하여 원심분리기(Eppendorf, Centrifuge 5415c)로 10,000 rpm에서 5분간 원심 분리한 후 상등액을 취하여 분석에 사용하였다. 리튬이온의 농도는 이온 크로마토그래피(ion chromatography, IC, Dionex, DX-120)를를 사용하여 분석하였다.
흡착제에 흡착된 리튬이온의 흡착량 qt(mg/g)은 아래 식을 이용하여 계산하였다.
여기서 qt는 시간 t에서 리튬이온의 흡착량(mg/g), Co는 리튬이온의 초기농도(mg/L), Ct는 t시간 후의 리튬이온 농도(mg/L), V는 리튬이온 용액의 부피(L), W는 사용한 흡착제의 양(g)이다.
온도변화에 따른 리튬이온의 흡착 특성을 살아보기 위하여 진탕배양기(Hanbaek, HB-201SF)를 사용하여 25℃, 40 ℃ 및 55 ℃에서 실험을 실시하였다. pH변화에 따른 영향을 알아보기 위해 0.1 N HCl과 NH3 용액을 이용하여 pH 5~10으로 조절하여 실험하였으며, 용액의 pH는 pH 미터(Orion, model 420A)를 사용하여 측정하였다.
해수에 존재하는 Na+, K+, Mg2+ 및 Ca2+들이 리튬이온의 흡착에 미치는 영향을 살펴보기 위하여 분배계수(Kd), 분리계수
그리고 농축계수(CF)를 아래와 같이 구하였다[12].
여기서 Me는 각각의 금속이온을 의미하며, qe는 평형 흡착량(mg/g)이다.
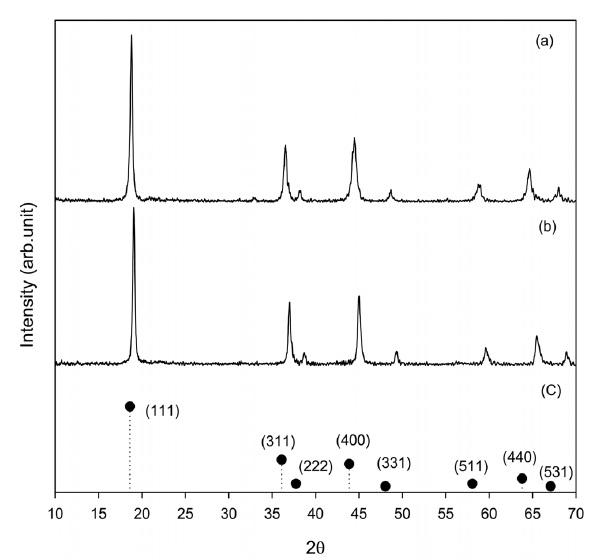
Figure 1은 합성한 LMO의 XRD 측정 결과를 나타낸 것이다. Figure 1(a)는 500 ℃에서 소성하여 합성한 LMO의 XRD 측정 결과이다. 그림에서 보이듯이 2θ의 값은 18.78, 36.52 및 44.48에서 회절 피크가 관측되었으며, 각각의 회절 피크는 리튬이 4면체 위치를 차지하고, 8면체 위치에 망간이 존재하여 형성된 (111), (311) 및 (400)의 스피넬 결정면을 나타낸다[13]. Figure 1(b)는 소성한 LMO를 산처리한 시료를 XRD 측정한 결과이다. 그림에서 보듯이 합성한 시료를 산처리하여 리튬이온을 용출한 후에도 산처리 전의 시료와 유사한 XRD 회절 피크를 보였다. Figure 1(c)는 스피넬 구조의 LMO의 JCPDS카드(# 35-782)를 나타낸 것으로, 산 처리 전과 후의 시료와 비교하였을 때, 주요 회절피크의 위치가 일치하였다. 이로 미루어보아 합성한 LMO를 산 처리 한 후에도 스피넬 구조는 유지되는 것으로 판단된다.
Figure 2는 합성한 LMO의 SEM 분석결과를 나타낸 것이다. 그림에서 보여지듯이 합성한 LMO는 크기가 약 2 μm 정도였다. Kim[10]은 탄산리튬과 탄산망간을 건식 혼합하여 합성한 경우에 약 4 μm 크기의 LMO가 얻어졌다고 하였다. Shi et al.[14]은 산화망간니즈와 수산화리튬를 원료로 하여 오토 클레이브로 210 ℃에서 10 h 동안 처리하여 합성한 LMO의 크기는 0.1~0.3 μm이었다고 하였다. 이와 같이 원료 물질과 합성방법에 따라 LMO의 크기는 달라지는 것으로 사료된다. 한편, Kim[10]의 연구에서 건식 혼합하여 합성한 LMO의 입자크기 4 μm와 본 연구에서 습식혼합으로 합성한 LMO의 입자크기 2 μm를 비교하였을 때 습식혼합의 경우에 더 작은 입자가 얻어졌다. 이는 원료물질을 습식혼합함으로써 건식혼합의
경우보다 혼합이 더 원활하게 이루어졌기 때문으로 사료된다.
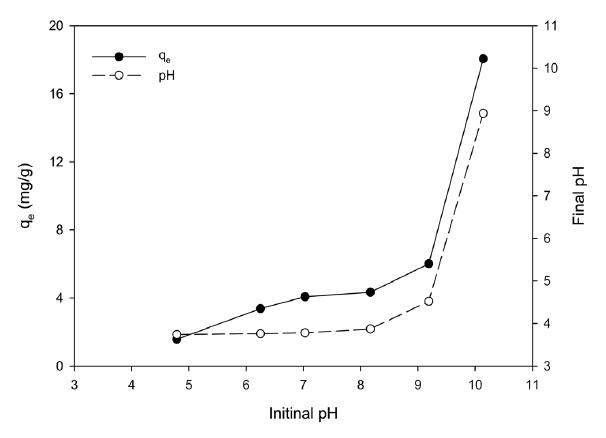
Figure 3은 pH 변화에 따른 용액의 pH 변화와 리튬이온의 흡착능을 살펴본 결과를 나타낸 것이다. pH가 증가함에 따라 리튬이온의 흡착량은 조금씩 증가하다가 pH 10에서 18 mg/g으로 가장 높은 흡착량을 보였다. Wang et al.[15]도 LMO를 이용한 흡착연구에서 pH가 증가함에 따라 리튬이온의 흡착이 잘 이루어지며, 특히 pH 10~12에서 리튬이온의 흡착이 흡착능이 가장 우수하였다고 하였다. 한편, 흡착 후 용액의 최종 pH는 초기 용액 pH보다 더 낮아졌는데, 이는 LMO내의 수소양이온이 용액내의 리튬이온과의 이온교환에 의해 수소양이온이 용액으로 배출되면서 용액의 pH가 감소하는 것으로 사료된다.
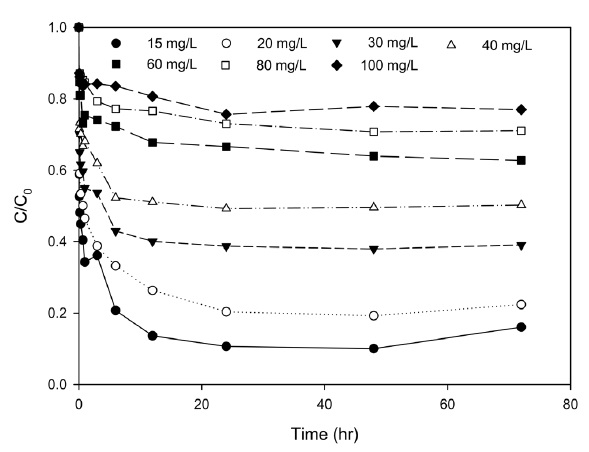
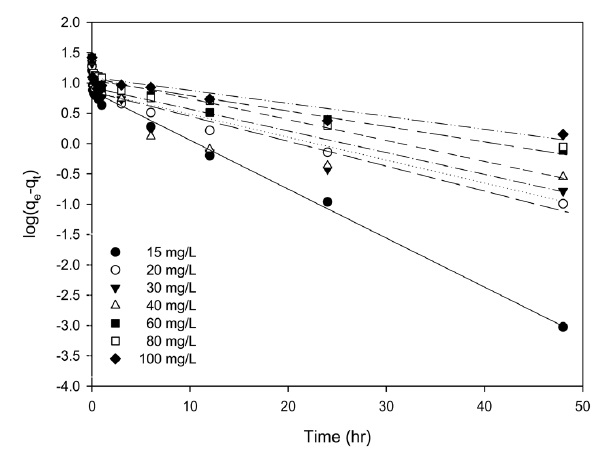
Figure 4는 초기 농도를 15~100 mg/L로 달리한 경우에 시간에 따른 리튬이온의 농도변화를 나타낸 것이다. 그림에서 보는 바와 같이 12 h까지는 농도가 급속히 감소하다가 이후 농도가 차츰 일정해 지면서 24 h에서 평형에 도달하는 것으로 나타났다. 이는 흡착의 초기 단계에는 흡착할 수 있는 흡착 점들이 많아 빠르게 흡착이 이루어지지만, 시간이 경과함에 따라 흡착점들이 포화하여 흡착이 평형에 도달하게 된 것으로 사료된다.
리튬이온의 흡착에 대한 속도론적 해석을 위하여 Figure 4 의 데이터를 이용하여 유사 1차 속도식과 유사 2차 속도식에 적용하여 그 적합성을 비교하였다. 유사 1차 속도 모델식은 다음과 같이 정의된다[16].
여기서 qe은 평형 흡착량(mg/g), k1은 유사 1차 속도상수(1/hr)이다.
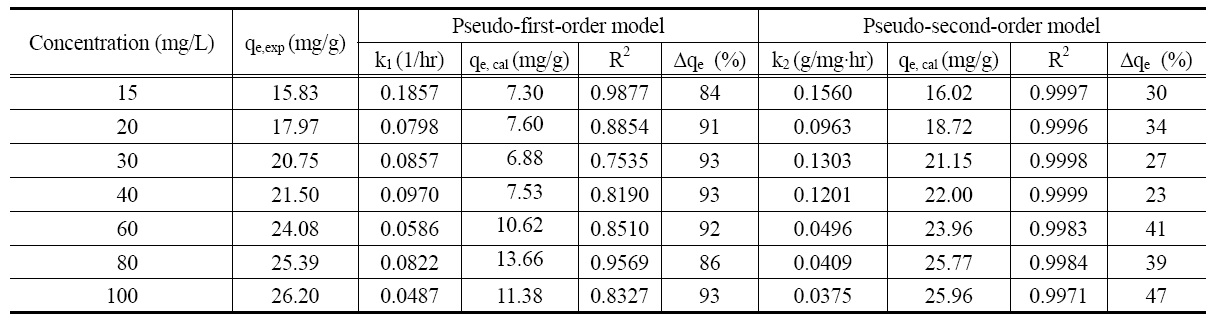
[Table 1.] Kinetic data calculated for the adsorption of lithium ion
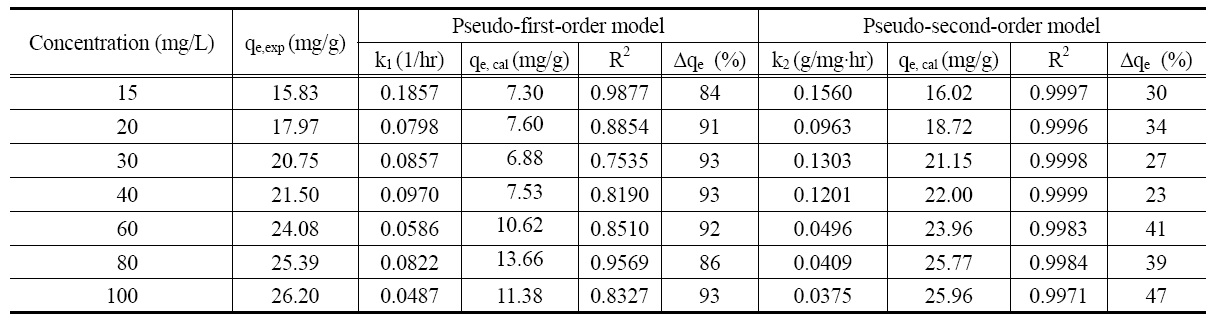
Kinetic data calculated for the adsorption of lithium ion
유사 2차 속도 모델식은 다음과 같이 정의된다[16].
여기서 k2은 유사 2차 속도 상수(g/mg・hr)이다.
검토된 흡착속도 모델식들을 평가하기 위하여 결정계수(R2) 값과 오차함수인 마쿼트의 백분율표준편차(Δqe)를 사용하여 각각의 흡착 속도 모델식에 적용하였으며, Δqe (%)는 다음과 같이 정의된다[16].
여기서 N은 실험 데이터들의 수, qt,exp는 실험으로부터 구한 흡착량(mg/g), qt,cal는 계산하여 구한 흡착량(mg/g)이다.
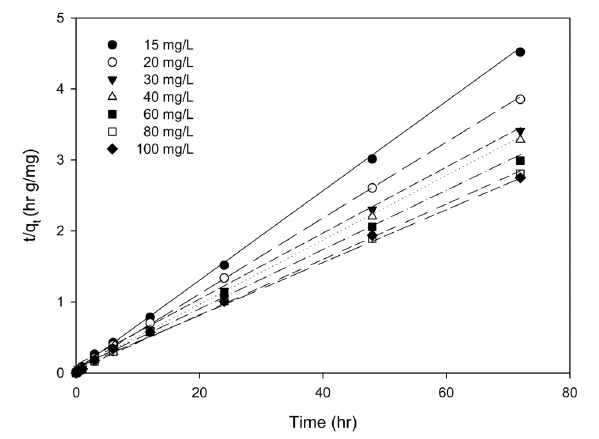
Figure 4의 흡착 실험 자료를 식 (5)과 식 (6)에 적용한 자료를 각각 Figure 5와 6에 나타내었으며, 이로부터 구한 파라미터
값들을 Table 1에 정리하였다. Table 1에서 보면 유사 1차 속도 모델식의 경우는 결정계수(R2)가 0.7535~0.9569이나, 유사 2차 속도식의 경우는 결정계수가 0.9971~0.9999로 리튬이온의 흡착은 유사 2차 속도 모델식에 만족하였으며, Δqe (%)의 결과 에서도 유사 2차 속도 모델식에 잘 만족하였다. 또한 유사 2차 속도식을 적용하여 계산된 흡착량을 살펴보면 농도가 증가함에 따라 증가하는데 이는 흡착 구동력인 농도차가 증가하기 때문으로 사료된다.
Langmuir 흡착 등온식은 다음과 같이 정의된다[16].
여기서 KL는 Langmuir 상수(L/mg) 그리고 qm은 리튬이온의 최대 흡착량(mg/g)이다.
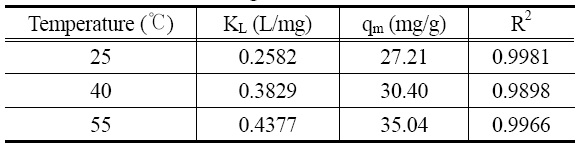
[Table 2.] Parameters of Langmuir isotherm model
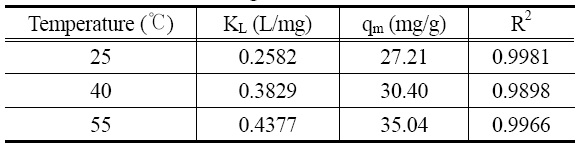
Parameters of Langmuir isotherm model
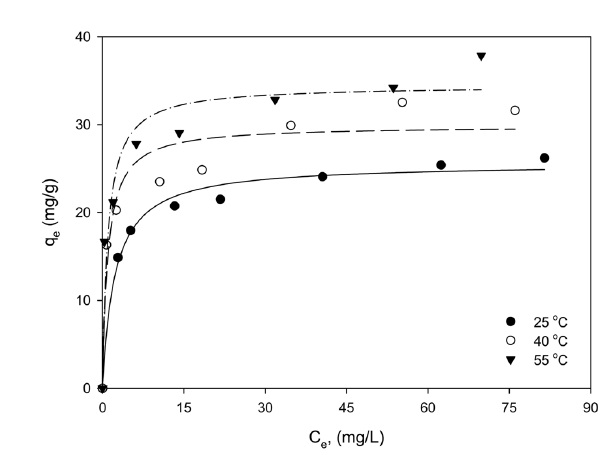
Figure 7은 온도를 25~55 ℃로 달리하여 행한 흡착등온실험 결과를 식 (8)에 적용하여 나타낸 것이다. Langmuir 흡착 등온식으로부터 구한 파라미터들을 Table 2에 나타내었다. Table 2에서 보면 결정계수(R2)의 값이 0.9936~0.9898로 Lang-muir 흡착등온식을 잘 만족하였으며, 최대 흡착량은 온도가 25~55 ℃로 증가함에 따라 27.21~35.04 mg/g으로 증가하였다. Shi et al.[14]과 Zhang et al.[12]도 수열합성으로 합성한 LMO를 흡착제로 한 리튬이온의 흡착 연구에서 Langmuir 흡착 등 온식에 잘 만족하였다고 하였다.
흡착반응에서 자유에너지(ΔG˚), 엔탈피(ΔH˚) 및 엔트로피(ΔS˚)는 중요한 열역학적 매개변수이다. 자유에너지, ΔG˚는 다음과 같이 정의된다[17].
여기서 R은 기체 상수(8.314 J/mol・K), T는 절대 온도(K), 식(9)을 식 (10)에 대입하면 아래와 같이 된다.
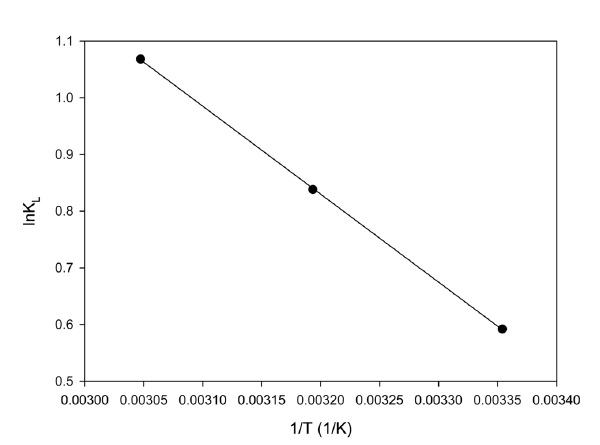
Figure 8은 각각의 온도에서 구해진 Langmuir 상수를 식 (11)에 적용하여 lnKL과 1/T를 도시한 그림이다. 이 그림과 식 (10)로부터 구한 ΔG˚, ΔH˚ 및 ΔS˚를 Table 3에 나타내었다.
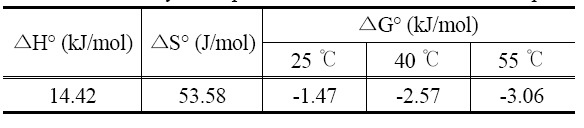
[Table 3.] Thermodynamic parameters for the lithium ion adsorption
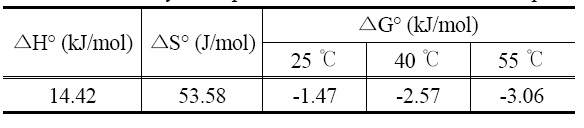
Thermodynamic parameters for the lithium ion adsorption
ΔG˚의 값은 각각의 온도에서 모두 음의 값을 나타내었으며, 이는 흡착이 자발적인 반응이라는 것을 나타낸다. ΔH˚는 14.42 kJ/mol로 양의 값을 가지며, 이는 리튬이온이 LMO에 흡착하는 과정이 흡열반응임을 의미한다. 또한, ΔS˚가 53.58 J/mol 로 양의 값을 가지며, 이는 흡착질과 흡착제의 경계면에서 불균일성이 증가한다는 것을 나타낸다[18].
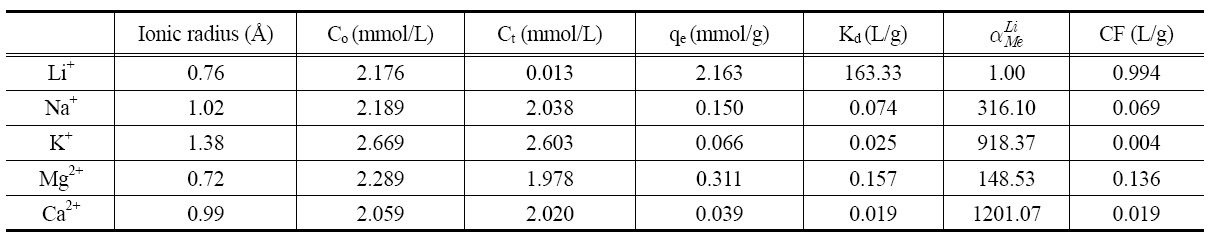
해수 내에 존재하는 Na+, K+, Mg2+ 및 Ca2+들이 리튬이온 흡착에 미치는 영향을 살펴보기 위하여 각 성분의 농도를 각각 2.5 mmol/L로 하여 흡착 평형시간인 24 h 후의 흡착실험 결과를 Table 4에 나타내었다. 분배계수(Kd)는 용액과 흡착제 내의 금속이온의 분배 정도를 나타내는 것으로 Na+, K+, Mg2+ 및 Ca2+들의 분배계수는 0.019~0.157 L/g의 값을 나타내는데 비해서 리튬이온은 163.33 L/g으로 약 1000배 정도 높은 수치를 보이므로 리튬이온이 다른 이온들에 비해서 LMO 내에 더 많이 흡착됨을 의미한다. 또한 리튬이온을 기준으로 하여 다른 금속이온들과 분리계수
의 값을 비교해보면 다른 금속이온들의 분리계수는 148~1,201로 높은 값을 보였다. 또한 Na+, K+, Mg2+ 및 Ca2+의 농축계수(CF)는 0.019~0.136 L/g인데 비하여 리튬이온은 0.994 L/g로 7배 이상 높은 값을 가졌다. 따라서 용액 내에 Na+, K+, Mg2+ 및 Ca2+들이 공존하는 경우에도 리튬이온의 흡착에 다른 금속이온들이 큰 영향을 미치지 않는 것을 알 수 있었다. 그러므로 합성한 LMO는 잔존하는 염이 많은 해수에서도 리튬이온만을 선택적으로 흡착할 수 있을 것으로 기대된다.
습식혼합에 의해서 LMO을 합성하였으며, XRD 분석을 통해 스피넬 구조의 LMO 회절 피크를 확인할 수 있었다. SEM 분석을 통하여 LMO 입자가 2 μm 크기로 형성됨을 확인하였다. 흡착속도는 유사 2차 속도식에 잘 만족하였다. LMO의 흡착은 Lanmguir 흡착 등온식과 잘 일치하였으며, 최대 흡착량은
[Table 4.] Adsorption selectivity of lithium ion
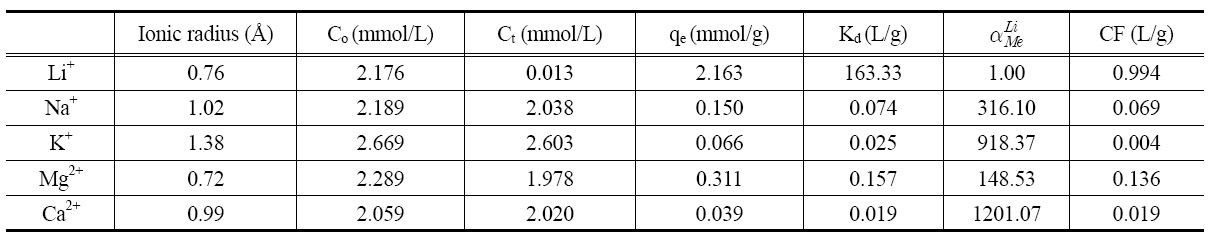
Adsorption selectivity of lithium ion
27.25 mg/g으로 계산되어졌다. 리튬이온의 흡착에서 ΔH˚는 14.42 kJ/mol로 양의 값을 가지므로 리튬이온이 LMO에 흡착하는 과정이 흡열 반응이며, ΔG˚는 -1.47~-3.06 kJ/mol로 흡착반응이 자발적으로 일어나는 반응임을 알 수 있었다. 용액의 pH가 10 이상일 때 높은 흡착능을 나타내었으나, pH가 감소함에 따라 흡착능은 감소하였다. 공존 이온의 영향에서 Na+, K+, Mg2+ 및 Ca2+의 Kd는 0.019~0.157 L/g의 값을 나타내는데 비해서 리튬이온은 163.33 L/g으로 약 1,000배 정도의 높은 값을 나타내어 리튬이온이 선택적으로 잘 흡착하는 것을 확인하였다.