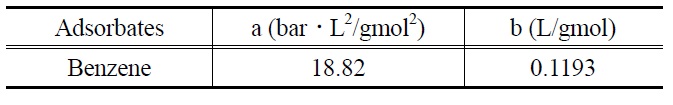본 연구에서는 국내에서 대표적으로 버려지는 폐벌목 중 잣나무에서 만든 활성탄을 이용하여 벤젠에 대한 정지(static)흡착실험을 수행하였다. 7.999 kPa에 이르는 압력 범위 내에서 온도 조건을 변화시켜 가며 303.15, 318.15, 333.15 K에서 흡착실험을 진행하였다. 등온흡착곡선은 Langmuir 등온흡착식, Freundlich 등온흡착식, Toth 등온흡착식을 적용하여 비교하였다. 벤젠의 흡착량(q)을 측정한 결과 Langmuir 등온흡착식과 Toth 등온흡착식으로 적용한 등온흡착곡선의 정확도가 높은 것으로 나타났다. 그리고 Langmuir 등온흡착식의 qmax 값을 이용하여 흡착제의 흡착량을 비교하였다. 또한, 폐벌목 활성탄과 상용활성탄의 세공 발달 여부를 비교하기 위해 주사전자현미경(scanning electron microscopy, SEM) 사진을 관찰하였다. SEM 사진 관찰 결과, 폐벌목 활성탄이 국내․외 상용활성탄(DARCO A.C., SPG-100 A.C.)에 비해 세공발달 정도가 우수하며, 벤젠흡착량(q)이 높은 것을 확인할 수 있었다. 본 연구 결과를 통해 폐벌목 활성탄의 상용화 가능성을 검증할 수 있었다.
본 연구에서는 폐벌목의 탄화물의 활성화를 이용한 휘발성 유기화합물(volatile organic compounds, VOCs)흡착에 관한 연구를 진행하였다. VOCs는 자동차, 각종 유기용제, 건축 등의 도장분야에서 많이 발생되고 있으며, VOCs를 제거하는 기술은 소각 및 분해에 의한 제거 기술과 VOCs를 회수하여 재사용 하는 회수 기술로 나눌 수 있는데, VOCs가 고가일 경우에는 회수기술의 사용이 생산비용 면에서 유리하다. 회수기술에는 흡착, 막분리, 응축 등의 다양한 방법이 있으나 이 중에서 흡착은 실제 공정에서 처리방법이 간단하며, 다양한 VOCs의 처리가 가능하고 운영비가 상대적으로 적게 드는 장점으로 인해 많은 연구가 진행되어 왔다. 특히 저농도의 경우 에는 활성탄 흡착방법에 의해 효과적으로 제거가 가능하며, 산업 유기용제의 회수, 에너지 절약 및 자원화 관점에서 흡착기술이 유리한 기술이라 할 수있다[1].
본 연구에서는 제조된 폐벌목 활성탄에 대한 VOCs 흡착제 로의 사용 가능성을 평가하기 위해, 수입 상용활성탄(DARCO Co., 12~20 mesh, granular)과 국내 상용활성탄(SGP-100, 삼천리 활성탄소, pellet)을 준비하여 VOCs 중 벤젠에 대한 정지흡착 비교실험을 수행하였다[2]. 또한 흡착특성을 확인하기 위하여 Langmuir 등온흡착식, Freundlich 등온흡착식과 Toth 등온흡착식을 이용하여 흡착등온식을 비교하였으며[3], 주사 전자현미경(scanning electron microscopy, SEM) 사진을 통해 각각 활성탄의 세공 발달 여부를 확인하였다.
본 연구를 통해 폐벌목 활성탄을 이용하여 VOCs 흡착제로
활용할 수 있는 방안을 마련할 수 있을 것이라 예상되며, 본 연구를 통해 우리나라의 경우 국토의 약 64.1% (국내 산림면적 6,389천 ha)에 해당하는 산지 [4]에서 생산되는 다양한 종류의 임목 중 임지에 방치 또는 수집되어 이용되지 못하는 목재, 다시 말해 폐벌목을 이용하여 고부가가치재라 할 수 있는 활성탄으로써 활용할 수 있는 기반이 마련될 것으로 예상 된다.
VOCs는 상온에서 일반적으로 액체 상태로 존재하다가 기상으로 기화되어 흡착이 이루어지게 된다. 따라서 정지흡착 실험을 수행함에 있어서 이러한 물질의 흡착량을 측정할 경우 기화시키는 부분이 필요하게 되며, 기화된 물질이 P-V-T 관계에서 일정한 상태를 유지하기 위한 저장 공간을 필요로 하게 된다. 본 연구에서는 정지흡착실험의 수행을 위해 Figure 1의 저압 정지흡착 실험장치를 이용하였다[5]. 실험 장치의 구성은 크게 네 부분으로 나뉜다. 원료를 공급해주는 부분과 시료가스를 저장하는 부분, 흡착제가 삽입되어 흡착이 일어나는 부분, 정확한 압력을 읽을 수 있는 측정부 등이다. 본 실험 장치에서는 진공펌프를 이용하여 1.3 × 10-5 kPa 까지 낮추어 초진공 상태를 유지하였다. 또한 가장 중요한 부분인 측정부는 온도와 압력을 측정하는 부분으로 구성되는데, 온도는 강제대류건조기의 온도센서를 이용하여 측정 할 수 있도록 하고 추가적으로 온도프로브를 설치하여 온도편차를 최소화하였다. 압력은 흡착질의 종류가 다양해짐에 따라 기체 특성에 영향을 받지 않는 격막식 압력계를 선택하였으며, 압력의 정밀도를 높이기 위하여 압력전송기(model : PAA-23S)를 설치하였다[5].
본 연구에서 최적의 폐벌목 활성탄을 제조하기 위해 폐벌목의 탄화조건과 화학적 활성화조건을 Table 1에 나타내었다. 우선 최적화된 폐벌목 탄화물[6]과 활성화제(KOH, NaOH)를 이용하여, 폐벌목 활성탄 제조의 최적조건을 찾았으며[7], 본 연구에서는 BET 표면적이 가장 우수한 400 wt%의 KOH를 이용하여 제조한 폐벌목 활성탄의 정지흡착실험을 진행하였다. 또한 연구를 진행하면서 폐벌목 활성탄과 수입 상용활성탄(DARCO Co., 12~20 mesh, granular) 그리고 국내 상용활성탄(SGP-100, 삼천리 활성탄소, pellet)의 벤젠의 흡착능력에 대한 비교평가를 진행하였다. Table 2에 수입 상용활성탄과 국내 상용활성탄의 기본 물성치와 용도를 나타내었다[5].
본 연구에서는 대표적인 VOCs인 벤젠(Cas No. 71-43-2, C6H6)을 흡착질로서 사용하였다. 벤젠은 독특한 냄새를 띠며 증기압이 높다는 특징을 가지고 있다. 벤젠의 높은 증기압으로 인해 대기 중에 빨리 증발되고 대기로 유출되는 속도 또한 다른 물질에 비해 크다고 할 수 있다.
Table 3에 흡착질로 사용된 벤젠의 기본물성을 설명하였다.
흡착질이 벤젠이므로 시료병에 시료를 20 mL 정도 채운 후,
[Table 1.] Optimal condition for the production of activated carbons from Pinus koraiensis[6]
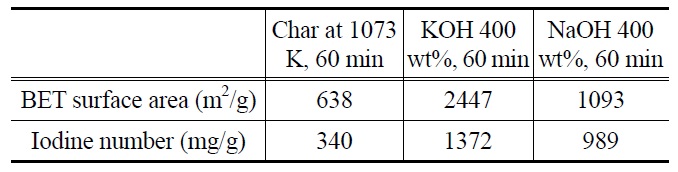
Optimal condition for the production of activated carbons from Pinus koraiensis[6]
[Table 2.] BET surface area of commercial adsorbents[5]
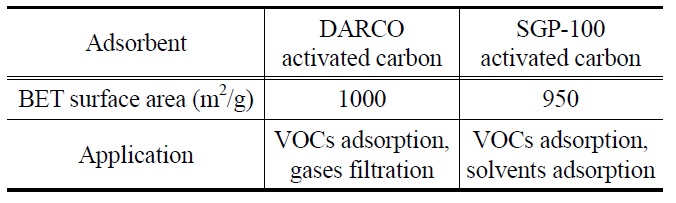
BET surface area of commercial adsorbents[5]
[Table 3.] Constants a and b of van der Waals equation
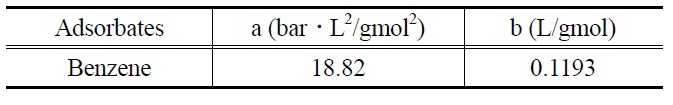
Constants a and b of van der Waals equation
1번과 2번 밸브를 열고 원하는 압력까지 흡착질을 기화시켜서 채운다. 다음, 각 밸브를 잠그고 20분 이상 지나서 정상상태에 도달한 압력, 온도(P1, T1)를 측정한다. 이 때 미리 측정 된 부피 값(V1)을 이용하여 기상의 몰수를 계산한다. 식 (1)인 van der Waals식을 이용하여 보정한다. 계수는 CRC-Handbook data 이용하여 구한다.
5번, 3번, 4번 밸브를 열어서 흡착시킨 후 평형상태에 도달 할 때까지 방치하는데, 보통 20분 정도 걸린다. 이것은 흡착 열에 의한 비평형이 있을 수 있으므로 행하는 것이다. 평형에 도달하면 압력, 온도, 부피(P2,T2,V2)를 측정하는데, 이 값들은 van der Waals식을 이용하여 흡착되고 난 후 기상에 남은 몰수를 계산하는데 사용할 수 있다.
이 때 감소된 기상의 몰수 m이 흡착제에 흡착한 흡착량(q) 인데 다음과 같은 식으로 나타내어진다.
흡착압력은 상온에서 벤젠의 증기압이 9.999 kPa (75 torr) 이므로 실험조건은 7.999 kPa (60 torr)에 이내의 압력범위 내 에서 정지흡착 실험을 진행하였다.
흡착온도는 대기압에서 벤젠의 끓는점이 353.15 K임을 고려하여 온도조건을 303.15 K, 318.15 K, 333.15 K로 각각 설정 하였다[5].
본 연구에서는 폐벌목 활성탄의 VOCs 흡착제로써의 사용 가능성을 평가하기 위해 벤젠의 증기압을 이용하여, 7.999 kPa에 이르는 압력범위와 303.15 K, 318.15 K, 333.15 K의 실험 온도에서 정지흡착실험을 수행하였다.
수입 상용활성탄(DARCO Co., 12~20 mesh, granular)과 국내 상용활성탄(SGP-100, 삼천리 활성탄소, pellet)을 준비하였으며 화학적 활성화 연구 결과[6] 가장 물성치가 우수했던 400 wt%의 KOH를 이용하여 제조한 폐벌목 활성탄의 벤젠에 대한 흡착능력 비교 평가를 진행하였다.
3.1. 주사전자현미경(scanning electron microscopy, SEM) 관찰
Figure 2에서는 각각의 활성탄소에 대한 세공 발달 여부를 SEM 사진을 통해 확인할 수 있었다. 배율은 모두 같은 500배로 하여 측정하였다. 국내 상용활성탄 (a) SGP-100 A.C.은 거대세공이 규칙적으로 발달되어 있는 것을 확인할 수 있었다. 수입 상용활성탄 (b) DARCO A.C.도 역시 거대세공이 규칙적 으로 발달되어 있는 것을 확인할 수 있었으며, 수입 상용활성탄 (b) DARCO A.C.의 거대세공 내부에 또 다른 세공들이 발달되어 있어 중간세공과 미세세공의 발달 가능성이 (a) SGP-100 A.C.에 비해 클 것이라 예상된다. 폐벌목 활성탄 (c) Pinus koraiensis A.C.의 경우에는 (a) SGP-100 A.C.와 (b) DARCO A.C.에 비해 세공의 분포가 보다 규칙적일 뿐만 아니라 세공의 크기 또한 균일하다. 또한 활성탄의 표면과 세공내부 역시 매우 깨끗하게 발달되어 있어 다른 상용활성탄에 비해 중간 세공 내부에 미세세공이 분포할 가능성도 높다[6].
앞서 2절에서 설명한 식 (1)부터 (5)까지의 식들을 이용하여 특정 압력에서의 흡착 몰수
Langmuir 식을 변형하면 다음과 같은 흡착속도식을 구할 수 있다.
여기서, 흡착이 가능한 공간은 (1-
물리흡착에 대한 탈착속도는 다음과 같이 정의할 수 있다.
여기서
식 (6)과 (8)을 동적 평형에 기초하여 흡착속도와 탈착속도가 같을 때 다음의 식이 유도된다.
여기에 식 (7)을 이용하여 새로운 Langmuir 흡착평형상수
식 (10)을 식 (9)에 대입하여 정리하면 식 (11)을 얻을 수 있다. 또한
이를 흡착량에 관한 식으로 다시 정리하면 다음과 같다.
식 (11)을 Langmuir의 일반적인 형태라고 할 수 있으며, 식 (12)에서
또한 식 (10)에서 온도가 증가함에 따라
여기서 -
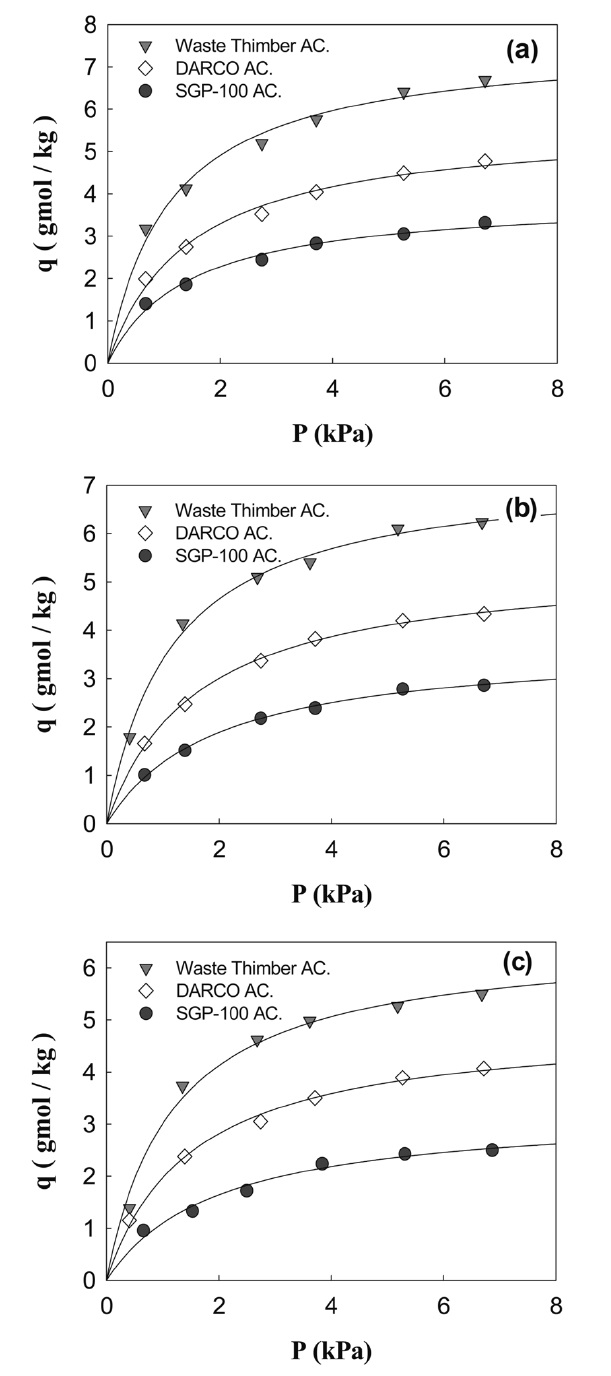
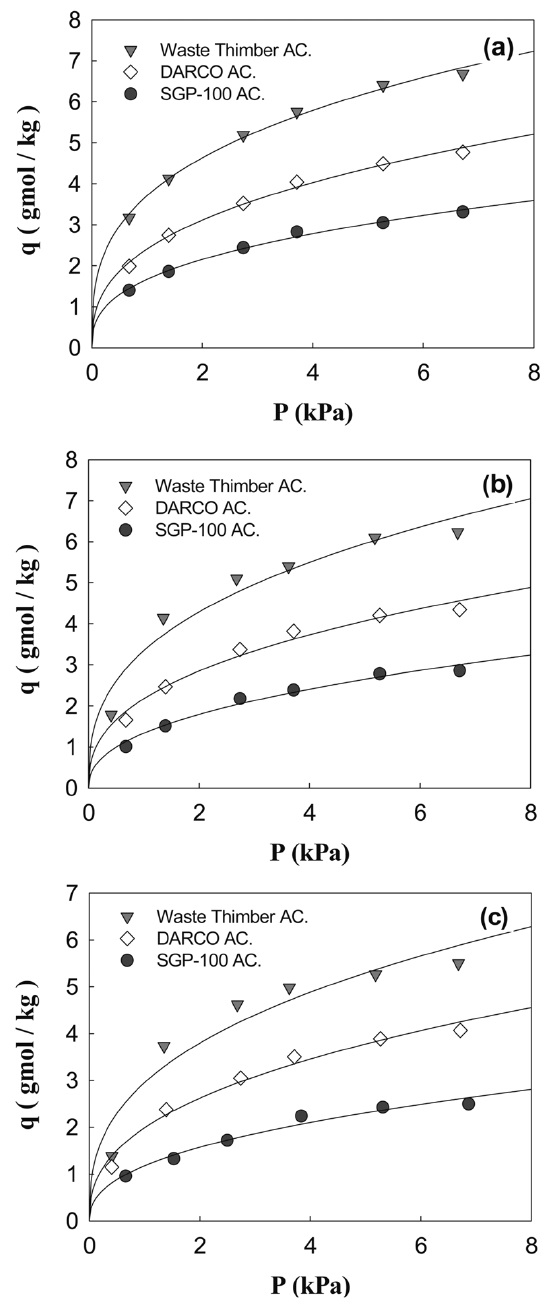
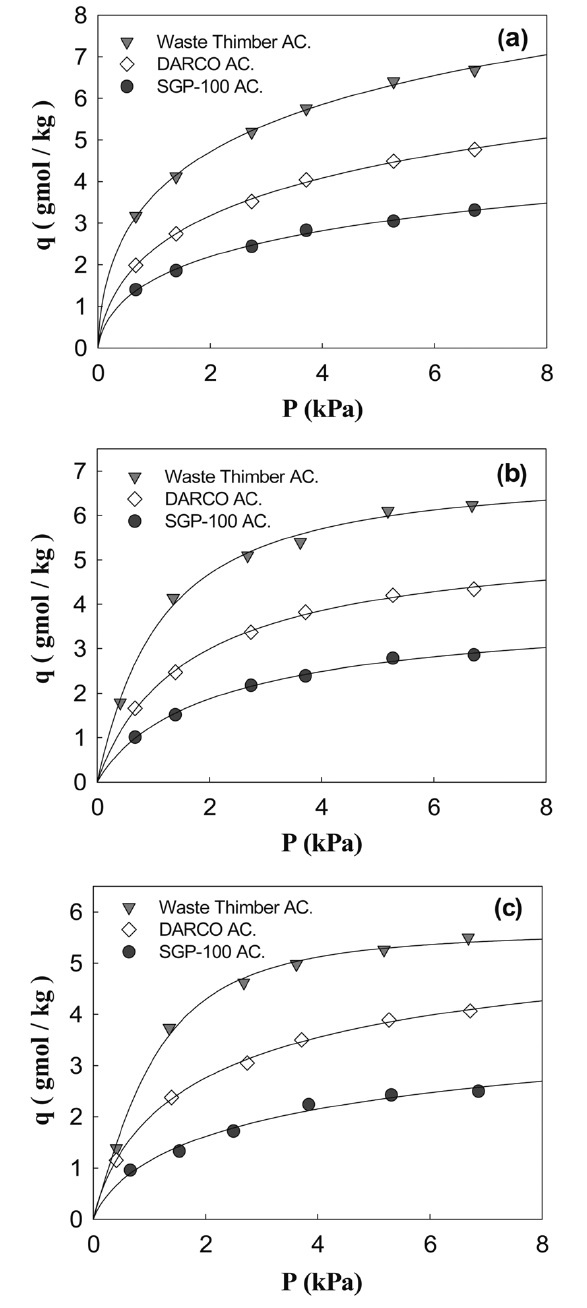
본 연구에서는 활성탄에 의한 벤젠의 흡착량(q)에 따른 실험 결과를 Figure 3~5에 Langmuir 등온흡착식, Freundlich 등온흡착식, Toth 등온흡착식으로 적용한 그래프로 나타내었다. 상온에서 VOCs 중 벤젠의 증기압이 9.999 kPa임을 고려하여, 실험조건은 7.999 kPa에 이내의 압력범위 내에서 정지흡착실험을 진행하였다. 온도 조건은 303.15 K, 318.15 K, 333.15 K로 각각 설정하였는데, 이는 벤젠의 끓는점이 353.15 K이므로 온도를 해당 온도 미만으로 하여 진행하였다. 각각 Langmuir isotherm, Freundlich 등온흡착식 그리고 Toth 등온흡착식을 통해 활성탄의 벤젠흡착실험에 부합하는 등온흡착곡선을 확인하였다[5].
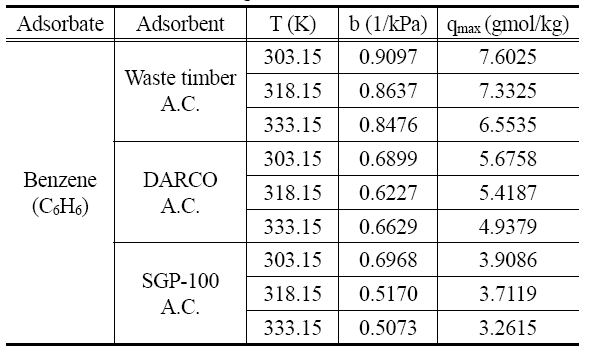
각각의 식으로 벤젠의 흡착량(q)을 적용한 결과 Langmuir 등온흡착식과 Toth 등온흡착식으로 적용한 등온흡착곡선이 큰 오차 없이 잘 맞는 것을 확인할 수 있었다. 따라서 어느 식을 사용하여도 무방하나 Toth 등온흡착식보다 파라미터가 적고 간편한 형태의 식인 Langmuir 등온흡착식이 더 적합할 것으로 생각된다[5]. Freundlich 등온흡착식은 저압영역에서 Henry 법칙을 만족하지 않고, 압력이 증가함에 따라 흡착량(q)이 무한대로 증가하기 때문에 미세세공을 가지는 흡착제의 흡착등온선에는 적합하지 않는 것으로 사료된다. 따라서 본 연구에서는 Langmuir 등온흡착식을 이용하여 활성탄의 벤젠의 흡착량(q)을 계산하여 Table 4에 정리하였으며, b와 qmax값을 정량적으로 표현하였다. Table 4에서 온도가 증가할수록 qmax값은
감소하는 경향을 보이는 것을 확인할 수 있었는데, 이는 흡착 원리와 잘 일치함을 알 수 있다.
외국 상용활성탄인 DARCO A.C.의 벤젠흡착량(q)에 비해 폐벌목 활성탄이 벤젠의 선택적 흡착력에서 우수함을 알 수 있다. 뿐만 아니라 폐벌목 활성탄의 최대 벤젠흡착량(qmax) 또한 DARCO A.C.의 최대 벤젠흡착량(qmax)인 5.6758 gmol/kg과 비교 시 우위에 있음을 확인할 수 있었다. 따라서 폐기물인 폐벌목으로 활성탄을 만들 경우 원료비가 안 들므로 국내․외 상용활성탄에 비해 경제성 면에서 우위에 있다고 판단된다.
[Table 4.] Parameters of langmuir isotherm
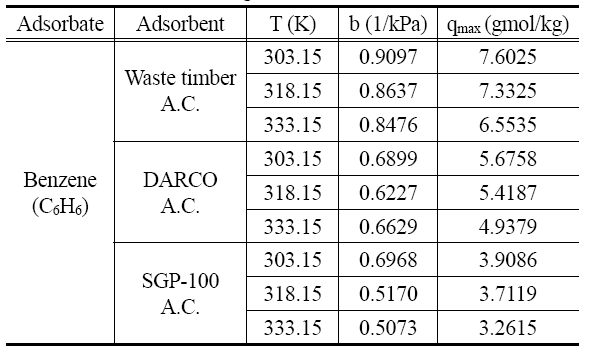
Parameters of langmuir isotherm
폐벌목 활성탄의 벤젠에 대한 흡착특성에 관한 연구를 통해 얻은 결론은 다음과 같다.
1) SEM 사진 관찰 결과 국내․외 상용활성탄은 거대세공이 규칙적으로 발달하였음을 확인할 수 있다. 폐벌목 활성탄의 경우 세공 발달이 규칙적이며, 국내․외 상용활성탄 보다 활성탄의 표면과 세공내부 역시 매우 깨끗하게 발달되어 있어 다른 국내․외 상용활성탄들에 비해 중간세공 내부에 미세세공이 분포할 가능성이 높다.
2) Langmuir 등온흡착식을 적용할 때 온도가 증가할수록 b, qmax값은 감소하고 있으며, 실험결과 폐벌목 활성탄의 최대 흡착량(qmax)이 가장 높게 나타나는 것을 확인할 수 있었다.
3) 실온조건에 가까운 303.15 K와 모든 온도조건에서 폐벌목 활성탄의 최대 벤젠흡착량(qmax)은 국내․외 상용활성탄의 최대 벤젠흡착량(qmax)과 비교하여 큰 값을 가졌다. 경제성 면을 고려해 볼 때 폐벌목 활성탄은 상용화될 수 있으므로 제조 공정 개선과 제조기술 보완 등을 통해 향후 폐벌목의 자원화 가능성을 예측해 볼 수 있다.
4) 실험에 사용한 기상이 벤젠만으로 이루어진 저압 영역에 국한되어 있으므로 향후 추가적인 흡착 실험을 통해 산업화에 필요한 최적의 조업조건을 찾는 연구가 보완되어야 할 것이라 판단된다.
![Experimental apparatus for low-pressure static adsorption[5]. (N : Inline Mixer, P : Pressure Transmitter, MFC : Mass Flow Controller)](http://oak.go.kr/repository/journal/12928/CJGSB2_2013_v19n4_430_f001.jpg)
![Optimal condition for the production of activated carbons from Pinus koraiensis[6]](http://oak.go.kr/repository/journal/12928/CJGSB2_2013_v19n4_430_T001.jpg)
![BET surface area of commercial adsorbents[5]](http://oak.go.kr/repository/journal/12928/CJGSB2_2013_v19n4_430_T002.jpg)