



2006년 필라델피아에서 열린 World Congress of Soil Science에서 일군의 과학자들은
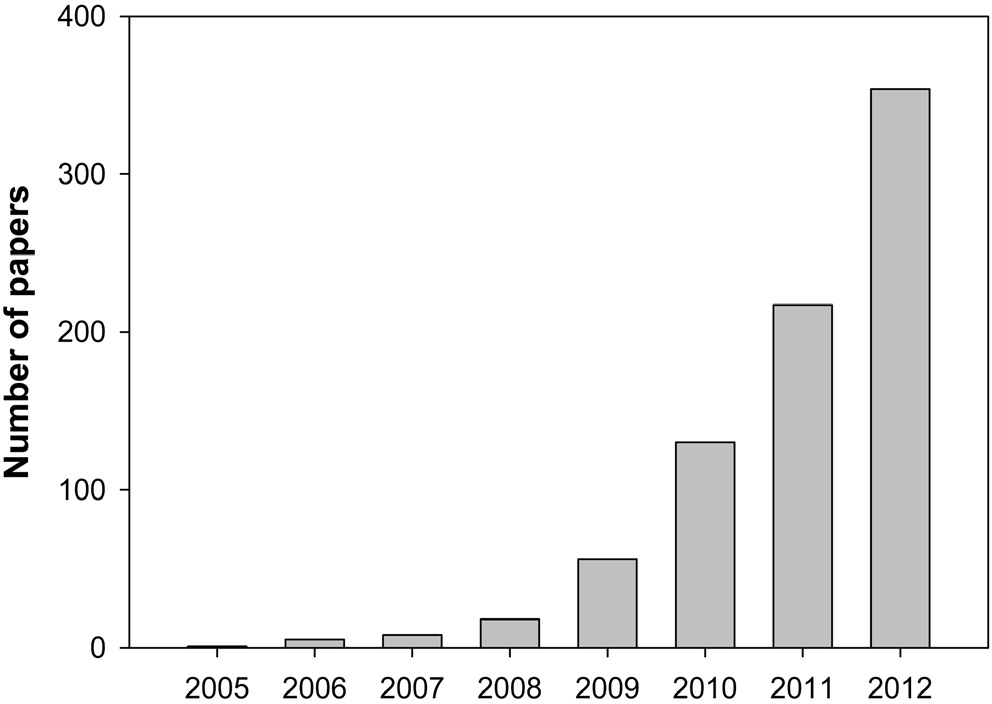
않은 바이오차 관련된 논문들이 2005년 이전에도 발표되었다는 것은 염두에 둘 필요가 있다. 특히 주목할 만한 것은 탄소격리 이슈의 중요성으로 인해 2006년 이후 지금까지 바이오차 관련된 논문이
1879년에 Herbert Smith는 아마존을 탐험하던 중 원주민의 설탕 농업에 대해, 사탕수수의 높이가 3 m에 굵기가 손목 두께에 이르며 경이로운 생산력을 가지고 있다고
바이오차는 농업 생산성 증가와 탄소격리에 있어서의 중요성을 포함하여 4가지 측면에서 연구와 활용의 필요성을 가지고 있다[4]. 즉, (1) 기후변화 대응, (2) 에너지 생산, (3) 토양개량, (4) 폐기물 관리 측면에서 볼 수 있다(Figure 2). 우선, 기후변화 측면에서는 대기중의 이산화탄소를 바이오차의 형태로 고정화하여 토양에 되돌려 넣음으로써 탄소 순환의 속도를 느리게 하고, 오랜 세월동안 이산화탄소 배출을 억제할 수 있다는 원리에 기초한다. 다른 한편으로는 바이오차를 적용함에 따라 이산화탄소보다 기후변화에 영향이 큰 메탄과 아산화질소의 배출량도 저감할 수 있다는 보고도 있다[5,6]. 최근에는 점화효과(priming effect, 바이오차 첨가가 다른 유기물의 이산화탄소 배출에 미치는 영향)에 대한 연구도 많이 진행되고 있다[7]. 두 번째로는 바이오차 생산과정에서 발생하는 기체(바이오가스)와 액체(바이오오일)는 에너지원으로 사용될 수 있다는 것이다. 특히 바이오가스는 바이오차 제조에 필요한 에너지원으로 활용될 수 있어, 고온으로 올리는데 필요한 에너지 필요량을 해소할 수 있다. 그리고 바이오오일은 수송용 연료로 사용될 수 있는데, 2012년 Coolplanet이라는 회사는 차량에 적용하여 시범 도로주행을 한 바 있고, 구글 및 BP의 투자를
받고 있다[8]. 이들에 따르면 일반 자동차의 경우 연간 +5.7톤의 이산화탄소를 배출하는 반면 이 기술은 연간 -3.5톤의 이산화탄소를 배출(즉, 이산화탄소의 저장)한다고 주장하고 있다. 세 번째 토양개량으로서의 중요성에 대해서는 특히 많은 연구가 진행되고 있는데, 바이오차를 토양에 첨가하면 pH 증가, 물 유지 능력 증가, 이온교환 능력의 증가, 미생물 주거지 제공 등 다양한 특성에 의해 농업 생산성을 향상시킬 수 있다는 것이다. 따라서 동남아시아나 아프리카 등과 같이 비료를 충분히 공급하지 못하는 지역에서 바이오차를 비료 대체 또는 비료 사용량 절감을 위해 사용될 수 있다. 네 번째로는 바이오차의 원료로서 목재와 같은 농업 폐기물 뿐만 아니라, 하수슬러지, 유기성 폐기물 등 다양한 폐기물 바이오매스가 재료로 이용될 수 있어, 환경관리 측면에서 유리한 점이 있다. 이 외에도 최근 많이 연구되는 분야로는 환경오염저감과 복원에 활용하는 것인데, 이미 수처리, 대기오염 방지 등에 광범위하게 활용되는 활성탄과 같이 높은 비표면적과 공극을 가지고 있어, 오염물질의 흡착제로 사용될 수 있다. 단순한 흡착제거용 뿐만 아니라, 오염지역에 적용하여 오염물질의 이동성을 제한함으로써 실질적인 인간 및 생태계 유해성을 저감할 수 있는 수단이 될 수 있다.
2007년 Lehmann 교수가
통해 생산되는 가스와 오일로부터 에너지를 회수하고, 바이오차는 토양으로 주입하여 탄소를 반영구적으로 저장함으로써 전체적으로 지구의 탄소함량을 줄일 수 있다는 개념이다(Figure 3)[2]. 이것이 가능한 이유는 바이오차의 안정성에 기인하는데 바이오차는 미생물 분해에 대해 강한 저항성을 가지고 오랜 세월 (수천 년까지) 동안 토양 내에 존재할 수 있기 때문이다. 전체적으로 보면 초기 바이오매스가 가지고 있는 탄소의 약 20%를 토양 속으로 바이오차의 형태로 격리시킬 수 있다.
한편 2008년에는 이 개념에 대한 반론 의견이
사용하는 경우보다 탄소 저감율이 높으며, 지구의 탄소 함량을 12% 저감할 수 있는 것으로 예측하였다.
토양 탄소는 주로 식물의 잎이나 뿌리 잔해물로부터 온다. 전 지구의 토양 탄소는 약 2,300 Gt을 함유하고 있어 식물이 보유하고 있는 550 Gt이나 대기가 보유하고 있는 800 Gt보다 각각 4.2배와 2.9배 더 많다(Figure 5)[15]. 매년 120 Gt의 탄소가 식물의 광합성에 의해 포획되어 반은 식물의 바이오매스로 들어가고 반은 호흡에 의해 이산화탄소로 다시 대기로 배출된다. 식물 바이오매스로 포획된 60 Gt의 탄소는 잔해물의 형태로 토양으로 들어가고, 이는 다시 토양 미생물에 의해 분해되어 대기로 배출됨으로써 균형을 이루게 된다[15]. 토양으로 들어간 식물 바이오매스 중 분해성 탄소 C는 1~5년 안에 분해가 되고, 비분해성 탄소 C는 수십 년에서 수천 년까지도 잔존할 수 있는데, 평균적으로는 약 5~10년의 주기로 순환하는 것으로 알려지고 있다[16]. 토양 유기물의 분해 및 순환 사이클을 느리게 하는 수단으로서 안정화된 유기물 형태인 퇴비가 하나의 대안이 될 수도 있으나, 실제 토양에서의 분해 속도는 일반 유기물과 유사한 것으로 나타났다[17]. 바이오차는 분해속도가 매우 느려 수백 년 이상 잔존할 수 있는데, 이론적으로는 광합성에 의해 포획되는 120 Gt의 20%인 24 Gt의 탄소가 바이오차로 저장될 수 있다[2]. 한편, 지구상의 “slash-andburn”(나무를 태워서 토양에 영양분을 공급하고 지력이 약해지면 경작을 쉬어야 하는 화전농업 방식) 관습에서 “slash-andchar”로 변경하면 0.2 Gt, 농업 및 산림 폐기물로부터 0.16 Gt의 탄소를 저장할 수 있다고 한다[18]. 전 세계의 농경지는 약 1.5 × 1010 ha 정도 있는 것으로 추정되며, Gaunt et al.[19]의 계산에 의하면 10년에 한번씩 이 땅에 바이오차를 적용한다고 볼 때 0.65 Gt/yr에 해당한다고 한다.
기존의 바이오매스 처리방법은 일반 도시 및 농촌의 바이오매스 폐기물의 경우 대부분 매립에 의존하고, 혐기성 환경에서 주로 메탄(CH4) 생성을 야기한다. 한편 질소 성분이 많은 축산 폐기물의 경우 분해되어 메탄이나 아산화질소(N2O)를 생성할 수 있다. 이러한 CH4와 N2O는 지구온난화지수(global warming potential, GWP)가 CO2에 비해 각각 25배와 298배에 이르러 지구온난화에 미치는 영향이 훨씬 크다. N2O는 지구적 CO2 환산가로 계산한 배출량의 8%, CH4는 14%에 달한다. Yanai et al.[5]은 바이오차를 처리한 경우 N2O 발생량이 최대치 기준으로 15% 수준으로 감소하였다고 한다. 토양에서 N2O가 발생하는 기작으로는 1) 질산화: 호기성 환경에서 암모늄 이온의 아질산 이온으로의 산화과정 중의 부산물, 2) 질산화 세균의 탈질 반응: 낮은 산소 농도에서 탈질 질산화 세균에 의해 아질산 이온이 전자수용체로 사용되는 과정에서 발생, 3) 탈질 반응: 혐기성 조건에서 질산 이온이나 아질산 이온의 환원 과정에서 발생한다[20]. 이러한 기작 중에서 DeLuca et al.[21]에 의하면 바이오차를 첨가하면 질산화가 오히려 증가하는 결과를 얻어 질산화 저해에 의한 N2O 발생량 감소는 아닌 것으로 보이고, N2O 환원 미생물의 증가로 보아 탈질 반응 저해에 의한 것으로 추정하고 있다[5]. 바이오차를 첨가하게 되면 토양의 겉보기 밀도가 증가할 뿐만 아니라, 바이오차의 높은 기공성으로 인해 토양의 환기성이 증가하게 된다. 이것은 대기중 메탄의 토양 내로 이동을 촉진하게 되고, 메탄 생성을 억제하는 주요원인인 것으로 추정하고 있다[6]. 이러한 환경에서는 N2O의 탈질 반응도 억제된다는 점에서 유리하다고 할 수 있다.
바이오차를 생산하기 위해서는 산소가 없는 환경에서 약 300~1,000 ℃로

Typical product yields (dry wood basis) obtained by different modes of pyrolysis of wood[22]
가열하는 열분해 기술을 이용한다. 열분해 방식에 따라 크게 다음과 같이 구분할 수 있다.
- 저속 열분해: 느린 가열 속도(5~7 K/min)
- 고속 열분해: 빠른 가열 속도(~300 K/min)
- 플래쉬 열분해: 매우 빠른 가열 속도, 짧은 가열 시간(수초 이내), 고압, 고온
이러한 열분해 방법 중 가열 속도가 느리고, 온도가 낮을수록 생성되는 고형물의 비율은 증가한다(Table 1)[22]. 따라서 바이오차 생산을 위해서는 주로 저속 열분해를 사용하고, 바이오오일 생산을 목표로 하는 경우 고속 열분해를 사용한다. 일반적으로 저속 열분해를 통해 얻는 바이오차 수율은 20~50% 정도로 보고되고 있다. 바이오차의 성분은 탄소가 대부분이며, 산소, 수소와 무기물을 포함한다. 바이오오일에는 수백 종류의 다양한 화학물질의 혼합물로서 산, 에스테르, 페놀류 등을 포함하고 있고, 바이오가스는 CO, CO2, H2, CH4 등으로 되어 있다. 원료가 되는 바이오매스는 파쇄, 건조와 같은 전처리를 거친 후 열분해 반응기에 투여되고, 발생하는 가스는 시스템의 열원으로 재이용될 수 있다(Figure 6)[23]. 바이오오일 성분은 산업용 연료유로 사용되거나 개조 후 수송용으로 사용될 수 있다.
열분해 기술의 적용은 인류의 문명과 함께 하며, 흙을 쌓아 화로를 만들고, 나무를 태우는 방식인 earth-mound kiln 등 다양한 형태로 개발되어 오늘날에까지도 사용되고 있다[24]. 18세기 말에는 기체를 응축하여 활용하는 기술을 사용하였다는 기록이 있고, 19세기 말에는 철로 만든 오븐을 사용하여 기술의 급격한 발전이 이루어져서 나무의 증류 산업이 생겨나게 되었다[24]. 1970년대 이후로 합성 가스(syngas)를 응축하여 바이오오일을 만드는 것에 초점을 둔 고속 열분해개념이 도입되었고, 1980년대 워털루 대학에서 현대의 고속 열분해 장치의 기본형이 개발되었다. 그 이후로 미국, 캐나다, 유럽 등지에서 유동층, 순환형, 회전형 콘, 진공 반응기 등의 다양한 형태의 공정이 개발되었다[24].
전 세계의 바이오차 생산량은 2005년 기준 44백만톤이며, 수율은 바이오매스의 20% 정도이다[25]. 브라질이 가장 큰 생산국으로 연간 9.9백만톤, 태국 3.9백만톤, 이디오피아 3.2백만톤, 탄자니아 2.5백만톤, 인도 1.7백만톤, 콩고 1.7백만톤의 순으로 대부분 개발도상국이나 후진국에서 생산되고 있다[25]. 그러나 대부분의 생산물은 미국에서 소비되고 있고, 그럼에도
불구하고, 대기오염을 발생한다는 이유로 미국에서는 거의 생산되지 않고 있다. 그러나 이러한 대부분의 생산국들이 낙후된 열분해 시설들을 이용함으로써 발생되는 휘발성 기체는 에너지로 회수되지 못하고 바로 대기로 방출되고 있어 여전히 많은 개선이 필요한 실정이다.
유기성 물질의 열분해를 통해 생성되는 재료는 열분해의 정도, 탄소의 함량, 관점 등에 따라 charcoal, soot, black carbon, char, agrichar 등 다양한 이름으로 불려왔다. 한편, 바이오차라는 용어가 2000년대 초반부터 도입되기 시작했는데, 모든 바이오 유기물이 원료가 될 수 있고, 다양한 응용 범위를 포함한다는 의미에서 charcoal이나 agrichar와는 구별하여 사용되고 있다[4]. 이러한 열분해 생성 물질은 구분이 명확하지 않아 연속체 범위에서 다른 성질을 가지는 연소 연속체 (combustion continuum)로 특징을 설명할 수 있다[26]. 바이오차가 생성되는 온도에 따라 낮은 온도에서는 낮은 탄소함량, 낮은 방향성, 높은 반응성, 환경요인에 따른 높은 변형 가능성, 큰 입자, 낮은 이동성을 가지게 되고 높은 온도에서 만들어진 바이오차는 반대의 특성을 가진다. 기공의 경우는 높은 온도로 갈수록 증가하다가 매우 높은 온도에서는 오히려 기공이 줄어드는 경향을 가진다.
열분해 온도를 증가시킴에 따라 결정성이 점차 증가하게 되고, 온도가 3,000 ℃까지 가게 되면 규칙적인 흑연 구조를 가지게 된다[27]. 그러나 일반적인 열분해 온도인 1,000 ℃ 이하에서는 방향성 구조가 형성되면서 일부에서 흑연 층이 존재하는 정도이다. 이 온도에서는 흑연 층과 같은 얇은 두께를 가지지 못하는데 이는 층의 모서리에 존재하는 산소를 포함하는 작용기의 반발력 때문이다. 열분해 온도를 증가시킴에 따라 표면적은 크게 증가한다. 특히 500 ℃ 이상이 되면 급격하게 증가하게 되고, 약 300~2,000 m2/g 정도가 된다. 온도가 800 ℃ 이상 더 고온이 되면 약간 감소하는 것으로 알려져 있다. 표면적의 증가는 주로 미세기공의 발달에 의해 일어나는데, 기공의 부피와 표면적은 거의 비례하는 것으로 나타나고 약 0.7 m3/g 정도까지 보고된 바 있다. 흡착의 관점에서는 크기 50 nm 이상의 거대기공은 크게 중요하지 않은 것으로 생각되어 왔으나, 바이오차가 토양 속에 있을 때는 공기순환을 증가시키고, 식물의 뿌리가 통과하게 되고, 미생물의 거주지 역할을 하는 등 중요한 역할을 하게 된다. 일반적으로 열분해를 하게 되면 원료 물질보다 입자의 크기는 줄어들게 된다. 그리고 열분해 온도가 증가할수록 입자의 크기는 더 감소하게 된다. 압력을 증가시키면 입자들의 응집이 일어나 입자의 크기는 증가하고 고체의 양이 증가하는 것으로 알려지고 있다[28]. 열분해가 진행되면 휘발성 물질이 빠져나가고 점점 더 흑연 결정성이 증가하게 되어 온도가 증가할수록 고체 밀도는 증가하게 된다. 그러나 기공 형성이 증가함에 따라 겉보기 밀도는 감소하게 되는데 800 ℃까지 8.3%에서 24% 정도 감소하는 것으로 나타난다는 결과를 보고한 바 있다[29]. 한편 온도가 더 올라가면 기공의 수축과 소결 현상 때문에 겉보기 밀도가 증가한다. 기계적 강도는 고체 밀도와 밀접하게 관련되어 있기 때문에 열분해를 통해 생성된 바이오차는 원료 물질보다 약 20% 정도 기계적 강도가 증가하는 것으로 나타난다.
바이오매스를 열분해하게 되면 온도가 증가함에 따라 수율은 감소하게 되는데, 바이오매스의 종류, 열분해 조건에 따라 다양하게 나타난다. 온도가 증가함에 따라 바이오차의 원소성분을 조사하면, 산소와 수소의 함량은 감소하고 탄소와 질소의 함량은 상대적으로 증가하게 된다[30]. 이러한 경향은 O/C 비율과 H/C 비율의 감소로 나타나게 되고, H/C 비율의 감소는
방향족 고리와 같이 불포화 탄소가 증가하는 것과 일치한다. 즉 온도 증가에 따라 지방족 탄화수소의 비율은 감소하고, 방향족 탄화수소의 비율은 증가한다. 일반적으로 식물의 셀룰로오스나 리그닌은 H/C 비가 약 1.5이고, 이 비가 0.2 이하이면 “black carbon”(분해가 거의 일어나지 않는 순수한 탄소)이라고 정의한다. 따라서 O/C 비와 H/C 비를 바이오차의 방향성 정도나 성숙도의 한 지표로 사용되기도 한다(Figure 7)[30].
바이오매스의 주요 성분인 셀룰로오스, 헤미셀룰로오스, 리그닌에 대해 TGA (thermogravimetric analyzer) 분석을 한 결과 220 ℃에서 헤미셀룰로오스의 분해가 시작되어 315 ℃에 대부분 분해되었다. 그러나 셀룰로오스의 경우는 315 ℃ 이후에 분해가 시작되어 400 ℃까지 분해가 되었고, 리그닌은 160 ℃에 분해가 시작되어 900 ℃까지 지속적으로 천천히 분해가 되면서도 약 40% 정도는 그대로 남아 있는 것을 볼 수 있었다[31].
토양 내로 주입된 바이오차는 오랜 세월이 지남에 따라 물리적, 화학적, 생물학적인 변화를 거치게 된다. 바이오차가 매우 안정적이고, 수천 년까지도 존재할 수 있는 것으로 알려져 있지만, 완전히 안정적인 것은 아니다. 만약 자연적인 산불에 의해 발생한 바이오차가 변하지 않고 그대로 있다면, 100,000년 만에 지구의 탄소는 모두 바이오차로 변해 있을 것이다[32]. 실제 아마존의
바이오차의 물리적 성질의 변화를 살펴보면 먼저 시간이 지남에 따라 입자 크기가 감소한다. 입자가 분쇄되어 가는 과정은 냉각-해동 사이클, 비와 바람, 식물 뿌리와 곰팡이 균사, 토양 생물에 의한 생물혼탁작용 등의 다양한 원인에 의해 일어날 수 있다. 또한 바이오차가 토양에 오랜 세월 있게 되면 유기물의 흡착이 일어나고, 기공들을 막게 된다. 이와 같이 오래된 바이오차의 경우 다른 유기물(예: 다환방향족 탄화수소)의 흡착능을 감소시키게 되는데, 기공을 막고 표면적을 감소시키기 때문만이 아니라, 표면에 흡착된 유기물과의 상호 관계에 의한 영향이 있으나, 그 이유가 명확하지는 않다.
바이오차가 토양에 주입된 후 시간이 지날수록 바이오차의 방향성 정도는 감소하게 된다. Cheng et al.[33]에 의하면 70 ℃의 고온에서는 비생물학적 산화가 일어나고, 산 작용기의 형성이 증가한다고 한다. 이와 같은 바이오차의 산화과정에 의해 carboxyl, hydroxyl, phenolic, carbonyl, quinone 등의 작용기들이 늘어나고 이는 O와 H의 비율을 증가시킨다. 또한 이러한 산화에 의해 바이오차의 표면은 점점 더 음의 전하를 띄게 되고, 이것이 양이온 치환능(cation exchange capacity, CEC)을 높게 하는 원인이 되기도 한다. 한편 바이오차는 미네랄 성분과의 상호관계를 통해 안정화될 수 있다. 바이오차는 자유롭게 점토나 실트 입자와 섞여 있을 수 있고, 작은 바이오차 입자가 큰 미네랄 표면에 결합되어 있을 수도 있고, 작은 미네랄 입자가 큰 바이오차 입자 표면에 결합되어 있을 수도 있다. 이러한 형태의 바이오차와 미네랄의 상호관계는 바이오차의 안정화를 크게 향상시킬 수 있고, 오랫동안 토양 속에 존재할 수 있게 한다.
Cheng et al.[33]에 의하면, 약 4개월간의 배양 실험을 통해 비생물학적 원인에 의해 바이오차 산화가 더 많이 일어나고, 생물학적 원인에 의한 것은 매우 작았다고 보고하였다. 그러나 다양한 연구를 통해 생물학적 원인에 의한 바이오차의 분해도 보고되고 있다. 백색부패 곰팡이가 내놓은 효소에 의해 바이오차 분해가 일어나기도 하고, 다양한 종류의 미생물 군락의 형성이 일어나기도 한다. 바이오차가 있는 토양에 포도당과 같은 풍부한 영양분을 첨가할 경우 공동대사에 의해 바이오차의 분해가 촉진되는 현상도 보고된 바 있다.
바이오차는 토양의 물리적, 화학적, 생물학적 환경에 큰 영향을 미칠 수 있고, 다양한 결과가 보고되고 있다. 일반적으로 토양의 양이온 치환능(CEC)은 식물이 섭취할 수 있는 형태의 영양분과 관계가 있다. 토양 내 유기물의 양이 증가할수록 CEC 값이 증가하며, 이는 바이오차도 마찬가지이다. 그러나 바이오차는 단위 탄소 당 양이온 흡착능이 일반적인 토양 유기물(soil organic matter, SOM) 보다 훨씬 크다. 그 이유는 표면적이 더 크고, 더 큰 음의 표면 전하를 가지고 있고, 전하 밀도가 더 크기 때문이다[35]. 일반적으로 토양 유기물의 CEC는 낮은 pH에서는 매우 낮고, pH가 증가할수록 증가한다. 바이오차에서도 이러한 경향은 마찬가지지만, 바이오차가 만들어지는 온도에 의존한다. 바이오차가 만들어지는 온도가 증가할수록 pH도 증가하고, CEC 값도 증가하는 경향을 보인다(Figure 8)[23]. 바이오차 제조 온도가 높을 경우 전기전도도가 높고, 추출가능한 질산성 질소 함량이 높은 반면, 제조 온도가 낮을 경우 추출 가능한 인, 암모늄 이온, 페놀의 양은 증가하는 것으로
보고된 바 있다[36]. 한편 바이오차가 만들어지는 온도가 증가할수록 탄소의 회수율이 감소하는 것을 고려하면 최적온도가 존재하게 되는데, 약 450-550 ℃ 범위가 최적이 된다. 특히 이러한 범위에서 표면적이 급격하게 증가하여, 바이오차의 물리화학적 특성도 크게 변화하고, 토양에 미치는 영향도 크게 증가한다.
바이오차는 토양 내 영양분의 흡착과 침출, 식물에 의한 이용성에 영향을 미친다. 바이오차는 제초제 등의 유기물에 대한 흡착을 촉진시킨다. 그 결과 제초제의 잡초에 대한 영향을 감소시켜, 잡초를 제거하기 위해 요구되는 제초제의 양을 증가시키기도 한다[37]. 바이오차의 토양 내 질소에 대한 영향은 매우 복잡한데, 바이오차의 첨가량이 높을 때 암모늄 이온의 침출량을 감소키기도 하고[38], 바이오차의 종류에 따라 큰 영향을 미치지 않는다는 보고도 있다[39]. 특히 바이오차 자체의 질소함량이 높을 경우에는 초기에 질산성 질소의 침출량이 증가하기도 한다[39]. 특이한 사실은 바이오차의 표면이 음의 전하를 가지고 있음에도 불구하고, 음이온인 인산의 흡착량이 일반 토양 유기물이나, 퇴비 유기물보다 훨씬 크다는 것이다. 이는 식물이 인을 흡수할 때 더 유리한 역할을 하는 원인이 되게 한다[33]. 바이오차를 토양에 첨가함에 따라 일반적으로 pH는 증가하게 되고 이러한 라임 효과는 토양 개량제로 흔히 사용되는 calcite의 약 33%에 해당하는 능력을 가지고 있는 것으로 보고된 바 있다[40].
바이오차를 토양에 첨가한 후 토양 내 미생물 군집 및 성장에 미치는 영향은 최근 몇몇 연구결과가 보고되고 있지만, 여전히 미지의 세계이다. 토양의 특성, 바이오차의 적용량, 바이오차의 특성, 미생물 환경, 토양의 유기물, 무기물 환경 등에 의해 미생물 성장이 증가하기도 하고, 감소하기도 하며, 별 영향을 받지 않는 경우도 있다. 바이오차의 일차적인 영향은 바이오차로 인해 증가하는 탄소와 영양분(질소, 인 등)에 의한 것이라고 할 수 있다. 그러나 바이오차로부터 미생물로의 탄소와 영양분의 이동에 대한 직접적인 단서가 여전히 부족하다[41,42]. Liang et al.[43]은 미생물 수가 증가하는 이유는 바이오차 토양의 유기물 이용성의 증가에 있다기 보다는 바이오차가 제공하는 미생물에게 유리하고 천적으로부터 보호될 수 있는 주거지에 있다고 보고하였다. Luo et al.[44]은 350 ℃와 700 ℃에서 만든 바이오차를 pH 3.7과 pH 7.6에 첨가하여 그 영향을 조사하였다[44]. 바이오차로부터 미생물로 전달된 탄소의 양은 낮은 pH에서는 바이오차 제조온도와 관계없이 모두 증가한 반면, 높은 pH에서는 고온에서 제조된 pH의 증가 효과가 거의 없었다[44]. 낮은 pH에서 고온제조 바이오차 첨가에 의한 미생물 성장의 증가 이유는 바이오차 첨가에 의한 pH 증가로 Al과 Mn의 독성 감소에 있다고 보았다. 바이오차 첨가에 의한 미생물, 바이오차, 토양, 화학물질 들의 상호 관계에 대한 Luo et al.[44]의 설명에 의하면 바이오차의 첨가에 의해 미생물 성장이 증가하는 이유는 크게 1) 바이오차로부터 공급되는 탄소 및 영양분의 증가, 2) 바이오차에 의해 제공되는 보다 유리한 미세 환경의 존재, 3) 특히 낮은 pH 토양의 경우, pH 증가를 통한 Al, Mn의 독성 감소와 용존성 영양분의 증가에 있는 것으로 보았다.
바이오차가 토양에 첨가된 후 토양화학 및 농작물에 미치는 영향에 관한 연구가 활발하게 진행되고 있다. 아마존 유역의 비옥한 흙인
바이오차를 토양에 첨가했을 때 작물에 미치는 영향은 너무나 복잡하고 다양하여 항상 그 결과가 좋다고 말할 수는 없다. 현재까지 많은 연구에서 바이오차 첨가가 농작물 생산성을 향상시킨 결과도 있지만 반대로 감소시킨 결과도 보고되고 있다. 2011년 Jeffery et al.[56]은 관련된 연구 16편에서 처리기준으로 177건에 대해 메타분석을 실시하여 그 영향을 조사하였다[56]. 최종 결과는 아주 크지는 않지만 통계적으로 유의미한 것으로 평균 10% 생산성 증가(-28%에서 +39%)를 보였다. 특히 생산성 증가를 보여준 조건으로는 산성 토양(14%), 중성 토양(13%), 큰 입자의 토양(10%), 중간 크기 입자의 토양(13%)이었다. 이러한 결과로부터 작물 생산성을 증가시키는 주요 기작은 pH 개량과 물 유지 능력에 있는 것으로 볼 수 있다. 작물 생산성을 가장 증가시킨 그룹 중 하나는 토양 적용량을 100 t/ha 이상일 때로 39% 향상 결과를 보였다. 한편 바이오차의 원료는 작물 생산성에 큰 영향을 미쳤는데, 가금류 폐기물로 만들 경우는 28% 향상, 슬러지로 만든 경우는 -28%로 오히려 가장 안 좋은 결과를 보였다. 가금류 폐기물은 풍부한 질소를 함유하기 때문인 것으로 생각이 되나, 슬러지의 경우는 그 원인이 명확하지 않다. 지금까지는 보통 1, 2년 정도의 결과들이며, 장기적인 효과에 대한 연구결과가 쌓여야 보다 정확한 해석이 가능할 것이다.
바이오차는 산불과 같은 자연적인 화재로부터 발생할 수 있는 자연의 산물이기도 하면서, 오래전부터 인류의 농업 생산성을 증대시키기 위해 효율적으로 생산되고 사용되어 온 인간의 산물이기도 하다. 오늘날 바이오차는 지구의 기후변화 저감을 위한 수단이 될 수 있다는 새로운 관점과 이를 뒷받침하는 다양한 과학적 증거들의 발견으로 인해 그 효용성이 크게 주목받고 있다. 인류의 미래를 위협하는 기후변화 문제, 식량문제, 날이 갈수록 심각해지는 에너지 문제, 주위에 넘쳐나는 유기성 폐기물의 문제, 물, 대기, 토양의 심각한 환경오염의 문제들과 밀접하게 관련이 있는 바이오차의 특성은 이를 어떻게 효율적으로 생산하고, 현명하게 시스템적으로 구성하여 활용하느냐에 따라 그 효용성이 결정된다고 할 수 있다. 이를 위해서는 1) 사회, 환경, 경제적 효용성을 기준으로 하는 효과적인 바이오매스 원료 확보 방안의 탐색, 2) 다양한 바이오매스를 원료로 하여 생산되는 바이오차의 특성 규명, 3) 효율적이고 경제적인 바이오차, 바이오에너지, 바이오가스의 생산방법 및 스케쥴링 연구, 4) 생산물의 다양한 응용분야(농업, 환경, 에너지 등) 발굴, 5) 원료에서 응용까지 유기적이고 종합적인 고려를 통한 효용성 극대화와 같은 연구 분야를 지속적으로 발굴하고 추진해야 할 필요가 있을 것이다.
![Motivation for applying biochar technology, reproduced from ref[4].](http://oak.go.kr/repository/journal/12617/CJGSB2_2013_v19n3_201_f002.jpg)
![Comparison of carbon negative biochar sequestration to carbon neutral photosynthesis[2], with permission from the publisher.](http://oak.go.kr/repository/journal/12617/CJGSB2_2013_v19n3_201_f003.jpg)
![Overview of the sustainable biochar concept[14], with permission from the publisher.](http://oak.go.kr/repository/journal/12617/CJGSB2_2013_v19n3_201_f004.jpg)
![The diagram of the global carbon cycle in billions of tons of carbon per year[15].](http://oak.go.kr/repository/journal/12617/CJGSB2_2013_v19n3_201_f005.jpg)
![Typical product yields (dry wood basis) obtained by different modes of pyrolysis of wood[22]](http://oak.go.kr/repository/journal/12617/CJGSB2_2013_v19n3_201_t001.jpg)
![The overall process of pyrolysis for the production of biochar[23], with permission from the publisher.](http://oak.go.kr/repository/journal/12617/CJGSB2_2013_v19n3_201_f006.jpg)
![Yield and elemental percentages associated with the heating of Pinus resinosa sapwood to the indicated temperatures, reproduced from ref[30].](http://oak.go.kr/repository/journal/12617/CJGSB2_2013_v19n3_201_f007.jpg)
![Temperature effects on carbon recovery, cation exchange capacity (CEC), pH, and surface area[23], with permission from the publisher.](http://oak.go.kr/repository/journal/12617/CJGSB2_2013_v19n3_201_f008.jpg)