가변부피 투시셀이 장착된 고압 상평형 장치를 사용하여 이산화탄소 + 계면활성제 이성분계와 이산화탄소 + 계면활성제 + 물 삼성분계의 상평형 거동을 318 K부터 348 K의 온도범위에서 관찰하였다. 계면활성제로는 소르비탄 모노팔미테이트를 사용하였다. 이산화탄소 + 소르비탄 모노팔미테이트 이성분계에서 관측된 운점압력은 온도가 상승함에 따라 증가하며, 소르비탄 모노팔미테이트의 조성이 0.226 wt%에서 최대 운점압력이 측정되었다. 반면에 계면활성제의 농도를 0.1 wt%로 고정한 삼성분계에서 관측된 운점압력은 온도와 물의 조성이 증가함에 따라 커지는 것을 확인할 수 있었다. 물의 농도를 0.2 wt%로 고정한 삼성분계에서의 압력-조성의 곡선은 상대적으로 수평의 형태를 나타냈다. 이 때, 운점압력은 온도와 계면활 성제의 조성이 증가함에 따라 상승함을 확인할 수 있다.
이산화탄소를 이용한 초임계 유체기술은 최근 다양한 화학산업분야에서 환경친화적인 새로운 공정의 개발에 응용되고 있다[1]. 확산이 빠르고 높은 용해성, 빠른 침투성, 빠른 물질이동 등의 초임계 유체 장점을 이용한 기술은 친환경, 에너지 절감, 고효율성을 가진 효과적이고 실용적인 방법으로써 적용되고 있다. 초임계 이산화탄소는 무색, 무취에 화학적 안정성을 가지며 인체에 독성이 없고 비교적 용이한 임계점을 가져 여러 산업분야에 광범위하게 이용되는 용매이다. 그러나 물이나 친수성 물질은 초임계 이산화탄소 내에서 굉장히 낮은 용해성을 지니기 때문에 이를 개선시키기 위해 이산화탄소와 물 사이의 미셀(micelle)을 형성함으로써 용해도를 향상시키는 역할을 하는 계면활성제를 활용한 연구 또한 다양하게 이루어지고 있다. 이와 같은 연구들은 혼합물의 상거동 측정을 함으로써 초임계 유체 내에서 시료의 상 분리 경계를 알 수 있으며 초임계 공정설계의 기초데이터로 사용될 수 있다[2-6].
미셀의 형태는 계면활성제의 농도에 따라 달라질 수 있으며, 용매의 온도에 따라 계면활성제의 구조가 바뀜을 확인할 수
있다. 마이크로 에멀젼을 형성시켜 초임계 이산화탄소 내 물의 용해도를 높이기 위해서 계면활성제의 적절한 조건과 이에 맞는 공정 조건(온도, 압력)을 조절해야 한다. 연구에 사용된 계면활성제인 소르비탄 모노팔미테이트의 평균 분자량은 대략 402.57로, 구조식은 Figure 1에 나타난 바와 같으며 팔마트산의 소르비탄 에스테르와 다이하이드리드로 구성된 무극성 계면활성제로써 주로 식품 공정이나 의약품공정에서 유화제의 역할을 한다[7].
소르비탄 모노팔미테이트의 HLB (Hydrophile-Lipophile Balance) 값은 6으로 상대적으로 친유성에 가까운 물질이다. HLB가 6인 계면활성제는 Water-oil 에멀젼을 형성하는데 더욱 안정적인 것을 문헌에 보고되고 있다[8,9].
본 연구는 등온 조건에서, 초임계 이산화탄소 + 소르비탄 모노팔미테이트의 이성분계의 조성의 변화에 따른 상전이 압력을 323~348 K의 온도범위에서 운점(cloud point)의 측정을 통하여 얻었다. 또한, 등온 조건에서 초임계 이산화탄소 + 소르비탄 모노팔미테이트 + 물의 삼성분계의 조성의 변화에 따른 평형압력은 318-348 K의 범위에서 운점압력을 측정하여 얻었다. 실험으로부터 측정된 데이터로부터 이산화탄소 + 소르비탄 모노팔미테이트의 이성분계와 이산화탄소 + 소르비탄 모노팔미테이트 + 물의 삼성분계에 대하여 평형조성 및 온도의 변화에 따른 운점압력 변화를 비교하였다.
본 연구에서 사용된 이산화탄소(PSG Co.)는 99.999%의 초고순도이며, 계면활성제로 사용된 소르비탄 모노팔미테이트 (Sigma Aldrich)는 99%의 순도로써 정제없이 그대로 사용하였다. 또한, 삼성분계 실험 시 사용한 증류수(distilled water, Samchun Pure Chemical Co. Ltd)는 순도 99.999%로 정제없이 그대로 사용하였다.
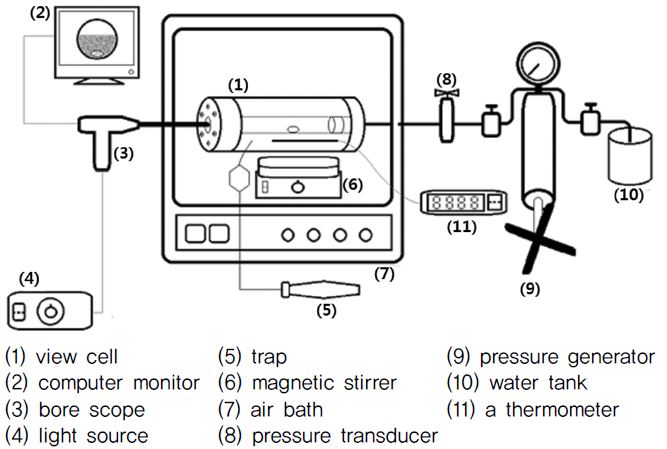
본 실험에서는 고압 상 평형 측정 실험으로 가변 부피 평형조를 이용하여 Figure 2와 같이 장치를 구성하였다[10]. 기본적으로 반응기 내부에 피스톤으로부터 계의 부피를 조절하여 압력을 조절할 수 있도록 하였고, 반응기 내부의 압력을 측정하기 위해서는 압력발생기(High Pressure Equipment Co., Model No 50-6-15)와 압력게이지(VALCOM Co., Model VPRQ-500K)를 사용하였다.
실험에 필요한 온도 조절은 항온조(대일엔지니어링, DMC-
122SP Model)를 이용하였으며, 반응기 내부의 변화를 관찰하기 위해서 보어스코프(Olympus, R100-038-000-50 Model)와 컴퓨터로 함께 연결된 CCD 카메라(Watec Co., WAT-202D Model)를 사용해 모니터로 확인하였다. 반응기의 피스톤 부위는 밀봉을 위하여 바이톤(Viton) 재질의 O-ring을 사용하였고, 반응기 내부에 주입된 이성분계, 혹은 삼성분계의 물질들이 잘 혼합되도록 마그네틱 바(magnetic bar)를 함께 넣어주며, 교반 속도조절은 외부 교반기를 이용해 조절하였다[11,12].
이물질이 남아 있지 않도록 완전히 세척이 된 평형조에 이산화탄소 + 계면활성제의 이성분계 실험에서는 계면활성제를, 이산화탄소 + 계면활성제 + 물의 삼성분계 실험에서는 계면활성제와 물을 평형조 내부로 주입한다. 계면활성제는 일회용 시약접시에 담아 전자저울로 무게를 측정한 후 주입하였고, 물은 주사기를 이용해 평형조 내부에 주입 전과 주입 후에 무게를 측정하였다. 계면활성제 및 물을 주입한 뒤 평형조 내부에 남아있는 공기를 없애기 위해 진공 펌프를 이용하였다. 평형조 내부가 진공상태가 된 후 액체 이산화탄소를 포함한 용기를 평형조에 연결하여 주입 전 후의 무게를 전자저울을 통해 측정하여 이산화탄소를 정량하였다. 평형조 내부에 물질을 주입한 뒤에는 Figure 2와 같이 설치하였다. 설치가 완료된 평형조의 압력을 올린 뒤 평형조를 포함한 항온조를 가열하였다. 반응기 내부의 온도와 압력이 일정하여 평형에 도달한 후에 압력을 천천히 낮추어 반응기 내부의 혼합물이 상전이가 일어나며 뿌옇게 흐려지는 지점(cloud point)에서의 압력을 측정하였다[13,14]. 348 K에서의 운점압력을 측정한 뒤 항온조의 온도를 보다 낮게 설정 후 새로운 설정온도에서 평형상태가 되도록 기다린 뒤 동일한 방법으로 운점압력을 측정하고, 각각 5 K간격으로 318 K까지 각 온도별 운점압력을 측정하였다.
3.1. 이산화탄소 + 소르비탄 모노팔미테이트 이성분계
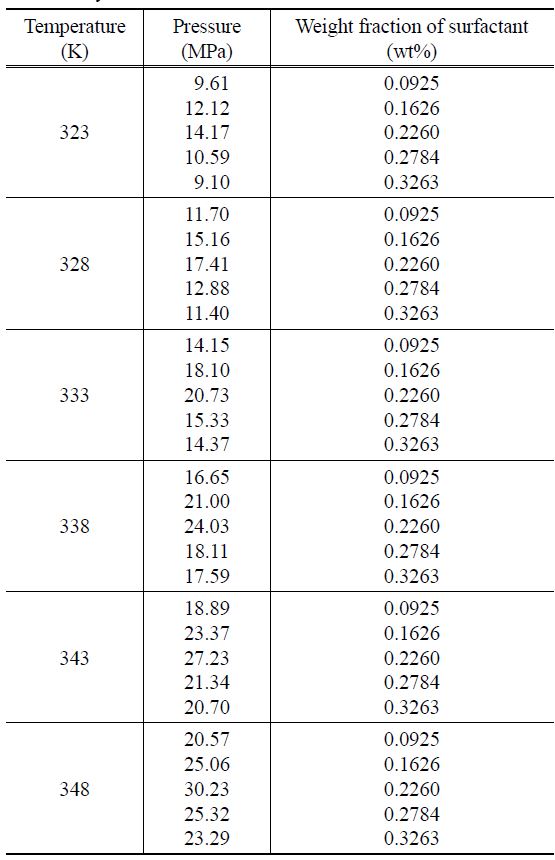
이산화탄소 + 소르비탄 모노팔미테이트 이성분계에서 운점압력은 계면활성제의 조성을 0.0925 wt%부터 0.3263 wt%의 범위로 변화시켜가며 측정하였다. 조성의 변화에 따른 측정된 운점압력 실험 결과는 Table 1과 Figure 3에 나타내었다. 일정량의
[Table 1.] Measured cloud points of CO2+ sorbitan monopalmitate system
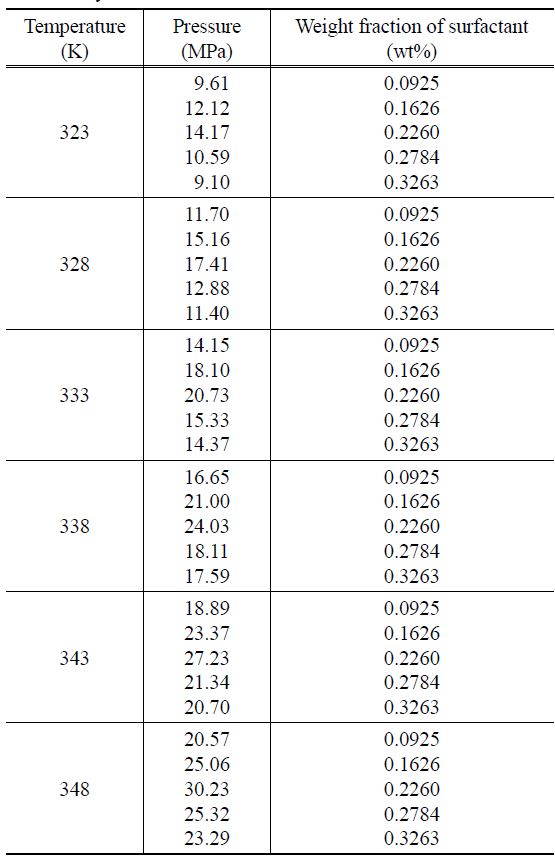
Measured cloud points of CO2+ sorbitan monopalmitate system
계면활성제를 포함한 경우 이산화탄소 + 소르비탄 모노팔미테이트 이성분계를 323 K에서 348 K까지의 온도범위에서 주어진 온도에 따른 상전이 압력인 운점압력을 측정하였다. 평형조 내부에 압력을 가함에 따라 혼합물은 계면활성제와 이산화탄소 사이의 마이크로 에멀젼을 형성하기 시작한 후, 더욱 높은 압력에서 균질상을 이루게 된다. 등온에서 반응기 내부에 압력을 감소시키게 되면 이산화탄소-계면활성제의 균질상이 두 상으로 분리되어 운점압력을 관측할 수 있으며 화면이 어두워지는 지점을 상전이 압력으로 측정하였다.
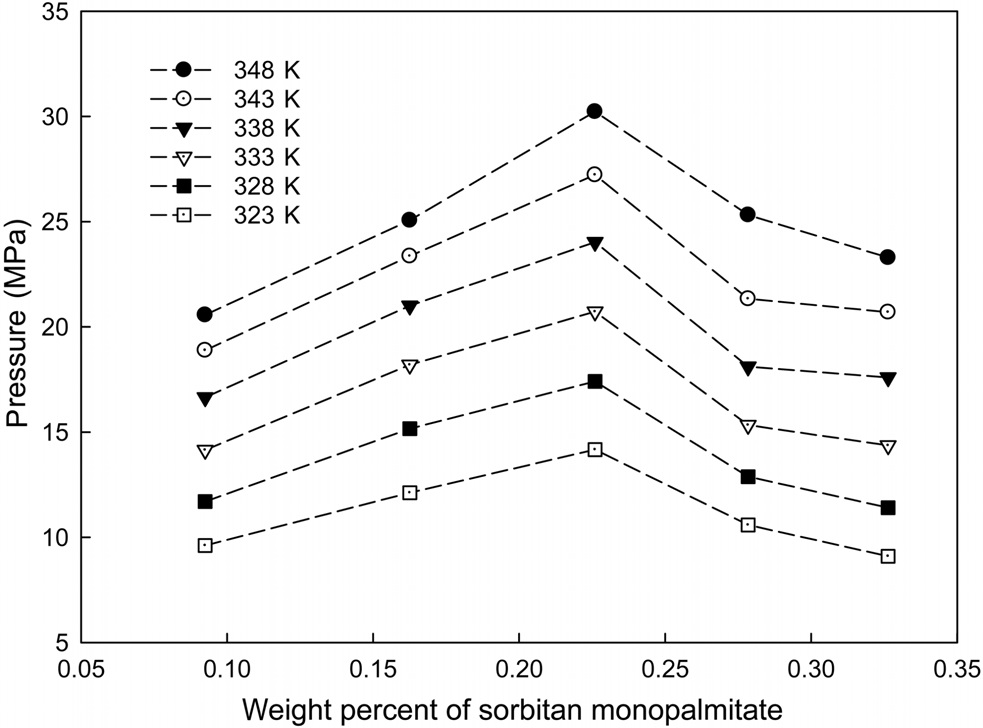
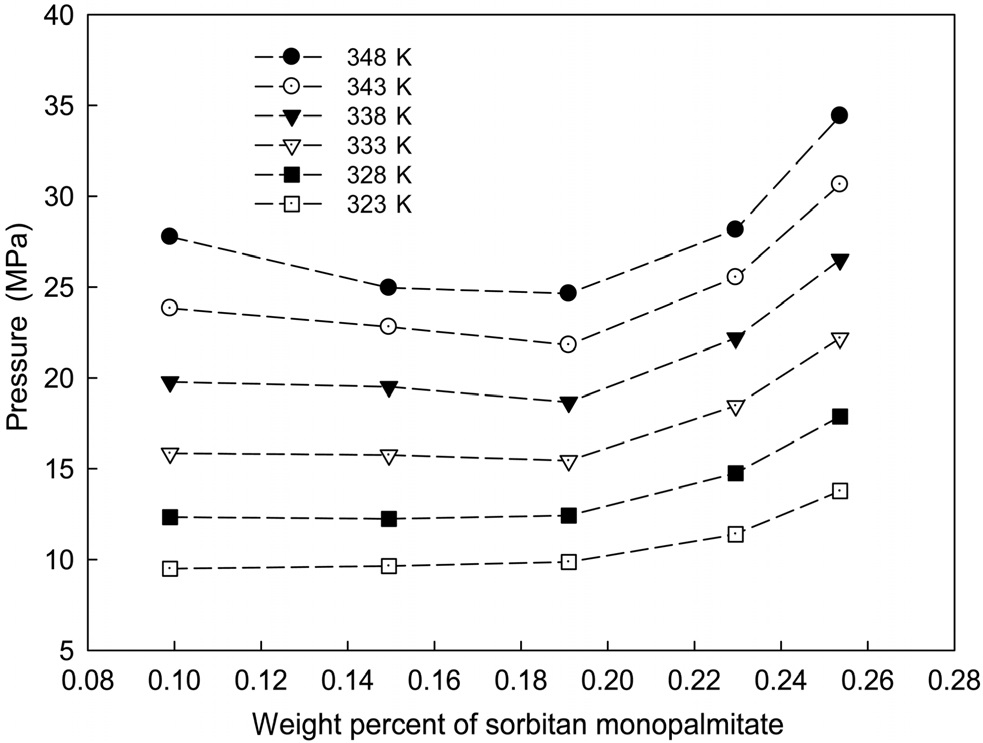
Figure 3으로부터 운점이 관측되는 압력은 온도가 상승함에 따라 증가하는 것을 확인할 수 있다. 일정한 온도조건에서 이산화탄소 + 소르비탄 모노팔미테이트의 상거동을 살펴보면, 계면활성제의 조성의 증가에 따라 운점압력이 상승하며, 0.226 wt% 부근에서 최대의 운점압력이 측정되며 계면활성제의 조성이 더 증가함에 따라 운점압력이 다시 감소함을 확인하였다.
3.2. 이산화탄소+소르비탄 모노팔미테이트+물 삼성분계
이산화탄소 + 소르비탄 모노팔미테이트 + 물 삼성분계 혼합물의 운점압력을 318 K에서 348 K의 온도범위에서 측정하였
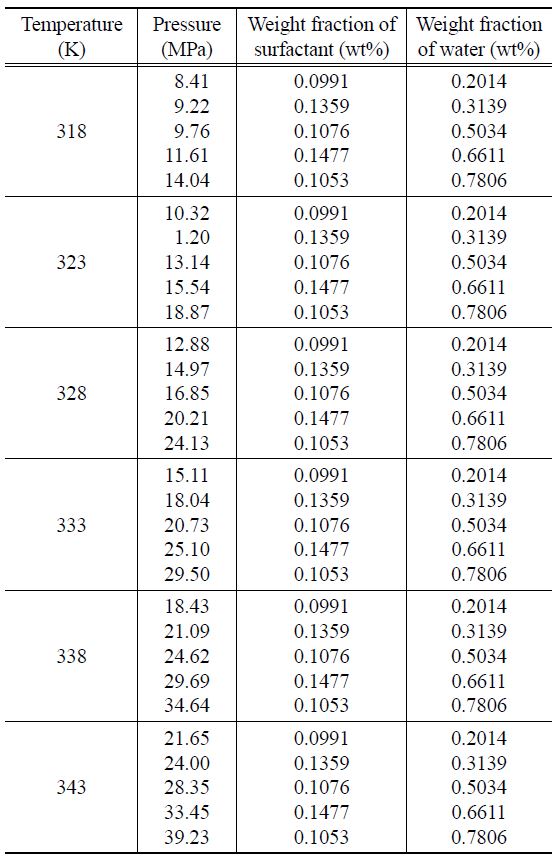
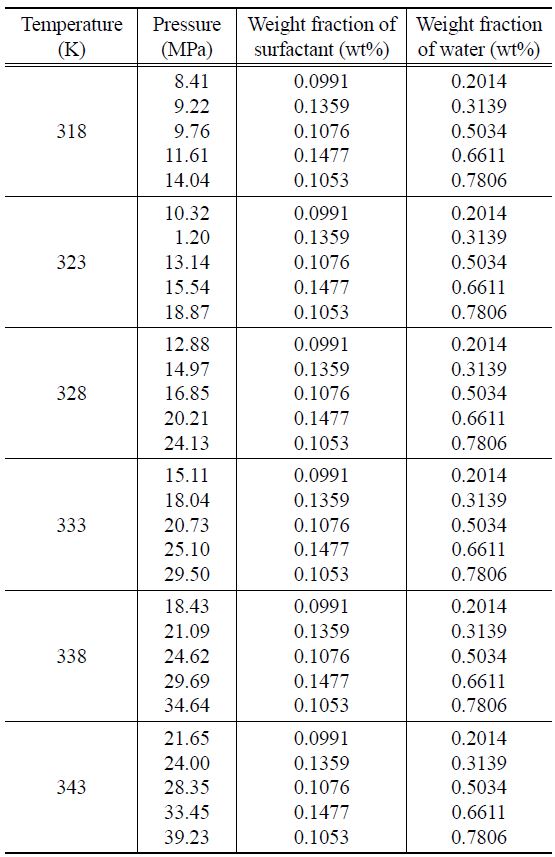
Measured cloud points of CO2+ sorbitan monopalmitate + water system at 0.1 wt% of Surfactant
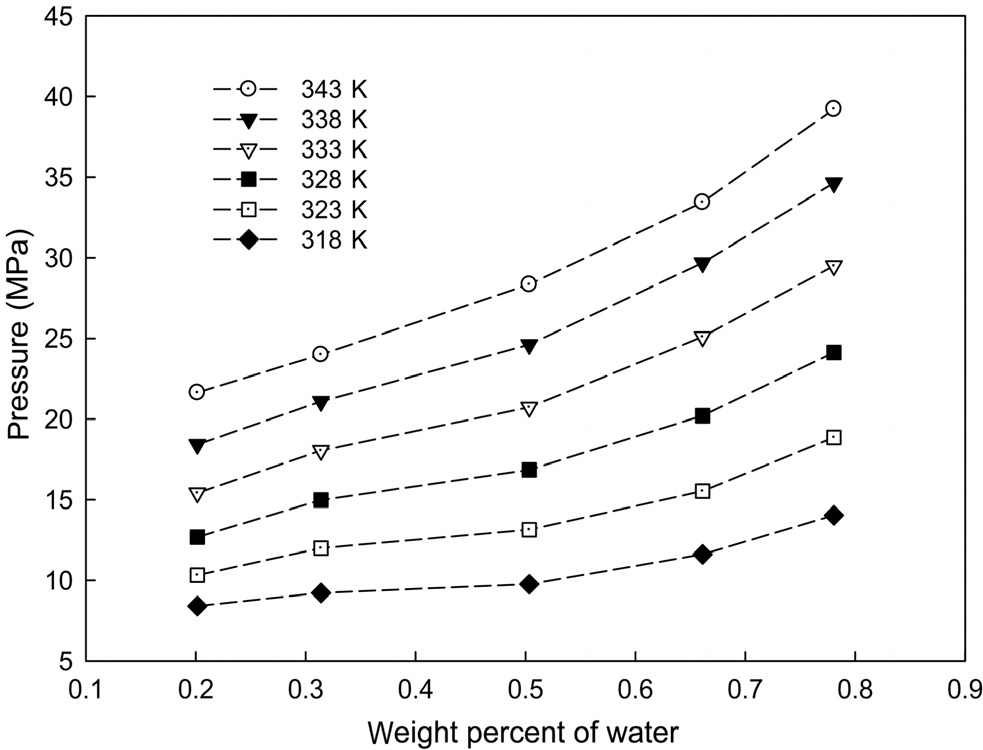
다. 등온에서 계면활성제의 조성을 약 0.1 wt%로 일정하게 두고 물의 조성을 약 0.2 wt%부터 0.8 wt%까지 변화시켰을 때 물의 조성변화에 따른 운점압력의 변화를 측정하였다. 계면활성제의 조성을 일정하게 유지한 삼성분 혼합물의 물의 조성 변화에 따른 상전이 압력의 실험결과값은 Table 2와 Figure 4에 나타내었다. 계면활성제와 물의 일정조성에서 온도가 상승함에 따라 상전이 압력이 증가됨을 확인할 수 있다. 또한, 삼성분 혼합물에 포함된 물의 조성이 증가할수록 운점압력이 상승함을 알 수 있다.
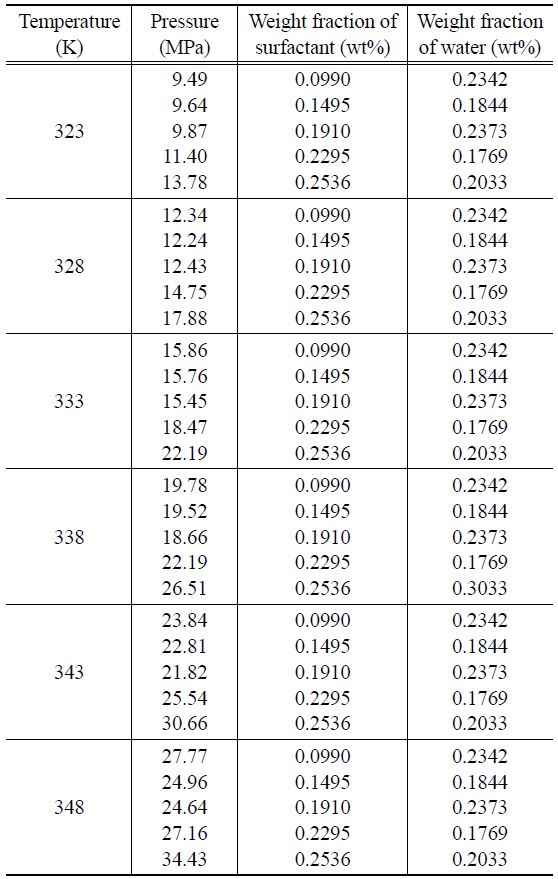
등온에서 물의 조성을 약 0.2 wt%로 일정하게 유지하고 계면활성제의 양을 0.09 wt%부터 0.25 wt%까지 증가시킬 때, 계면활성제 조성의 변화에 따른 상전이 압력의 관계는 Table 3과 Figure 5에 나타내었다. 물과 계면활성제의 일정조성에서 온도가 증가함에 따라 상전이 압력이 상승하고 있으며, 계면활성제의 조성이 증가함에 따라 상전이 압력이 미세하게 상승하고 있음을 알 수 있다.
[Table 3.] Measured cloud points of CO2+ sorbitan monopalmitate + water system at 0.2 wt% of water
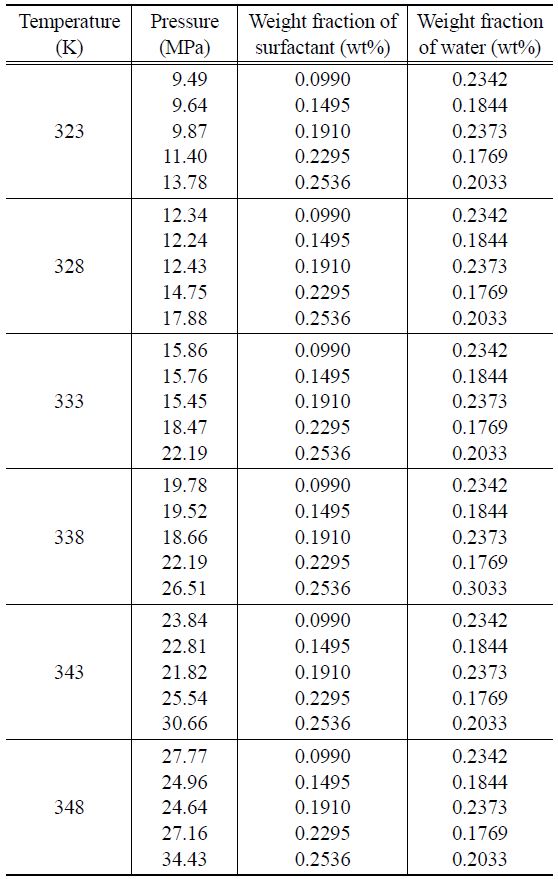
Measured cloud points of CO2+ sorbitan monopalmitate + water system at 0.2 wt% of water
이산화탄소 + 소르비탄 모노팔미테이트의 이성분 혼합물과 이산화탄소 + 소르비탄 모노팔미테이트 + 물의 삼성분 혼합물의 상거동 자료를 얻기 위해 가변부피 상거동 측정장치를 이용하여 온도변화에 따른 운점의 상전이 압력을 측정하였다. 각각의 이성분계와 삼성분계 실험의 온도조건은 318 K, 323 K, 328 K, 333 K, 338 K, 343 K, 348 K의 일정온도 조건에서 실험을 수행하였으며, 이때 측정된 상거동 압력범위는 약 8-40 MPa로 나타났다. 이산화탄소 + 소르비탄 모노팔미테이트의 이성분계 실험에서는 계면활성제의 조성이 0.226 wt% 부근에서 최대의 운점압력이 측정되었으며, 계면활성제의 조성이 0.226 wt% 이상일 때 조성이 증가할수록 측정된 운점압력은 낮아지는 경향이 나타나 위로 볼록한 형태의 그래프가 나타났다.
이산화탄소 + 소르비탄 모노팔미테이트 + 물인 삼성분계의 상거동을 관찰하기 위해서는 온도, 압력, 계면활성제의 질량분율 그리고 물의 질량분율의 4가지 변수 중 계면활성제의 질량분율을 약 0.1 wt%로 일정하게 두고 물의 질량분율 변화에 따른 상전이 온도와 압력의 변화를 측정하였고, 물의 질량분율을 약 0.2 wt%로 일정하게 두고 계면활성제의 질량분율 변화에 따른 상전이 온도와 압력의 변화 측정하였다. 계면활성제의 질량분율을 일정하게 둔 경우 물의 질량분율이 증가함에 따라 상전이 압력인 운점압력 값이 상승하는 경향을 관찰하였다. 또한, 물의 질량분율을 고정시킨 경우 계면활성제의 질량분율이 0~0.191 wt%에서는 계면활성제의 조성이 증가함에 따라 상전이 압력이 일정하게 유지되고, 계면활성제의 질량분율이 0.191 wt% 이상인 경우 조성이 증가함에 따라 상전이 압력이 상승하는 경향을 보여주고 있다.