오늘날 경제 성장에 따른 도시고형폐기물(Municipal Solid Waste, MSW)의 발생량 증가로 MSW의 환경적인 처리 및 에너지 회수측면에서 폐기물 가스화에 대한 연구가 활발히 진행되고 있다. 본 연구에서는 폐기물 가스화 공정을 통하여 생산된 합성가스의 활용연구를 위하여 폴리아마이드 복합막을 이용한 일산화탄소 및 수소 혼합가스의 분리특성 연구를 수행하였다. 폐기물 합성가스의 분리특성 실험을 위하여 순수 일산화탄소와 수소를 혼합한 모사가스를 활용하였으며, 주입 기체의 유량과 스테이지 컷(stage cut)의 변화에 따른 분리특성에 있어서 온도의 영향을 고찰하였다. 각 실험조건에서 일산화탄소와 수소의 투과도를 평가하였으며, 이때 퍼미에이트(permeate)에서의 수소에 대한 선택도를 평가하였다. 또한 본 연구에서 일산화탄소와 수소의 기체 분리막에 대한 투과 활성화 에너지를 얻기 위하여 Arrhenius 도시를 이용한 분석연구를 함께 수행하였다.
폐기물 가스화 공정은 폐기물의 적정 처리와 함께 합성가스를 생산할 수 있다는 측면에 있어서 최근 관심의 대상이 되고 있다. 특히 오늘날 세계적으로 경제가 급격히 성장함에 따라 폐기물의 발생량 또한 급격히 증가하고 있어 환경적 및 사회적으로 도시고형폐기물(Municipal Solid Waste, MSW)의 처리가 주요문제가 되고 있다[1,2]. MSW의 처리에 있어서 현재 대부분 매립 및 소각이 활용되고 있으나 사회적 비용과 2차 환경오염 발생 등의 문제로 폐기물의 가스화 방법에 대한 연구가 활발히 진행 중에 있으며, 이러한 가스화 기술은 다른 처리 기술에 비하여 다이옥신 등과 같은 2차 오염물의 배출이 적고 특히 에너지 또는 화학원료를 생산할 수 있다는 측면에서 환경적인 문제를 해결함과 동시에 신재생에너지를 확보할 수 있다는 장점으로 인하여 더욱 매력적인 공정이라고 할 수 있다[3-5].
페기물 가스화 공정으로부터 생성되는 합성가스 성분은 일산화탄소, 이산화탄소, 수소, 메탄 등으로 구성되며 이 중 일산화탄소와 수소가 주성분을 차지하고 있다[6]. 특히 주성분인 일산화탄소는 C1화학공정에 있어서 기본적인 화학물질의 합성을 위한 기초물질로 활용되고 있으며 따라서 이러한 합성가스로부터의 일산화탄소를 분리, 정제하는 기술은 매우 중요한 공정 중 하나이다[7]. 현재 일산화탄소와 수소 혼합가스의 분리공정에 있어서 기체분리막 공정은 흡착법, 흡수법, 심냉법과 같은 다른 분리공정들과 꾸준히 경쟁하고 있다[8]. 기체분리막 공정의 특징은 다른 공정들과 비교할 때 어떠한 상변화도 요구되지 않으며, 혼합물질을 분리하는데 특별히 다른 물질의 첨가가 필요하지 않고, 장치가 단순할 뿐만 아니라 구동장치가 거의 없어 에너지 측면에서 매우 유리하다. 또한 공기 중에 유해 물질의 배출이나, 폐수 발생 등의 문제가 없어 환경 친화적인 공정이라고 할 수 있으며, 상대적으로 운전 및 제어 그리고 용량증가가 용이하다는 장점을 가지고 있어 매우 매력적인 공정으로 인식되고 있다. 따라서 석유화학 공정, 수소의 분리 및 정제, 천연가스 정제, 매립지 가스 회수, 탈기 및 헬륨 회수 등과 같은 다양한 분야에 대한 연구가 활발히 진행 중에 있다[9-13].
본 연구에서는 폐기물 합성가스로부터 일산화탄소를 분리회수하기 위하여 다공성 폴리이미드에 폴리아마이드가 침적된 상용화 중공사 복합막을 이용하여 일산화탄소 및 수소의 혼합가스로부터 일산화탄소의 분리특성 연구를 수행하였으며 이 때 각 실험조건에 따른 온도의 영향을 고찰하였다. 실험조건으로는 운전온도, 주입 기체의 유량 그리고 스테이지 컷(stage cut)을 변화시키며 일산화탄소와 수소의 투과도를 평가하였으며, 또한 Arrhenius 도시를 이용하여 일산화탄소와 수소의 기체 분리막에 대한 투과 활성화 에너지 연구를 함께 수행하였다.
본 논문에 사용된 고분자 분리막은 SepraTek Co. (Korea)에서 생산된 상용화 복합 고분자 막으로 활성화 층을 구성하고 있는 폴리아마이드 층에서 기체분자가 막성분과의 친화력에 의하여 용해된 후 용해된 기체분자는 막 내부의 자유부피(free volume)를 통해 확산된다.
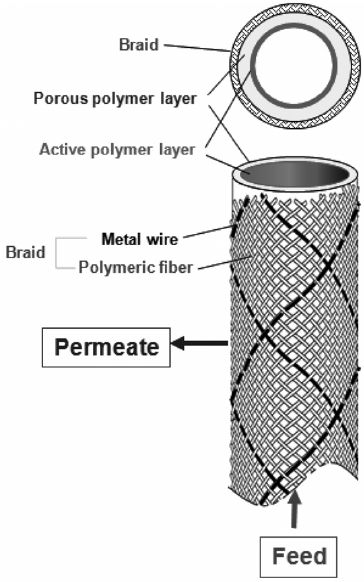
이후 확산된 기체는 지지층으로 사용된 폴리이미드 층을 통과하여 저압측의 계면에서 탈리되어 배출되는 형태로 막의 총 표면적은 0.55 m2이며 Figure 1에 본 연구에 사용된 기체분리막의 개념도를 나타내었다. Figure 1로부터 중공사막 내부에는 활성 고분자층인 폴리아마이드와 다공성 고분자층인 폴리이미드 구성되어 있으며, 중공사막 외부는 분리막의 안전성을 위하여 금속 wire와 고분자 섬유로 강화되어 있는 브레이드(braid) 층으로 구성되어 있음을 볼 수 있다. 또한 Figure 2에 중공사막의 내부를 구성하고 있는 고분자 분리막층에 대한 주사현미경(Scanning Electron Microscope, SEM)사진을 나타내었다. Figure 2로부터 다공성 폴리이미드에 폴리아마이드막이 균일하게 침적되어 있음을 볼 수 있다.
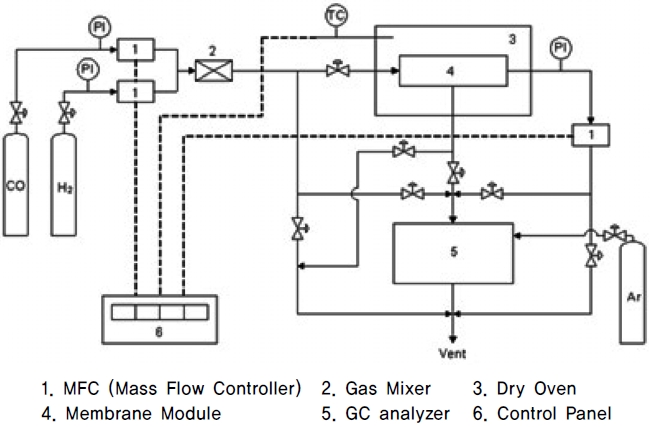
일산화탄소 및 수소의 혼합가스 분리특성 실험을 위하여 본 연구에서 사용된 기체분리막 실험장치도를 Figure 3에 나타내 었다. 실험에 사용된 모사기체로는 순도 99.95%의 일산화탄소와 순도 99.999%의 수소를 사용하였으며, 주입가스의 각 성
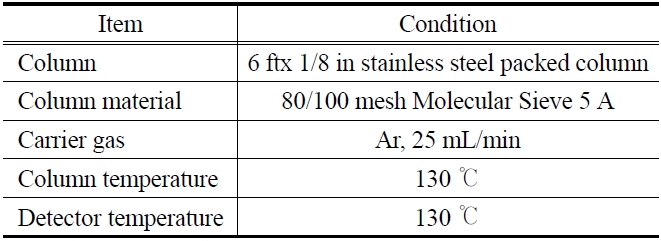
분의 농도가 50%가 되도록 유량제어기(Mass Flow Contoller, MFC)를 이용하여 주입 유량을 조절하면서 연구를 수행하였다. 일반적으로 폐기물 합성가스의 경우 일산화탄소와 수소성분만을 고려할 경우 일산화탄소의 함량이 55%를 차지하게 되며 따라서 본 연구에서는 고순도의 일산화탄소회수를 위한 기체분리막 특성의 연구를 수행하기 위하여 이보다 일산화탄소의 함량이 다소 낮은 50%를 주입가스의 일산화탄소농도로 설정하였다. 주입된 기체는 기체혼합기에서 균일하게 혼합된 후 분리막 모듈로 주입되며, 이때 온도에 대한 기체 분리특성을 연구하기 위해 분리막 모듈을 건조기내에 설치하였다. 혼합된 기체는 분리막 모듈을 거치면서 수소의 함유량이 높은 기체는 퍼미에이트(permeate)로 그리고 일산화탄소의 함유량이 높은 기체는 리텐테이트(retentate)로 배출되며, 리텐테이트의 기체 배출라인에 연결된 MFC를 이용하여 기체 배출량을 조절함으로써 스테이지 컷을 조절할 수 있도록 하였다. 또한 실험과정에서 각 기체의 성분을 실시간으로 분석하기 위하여 퍼미에이트와 리텐테이트의 배출라인에 바이패스(by-pass) 라인을 설치하였으며, 바이패스 라인과 연결된 GC analyzer (iGC7200 DS SCIENCE, Korea)를 이용하여 각 기체의 조성을 분석하였다. GC analyzer의 운반기체(carrier gas)로는 아르곤 기체를 사용하였으며, 본 연구에 사용된 GC analyzer의 분석조건을 Table 1에 나타내었다. 본 연구에서는 폴리아마이드 복합막을 이용한 일산화탄소와 수소의 분리특성에 대한 온도의 영향을 고찰하기 위하여 600 cm3/min의 기체유량에서 30~70 ℃로 운전온도를 변화시키며 실험을 수행하였다. 기체분리막모듈의 경우 운전온도의 변화에 따라 기체의 부피변화로 인하여 운전압력 또한 변화될 수 있으며 이러한 운전압력의 변화는 운전온도에 대한 영향을 고찰하는데 있어서 방해요인으로 작용할 수 있다. 따라서 본 연구에서는 일정한 운전압력에서의 운전온도에 대한 영향을 고찰하고자 600~800 cm3/min의 기체유량 변화와 50~69%의 스테이지 컷을 변화시켜 일정한 운전압력 조건에서의 온도에 따른 분리특성 연구를 함께 수행하였다.
또한 각 운전 조건별 실험 결과를 분석하기 위해 다음과 같이 정의된 측정변수를 이용하여 혼합기체로부터의 일산화탄소 분리특성을 고찰하였으며, 이 때 일산화탄소와 수소의 투과도는 다음과 같이 분리막 모듈의 압력과 표면적 그리고 퍼미에이트의 유량과 관계된다.
[Table 1.] Operation conditions of GC analyzer used in this work
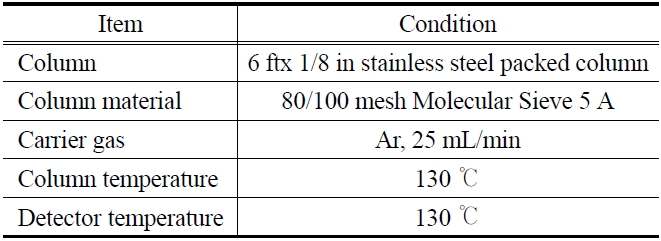
Operation conditions of GC analyzer used in this work
위의 식에서
여기서
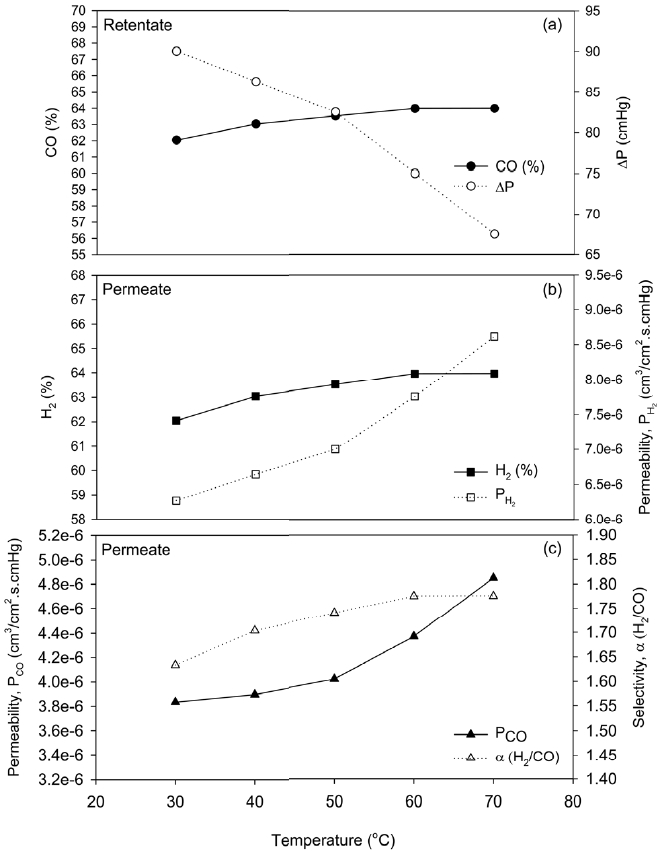
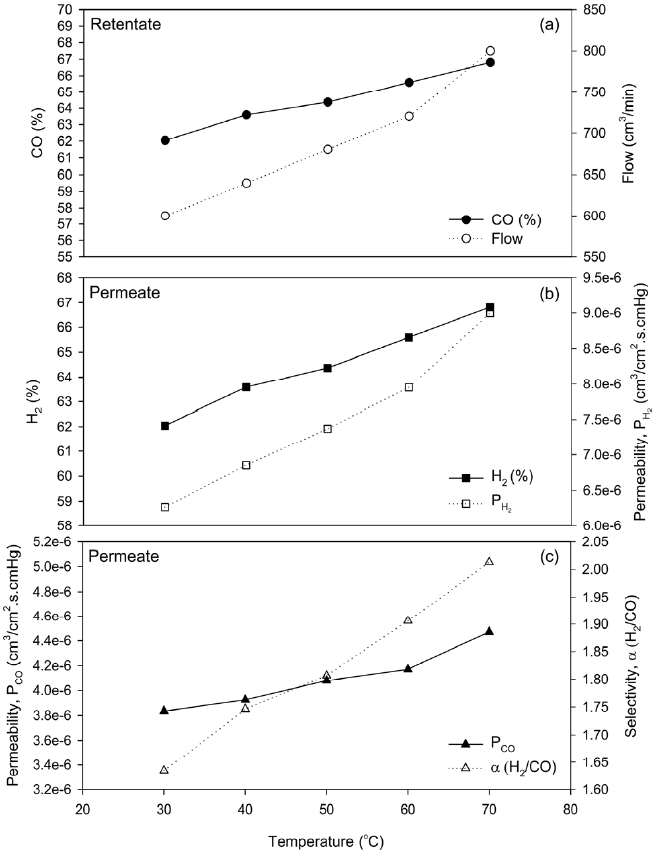
본 연구에서는 폴리아마이드 복합막을 이용한 일산화탄소 및 수소의 혼합기체로부터 일산화탄소의 분리특성에 대한 온도의 영향을 고찰하기 위하여 450 cmHg의 초기 기체 주입압력과 600 cm3/min의 기체 주입유량 그리고 50%의 스테이지 컷 운전조건에서 30~70 ℃로 분리막의 운전온도를 변화시켜 일산화탄소 분리특성 실험을 하였으며, 그 결과를 Figure 4에 나타내었다.
각 실험결과에서 실제 운전압력이 450 cmHg의 초기 기체 주입압력에 비하여 낮아지는 이유는 주입된 혼합 기체가 기체혼합기 및 분리막 모듈 시스템의 부피증가로 인하여 압력손실이 발생하기 때문으로 판단되어 실제 운전압력은 퍼미에이트와 리텐테이트의 압력차로 본 연구의 퍼미에이트의 압력이 대기압임을 고려할 경우 압력차는 실제 분리막에 적용되는 운전압력으로 고려될 수 있다. 온도에 따른 운전압력의 변화를 나타내는 (a)로부터 온도가 증가함에 따라 리텐테이트에서의 압력이 감소함을 볼 수 있다. 이는 리텐테이트의 기체라인에 설치된 MFC의 경우 표준상태의 조건에서 보정되어 있는 관계로 운전온도의 증가에 따라 리텐테이트로 배출되는 기체의 온도 또한 상승하여 실제 MFC을 통하여 조절된 기체유량이 온도에 따라 변화되었기 때문으로 판단된다. 분리막공정에서의 분리효율은 각 성분의 분리막으로의 용해도와 자유부피에 의한 확산에 의해 결정된다. 일반적으로 온도가 증가할수록 자유부피에 의한 확산은 증가하나 용해도는 감소하며, 두 상호작용에 따라 기체 분리막에서의 기체 투과도는 결정된다[14]. 그러나 (b), (c)로부터 온도가 증가할수록 퍼미에이트로 배출되는 일산화탄소 및 수소의 투과도는 모두 증가하
였으며, 따라서 본 연구에 사용된 폴리아마이드 복합막의 경우 온도의 증가에 따른 용해도 감소에 의한 영향에 비하여 기체의 확산속도 증가에 의한 영향이 보다 크게 작용함을 볼 수 있었다. 또한 (c)로부터 온도가 증가함에 따라 퍼미에이트에서의 수소 선택도가 증가함을 볼 수 있었으며, 이는 온도가 증가함에 따라 수소의 투과도가 일산화탄소의 투과도에 비하여 보다 크게 증가하였기 때문으로 판단된다. 따라서 온도에 대한 영향이 일산화탄소에 비하여 수소의 투과도에 더 민감하게 작용한다는 것을 확인할 수 있었다.
Figure 4의 경우 온도가 증가함에 따라 운전 압력이 변화되었으며 이러한 운전압력의 변화는 분리특성에 대한 온도의 영향을 고찰하는데 있어서 결과를 왜곡할 소지가 있다. 따라서 본 연구에서는 운전 온도변화에 따른 운전압력의 변화를 최소화하기 위하여 주입기체의 유량과 스테이지 컷을 조절하며 실험을 하였다. 이때 운전압력이 90 cmHg로 유지될 수 있도록 주입 기체유량은 600~800 cm3/min, 스테이지 컷은 50~69%의 범위에서 조절하였으며, 그 실험결과를 Figure 5와 6에 각각 나타내었다.
스테이지 컷을 50%로 일정하게 하고 주입 기체유량으로 압력을 보정한 Figure 5의 경우 Figure 4와 같이 온도가 증가함에 따라 퍼미에이트에서 일산화탄소와 수소의 투과도 모두 증가하였다. 또한 Figure 4의 경우와 비교할 때 그 증가폭이 보다
높음을 알 수 있으며, 특히 온도의 증가에 따른 수소의 투과도 증가가 크게 나타났으며, 이로 인하여 퍼미에이트에서의 수소에 대한 선택도 또한 Figure 4의 경우에 비하여 높게 나타남을 알 수 있다. 퍼미에이트에서 수소의 선택도 증가는 결과적으로 일산화탄소와 수소의 혼합기체로부터 일산화탄소의 분리효율이 증가함을 의미한다. 일반적으로 기체분리막을 이용한 혼합기체의 분리에 있어서 운전압력은 매우 중요한 인자로 작용한다. 따라서 운전압력이 감소한 Figure 4의 경우에 비하여 Figure 5의 경우 일정하게 운전압력이 유지됨에 따라 퍼미에이트에서의 수소의 선택도가 보다 높게 나타났다고 판단된다.
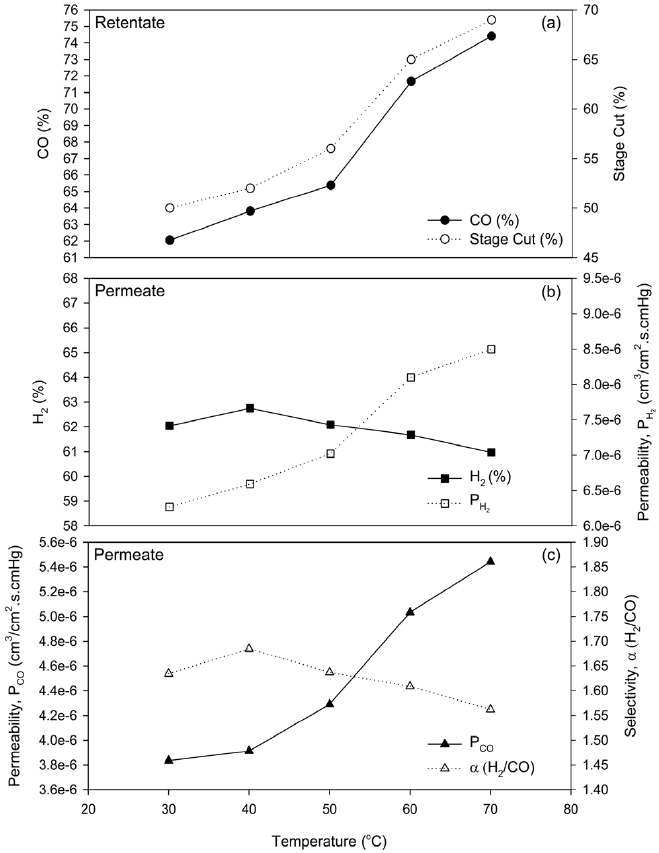
Figure 5의 경우 운전압력을 보정하기 위해 기체의 주입 유량을 변화시켰다. 그러나 기체분리막의 경우 기체의 주입유량에 따라 분리막 효율이 영향을 받을 수 있으며 따라서 본 연구에서는 기체 주입유량의 영향을 최소화한 상태에서 분리막에 작용하는 압력을 일정하게 보정하기 위하여 스테이지 컷을 조절하여 운전온도별 분리실험을 수행하였다. 이때 혼합기체의 주입 유량은 600 cm3/min으로 일정하게 유지시켰으며 그 결과를 Figure 6에 나타내었다. Figure 6의 경우 또한 Figure 4 및 5와 같이 온도 증가함에 따라 일산화탄소와 수소의 투과도는 모두 증가하였으나 퍼미에이트에서 수소의 선택도는 거의 일정함을 볼 수 있다. 이는 일산화탄소와 수소의 투과도가 온도
의 증가에 따라 거의 유사하게 증가하였기 때문으로 판단된다. 그러나 실제 기체분리막에 있어서 기체의 유입유량 또한 분리특성에 영향을 미칠 수 있으며 따라서 기체의 유입유량을 일정하게 하고 스테이지 컷을 조절한 Figure 6의 실험결과가 일산화탄소와 수소의 분리특성에 있어서의 온도의 영향을 보다 정확히 나타낼 수 있다고 판단된다.
분리막을 통한 기체의 투과도는 앞에서 언급한 바와 같이 기체의 막에 대한 용해도와 확산계수의 영향을 받으며 용해도 및 확산계수는 다음과 같은 Arrhenius형으로 나타낼 수 있다[15].
여기서
식 (7)에서
본 연구에서는 폴리아마이드 복합막을 이용한 일산화탄소와 수소의 혼합기체로부터 일산화탄소의 분리특성 연구를 수행하였으며 이때 각 실험조건에 따른 온도의 영향을 고찰하였다. 본 연구로부터 운전온도가 증가함에 따라 일산화탄소와 수소의 경우 모두 분리막에 대한 용해도 감소에 의한 영향에 비하여 기체의 확산속도 증가에 의한 영향이 보다 크게 작용함에 따라 일산화탄소 및 수소의 투과도는 모두 증가함을 확인할 수 있었다.
퍼미에이트에서의 수소 선택도의 경우, 분리막에서의 운전 압력을 일정하게 유지시키기 위하여 기체의 주입유량을 변화시킨 경우 운전온도의 증가에 따라 선택도가 증가한 반면에 기체의 주입유량을 일정하게 유지시키고 스테이지 컷을 변화시킨 경우 선택도는 거의 변화가 없었다. 그러나 실제 기체분리막에 있어서 기체의 유입유량 또한 분리특성에 영향을 미칠 수 있으며 따라서 기체의 유입유량을 일정하게 하고 스테이지 컷을 조절한 경우의 실험결과가 일산화탄소와 수소의 분리특성에 대한 온도의 영향을 보다 정확히 나타낼 수 있다고 판단된다.
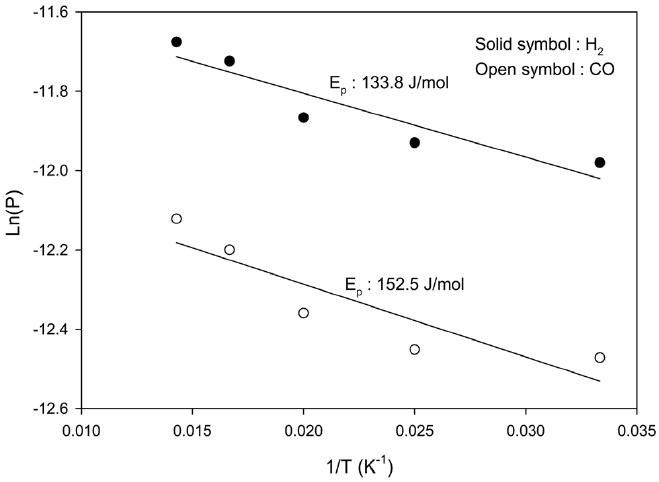
또한 기체분리막을 이용한 일산화탄소와 수소의 투과 활성화 에너지를 얻기 위한 Arrhenius 도시로부터 일산화탄소의 경우 152.5 J/mol의 투과 활성화 에너지와 수소의 경우 133.8 J/mol의 투과 활성화 에너지를 각각 얻을 수 있었으며, 이때 투과계수는 일산화탄소의 경우 6.66 × 10-6 cm3/cm2?s?cmHg 그리고 수소의 경우 1.03 × 10-5 cm3/cm2?s?cmHg을 각각 얻을 수 있었다.